TIB-Chemicals — Цинковые химикаты
Начинать ‣ Продукты и решения ‣ Металлохимия и отделочные материалы ‣ Наша химия ‣ Цинковые химикаты
Химическая нитрат цинка представляет собой цинковую соль азотной кислоты с химической формулой Zn(NO3)2. Молекулярная масса соединения 225,18 г/моль. Нитрат цинка зарегистрирован под номером CAS 7779-88-6, номером ЕС 231-943-8 и номером ООН: 1514.
Нитрат цинка кристаллический представляет собой бесцветное окисляющееся твердое вещество. Разлагается при нагревании, при этом образуются оксиды азота и оксид цинка, выделяемые ранее выше 105°С кристаллизационной водой. Из азотнокислого цинка существуют различные соли с различным количеством кристаллизационной воды. Самый известный содержит шесть эквивалентов воды (гексагидрат).
Гидрат нитрата цинка очень хорошо растворяется в воде и этаноле. Плотность концентрированного водного раствора от бесцветного до бледно-желтого цвета составляет около 1,5 г/мл при рН 1.
В международном обороте следующие термины используются для нитрата цинка e:
- Нитрат цинка и гексагидрат нитрата цинка (США и Соединенное Королевство)
- Nitrato de cinc (Испания и Латинская Америка)
- Нитраты цинка (Франция)
- Нитрато ди цинко (Италия)
Использование раствора нитрата цинка Zn (NO3) 2 в виде раствора (680 г на литр, номера CAS: 779-88-6)
Для использования в промышленности и производстве Нитрат цинка можно приобрести в TIB Chemical s в виде раствора 680 граммов на литр и № CAS. 779-88-6 оптимально подходит и прост в обращении.
Нитрат цинка используется в различных областях. С одной стороны нитрат цинка является важным химическим веществом для синтеза других родственных химикатов цинка и поэтому широко используется в качестве сырья в химической промышленности. С другой стороны, нитрат цинка используется во многих отраслях промышленности для различных целей. Например, нитрат цинка используется в текстильной промышленности в качестве катализатора для достижения определенных эффектов на текстиле. Нитрат цинка , например, обеспечивает более высокий уровень сшивания — по сравнению с хлоридом магния — при производстве целлюлозных волокон, например, в сочетании с более высокой кислотостойкостью волокон.
С другой стороны, нитрат цинка используется во многих отраслях промышленности для различных целей. Например, нитрат цинка используется в текстильной промышленности в качестве катализатора для достижения определенных эффектов на текстиле. Нитрат цинка , например, обеспечивает более высокий уровень сшивания — по сравнению с хлоридом магния — при производстве целлюлозных волокон, например, в сочетании с более высокой кислотостойкостью волокон.
Нитрат цинка также незаменим при гальванике и окрашивании ацетатных волокон. Нитрат цинка набухает на ацетатных волокнах, так что результат окрашивания становится более равномерным, а основные красители могут глубже проникать в волокно.
В химии металлов и поверхностей нитрат цинка используется в качестве отбеливателя и протравы. Там нитрат цинка особенно востребован в качестве раствора, так как они позволяют еще легче обращаться. С помощью жидкости нитрат цинка , например, различные поверхности могут быть предварительно обработаны индивидуально в соответствии с соответствующими требованиями. Основными областями применения являются защита от коррозии (увеличение срока службы различных компонентов и деталей), снижение адгезии, трения и износа, а также электроизоляция.
С помощью жидкости нитрат цинка , например, различные поверхности могут быть предварительно обработаны индивидуально в соответствии с соответствующими требованиями. Основными областями применения являются защита от коррозии (увеличение срока службы различных компонентов и деталей), снижение адгезии, трения и износа, а также электроизоляция.
Нитрат цинка Zn (NO3) 2 в виде раствора с 680 г на литр (номер CAS: 779-88-6)
Как опытный производитель, TIB Chemicals предлагает широкий ассортимент из химикаты для цинка и другие химикаты для широкого спектра применений. Конечно, помимо нитрата цинка , наш ассортимент также включает другие химикаты цинка ls и соединения. Если, вопреки ожиданиям, наш стандартный ассортимент не соответствует вашим требованиям, также возможно изготовление подходящего для вас продукта в рамках контрактного производства. По любым вопросам о заказе, отдельных продуктах или индивидуальных предложениях обращайтесь к нашим компетентным консультантам в любое время.
zn(no3)2
zn(no3)2 —
Имена и идентификаторы| Name | Zinc Nitrate Hexahydrate |
| Synonyms | ZN(NO3)2 Zinc nitrate zinc dinitrate ZINC NITRATE 6h3O Zinc nitrate hydrate ZINC NITRATE, 6-HYDRATE Zincnitrate(metalsbasis) Zinc Нитрат гексагидрат ZINC NITRATE-6-HYDRATE PURE ZINC ICP STANDARD, ZN(NO3)2 |
| CAS | 10196-18-6 |
| EINECS | 600-255-3 |
| InChI | InChI=1/NO3.6h3O .Zn/c2-1(3)4;;;;;;;/h;6*1h3;/q-1;;;;;;;;+2 |
| ИнЧИКей | JGPSMWXKRPZZRG-UHFFFAOYSA-N |
zn(no3)2 —
Физико-химические свойства| Молекулярная формула | h22N2O12Zn |
| Molar Mass | 297. 49 49 |
| Density | 2.065g/mLat 25°C(lit.) |
| Melting Point | 36°C(lit.) |
| Water Solubility | 1800 G/L (20 ºC) |
| Solubility | water: soluble(lit.) |
| Appearance | Solid |
| Specific Gravity | 2.07 |
| Color | White |
| Merck | 14,10144 |
| PH | pH(100g/l, 25℃) : 3.5~5.4 |
| Sensitive | Hygroscopic |
| Physical and Химические свойства | Характер: бесцветные тетрагональные кристаллы. точка плавления 36,4 ℃ относительная плотность 2,065 (14 ℃) растворим в воде и этаноле. Его водный раствор кислый. |
| Использование | В основном используется для цинкования деталей велосипедов, подготовки фосфатирующего агента для стали |
zn(no3)2 —
Риск и безопасность| Коды риска | R8 — Контакт с горючим материалом может вызвать пожар R22 — Вреден при проглатывании R36/37/38 — Раздражает глаза, дыхательные пути и кожу.  R38 — Раздражает кожу |
| Описание техники безопасности | S17 — Хранить вдали от горючих материалов. S26 — При попадании в глаза немедленно промыть большим количеством воды и обратиться к врачу. |
| UN IDs | UN 1514 5.1/PG 2 |
| WGK Germany | 3 |
| RTECS | Zh5775000 |
| TSCA | Yes |
| HS Code | 28342990 |
| Класс опасности | 5,1 |
| Группа упаковки | II |
441911.9003
4.1005
90034.1003
4.10034444.1000.9003
4.44.
Сырье Гипооксид цинка
Азотная кислота
Оксид цинка
zn(no3)2 —
Природа бесцветный 90s. Безвкусный. Температура плавления приблизительно 36 °С; д 2.065. Растворим примерно в 0,5 части воды, водный раствор кислый, рН 5% водного раствора 5,1. Расплывчатость. Растворим в этаноле. Его растворяли в кристаллизационной воде при нагревании до 37°С. Вся кристаллизационная вода терялась при 105-131°С. При разложении при высокой температуре образуется газ оксидов азота, который раздражает и обладает высокой токсичностью, вызывая отравление при вдыхании. Когда горючие материалы горят, они могут способствовать возникновению пожара. С серой, фосфором, углеродом, медью, сульфидами металлов и органикой контактирует интенсивная реакция.
Безвкусный. Температура плавления приблизительно 36 °С; д 2.065. Растворим примерно в 0,5 части воды, водный раствор кислый, рН 5% водного раствора 5,1. Расплывчатость. Растворим в этаноле. Его растворяли в кристаллизационной воде при нагревании до 37°С. Вся кристаллизационная вода терялась при 105-131°С. При разложении при высокой температуре образуется газ оксидов азота, который раздражает и обладает высокой токсичностью, вызывая отравление при вдыхании. Когда горючие материалы горят, они могут способствовать возникновению пожара. С серой, фосфором, углеродом, медью, сульфидами металлов и органикой контактирует интенсивная реакция. Последнее обновление:2022-01-01 09:07:38
zn(no3)2 —
Способ приготовления
Азотная кислота
Оксид цинка
 Безвкусный. Температура плавления приблизительно 36 °С; д 2.065. Растворим примерно в 0,5 части воды, водный раствор кислый, рН 5% водного раствора 5,1. Расплывчатость. Растворим в этаноле. Его растворяли в кристаллизационной воде при нагревании до 37°С. Вся кристаллизационная вода терялась при 105-131°С. При разложении при высокой температуре образуется газ оксидов азота, который раздражает и обладает высокой токсичностью, вызывая отравление при вдыхании. Когда горючие материалы горят, они могут способствовать возникновению пожара. С серой, фосфором, углеродом, медью, сульфидами металлов и органикой контактирует интенсивная реакция.
Безвкусный. Температура плавления приблизительно 36 °С; д 2.065. Растворим примерно в 0,5 части воды, водный раствор кислый, рН 5% водного раствора 5,1. Расплывчатость. Растворим в этаноле. Его растворяли в кристаллизационной воде при нагревании до 37°С. Вся кристаллизационная вода терялась при 105-131°С. При разложении при высокой температуре образуется газ оксидов азота, который раздражает и обладает высокой токсичностью, вызывая отравление при вдыхании. Когда горючие материалы горят, они могут способствовать возникновению пожара. С серой, фосфором, углеродом, медью, сульфидами металлов и органикой контактирует интенсивная реакция.Последнее обновление:2022-01-01 09:07:38
zn(no3)2 —
Способ приготовленияВодный раствор азотной кислоты нагревали, в раствор несколько раз добавляли частицы цинка, растворяли , фильтруют, фильтрат упаривают до относительной плотности 1,61 пар, охлаждают и отсасывают.
Последнее обновление:2022-01-01 09:07:38
zn(no3)2 —
Используйте определение серы в аналитических реагентах, таких как кровь. Также используется в латексном коагулянте, катализаторе, протраве для печати и окрашивания, цинковании, фосфатировании стали.
Также используется в латексном коагулянте, катализаторе, протраве для печати и окрашивания, цинковании, фосфатировании стали.
Последнее обновление:2022-01-01 09:07:39
zn(no3)2 —
БезопасностьХранить в прохладном вентилируемом складе. Хранить вдали от огня и источников тепла. Упаковка должна быть полностью герметичной, чтобы предотвратить впитывание влаги. Он должен храниться отдельно от горючих материалов, горючих материалов, восстановителей, порошков активных металлов и т. д. и не должен смешиваться.
Последнее обновление:2022-01-01 09:07:39
zn(no3)2 —
Справочная информация| токсичность | его пыль повреждает верхние дыхательные пути, трахею и слизистую оболочку бронхов. Его концентрированный раствор может вызвать язвы на коже. При длительном контакте с этим продуктом возникнет дерматит. Производственные рабочие должны носить спецодежду, защитные маски, латексные перчатки и другие средства охраны труда для защиты кожи и органов дыхания. Производственное оборудование должно быть закрытым, вентиляция должна быть хорошей. Примите горячий душ после работы. Производственное оборудование должно быть закрытым, вентиляция должна быть хорошей. Примите горячий душ после работы. |
| Применение | в основном используется для цинкования деталей машин и велосипедов, протравы для окрашивания текстиля и т. д. используется для цинкования деталей машин и велосипедов. Приготовление фосфатирующего агента для стали, крашения ткани, используемого в качестве протравы, синтетического консерванта красителя, используемого в качестве латексного коагулянта. используется в качестве аналитического реагента, а также используется в фармацевтической промышленности |
| метод производства | метод оксида цинка в реактор добавляют определенное количество воды, медленно добавляют азотную кислоту и оксид цинка в реакцию до рН 1,6~4 при перемешивании в соответствии с соотношением ингредиентов 100%: 1 (из расчета по содержанию 3,5), выдерживают 24 ч, фильтруют, фильтрат разбавляют водой до 30~36°Ве, доводят до рН 3 азотной кислотой, добавляют порошок цинка, перемешивают несколько минут для замены Cu2+, Pb2+ плазмы, и затем осветляют, прозрачную жидкость, полученную фильтрованием с отсасыванием, подкисляют, концентрируют до 60-63°Ве выпариванием, а затем охлаждают до температуры ниже 50°С при перемешивании до получения готового продукта нитрата цинка.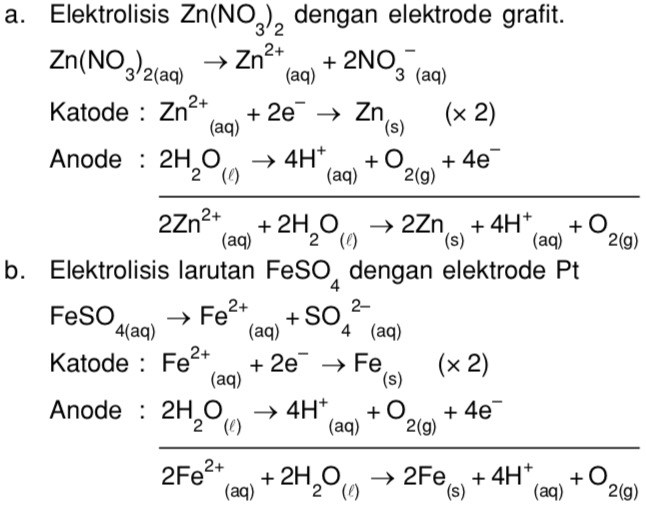 |
