Газы | Формула | Плотность при нормальных условиях ρ, кг/м3 |
Азот | N2 | 1,2505 |
Аммиак | NH3 | 0,7714 |
Аргон | Ar | 1,7839 |
Ацетилен | C2H2 | 1,1709 |
Ацетон | C3H6O | 2,595 |
Бор фтористый | BF3 | 2,99 |
Бромистый водород | HBr | 3,664 |
Н-бутан | C4H10 | 2,703 |
Изо-бутан | C4H10 | 2,668 |
Н-бутиловый спирт | C4H10O | 3,244 |
Вода | H2O | 0,768 |
Водород | H2 | 0,08987 |
Воздух (сухой) | — | 1,2928 |
Н-гексан | C6H14 | 3,845 |
Гелий | He | 0,1785 |
Н-гептан | C7H16 | 4,459 |
Германия тетрагидрид | GeH4 | 3,42 |
Двуокись углерода | CO2 | 1,9768 |
Н-декан | C10H22 | 6,35 |
Диметиламин | (CH3)2NH | 1,966* |
Дифтордихлорметан | CF2Cl2 | 5,51 |
Дифенил | C12H10 | 6,89 |
Дифениловый эфир | C12H10O | 7,54 |
Дихлорметан | CH2Cl2 | 3,79 |
Диэтиловый эфир | C4H10O | 3,30 |
Закись азота | N2O | 1,978 |
Йодистый водород | HI | 5,789 |
Кислород | O2 | 1,42895 |
Кремний фтористый | SiF4 | 4,9605 |
Кремний гексагидрид | Si2H5 | 2,85 |
Кремний тетрагидрид | SiH4 | 1,44 |
Криптон | Kr | 3,74 |
Ксенон | Xe | 5,89 |
Метан | CH4 | 0,7168 |
Метиламин | CH5N | 1,388 |
Метиловый спирт | CH4O | 1,426 |
Мышьяк фтористый | AsF5 | 7,71 |
Неон | Ne | 0,8999 |
Нитрозилфторид | NOF | 2,176* |
Нитрозилхлорид | NOCl | 2,9919 |
Озон | O3 | 2,22 |
Окись азота | NO | 1,3402 |
Окись углерода | CO | 1,25 |
Н-октан | C8H18 | 5,03 |
Н-пентан | C5H12 (CH3(CH2)3СН3) | 3,457 |
Изо-пентан | C5H12 (СН3)2СНСН2СН3 | 3,22 |
Пропан | C3H8 | 2,0037 |
Пропилен | C3H6 | 1,915 |
Радон | Rn | 9,73 |
Силан диметил | SiH2(CH3)2 | 2,73 |
Силан метил | SiH3CH3 | 2,08 |
Силан хлористый | SiH3Cl | 3,03 |
Cилан трифтористый | SiHF3 | 3,89 |
Стибин (15°С, 754 мм.рт.ст.) | SbH3 | 5,30 |
Селеновая кислота | H2Se | 3,6643 |
Сернистый газ | SO2 | 2,9263 |
Сернистый ангидрид | SO3 | 3,575 |
Сероводород | H2S | 1,5392 |
Сероокись углерода | COS | 2,72 |
Сульфурил фтористый | SO2F2 | 3,72* |
Триметиламин | (CH3)3N | 2,58* |
Триметилбор | (CH3)3B | 2,52 |
Фосфористый водород | PH3 | 1,53 |
Фосфор фтористый | PF3 | 3,907* |
Фосфор оксифторид | POF3 | 4,8 |
Фосфор пентафторид | PF5 | 5,81 |
Фреон-11 | CF3CI | 6,13 |
Фреон-12 (дифтордихлорметан) | CF2CI2 | 5,51 |
Фреон-13 | CFCI3 | 5,11 |
Фтор | F2 | 1,695 |
Фтористый кремний | SiF4 | 4,6905 |
Фтористый метил | CH3F | 1,545 |
Фторокись азота | NO2F | 2,9 |
Хлор | Cl2 | 3,22 |
Хлор двуокись | ClO2 | 3,09* |
Хлор окись | Cl2O | 3,89* |
Хлористый водород | HCl | 1,6391 |
Хлористый метил (метилхлорид) | CH3Cl | 2,307 |
Хлористый этил | C2H5Cl | 2,88 |
Хлороформ | CHCl3 | 5,283 |
Хлорокись азота | NO2Cl | 2,57 |
Циан, дициан | C2N2 | 2,765 (2,335*) |
Цианистая кислота | HCN | 1,205 |
Этан | C2H6 | 1,356 |
Этиламин | C2H7N | 2,0141 |
Этилен | C2H4 | 1,2605 |
Этиловый спирт | C2H6O | 2,043 |
infotables.ru
Кислород плотность — Справочник химика 21
Установите молекулярную формулу вещества, содержащего 81,6% хлора и 18,4 % кислорода. Плотность этого вещества по водороду 43,5. [c.142]Соединение содержит 39,14% углерода, 8,7% водорода, 52,16% кислорода. Плотность паров по водороду равна 46. Определить истинную формулу соединения. [c.16]
Пример. Анализ уксусной кислоты показывает, что в ней на 2,1 весовой части углерода приходится 0,35 весовой части водорода и 2,8 весовой части кислорода. Плотность пара уксусной кислоты по водороду равна [c.46]
Один из оксидов хлора содержит 47,4% кислорода. Плотность по водороду этого оксида в газообразном состоянии равна 33,75. Установите формулу оксида. [c.219]
Содержание кислорода, % Плотность при 20 °С, г/см з [c.540]
Электрофлотационный способ является одним из наиболее эффективных при очистке воды нефтепродуктов, тонкодисперсных частиц, растворенных органических соединений. Наиболее высокая степень очистки сточных вод достигается в электрофлотационных аппаратах, имеющих наряду с флотационной камерой и камеру электрокоагуляции. В этом случае сточные воды предварительно подвергаются воздействию как электрического поля, так и образующихся при электрокоагуляции оксидов металлов — продуктов растворения анодных электродных пластин. В качестве таких пластин используют сталь Ст.З. В камере электрокоагуляции в результате адсорбции загрязнений на хлопьях гидрооксида железа образуются агрегаты, которые включают также пузырьки выделяющихся при электролизе водорода и кислорода. Плотность этих агрегатов меньше, чем плотность воды. Однако скорость их флотационного отделения от воды невелика. Для интенсификации отделения этих агрегатов от воды и доочистки осветленной жидкости используют электрофлотацию с применением нерастворимого анода. Как показали экспериментальные исследования, продолжительность электрокоагуляции и флотации сточных вод должна быть одинаковой. При этом максимальная общая продолжительность электрокоагуляции и флотации сточных вод составляет 30 — 40 мин (0,5-0,65 ч).
Кислород малорастворим в воде (5 объемов в 100 объемах воды), ко все же лучше, чем другие газы атмосферы, поэтому вода обогащается кислородом. Плотность кислорода при нормальных условиях р = 1,429 г/л. При —183 °С кислород конденсируется в бледно-голубую жидкость (р = 1,13 г/см ), а при —218,7 С образует синие кристаллы. [c.111]
Кислород — наиболее распространенный элемент земной коры. Он составляет 89% массы воды, 23% массы воздуха (21% по объему) и почти 50% массы обычных минералов (силикатов). В элементном состоянии кислород состоит из двухатомных молекул, строение которых описано ниже. Зто бесцветный газ, не имеющий запаха и слабо растворимый в воде 1 л еоды при 0°С и 1 атм растворяет 48,9 мл газообразного кислорода. Плотность кислорода при 0°С и 1 атм равна 1,429 Г-Л-. Кислород конденсируется в бледно-голубую жидкость при температуре кипения —183,0 °С и при дальнейшем охлаждении отвердевает при —218,4 °С, образуя бледно-голубое кристаллическое вещество. [c.178]
Имеется смесь метана и кислорода плотностью [c.10]
В эвдиометре сожгли 20 мл газовой смеси, состоящей из азота, водорода и кислорода. Плотность смеси по водороду равна 14,0. После конденсации воды и приведения газовой смеси к начальным условиям объем ее был равен 17 мл. К образовавшейся смеси прибавили 50 мл воздуха и снова сожгли. Объем смеси не изменился. Определить процентный состав взятой газовой смеси. [c.11]
Определить формулу соединения, содержащего 39,14% углерода, 8,7% водорода и 52,16% кислорода. Плотность пара этого вещества по водороду равна 46. [c.64]
Задача 5. Анализ показал, что соединение состоит из 30,43% азота и69,57% кислорода. Плотность этого вещества по водороду равна 46. Определить его молекулярный вес и формулу. [c.56]
В обоих случаях защищаемая конструкция подвергается катодной поляризации, которая смещает ее потенциал к отрицательным значениям, а pH электролита, контактирующего непосредственно с металлом, сдвигается в щелочную область. Благодаря высокому pH на поверхности металла осаждаются гидроокись магния, карбонаты кальция и магния, образуя пленку подобно накипи. Эта пленка экранирует металлическую поверхность и затрудняет диффузию кислорода. Плотность защитного тока можно уменьшить за счет увеличения толщины защитной пленки. [c.66]
Вывести истинную формулу кислоты, в составе которой на 2,1 в. ч. углерода приходится 0,35 в. ч. водорода и 2,8 в. ч. кислорода. Плотность пара кислоты по водороду Вп = 30. [c.35]
Составьте уравнение реакции получения кислорода из перманганата калия (КМпО ) и вычислите массу перманганата калия, необходимого для получения 10 л (при н.у.) кислорода (плотность кислорода 1,43 г/л). [c.36]
Для цинкования берут железный гвоздь или стальную пластинку. Работу проводят, как и в предыдуш,ем опыте. На катоде выделяется цинк и водород, на аноде — кислород. Плотность тока около [c.254]
Пример 3. Вывести молекулярную формулу вещества, содержащего 40,00% углерода, 6,70% водорода и 53,30%о кислорода. Плотность пара по водороду равна 30. [c.6]
Сила основания определяется стабильностью образующегося катиона (сопряженной кислоты). Чем стабильней катион, тем сильнее основание. Стабильность катиона определяется суммой тех же факторов, что и стабильность аниона, с той лишь разницей, что влияние этих факторов на основность противоположно тому влиянию, которое они оказывали на кислотность. Например, наличие в углеводородном радикале электронодонорных заместителей будет способствовать стабилизации катиона и, следовательно, повышать силу основания. Напротив, электроноакцетхзрные заместители будут дестабилизировать катион и уменьшать основность соединения. Исходя из природы атомов кислорода, азота и серы, можно сделать вывод, что наиболее электроотрицательный атом кислорода за счет более прочного удерживания неподеленной пары электронов менее склонен присоединять протон по сравнению, например, с атомом азота. Действительно, амины обычно более сильные основания, чем спирты. Электроны атомов азота и серы менее прочно удерживаются ядром и более доступны для связи с протоном. Однако у атома серы электронная плотность рассредоточена в большем объеме по сравнению с атомом азота и кислорода. Плотность заряда становится меньшей и атом серы слабее связывает протон. Поэтому тиолы более слабые основания, чем амины и спирты. [c.159]
www.chem21.info
| / 7 августа 2006 года / Физика / habit.ru В таблице приведены плотности и формулы для основных газов и паров.
* – при t = 20°C Есть что сказать? Выразите своё мнение к статье! Читайте также:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Любой из материалов, опубликованных на этом сайте, не может быть воспроизведен в какой бы то ни было форме и какими бы то ни было средствами без письменного разрешения владельцев авторских прав. Все статьи имеющиеся на ресурсе размещены с разрешения авторов. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
www.habit.ru
Плотность — кислород — Большая Энциклопедия Нефти и Газа, статья, страница 1
Плотность — кислород
Cтраница 1
Плотность кислорода при температуре 300 К и давлении 1 6 — Ю5 Па равна 2 05 кг / м3; масса кислорода, занимающего при заданных условиях объем 200 0 м3, составляет 410 кг. [1]
Плотность кислорода при температуре 27 С и давлении 1200 мм рт. ст. равна 2 05 кг / м3; масса 200 лг3 кислорода при этих условиях равна 410 кг. [2]
Плотность кислорода больше потому, что масса молекулы кислорода примерно в 16 раз больше массы молекулы водорода. [3]
Здесь плотность кислорода определена при средней его температуре а экономайзерном участке, ориентировочно принятой f эк 94 2 К. [4]
Из этого графика видно, что плотность кислорода уменьшается вдвое на высоте z да 5 км, тогда как плотность водорода становится вдвое меньше на высоте 2 80 км; для гелия такая высота г равна 40 км. [5]
Более точные определения, основанные на данных измерения плотности кислорода при низком давлении, когда по своим свойствам он приближается к идеальному газу, позволили получить значение 22 4140 л для молярного объема газа. [6]
Во сколько раз отличается плотность метана ( СН4) от плотности кислорода ( 02) при одинаковых условиях. [7]
Па — давление газа, р01 43 кг / мэ — плотность кислорода при нормальных условиях, р0 1 013 — 105 Па — нормальное атмосферное давление, ц32 — 10 — 3 кг / моль — молярная масса кислорода, 8 314 Дж / ( моль — К) — молярная газовая постоянная. [8]
На глубине Нл от поверхности пластины ( см. рис. 14) плотность распределенного кислорода примерно вдвое меньше плотности, соответствующей стехиометрическому соотношению. [9]
Плотность смеси оксидов углерода ( II) и ( IV) равна плотности кислорода. [10]
Далее, из графика видно, что при подъеме на одну и ту же высоту плотность кислорода убывает гораздо быстрее, чем плотность более легких газов. [11]
Найдите в периодической таблице элемент, образующий газообразное водородное соединение, плотность которого почти равна плотности кислорода. [12]
На рис. 14 представлены кривые распределения средней плотности пропитанного жидким кислородом пенополистирола рр по толщине пластины и плотности распределенного кислорода р при пропитке с одной стороны в зависимости от расстояния Н до поверхности пластины. [14]
Какой объем озона следует добавить к 1 л воздуха, чтобы получить газовую смесь, плотность которой равна плотности кислорода при той же температуре. [15]
Страницы: 1 2 3
www.ngpedia.ru
Плотность — кислород — Большая Энциклопедия Нефти и Газа, статья, страница 2
Плотность — кислород
Cтраница 2
Какой объем озона следует добавить к 1 л воздуха, чтобы получить газовую смесь, плотность которой равна плотности кислорода при той же температуре. [16]
Для отделения азота от кислорода нельзя воспользоваться различием в плотностях обоих газов, потому что они очень близки: плотность кислорода в 16, азота в 14 раз более плотности водорода, а потому здесь нельзя употребить пористых сосудов; разность во времени просачивания для обоих газов будет ничтожною. [17]
К — температура газа, / 71 6 — 105 н / м2 — давление газа, ро1 43 кг / м3 — плотность кислорода при нормальных условиях, ро 1 013 — 105 н / м2 — нормальное атмосферное давление, i 32 кг / кмоль — масса киломоля кислорода, R 8314 дж / кмоль-град — универсальная газовая постоянная. [18]
Статья Рэлея, написанная в марте 1893 г. [18], свидетельствует о новом подходе к исследованию плотности газа, а именно вместо измерений отношения плотностей кислорода и водорода на первый план выступило измерение отношения плотностей кислорода и азота. [19]
Далее, Беккером, применившим для исследования эмиссионный микроскоп-проектор [18], было опубликовано доказательство существования на поверхности вольфрама адсорбционных центров двух видов, различающихся по плотности кислорода. Эти два вида центров характеризуются различными энергиями связи, причем одна из них соответствует теплоте адсорбции 4 эв, а вторая — 2 эв. Подобное доказательство можно вывести из данных по адсорбции азота, полученных Гринхальфом и сотрудниками [19], которые показали, что на некоторых металлах наблюдается необратимый и обратимый тип хемосорб-ции, особенности которой зависят от рода металла и адсорбата. По-видимому, скорости физической адсорбции на адсорбционных центрах обоих видов одинаковы, а скорости перехода в хемосорбированное состояние различны. Этим обусловливается наблюдаемое быстрое и медленное поглощение. [20]
Дано: У 200 0 м8 — объем газа, Г300 К — температура газа, р1 6 105 Па — давление газа, р01 43 кг / м3 — плотность кислорода при нормальных условиях, р0 1 013 — 105 Па — нормальное атмосферное давление, М 32 — 10 3 кг / моль — молярная масса кислорода, R 8 314 Дж / ( моль — К) — газовая постоянная. [21]
Дано: У200 0м3 — объем газа, Г300 К — температура газа, р1, 6 — 105 Па — давление газа, р 1 43 кг / м3 — плотность кислорода при нормальных условиях, р0 1 013 — 105 Па — нормальное атмосферное давление, р32 — 10 3 кг / моль — молярная масса кислорода, 8 314 Дж / ( моль — К) — молярная газовая постоянная. [22]
Дано: V200 0 м3 — объем газа, Г300 К — температура газа, р1 6 — 105 Па — давление газа, р 1 43 кг / м3 — плотность кислорода при нормальных условиях, рв1 013 — 105 Па — нормальное атмосферное давление, ц32 — 10 — 3 кг / моль — молярная масса кислорода, Я8 314 Дж / ( моль — К) — молярная газовая постоянная. [23]
Статья Рэлея, написанная в марте 1893 г. [18], свидетельствует о новом подходе к исследованию плотности газа, а именно вместо измерений отношения плотностей кислорода и водорода на первый план выступило измерение отношения плотностей кислорода и азота. [24]
Дано: V-50 л5 0 — 10-а м — 8 — объем выделенного кислорода, Т300 К — температура кислорода, р0Ю1 3 кПа — нормальное атмосферное давление, р01 43 кг / м3 — плотность кислорода при нормальных условиях, 8 29 — 10 — 8 кг / Кл — электрохимический эквивалент кислорода. [25]
Дано: V5 л5 — 10 — 3 м — 3 — объем выделенного кислорода, Т300 К — температура кислорода, ра 101 3 кПа — нормальное атмосферное давление, р01 43 кг / м3 — плотность кислорода при нормальных условиях, / г — 8 29 X X 10 — 8 кг / Кл — электрохимический эквивалент кислорода. [26]
Дано: V 5 0 л — 5 0 — 10 — 3 м — объем выделенного кислорода, / 27 С; Т 300 К — температура кислорода, ро 760 мм рт. ст. — нормальное атмосферное давление, ро 1 43 кг / л3 — плотность кислорода при нормальных условиях, Дг 8 29 — 10 — кг / к — электрохимический эквивалент кислорода. [27]
При температуре 20 С в одном литре воды растворяется 28 см3 кислорода. Какова плотность кислорода в воде, свободная поверхность которой граничит с атмосферным воздухом, при нормальном давлении. Принять, что масса кислорода составляет 23 % массы воздуха. [28]
Кислород ( как и любой из газов) в зависимости от условий может находиться в газообразном, жидком или твердом состоянии. В каком из состояний плотность кислорода наибольшая; наименьшая. [29]
Одновременно он указал на возможность использования ее для установления атомного состава сложных газообразных веществ и дал новый метод определения атомных и молекулярных весов: Исходя из этой гипотезы, видно, что мы имеем средство легко определять относительные массы молекул для тех веществ, которые можно перевести в газообразное состояние, а также относительное число молекул в соединениях, потому что отношения молекулярных масс те же самые, что и отношения плотностей различных газов, при одинаковой температуре и давлении, а относительное число молекул в соединении дано непосредственно отношением объемов тех газов, которые образуют данное соединение. Например, числа 1 10359 и 0 07321 выражают плотности кислорода и водорода, если принять плотность воздуха равной единице; отношение же этих двух чисел показывает, следовательно, отношение между массами двух равных объемов данных газов; это же самое отношение выразит, согласно Предложенной гипотезе, отношение масс их молекул. Так, масса молекулы кислорода будет приблизительно в 15 раз больше массы молекулы водорода [ 20, стр. С другой стороны, так как мы знаем, что отношение объемов водорода и кислорода при образовании воды равняется 2: 1, то отсюда следует, что вода образуется путем соединения одной молекулы кислорода с двумя молекулами водорода. Таким же образом — согласно объемным отношениям, установленным Гей-Люссаком для элементов, составляющих аммиак, окись азота, селитряный газ и азотную кислоту — аммиак должен образовываться путем соединения одной молекулы азота с тремя молекулами водорода, закись азота — из одной молекулы кислорода и двух молекул азота, селитряный газ — из одной молекулы азота и одной молекулы кислорода… [30]
Страницы: 1 2 3
www.ngpedia.ru
Плотность кислорода жидкого — Справочник химика 21
Кислород жидкий — прозрачная легкоподвижная жидкость голубоватого цвета, быстро испаряющаяся при обычных т-рах. Кипит при —183° С имеет плотность 1,13. [c.274]Плотность жидкого кислорода при—183°С 1,14 г/см . Во сколько раз увеличится объем кислорода при переходе его из жидкого в газообразное состояние при нормальных условиях [c.28]
Метод пьезометра постоянного объема был использован при исследовании плотности жидкого кислорода при низких температурах [17]. Количество вещества, выпускаемого из пьезометра, измерялось в специальном термостатированном устройстве (газометре) следующим образом. Предварительно точно устанавливался объем газометра. Измерялось давление кислорода, заполнившего газометр. После установления равновесия массу вещества в газометре определяли по известной плотности кислорода при низком давлении и температуре термостата. [c.438]
Озон — один из наиболее сильных окислителей. Он является аллотропическим видоизменением кислорода. Молекула его содержит три атома кислорода. Жидкий озон имеет темно-синий цвет, кипит при температуре —112 и замерзает при температуре —251° С, плотность его равна 1,46. [c.125]
Для выявления условий накопления опасных примесей В воздухоразделительных аппаратах немаловажную роль играют данные по их плотности в жидком кислороде. [c.95]
Так, плотность кислорода в жидком состоянии при температуре кипения равна 1,14, а жидкого фтора — 1,51. Этим отчасти и объясняется большая эффективность фтора как окислителя по сравнению с кислородом. [c.225]Помимо удельной тяги, на скорость и дальность полета ракеты в значительной степени влияет плотность топлива, определяющаяся плотностью его компонентов. Плотность фтора в жидком состоянии при температуре кипения 1,51, а соответствующая плотность кислорода 1,14. Этим отчасти объясняется большая эффективность фтора как окислителя по сравнению с кислородом. [c.36]
Эти свойства кислорода требуют применения специальных материалов для изготовления сосудов, трубопроводов, арматуры и деталей, соприкасающихся с кислородом. Кроме того, при работе с жидким и газообразным кислородом в помещениях, в которых производится, хранится и газифицируется кислород, а также там, где проходят кислородопроводы, требуется соблюдать специальные меры предосторожности. Следует иметь в виду во всех случаях, что плотность кислорода больше, чем воздуха (плотность кислорода по отношению к воздуху составляет 1,1). При утечках кислород вытесняет воздух и смешивается с ним, создавая опасность взрыва, особенно в нижней части помещений, в траншеях и углублениях, где может оставаться долгое время. [c.369]
На рис. 14 представлены кривые распределения средней плотности пропитанного жидким кислородом [c.33]
Кремнийорганическими соединениями называют большую группу веществ, представляющих собой соединения кремния с водородом или кислородом и различными органическими радикалами. Кремнийорганические соединения являются продуктами различной плотности —от жидких до твердых. Высокомолекулярные кремнийорганические соединения, содержащие кислород, обладают каучукоподобными свойствами. Их называют силиконами. Силиконы отличаются своей исключительной теплостойкостью. [c.238]
Этот же метод позволяет проверить, в какой степени различные исследуемые парафиновые углеводороды — метан, этан, пропан и бутан — смешиваются между собой в пределах изучаемой температуры. Из соображений удобства опыты проводились при температуре кипения сжиженного кислорода (—183° С) и сжиженного метана (—161° С). Чистота всех изучаемых газов находилась в пределах 99—99,9%. Полученные значения плотности наносились на график (рис. 10), где одновременно представлены взятые из литературы плотности в жидком состоянии чистых метана, этана, пропана и бутана при различных температурах. Плотность чистого бутана, [c.44]
Плотность растворов кислорода во фторе найдена при допущении, что растворы являются идеальными. При этом плотность жидкого фтора принята согласно работе Джерри и Миллера [47], а плотность кислорода взята из справочника Варгафтика [14]. [c.20]
На рис. V. 9 показан общий вид контактного трехзажимного (трехэлектродного) коаксиального преобразователя для опреде-j ления диэлектрической проницаемости криогенных жидкостей и газов в широком диапазоне температур и давлений [137] на осно- вании отношения измеренной емкости преобразователя с веществом к емкости с вакуумом (и
www.chem21.info
Плотность газов и паров: таблица при различных температурах
Плотность газов и паров при нормальных условиях
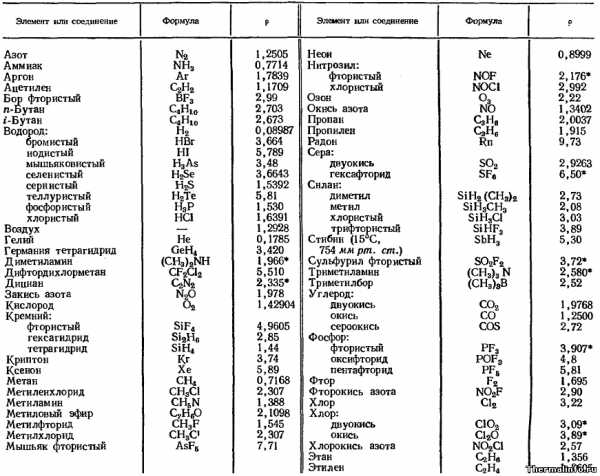
В таблице приведена плотность газов и паров при нормальных условиях – температуре 0°С и нормальном атмосферном давлении (760 мм. рт. ст.). Для некоторых газов, например газа стибина, плотность дана при температуре 15°С и давлении 754 мм. рт. ст.
Значение плотности газов в таблице указано в размерности кг/м3 для следующих газов и паров: азот N2, аммиак NH3, аргон Ar, ацетилен C2H2, бор фтористый BF3, бутан C4H10, водород: бромистый HBr, йодистый HI, мышьяковистый H3As, селенистый H2Se, сернистый H2S, теллуристый H2Te, фосфористый H3P, хлористый HCl, воздух, гелий He, германия тетрагидрид GeH4, диметиламин (CH3)2NH, дифтордихлорметан CF2Cl2, дициан C2N2, закись азота N2O, кислород O2, кремний фтористый SiF4, гексагидрид Si2H6, тетрагидрид SiH4, криптон Kr, ксенон Xe, метан CH4, метиленхлорид CH3Cl, метиламин CH5N, метиловый эфир C2H6O, метилфторид CH3F, метилхлорид CH3Cl, мышьяк фтористый AsF5, неон Ne, нитрозил фтористый NOF и хлористый NOCl, озон O3, окись азота NO, пропан C3H8, пропилен C3H6, радон Rn, двуокись серы SO2 и гексафторид серы SF2, силан диметил SiH2(CH3)2, метил SiH3CH3, хлористый SIH3Cl, трифтористый SiHF3, стибин SbH3, сульфурил фтористый SO2F2, триметиламин (CH3)3N, триметилбор (CH3)3B, двуокись углерода CO2, окись углерода CO, сероокись COS, фосфор фтористый PF2, оксифторид POF3, пентафторид PF5, фтор F2, фторокись азота NO2, двуокись хлора ClO2, окись хлора Cl2O, хлорокись азота NO2Cl, этан C2H6, этилен C2H4, окись азота NO.
Плотность газов вычисляется, как отношение молярной массы газа к его молярному объему, который при 0°С и давлении 1 атм. равен 22,4 л/моль.
Следует отметить, что самым легким газом является водород — плотность этого газа при нормальных условиях равна 0,0899 кг/м3. Для удобства восприятия плотность газов приводят именно к плотности водорода, используя при этом относительную плотность по водороду. Например, относительная плотность газа азота N2 по водороду равна 13,9.
Наибольшую плотность имеет газ радон. Этот радиоактивный газ имеет плотность при нормальных условиях 9,73 кг/м3, а его относительная плотность по водороду составляет величину 108,2.
Необходимо отметить, что при увеличении давления газов и паров, их плотность увеличивается пропорционально.
Примечание: Для газов и паров, рядом со значением плотности которых, присутствует символ *, ее величина в таблице приведена при температуре 20°С.
Из анализа данных, представленных в таблице, видно, что плотность рассмотренных газов находится в диапазоне от 0,089 до 9,73 кг/м3.
Плотность газов в жидком и твердом состояниях при различных температурах
Значения плотности газов и паров в жидком и твердом состояниях приведены в таблице в зависимости от температуры при нормальном атмосферном давлении. Величина плотности газов указана в основном при низких температурах (в интервале от -268 до 20°С), при которых они находятся в жидком, или твердом состояниях.
При низких температурах плотность некоторых газов сравнима с плотностью металлов. К плотным (тяжелым) газам в жидком состоянии можно отнести такие газы, как этилен, криптон (плотность 2371 кг/м3) и ксенон (плотность 3060 кг/м3). Например, плотность газа этилена при температуре -102°С имеет значение 5566 кг/м3, что почти в полтора раза больше плотности алюминия. При этом этилен находится в жидком состоянии.
Газы в твердом состоянии имеют плотность немногим больше, чем в жидком. Твердое состояние газа достигается при более низкой температуре.
Например, углекислый газ находится в виде жидкости при температуре -60°С (при атмосферном давлении), но уже при -79°С становиться твердым и имеет плотность 1530 кг/м3.
Плотность газов в таблице дана в т/м3и приведена для следующих газов: азот N2, окись азота NO, аммиак NH3, аргон Ar, ацетилен C2H2, водород: сернистый H2S, фосфористый H3P, фтористый HF, хлористый HCl, воздух, гелий He, криптон Kr, ксенон Xe, кислород O2, метан CH4, метилхлорид CH3Cl, неон Ne, озон O3, сера двуокись SO2, углерод: двуокись CO2, окись CO, фтор F2, хлор Cl2, этан C2H6, этилен C2H4.
 Источник:
Источник:
Таблицы физических величин. Справочник. Под ред. акад. И.К. Кикоина. М.: Атомиздат, 1976. — 1008 с.
thermalinfo.ru
