теория 2 сем / Tsepochki
ЦЕПОЧКИ
Mn=MnSO4=K2MnO4=MnO2
Mn+h3SO4(разб)=MnSO4+h3
2MnSO4+8h3O+5K2S2O8=(t)=2KMnO4+4K2SO4+8h3SO4
2KMnO4=(t)=K2MnO4+MnO2+O2
3K2MnO4=(t)=2K3MnO4+MnO2+O2
CaCO3=…=CaC2=Ca(OH)2=Ca(ClO)2
CaCO3=(t)=CaO+CO2
CaO+3C=(t)=CaC2+CO
CaC2+2h3O=Ca(OH)2+C2h3
Ca(OH)2+2NaClO(хол)=
Ca(ClO)2+2NaOH
Nh3OH=Nh4OHCl=N2=Nh4=NO
Nh3OH+HCl(конц)=Nh4OHCl
2Nh4OHCl+HClO=N2+3HCl+3h3O
N2+3LiH=Li3N+Nh4
4Nh4+5O2=4NO+6h3O
As2S3=(Nh5)3AsS3=As2S3=Na3AsO3=Na3AsO4
As2S3+6Nh5OH=(Nh5)3AsS3+(Nh5)3AsO3+3h3O
As2S3+6NaOH(конц)=Na3AsO3+Na3[AsS3]+3h3O
Hg=Hg(NO3)2=Hg=Hg2(NO3)2=K2[Hg(CN)4]
Hg+4HNO3(конц)=Hg(NO3)2+2NO2+2h3O
Hg(NO3)2+Hg=Hg2(NO3)2
Hg2(NO3)2+4HNO3(конц)=2Hg(NO3)2+2NO2+2h3O
Hg(NO3)2+4KCN(конц)=K2[Hg(CN)4]+2KNO3
Ca3(PO4)2=P=h4PO4=Na3PO4
2Ca3(PO4)2+10C+6SiO2=6CaSiO3+4P+10CO
P+5HNO3=h4PO4+5NO2+h3O
h4PO4+3NaOH=Na3PO4+3h3O
NaBiO3=Bi(NO3)3=…=Bi2(SO4)3=K3BiO4=K[BiI4]
4Bi(NO3)3=(t)=2Bi2O3+12NO2+3O2
Bi2O3+3h3SO4=Bi2(SO4)3+3h3O
CrO3=K2Cr2O7=Cr2(SO4)3=Cr(OH)3=CrCl2
CrO3+2KOH=K2CrO4+h3O
2K2CrO4+h3SO4(разб)=K2Cr2O7+K2SO4+h3O
KI+K2Cr2O7+7h3SO4=3I2+Cr2(SO4)3+K2SO4+7h3O
Cr2(SO4)3+6NaOH=2Cr(OH)3+3Na2SO4
Cr(OH)3+3HCl=CrCl3+3h3O
2CrCl3=(t)=2CrCl2+Cl2
CO=COCl2=CO2=Na2CO3=(MgOH)2CO3
CO+Cl2=COCl2
COCl2+h3O=CO2+2HCl
CO2+NaOH(конц)=Na2CO3+h3O
Na2CO3(нед)+2Mg(OH)2=(MgOH)2CO3+2NaOH
B=h4BO3=Na2B4O7=B2O3=BCl3
B+3HNO3(конц)=h4BO3+3NO2
4h4BO3+2NaOH=Na2B4O7+7h3O
Na2B4O7+2h3SO4+12C2H5OH=4B(C2H5O)3+2NaHSO4+7h3O
2B(C2H5O)3+18O2=B2O3+12CO2+15h3O
B2O3+3C+3Cl2=2BCl3+3CO
K=KO2=KOH=KClO=KCl
K+O2(изб)=(t)=KO2
4KO2+2h3O=4KOH+3O2
2KOH(конц)+Cl2=KClO+KCl+h3O
3KClO=(t)=2KCl+KClO3
N2O4=HNO3=Nh4=.
CrCl3+Cr=3CrCl2 Al=Na3[Al(OH)6]=NaAlO2=AlCl3=Al(OH)3 2Al+6NaOH+6h3O=2Na3[Al(OH)6]+3h3 Na3[Al(OH)6]=NaAlO2+2NaOH+2h3O NaAlO2+4HCl(конц)=NaCl+AlCl3+2h3O AlCl3+3h3O(гор)=Al(OH)3 h3SeO3=Se=…=h3SeO4=Al2(SeO4)3 h3SeO3+4HCl=Se+2Cl2+3h3O Se+O2=SeO2 SeO2+h3O2=h3SeO4 6h3SeO4+2Au=Au2(SeO4)3+3SeO2+6h3O
Mn=MnSO4=K2MnO4=MnO2
Mn+h3SO4=MnSO4+h3
2MnSO4+8h30+5K2S2O6=2KMnO4+4K2SO4+8h3SO4
2KMnO4+2KOH+K2SO3=2K2MnO4+2K2SO4+h3O
3K2MnO4+4HCl=2KMnO4+MnO2+4KCl+2h3O
S=SO2=SOCl2=BaSO4=BaS
S+O2=SO2(280C)
SO2+CL2=SO2CL2(HU)
SO2Cl2+BaO=BaSO4+BaCl2
BaSO4+4C(кокс)=BaS+4CO(1200C)
Pb2O3=PbO2=Pb(NO3)2PbS=PbSO4
Pb2O3+2HNO3(разб)=Pb(NO3)2+PbO2+h3O
PbO2+2HNO3(р)+h3O2(к)=Pb(NO3)2+O2+2h3O
Pb(NO3)2+Na2S=PbS+2NaNO3
PbS+4h3SO4(к)=PbSO4+4SO2+4h3O
NaCl=NaOH=Na=NaH=NaCl
2NaCl+h3O=h3+Cl2+2NaOH(DC)
4NaOH=4Na+O2+2h3O(DC)
2Na+h3=2NaH(400C)
NaH+HCl=NaCL+h3
SiO2=Si=Sih5=Na2SiO3=h3SiO3
SiO2+2Mg=2MgO+SI(800C)
Si+2Mg=Mg2Si
Mg2SI+4HCL=Sih5+2MgCl2
SIh5+4NaOH
Na4SIO4+4h3
Na4SIO4=Na2SiO3+Na2O(>1200C)
NaSiO3+h3O(пар)=2NaOH+h3SiO3
Sn=SnO2=.
Соседние файлы в папке теория 2 сем
- #
12.10.201959.39 Кб4Schelochnye_metally_teoria.doc
- #
12.10.2019138.79 Кб7Svoystva_elementov.docx
- #
12.10.201936.86 Кб5S_Se_Te.doc
- #
12.
 10.2019343.55 Кб6Teoria (1).doc
10.2019343.55 Кб6Teoria (1).doc - #
12.10.201923.55 Кб3Tsarskaya_vodka.doc
- #
12.10.201916.8 Кб7Tsepochki.docx
- #
12.10.201973.73 Кб7Tsepochki_i_reaktsii_po_biletam.doc
- #
12.10.201958.43 Кб8Tsepochki_reaktsii_i_zadachki_po_biletam.docx
- #
12.10.201939.42 Кб6Zn_Kd_Hg.doc
Онлайн-конвертеры, калькуляторы и учебные пособия
EndMemo — Онлайн-конвертеры, калькуляторы и учебные пособияФизика
- Об/мин Линейная
- Удельная теплоемкость
- Закон охлаждения
- Закон Кулона
- Закон Ома
- Снеллс
- Сопротивление
- подробнее …
- Моль в Грамм
- Имя Формула Поиск
- РН+
- Молярность
- Балансир
- Молярная масса
- Периодическая таблица
- подробнее .
 ..
..
Преобразование единиц измерения
- Удельная теплоемкость
- Концентрация
- Длина
- Энергия
- Масса
- Объем
- Индуктивность
- Номер
- Скорость
- подробнее …
Медицина, здоровье
- Группа крови
- Преобразователи медицинских блоков
- ИМТ
- Беременность
- Осмоляльность сыворотки
- БАК
- Пищевые продукты питания
- подробнее …
Геометрия
- Парабола
- Гипербола
- Треугольник
- Изотреугольник
- Эллипс
- Цилиндр
- Трапеция
- Прямоугольник
- Круг
- подробнее …
Биология
- Г об/мин
- Разбавление
- Номер копии ДНК
- ОД260
- ОД280
- ГК%
- Нарисовать GC
- Молярность ДНК/РНК
- подробнее .
 ..
..
Учебники по программированию
- R
- Джаваскрипт
- HTML
- Питон
- PHP
- С#
Словарь и фразы
- Поиск слов
- Словесная подсказка
- Имя Популярность
- Аббревиатура
- Общие слова
- Префиксы
- Имена мальчиков
- Имена девушек
Статистика
- Коэффициент корреляции
- Площадь Чи
- ЮВ, СД
- Медиана
- Пуассон
- Линейная регрессия
- подробнее …
Алгебра
- Пересечения X Y
- Площадь Сум
- Коэффициент экспоненты
- Лог2
- Журнал10
- Лн
- Квадрат
- Квадратный корень
- подробнее …
Тригонометрия
- Синус
- Косинус
- Касательная
- Котангенс
- Гиперболический синус
- Арксинус
- Арккосинус
- подробнее .
 ..
..
Математика
- Правило Крамера
- Матричное умножение
- Комплексный номер
- Абсолютное значение
- Номер сортировки
- Коэффициент
- Случайный порядок
- подробнее …
Популярные
- Акции
- Дюймы в см
- Дюймы в футы и дюймы
- кг фунтов
- торр атм
- мл унций
- млн млрд
- Юникод
- Часовые пояса
- Список сайтов
- Участок
Кислоты и основания Аррениуса – Введение в химию – 1-е канадское издание
Глава 12. Кислоты и основания
- Определите кислоту Аррениуса и основание Аррениуса.
- Напишите химическую реакцию между кислотой Аррениуса и основанием Аррениуса.
Исторически сложилось так, что первое химическое определение кислоты и основания было предложено шведским химиком Сванте Аррениусом в 1884 году.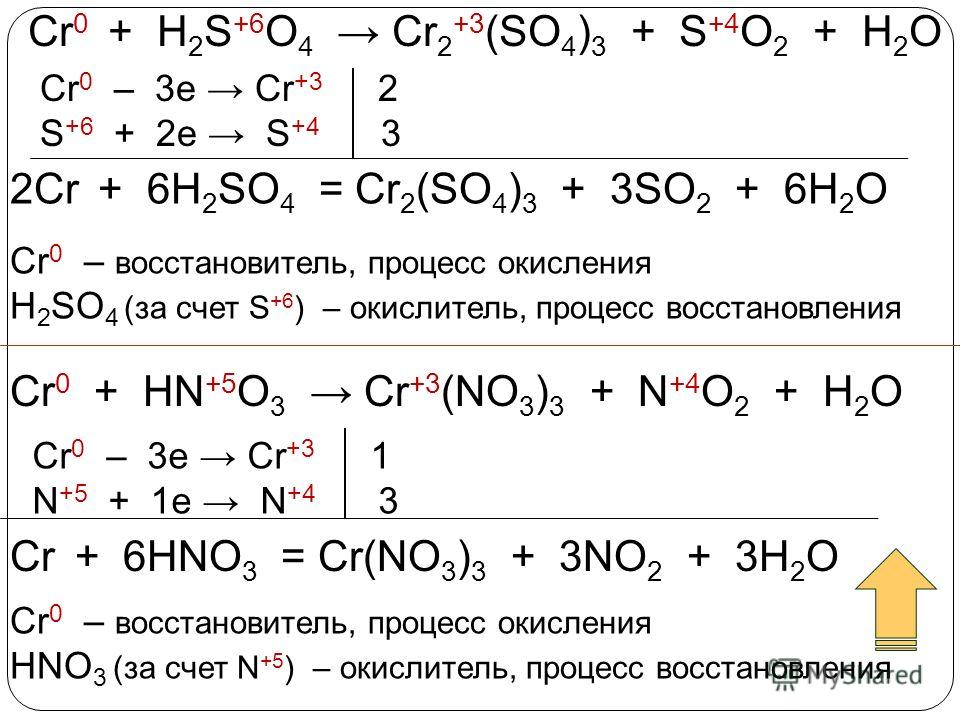 Ион H +
Ион H +
| Формула | Имя |
|---|---|
| HC 2 H 3 O 2 (также пишется CH 3 COOH) | уксусная кислота |
| HClO 3 | хлористоводородная кислота |
| HCl | соляная кислота |
| HBr | бромистоводородная кислота |
| Привет | иодистоводородная кислота |
| ВЧ | фтористоводородная кислота |
| HNO 3 | азотная кислота |
| Н 2 С 2 О 4 | щавелевая кислота |
| HClO 4 | хлорная кислота |
| Н 3 Заказ на покупку 4 | фосфорная кислота |
| Н 2 SO 4 | серная кислота |
| Н 2 SO 3 | сернистая кислота |
Основание Аррениуса представляет собой соединение, которое увеличивает концентрацию ионов ОН  Ионные соединения иона ОН — являются классическими основаниями Аррениуса.
Ионные соединения иона ОН — являются классическими основаниями Аррениуса.
Идентифицируйте каждое соединение как кислоту Аррениуса, основание Аррениуса или ни то, ни другое.
- HNO 3
- CH 3 ОН
- Мг(ОН) 2
Раствор
- Это соединение представляет собой ионное соединение между ионами H + и ионами NO 3 − , поэтому это кислота Аррениуса.
- Хотя в этой формуле есть ОН, мы не признаем оставшуюся часть молекулы катионом. Это не кислота и не основание. (На самом деле это формула метанола, органического соединения.)
- В этой формуле также есть OH, но на этот раз мы признаем, что магний присутствует в виде Mg 9.0315 2+ катионы. Таким образом, это ионное соединение иона OH — и основание Аррениуса.
Проверьте себя
Идентифицируйте каждое соединение как кислоту Аррениуса, основание Аррениуса или ни то, ни другое.
- КОН
- H 2 SO 4
- С 2 Н 6
Ответ
- База Аррениуса
- Кислота Аррениуса
- ни
Кислоты имеют некоторые общие свойства. Они окрашивают лакмус, растительный экстракт, в красный цвет. Они реагируют с некоторыми металлами с выделением газа H 2 . Они реагируют с карбонатными и гидрокарбонатными солями с выделением газа CO 2 . Кислоты, которые попадают внутрь, обычно имеют кислый, острый вкус. (Название кислота происходит от латинского слова acidus , означающего «кислый».) Основания также имеют некоторые общие свойства. Они скользкие на ощупь, окрашиваются лакмусом в синий цвет и имеют горький вкус при попадании внутрь.
Кислоты и основания обладают еще одним свойством: они реагируют друг с другом, образуя воду и ионное соединение, называемое солью. Соль в химии представляет собой любое ионное соединение, полученное путем объединения кислоты с основанием. Реакция между кислотой и основанием называется реакцией нейтрализации и может быть представлена следующим образом:
Реакция между кислотой и основанием называется реакцией нейтрализации и может быть представлена следующим образом:
кислота + основание → H 2 O + соль
Стехиометрия сбалансированного химического уравнения зависит от количества H + ионов в кислоте и количество ионов ОН − в основании.
Напишите сбалансированное химическое уравнение реакции нейтрализации H 2 SO 4 и KOH. Как называется образовавшаяся соль?
Раствор
Общая реакция выглядит следующим образом:
H 2 SO 4 + KOH → H 2 O + соль
Поскольку в формуле кислоты два иона H + нужно два ОН − ионов реагировать с ним, образуя две молекулы H 2 O в качестве продукта. Остальные ионы, K + и SO 4 2– , образуют соль сульфата калия (K 2 SO 4 ). Сбалансированная химическая реакция выглядит следующим образом:
H 2 SO 4 + 2KOH → 2H 2 O + K 2 SO 4
- Напишите уравнение химической нейтрализации реакция между HCl и Mg(OH) 2 .
- Кислота Аррениуса представляет собой соединение, которое увеличивает концентрацию ионов H + в водном растворе.
- Основание Аррениуса представляет собой соединение, которое увеличивает концентрацию ионов OH − в водном растворе.
- Реакция между кислотой Аррениуса и основанием Аррениуса называется нейтрализацией и приводит к образованию воды и соли.
- Дайте определение Кислота Аррениуса .
- Определить Основание Аррениуса .
- Каковы некоторые общие свойства кислот Аррениуса?
- Каковы некоторые общие свойства базисов Аррениуса?
- Идентифицируйте каждое вещество как кислоту Аррениуса, основание Аррениуса или ни то, ни другое.
- NaOH
- С 2 Н 5 ОХ
- Н 3 ПО 4
- Идентифицируйте каждое вещество как кислоту Аррениуса, основание Аррениуса или ни то, ни другое.

- С 6 Н 12 О 6
- HNO 2
- Ба(ОН) 2
- Напишите сбалансированное химическое уравнение реакции нейтрализации KOH и H 2 C 2 O 4 . Что такое соль?
- Напишите сбалансированное химическое уравнение для реакции нейтрализации между Sr(OH) 2 и H 3 PO 4 . Что такое соль?
- Напишите сбалансированное химическое уравнение реакции нейтрализации HCl и Fe(OH) 3 . Что такое соль?
- Напишите сбалансированное химическое уравнение для реакции нейтрализации H 2 SO 4 и Cr(OH) 3 . Что такое соль?
- CaCl 2 будет продуктом реакции какой кислоты и какого основания?
- Zn(NO 3 ) 2 будет продуктом реакции какой кислоты и какого основания?
- BaSO 4 будет продуктом реакции какой кислоты и какого основания?
- Na 3 PO 4 будет продуктом реакции какой кислоты и какого основания?
- Соединение, повышающее концентрацию H + в воде.

 Как называется образовавшаяся соль?
Как называется образовавшаяся соль? Ответ
2HCl + Mg(OH) 2 → 2 H 2 O + MgCl 2 ; хлорид магния

 10.2019343.55 Кб6Teoria (1).doc
10.2019343.55 Кб6Teoria (1).doc ..
.. ..
.. ..
..
