к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.РЕАГИРУЮЩИЕ ВЕЩЕСТВА А) CaO и h3SO4 Б) Ca и h3SO4 (р-р) В) Ca и h3SO4 (конц.) Г) CaO и SO3 ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ 1) CaSO3 2) CaSO4, h3S и h3O 3) CaSO3 и h3O 4) CaSO4 5) CaSO4 и h3 6) CaSO4 и h3O
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.РЕАГИРУЮЩИЕ ВЕЩЕСТВА А) CaO и h3SO4 Б) Ca и h3SO4 (р-р) В) Ca и h3SO4 (конц.) Г) CaO и SO3 ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ 1) CaSO3 2) CaSO4, h3S и h3O 3) CaSO3 и h3O 4) CaSO4 5) CaSO4 и h3 6) CaSO4 и h3OУчебник Курсы Книги Тесты Вопросы Личный кабинет
Учебник Курсы Книги Тесты Вопросы
Личный кабинет
Новогодние скидки 50% на все курсы
Задание ЕГЭ по химии
Наслаждайтесь интересным учебником и решайте десятки тестов на Studarium,
мы всегда рады вам! =)
7910. Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Установите соответствие между реагирующими веществами и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) CaO и H2SO4
Б) Ca и H2SO4 (р-р)
В) Ca и H2SO4 (конц.)
ПРОДУКТЫ ВЗАИМОДЕЙСТВИЯ
1) CaSO3
2) CaSO4, H2S и H2O
3) CaSO3 и H2O
4) CaSO4
5) CaSO4 и H2
6) CaSO4 и H2O
Верный ответ: 6524
P.S. Нашли ошибку в задании? Пожалуйста, сообщите о вашей находке 😉
При обращении указывайте id этого вопроса — 7910.
P. S. Мы нашли статью, которая относится к данной теме, изучите ее — Щелочноземельные металлы 😉
S. Мы нашли статью, которая относится к данной теме, изучите ее — Щелочноземельные металлы 😉
Ответы на итоговую контрольную работу за курс основной школы(Габриелян) решебник
Вариант 1.
ЧАСТЬ А. Тестовые задания с выбором ответа
1. Схема распределения электронов по энергетическим уровням в атоме химического элемента, образующего соединения, соответствующие общим формулам Н2Э и Э03:
В. 2е, 8е, 6е.
2 . Электронное строение иона [+х )]+
соответствует элементу, символ которого:
Б. Н.
3. Ряд элементов, расположенных в порядке увеличения атомных радиусов:
A. S—Р—Si.
4. Термин «молекула» нельзя использовать при характеристике соединения, формула которого:
Б. К20.
5. Оксид углерода (IV) является:
Б. Кислотным.
6. Ряд формул веществ, реагирующих с разбавленной серной кислотой:
Г. Mg, СuО, ВаСl2.
7. Необратимая химическая реакция произойдет при сливании растворов веществ, формулы которых:
В. СuСl2 и КОН.
8. Степень окисления +3 у атома хрома в соединении с формулой:
Б. Сr203.
9. Уравнению реакции 2NO + 02 = 2N02 соответствует схема превращения:
Г. N +2→ N +4.
10. Формула предельного одноатомного спирта:
В. СН40.
ЧАСТЬ Б. Задания со свободным ответом
11. Составьте уравнения химических реакций между веществами, формулы которых:
А. Са и S.
В. СаО и Н20.
Б. Са(ОН)2 и h3S04.
Г. Са и 02.
Ca + S → CaS
Ca(OH)2+ h3SO4 => CaSO4 + 2h3O
СаО + Н2О = Са(ОН)2
2Са+ О2= 2СаО
12. Составьте генетический ряд кальция.
Ca→CaO→Ca(OH)2→CaCl2 →Ca3(PO4)
2Ca+O2=2CaO
CaO+h3O=Ca(OH)2
Ca(OH)2+2HCl=CaCl2+2h3O
3CaCl2+2h4PO4=Ca3(PO4)2+6HCl
13. Составьте молекулярное уравнение реакции, соответствующее схеме
N2 → 2N -3
Разберите его с точки зрения ОВР.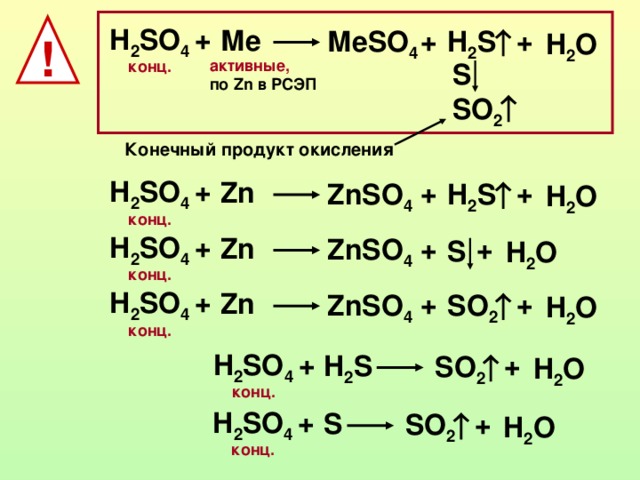
3h30 + N20 = 2N−IIIh4+I
N20 +2*3е→2N-3 окислитель
h30 -2*1е→2H+1 восстановитель
14. По краткому ионному уравнению
Cu2+ + 20Н- = Cu(OH)2 ↓
составьте молекулярное уравнение.
CuCl2 + 2NaOH = Cu(OH)2↓ + 2NaCl
15. Какой объем оксида углерода (IV) образуется при сгорании 11,2 л пропана?
С3Н8 + 5О2 = 4Н2О +3СО2
n(CO2) = 3n(C3H8)
n(C3H8) = 11,2/22,4= 0,5 моль
n(CO2) = 0,5*3= 1,5 моль
V(CO2) = 1,5*22,4 =33,6 л
Вариант 2.
ЧАСТЬ А. Тестовые задания с выбором ответа
1. Схема распределения электронов по энергетическим уровням в атоме химического элемента, образующего соединения, соответствующие общим формулам ЭН2 и ЭО:
В. 2е, 8е, 2е.
2. Электронное строение иона [+х )2)8)8]-
соответствует элементу, символ которого:
Б. Сl.
3. Ряд элементов, расположенных в порядке увеличения атомных радиусов:
Г. Be—Mg—Са.
4. Термин «молекула» нельзя использовать при характеристике соединения, формула которого:
Б. КСl.
КСl.
5. Оксид кальция является:
Г. Основным.
6. Ряд формул веществ, реагирующих с раствором гидроксида натрия:
Г. HCl, Zn(OH)2, C02.
7. Необратимая химическая реакция произойдет при сливании растворов веществ, формулы которых:
Г. КОН и СuСl2.
8. Наивысшая степень окисления у атома хлора в соединении, формула которого:
Г. КСl04.
9. Уравнению реакции
2S02 + 02 = 2S03
соответствует схема превращения:
A. S +4 → S +6.
10. Формула непредельного углеводорода:
Г. С3Нб.
ЧАСТЬ Б. Задания со свободным ответом
11. Составьте уравнения химических реакций между веществами, формулы которых:
A. S03 и Н20.
Б. НСl и Na2S.
В. Na20 и h3S04.
Г. h3S и 02.
SO3+h3O=h3SO4
Na2S + 2HCl = 2NaCl + h3S
Na2O+h3SO4=Na2SO4+h3O
2Н2S + 3O2 = 2SO2 + 2h3O
12. Составьте генетический ряд серы.
S–>SO₂–>H₂SO₃–>Na₂SO₃
S+O₂=SO₂
SO₂+H₂O=H₂SO₃
H₂SO₃+2NaOH=Na₂SO₃+2H₂O
13. Составьте молекулярное уравнение реакции, соответствующее схеме
Составьте молекулярное уравнение реакции, соответствующее схеме
Сu +2→ Сu.
Разберите его с точки зрения ОВР.
CuO + h3 = Cu + h3O
Cu2+ + 2е = Сu0 окислитель
Н02 – 2е = 2Н+ восстановитель
14. По краткому ионному уравнению
СО3 2- + 2Н+ = С02↑ + Н20
составьте молекулярное уравнение.
Na2CO3 + 2HCl → 2NaCl + h3O + CO2↑
15. Какой объем кислорода потребуется для сгорания 10 л этена?
C2h5 + 3O2 → 2CO2 + 2h3O
1 моль этена = 3 моль кислорода
V1/V2 = n1/n2
10 л этена =30 л кислорода
Вариант 3.
ЧАСТЬ А. Тестовые задания с выбором ответа
1. Схема распределения электронов по энергетическим уровням в атоме химического элемента, образующего соединения, соответствующие общим формулам НЭ, Э207:
Б. 2е, 8е, 7е.
2. Электронное строение иона [+х)2)8]2+ соответствует элементу, символ которого:
Б. Mg.
3. Ряд элементов, расположенных в порядке увеличения атомных радиусов:
Б. F—Сl—Вг.
F—Сl—Вг.
4. Термин «молекула» нельзя использовать при характеристике соединения, формула которого:
Г. NaBr.
5. Оксид алюминия является:
А. Амфотерным.
6. Ряд формул веществ, реагирующих с соляной кислотой:
В. Mg, ZnO, NaOH.
7. Необратимая химическая реакция произойдет при сливании растворов веществ, формулы которых:
В. СаСl2 и Na2C03.
8. Степень окисления -3 у атома азота в соединении, формула которого:
Г. Nh4.
9. Уравнению реакции
4Nh4 + 502 = 4N0 + 6Н20
соответствует схема превращения:
Г. N -3 → N +2.
10. Формула предельной одноосновной карбоновой кислоты:
В. С2Н402.
ЧАСТЬ Б. Задания со свободным ответом
11. Составьте уравнения химических реакций между веществами, формулы которых:
A. Fe и НСl.
Б. Fe(OH)3 и НСl.
В. FeCl3 и NaOH.
Г. Fe и Сl2.
Fe+2HCl= FeCl2+h3
Fe(OH)3 + 3HCl = FeCl3 + 3h3O
FeCl3 + 3NaOH = Fe(OH)3 ↓+ 3NaCl
2Fe+3Cl2= 2FeCL3
12. Составьте генетический ряд углерода.
Составьте генетический ряд углерода.
С→СО2→ Н2СО3→ Na2СО3 или СаСО3
C+O2 → CO2
CO2+ h3O→h3CO3
h3CO3+2NaOH→Na2СО3+h3O
CO2 + Ca(OH)2 → CaCO3 + h3O
13. Составьте молекулярное уравнение реакции, соответствующее схеме Р 0 →Р+5.
Разберите его с точки зрения ОВР.
4P + 5O2 = 2P2O5
P0 – 5e=P+5 восстановитель
O20+4e=2O-2 окислитель
14. По краткому ионному уравнению
Аl3+ + ЗОН- = Аl(ОН)3↓
составьте молекулярное уравнение.
AlCl3 + 3NaOH = Al(OH)3 ↓ + 3NaCl
15. Какой объем оксида углерода (IV) образуется при сгорании 16 г метилового спирта?
2Ch4OH +3O2 ->2CO2 +4h3O
2 моль метанола = 2 моль CO2
n (Ch4OH) = 16/32 = 0,5 моль
n (CO2) = 0,5 моль
V(CO2) = 0,5*22,4 = 11,2 л
Вариант 4.
ЧАСТЬ А. Тестовые задания с выбором ответа
1. Схема распределения электронов по энергетическим уровням в атоме химического элемента, образующего соединения, соответствующие общим формулам ЭН, Э20:
А. 2е, 8е, 1е.
2е, 8е, 1е.
2. Электронное строение иона [+х)2)8)8]2- соответствует элементу, символ которого:
В. S.
3. Ряд элементов, расположенных в порядке увеличения атомных радиусов:
Б. N—Р—As.
4. Термин «молекула» нельзя использовать при характеристике соединения, формула которого:
Г. КСl.
5. Оксид углерода (II) является:
В. Несолеобразующим.
6. Ряд формул веществ, реагирующих с раствором гидроксида кальция:
A. h3S04, С02, Na2C03.
7. Необратимая химическая реакция произойдет при сливании растворов веществ, формулы которых:
A. FeS04 и NaOH.
8. Высшая степень окисления серы в соединении, формула которого:
В. Na2S04.
9. Уравнению реакции
N2 + 3Н2 = 2Nh4 соответствует схема превращения:
В. N → N +2.
10. Формула органического соединения, изменяющего окраску лакмуса с фиолетовой на красную:
Б. СН3—СООН.
ЧАСТЬ В. Задания со свободным ответом
11. Составьте уравнения химических реакций между веществами, формулы которых:
Составьте уравнения химических реакций между веществами, формулы которых:
А. Р и 02.
Б. Р205 и Н20.
В. Н3Р04 и Са(ОН)2.
Г. Р и Сl2.
4P + 5O2 = 2P2O5
P2O5 + 3h3O = 2h4PO4
2Н3РО4 + 3Са(ОН) 2 = Са3(РО4)2 + 6Н2О
2P + 3CI2 = 2PCI3
12. Составьте генетический ряд фосфора.
P–Ca3P2–Ph4–P2O5–h4PO4–Na3PO4
1)2P+3Ca=Ca3P2
2)Ca3P2+6HCl=2Ph4+3CaCl2
3) 2Ph4+4O2=P2O5+3h3O
4) P2O5+3h3O=2h4PO4
5) 2h4PO4+6Na=2Na3PO4+3h3
13. Составьте молекулярное уравнение реакции, соответствующее схеме
2Н +1 → Н2.
Разберите его с точки зрения ОВР.
2Н+ + 2е = Н20 окислитель
2O-2 -4e O20 восстановитель
14. По краткому ионному уравнению
Fe3+ + 3ОН- = Fe(OH)3↓
составьте молекулярное уравнение.
FeCl3 + 3NaOH = Fe(OH)3 ↓+ 3NaCl
15. Какой объем воздуха потребуется для полного сгорания 20 л метана?
Ch5 + 2О2 = СО2 + 2Н2О
V1/V2 = n1/n2
n(O2) = 40 л.
40 л кислорода= 21%
Х л воздуха = 100%
V возд.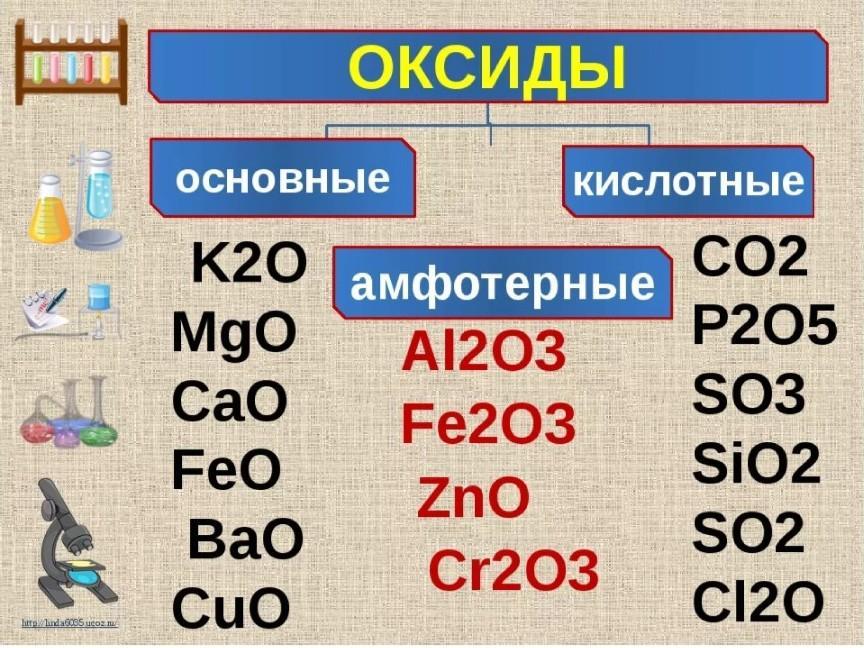 = 40*100/21 = 190,47 л
= 40*100/21 = 190,47 л
Ca(OH)2+h3SO4=>CaSO4+h3O. 100 г серной кислоты реагируют с 78 г гидроксида кальция. Предельный реагент, теоретический выход +% выхода h3O, произведенного реагентом, если фактический выход составляет 34 г h3O?
Химия Стехиометрия Кислотно-основная реакция
Кейтлин М.
спросил 28.05.19Подписаться І 2
Подробнее
Отчет
1 ответ эксперта
Лучший Новейшие Самый старыйАвтор: Лучшие новыеСамые старые
Эллен Э. ответил 28.05.19
Репетитор
4.9 (80)
Репетитор по химии — средняя школа, AP, колледж
См. таких репетиторов
Смотрите таких репетиторов
Всегда, Всегда, ВСЕГДА проверяйте сбалансированность реакции:
Ca(OH) 2 (водн.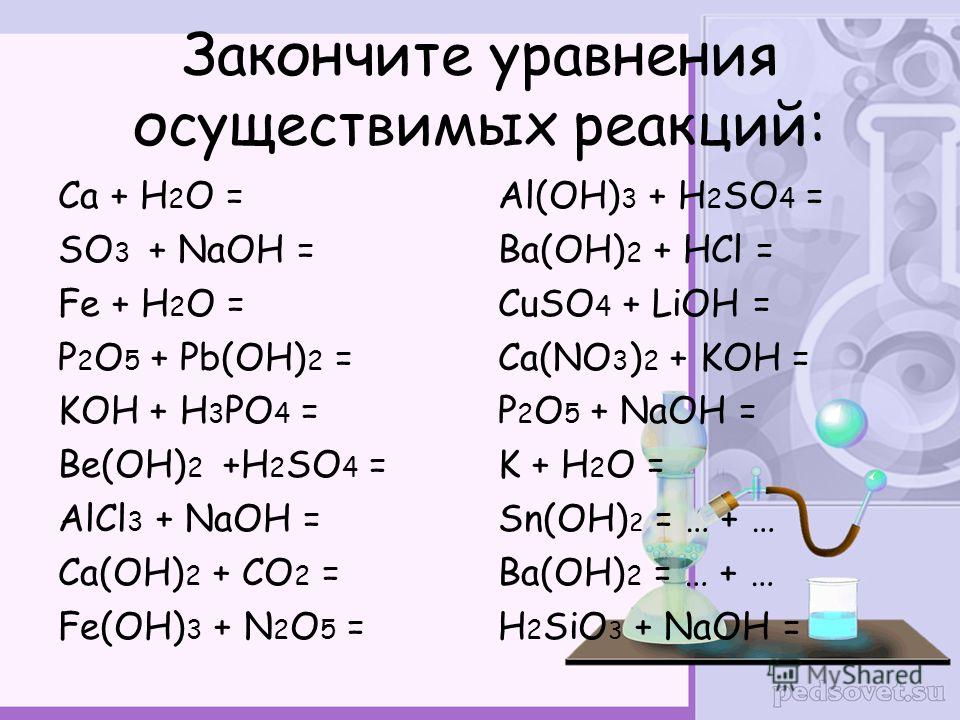 ) + H 2 SO 4 (водн.) à CaSO 4 (водн.) + H 2 O (л)
) + H 2 SO 4 (водн.) à CaSO 4 (водн.) + H 2 O (л)
Это не совсем так!
Сначала сбалансируйте:
Ca(OH) 2
(водн.) + H 2 SO 4 (водн.) à CaSO 4 (водн.) + 2H 2 1)3’00 O (l) O это для балансировки.Теперь вопрос о лимитирующем реагенте….
Я всегда просто спрашиваю себя, сколько продукта я мог бы теоретически произвести из каждого количества реагента. Меньшее число является ОГРАНИЧИВАЮЩИМ реагентом.
Это как если бы у меня был рецепт, который требует 2 стакана муки и 6 яиц. Я смотрю на свою кухню и у меня есть 4 стакана муки и 4 дюжины яиц. У меня муки хватит на 2 раза по рецепту. У меня достаточно яиц, чтобы приготовить рецепт (48/6) 8 раз. Я ОГРАНИЧЕН мукой. Хотя у меня достаточно яиц, чтобы приготовить рецепт 8 раз, муки хватило только на 2 раза.
SO, в данном случае нам дают определенное количество гидроксида кальция и определенное количество серной кислоты:
78 г Ca(OH) 2 x (1 моль / 74,10 г Ca(OH) 2 ] x [2 моль H 2 O/1 моль Ca(OH) 2 ] = 2,105 моль H
100 G H 2 SO 4 X (1 моль / 98,08 г ч 2 SO 4 ] X [2 моль H 2 O / 1 -MOL H 2 SO 5 2 O / 1 -MOL H 2 SO 55 2 O / 1 -MOL H 2 SO 4 ] = 2,039 моль H 2 O
Это близкая гонка, но вы можете сделать немного МЕНЬШЕ H 2 O исходя из количества H 2 SO 4 , чем можно, исходя из количества присутствующего Ca(OH) 2 . То есть Ca(OH) 2 достаточно для получения 2,1 моля H 2 O, но H 2 SO 4 достаточно только для получения 2,04 моля H 2 O.
То есть Ca(OH) 2 достаточно для получения 2,1 моля H 2 O, но H 2 SO 4 достаточно только для получения 2,04 моля H 2 O.
Поэтому выход ОГРАНИЧЕН H 2 SO 4 . H 2 SO 4 – ограничивающий реагент.
Рассчитаем теоретический выход на основе ОГРАНИЧИВАЮЩЕГО РЕАГЕНТА:
Теоретически мы можем получить 2,039 моль H 2 O, что составляет (2,039 * 18,00 г/моль) 36,7 грамма H 2 O.
Не знаю, любит ли ваш учитель значащие числа, но технически у нас есть только 1 значащая цифра, и ответ будет 40 граммов H 2 O.
Кроме того, задача говорит нам, что вы смогли восстановить только 34 грамма H 2 O.
Выход в процентах равен (ФАКТИЧЕСКИЙ УРОЖАЙ/ТЕОРЕТИЧЕСКИЙ УРОЖАЙ) * 100
SO (34/36,7)*100 = 92,6%;
Только с одной значащей цифрой вы технически должны говорить о 90% доходности.
Голосовать за 1 голос против
Подробнее
Отчет
Все еще ищете помощь? Получите правильный ответ, быстро.

Задайте вопрос бесплатно
Получите бесплатный ответ на быстрый вопрос.
Ответы на большинство вопросов в течение 4 часов.
ИЛИ
Найдите онлайн-репетитора сейчас
Выберите эксперта и встретьтесь онлайн. Никаких пакетов или подписок, платите только за то время, которое вам нужно.
CaS + h3SO4 → CaSO4↓ + h3S↑ | CaS ра CaSO4 | CaS ra H3S
- Тайское приложение VietJack. Xem lời giải nhanh hơn!
Trang trước
Trang sau
Phản ứng CaS + H 2 SO 4 hay CaS ra CaSO 4 hoặc CaS ra H 2 S hoặc H 2 SO 4 ra H 2 S thuộc loại phản ứng trao đổi đã được can bằng chính xác và chi tiết nhất.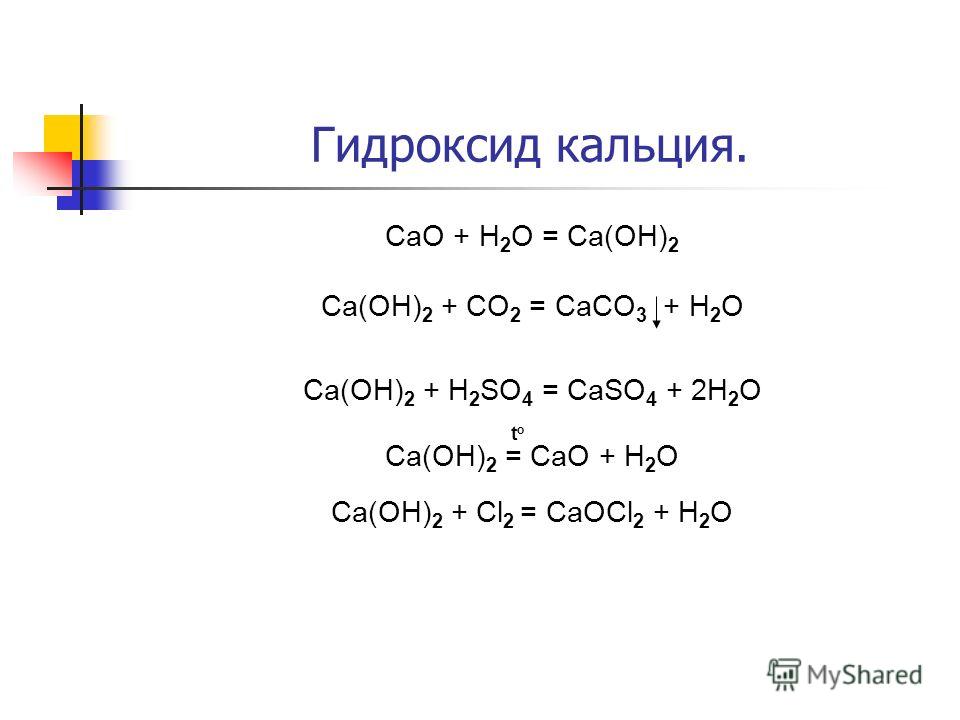
CAS + H 2 SO 4 → Caso 4 + H 4 → Caso 4 + H 40036 → CASO 4 + H → CASO 4 + H → CASO 4 + H → CASO 4 + H .0035 2 S ↑
quảng cáo
điều kiện phản ứng
— Không Có
Cách Thực hiện Phản ứng 9000 2 Cách Thực hiện Phản ứng 9000 2 9000 9000 9000 .
hiện tượng nhận biết phản ứng
— canxi sunfua tan dần trong dung dịch axit sunfuric và sinh ra khí mùi trứng thối hidro sunfua
bại rứng thối hidro
9000 2 bại cóng hidro 9000 2 bại rứng hidro bại rứng hidro Bạ MùI Cóng. 119 2 10 Bạ MùI Cóng Dung Hidro ví dụ 1: ứ -ngyg ngog ngo hr đ đ đ đ đ ng ng ng hr hr. h3O)?
h3O)?
A. Bó bột khi gẫy xương.
Б. Дук Хуон.
C. Thức ăn cho người và động vật.
Д. Нанг Лунг.
Hướng dẫn giải:
Đáp án C
Giai thích
Vì thạn cao khôİng
Quảng cáo
Ví dụ 2: Thành phần hóa học chính của thạch cao là:
A. CaCO3. Б. Са(NO3)2. С. CaSO4. Г. Са3(РО4)2.
Hướng dẫn giải:
Đáp án C
Giới thiệu kênh Youtube VietJack
Ngân hàng trắc nghiệm miễn phí ôn thi THPT Quốc Gia tại
khoahoc.vietjack.com- Hơn 75.000 cau trắc nghiệm Toán có đáp án
- Hơn 50.000 cau trắc nghiệm Hóa có đáp án chi tiet
- Gần 40.000 cau trắc nghiệm Vật lý có đáp án
- Hơn 50.000 cau trắc nghiệm Tiếng Anh có đáp án
- Кхо Трук Нгхим Как Мон Кхак
CHỉ CòN 250K 1 KHOA HọC BấT Kì, Vietjack Hỗ TRợ DịCH COVID
TổNG HợP Các Video Dạy HọC Từ Các giáo Viên giỏ nhất — chỉ học từ 210210210210210210.
