|
Random converter |
Вычисление молярной массыКонвертер длины и расстоянияКонвертер массыКонвертер мер объема сыпучих продуктов и продуктов питанияКонвертер площадиКонвертер объема и единиц измерения в кулинарных рецептахКонвертер температурыКонвертер давления, механического напряжения, модуля ЮнгаКонвертер энергии и работыКонвертер мощностиКонвертер силыКонвертер времениКонвертер линейной скоростиПлоский уголКонвертер тепловой эффективности и топливной экономичностиКонвертер чисел в различных системах счисления.Конвертер единиц измерения количества информацииКурсы валютРазмеры женской одежды и обувиРазмеры мужской одежды и обувиКонвертер угловой скорости и частоты вращенияКонвертер ускоренияКонвертер углового ускоренияКонвертер плотностиКонвертер удельного объемаКонвертер момента инерцииКонвертер момента силыИмпульс (количество движения)Импульс силыКонвертер вращающего моментаКонвертер удельной теплоты сгорания (по массе)Конвертер плотности энергии и удельной теплоты сгорания топлива (по объему)Конвертер разности температурКонвертер коэффициента теплового расширенияКонвертер термического сопротивленияКонвертер удельной теплопроводностиКонвертер удельной теплоёмкостиКонвертер энергетической экспозиции и мощности теплового излученияКонвертер плотности теплового потокаКонвертер коэффициента теплоотдачиКонвертер объёмного расходаКонвертер массового расходаКонвертер молярного расходаКонвертер плотности потока массыКонвертер молярной концентрацииКонвертер массовой концентрации в раствореКонвертер динамической (абсолютной) вязкостиКонвертер кинематической вязкостиКонвертер поверхностного натяженияКонвертер паропроницаемостиКонвертер плотности потока водяного параКонвертер уровня звукаКонвертер чувствительности микрофоновКонвертер уровня звукового давления (SPL)Конвертер уровня звукового давления с возможностью выбора опорного давленияКонвертер яркостиКонвертер силы светаКонвертер освещённостиКонвертер разрешения в компьютерной графикеКонвертер частоты и длины волныОптическая сила в диоптриях и фокусное расстояниеОптическая сила в диоптриях и увеличение линзы (×)Конвертер электрического зарядаКонвертер линейной плотности зарядаКонвертер поверхностной плотности зарядаКонвертер объемной плотности зарядаКонвертер электрического токаКонвертер линейной плотности токаКонвертер поверхностной плотности токаКонвертер напряжённости электрического поляКонвертер электростатического потенциала и напряженияКонвертер электрического сопротивленияКонвертер удельного электрического сопротивленияКонвертер электрической проводимостиКонвертер удельной электрической проводимостиЭлектрическая емкостьКонвертер индуктивностиКонвертер реактивной мощностиКонвертер Американского калибра проводовУровни в dBm (дБм или дБмВт), dBV (дБВ), ваттах и др. Химическая формула Использование калькулятора молярной массы
Уровень звукового давленияЗнаете ли вы почему певцы не используют измерительные микрофоны для студийной записи? Ведь они очень качественные! Всего один щелчок — и вы узнаете почему! Моль Молярная масса Молярная масса элементов и соединений Молекулярная масса Расчет молярной массы МольВсе вещества состоят из атомов и молекул. Постоянная Авогадро NA = 6.02214076×10²³ моль⁻¹. Число Авогадро — 6.02214076×10²³. Другими словами моль — это количество вещества, равное по массе сумме атомных масс атомов и молекул вещества, умноженное на число Авогадро. Единица количества вещества моль является одной из семи основных единиц системы СИ и обозначается моль. Поскольку название единицы и ее условное обозначение совпадают, следует отметить, что условное обозначение не склоняется, в отличие от названия единицы, которую можно склонять по обычным правилам русского языка. Молярная массаМолярная масса — физическое свойство вещества, определяемое как отношение массы этого вещества к количеству вещества в молях. Говоря иначе, это масса одного моля вещества. В системе СИ единицей молярной массы является килограмм/моль (кг/моль). Однако химики привыкли пользоваться более удобной единицей г/моль. молярная масса = г/моль Горение — высокотемпературная экзотермическая окислительно-восстановительная реакция. Молярная масса элементов и соединенийСоединения — вещества, состоящие из различных атомов, которые химически связаны друг с другом. Например, приведенные ниже вещества, которые можно найти на кухне у любой хозяйки, являются химическими соединениями:
Молярная масса химических элементов в граммах на моль численно совпадает с массой атомов элемента, выраженных в атомных единицах массы (или дальтонах). Молекулярная массаМолекулярная масса (старое название — молекулярный вес) — это масса молекулы, рассчитанная как сумма масс каждого атома, входящего в состав молекулы, умноженных на количество атомов в этой молекуле. Молекулярная масса представляет собой безразмерную физическую величину, численно равную молярной массе. То есть, молекулярная масса отличается от молярной массы размерностью. Несмотря на то, что молекулярная масса является безразмерной величиной, она все же имеет величину, называемую атомной единицей массы (а.е.м.) или дальтоном (Да), и приблизительно равную массе одного протона или нейтрона. Атомная единица массы также численно равна 1 г/моль. Расчет молярной массыМолярную массу рассчитывают так:
Например, рассчитаем молярную массу уксусной кислоты CH₃COOH Она состоит из:
Расчет:
Наш калькулятор выполняет именно такой расчет. Можно ввести в него формулу уксусной кислоты и проверить что получится. Автор статьи: Anatoly Zolotkov Вас могут заинтересовать и другие конвертеры из группы «Другие конвертеры»:Конвертер десятичных приставок Передача данных Конвертер единиц типографики и обработки изображений Конвертер единиц измерения объема лесоматериалов Курсы валют Размеры мужской одежды и обуви Размеры женской одежды и обуви Вычисление молярной массы Список соединений Химические соединения по-русски и по-английски Вы затрудняетесь в переводе единицы измерения с одного языка на другой? Коллеги готовы вам помочь. |
Молярная масса вещества — AbakBot-online calculators
| Химическая формула |
| Молярная масса вещества (Грамм/Моль) |
| Формула химического вещества |
Введение в химические формулы
Не секрет , что химические знаки позволяют изобразить состав сложного вещества в виде формул.
Химическая формула — это условная запись состава вещества посредством химических знаков и индексов.
Формулы различают молекулярные, структурные, электронные и другие.
Молекулярные формулы (h4P04, Fe203, А1(ОН)3, Na2S04, 02 и т.д.) показывают качественный (т.е. из каких элементов состоит вещество) и количественный (т.е. сколько атомов каждого элемента имеются в веществе) состав.
Структурные формулы показывают порядок соединения атомов в молекуле, соединяя атомы черточками (одна черточка — одна химическая связь между двумя атомами в молекуле).
Относительная атомная и молекуряная масса
Относительная атомная масса вещестав или элемента — это безразмерная величина. Почему безразмерная, ведь масса должна иметь размерность?
Причина в том что атомная масса вещества в кг очень мала и выражается порядком 10 в минус 27 степени. Что бы в расчетах не учитывать этот показатель, массу каждого элемента привели к отношению 1/12 массы изотопа углерода. По этой причине относительная атомная масса углерода и составляет 12 единиц.
По этой причине относительная атомная масса углерода и составляет 12 единиц.
Современные значения относительных атомных масс приведены в периодической системе элементов Д.И.Менделеева. Для большинства элементов указаны
среднеарифметические значения атомных масс природной смеси изотопов этих элементов.
Например, относительная масса водорода равна 1, а кислорода 16.
Относительная молекулярная масса простых и сложных веществ численно равна сумме относительных атомных масс атомов, входящих в состав молекулы.
Например, относительная молекулярная масса воды , состоящей из двух атомов водорода и одного атома кислорода, равна
1*2+16 =18
Массовая доля элемента. Эта величина выражается в % или долях единицы.
По химической формуле можно вычислить как химический состав, так и молекулярную массу.
Определяемый по химическим формулам количественный состав имеет огромное значение для многочисленных расчетов, которые производятся по химическому составу.
Вычисление относительной молекулярной массы вещества по химической формуле производится путем сложения произведений относительных атомных масс элементов на соответствующие индексы в химической формуле.
Как рассчитывается молекулярная масса вещества мы рассмотрели чуть выше.
И именно эту задачу автоматизирует наш химический калькулятор.
Зная молекулярную массу вещества, нам ничего не стоит рассчитать и молярную массу.
Моль — есть количество вещества системы, содержащей столько же структурных элементов, сколько содержится атомов в углероде-12 массой 12 грамм
Таким образом, молярная масса вещества с точностью соответствует относительной молекулярной массе и имеет размерность грамм/моль
Таким образом молярная масса воды равна 18 грамм/моль.
Молярную массу вещества можно определить как отношение массы данной порции вещества к количеству вещества в этой порции
Отличительные особенности
В отношении других калькуляторов, рассчитывающих молярную массу вещества, этот калькулятор обладает следующими особенностями:
— Формула может содержать скобки например
— Формула может содержать коэффициент
Если есть необходимость рассчета массовых долей каждого химическго элемента в формуле то стоит воспользоваться калькулятором Массовая доля вещества онлайн
Интересные факты
Молярные массы каких химических элементов не округляются?
Логично, предположить если вы прочитали, откуда появляется понятие «относительная масса», что «не округленная» масса будет у одного элемента — углерода.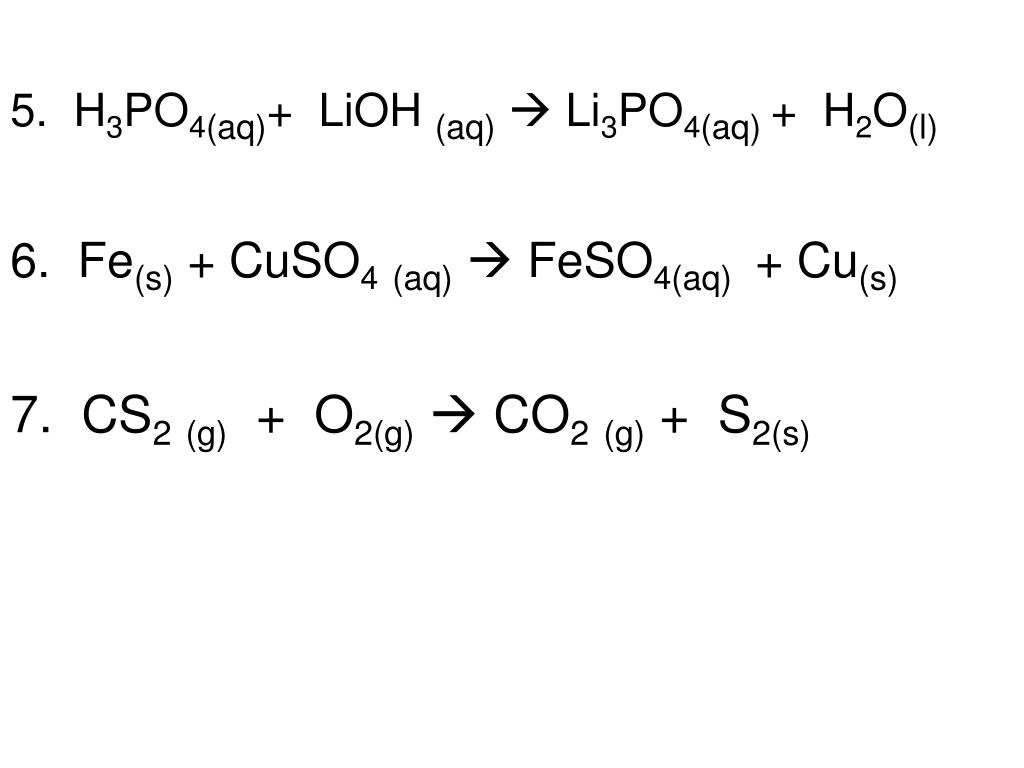 Будут ли встречаться другие химические элементы с «не округленными» массами? Сомневаюсь.
Будут ли встречаться другие химические элементы с «не округленными» массами? Сомневаюсь.
синтаксис
molar формула[!]
где формула — произвольная формула химического вещества.
Внимание! Химические элементы в формуле должны быть указаны так, как в таблице Менделеева.
простой пример покажет какая цена ошибки не соблюдать регистр (прописные или строчные символы) букв
Если напишем CO — то это углерод и кислород, а если напишем Co — то это кобальт.
В любую часть формулы, можно вставить служебный символ(восклицательный знак).
Что же он нам дает?
Он все параметры огругляет до того уровня точности, который используется в школьной программе. Это очень удобно именно для тех, кто решает школьные задачи.
Например молярная масса воды в школьных учебниках равна 18, а если учитывать более точные алгоритмы, то получаем что молярная масса равна 18.01528. Разница небольшая, но если делать расчет например массовой доли химического вещества, получается небольшое, но очень неприятное расхождение в выходных параметрах, которое может ввести в заблуждение неопытных пользователей калькулятора.
Примеры
Рассчитать молярную и молекулярную массу вещества
пишем запрос molar NaMgU3O24C18h37
получаем ответ
| Молярная масса вещества (Грамм/Моль) |
|
1388.80945 |
| Формула химического вещества |
Если же в входных параметрах написать символ- восклицательный знак, то получим такой ответ
Молярная масса вещества равна 1389
Рассчитать молярную массу
Пишем K4[Fe(CN)6]
| Молярная масса вещества (Грамм/Моль) |
|
368.3464 |
| Формула химического вещества |
Узнаем молекулярную, а также молярную массу
В результате запроc выглядит так molar CuSO4*5h3O
И ответ выглядит так
| Молярная масса вещества (Грамм/Моль) |
|
249. |
| Формула химического вещества |
Как уже было сказано в статье выше, молярная масса и молекулярная масса вещества равны друг другу и отличаются лишь тем, что молекулярная масса безразмерная величина, в отличии от молярной массы (грамм/моль)
Удачных Вам расчетов!
Пентагидрат сульфата меди (сульфат меди) [CuSO4.5h3O] [CAS_7758-99 — Wintersun
Пентагидрат сульфата меди (сульфат меди) [CuSO4.5h3O] [CAS_7758-99 – Wintersun- Корзина: 0 шт.
- Авторизоваться или Завести аккаунт
Главная > Продукты >
количество
| Код Wintersun: | 03-030-ОБ |
| Номер CAS: | 7758-99-8 |
| 5H<sub>2</sub>O»> Молекулярная формула: | CuSO 4 .5H 2 O |
| Молекулярный вес: | 249,68 г/моль |
Применение
Промышленное производство, корма для животных, альгициды, фунгициды, гербициды, пестициды.
Спецификация для продажи
- Физическое состояние и внешний вид: Прозрачные голубые кристаллы, гранулы или порошок
- Cu: 24,5% мин.
- Чистота: 98% мин.
- Cd: макс. 20 (частей на миллион)
- Pb: макс. 50 (частей на миллион)
- Как: 20 макс. (стр./млн)
Упаковка
В 50-фунтовом мешке
Транспортировка
- Надлежащее отгрузочное наименование: Вещество, опасное для окружающей среды, твердое, Н.У.К. (сульфат меди)
- № ООН: 3077
- Класс опасности: 9
- Группа упаковки: III
Сопутствующие товары
Распродажа
4-хлор-3,5-диметилфенол (PCMX) [CAS_88-04-0] [C8H9ClO] 98,5% мин.
 белый порошок 55,12 фунта мешок Винтерсан Кемикал
белый порошок 55,12 фунта мешок Винтерсан Кемикал Распродажа
Сульфат алюминия в гранулах [Al2(SO4)3] [CAS_10043-01-3] 99+% белый (2204,6 фунта Super Sack)
Винтерсан Кемикал $ 815.00 РаспроданоРаспродажа
Сульфат алюминия в гранулах [CAS_10043-01-3] [Al2(SO4)3] 99+% белый, мешок 55,12 фунта
Винтерсан КемикалРаспродажа
Порошок сульфата алюминия [10043-01-3 ] [CAS_Al2(SO4)3] 99+% Белый Мешок 55,12 фунта
Винтерсан КемикалРазница между CuSO4 и CuSO4 5h3O
Основное различие между CuSO4 и CuSO4 5h3O заключается в том, что CuSO4 является аморфным, тогда как CuSO4 5h3O является кристаллическим.
CuSO4 — это химическая формула сульфата меди (II), а CuSO4 5h3O — это гидратированная форма сульфата меди (II). Термин «гидратированный» указывает на то, что это соединение имеет одну или несколько связанных с ним молекул воды. Поэтому CuSO4 — обычное название безводной формы.
СОДЕРЖАНИЕ
1. Обзор и ключевые отличия
2. Что такое CuSO4
3. Что такое CuSO4 5h3O
4. Сравнение бок о бок – CuSO4 и CuSO4 5h3O в табличной форме
5. Резюме
Что такое CuSO4?
CuSO4 представляет собой сульфат меди (II), который имеет металлическую медь в степени окисления +2. Это неорганическое соединение, с которым не связаны молекулы воды. Поэтому мы называем его безводной формой сульфата меди. Более того, это безводное соединение встречается в виде белого порошка.
Промышленное производство сульфата меди включает обработку металлической меди серной кислотой в горячей и концентрированной форме. Кроме того, это соединение можно получить и с использованием оксидов меди. Здесь это делается путем обработки оксида меди разбавленной серной кислотой. Кроме того, еще одним методом производства является медленное выщелачивание низкосортной медной руды на воздухе. Можно использовать бактерии для катализа этого процесса.
Здесь это делается путем обработки оксида меди разбавленной серной кислотой. Кроме того, еще одним методом производства является медленное выщелачивание низкосортной медной руды на воздухе. Можно использовать бактерии для катализа этого процесса.
Рисунок 02: Сульфат меди безводный
При рассмотрении химических свойств этого соединения молярная масса составляет 159,6 г/моль. Он появляется в серо-белом цвете. Плотность 3,60 г/см3. При рассмотрении температуры плавления сульфата меди она составляет 110 °С, при дальнейшем нагревании соединение разлагается.
Что такое CuSO4 5h3O?
CuSO4 5h3O – пентагидрат сульфата меди(II). Он имеет пять молекул воды, связанных с молекулой сульфата меди. Он выглядит как твердое вещество ярко-синего цвета. Кроме того, это наиболее распространенная гидратированная форма сульфата меди. Кроме того, некоторые распространенные названия этого соединения: медный купорос, медный купорос, медный купорос, римский купорос и т. д.
д.
Рисунок 02: Внешний вид пентагидрата сульфата меди
Кроме того, это соединение экзотермически растворяется в воде. Затем он образует аквакомплекс, содержащий одну молекулу CuSO4 в ассоциации с шестью молекулами воды, и этот комплекс имеет октаэдрическую молекулярную геометрию. Молярная масса его составляет 249,65 г/моль. Что касается температуры плавления, то при нагревании выше 560 °С соединение разлагается. Это значит; соединение разлагается до плавления. Там это соединение удаляет две молекулы воды при 63 °C и еще две при 109 °C.°С. Более того, последняя молекула воды высвобождается при 200 °C.
В чем разница между CuSO4 и CuSO4 5h3O?
CuSO4 представляет собой сульфат меди (II), который имеет металлическую медь в степени окисления +2. CuSO4·5h3O – пентагидрат сульфата меди(II). Основное различие между CuSO4 и CuSO4·5h3O заключается в том, что CuSO4 является аморфным, тогда как CuSO4·5h3O является кристаллическим. Кроме того, сульфат меди является безводным, тогда как пентагидрат сульфата меди представляет собой гидратированную форму.


 В химии важно точно измерять массу веществ, вступающих в реакцию и получающихся в результате нее. По определению моль является единицей количества вещества в СИ. Один моль содержит точно 6,02214076×10²³ элементарных частиц. Это значение численно равно константе Авогадро NA, если выражено в единицах моль⁻¹ и называется числом Авогадро. Количество вещества (символ n) системы является мерой количества структурных элементов. Структурным элементом может быть атом, молекула, ион, электрон или любая частица или группа частиц.
В химии важно точно измерять массу веществ, вступающих в реакцию и получающихся в результате нее. По определению моль является единицей количества вещества в СИ. Один моль содержит точно 6,02214076×10²³ элементарных частиц. Это значение численно равно константе Авогадро NA, если выражено в единицах моль⁻¹ и называется числом Авогадро. Количество вещества (символ n) системы является мерой количества структурных элементов. Структурным элементом может быть атом, молекула, ион, электрон или любая частица или группа частиц. Один моль чистого углерода-12 равен точно 12 г.
Один моль чистого углерода-12 равен точно 12 г. Молярная масса соединений равна сумме молярных масс элементов, из которых состоит соединение, с учетом количества атомов в соединении. Например, молярная масса воды (H₂O) приблизительно равна 1 × 2 + 16 = 18 г/моль.
Молярная масса соединений равна сумме молярных масс элементов, из которых состоит соединение, с учетом количества атомов в соединении. Например, молярная масса воды (H₂O) приблизительно равна 1 × 2 + 16 = 18 г/моль.
 Опубликуйте вопрос в TCTerms и в течение нескольких минут вы получите ответ.
Опубликуйте вопрос в TCTerms и в течение нескольких минут вы получите ответ.
 », то есть «…умножить на десять в степени…». Компьютерная экспоненциальная запись широко используется в научных, математических и инженерных расчетах.
», то есть «…умножить на десять в степени…». Компьютерная экспоненциальная запись широко используется в научных, математических и инженерных расчетах. 68
68