Cl2 Naoh Nacl Naclo3 h3o
Wednesday, September 14, 2022 Add Comment Edit
Balance the equation Cl2 NaOH NaCl NaClO3 h3O using the algebraic method. Reaction of Cl2 clo react with NaOH natri hidroxit produce h3O nước and NaClO3 Natri clorat temperature condition Nhiệt độ.
Sodium Hydroxide And Chlorine Gas Reaction Naoh Cl2
NaOH Cl2 NaClO3 NaCl h3O CUAL ES SU BALANCEO REDOX 1 Ver respuesta 5 Cl0 5 e- 5 Cl-I reducción Cl0 — 5 e- ClV oxidación creo que es asi Publicidad.
. Label each compound reactant or product in the equation with a. CategoriesSwimming Pool Coping Plastering Tiling. Get reviews hours directions coupons and more for Nacl Inc at 115 Silvia St Ewing NJ 08628.
Cl2 naoh h3o nacl naclo3 Chemical Equation Balancer Khớp với kết quả tìm kiếm. 13 Glen Lake Dr Medford NJ 08055. Label Each Compound With a Variable.
The limiting reagent row will be highlighted in pink. Reaction that produces substance Cl2 clo chlorine. A soft silver-white metal A burns with golden yellow flame to give a yellow power B which on treatment with water liberates oxygen giving a clear solution C.
A soft silver-white metal A burns with golden yellow flame to give a yellow power B which on treatment with water liberates oxygen giving a clear solution C.
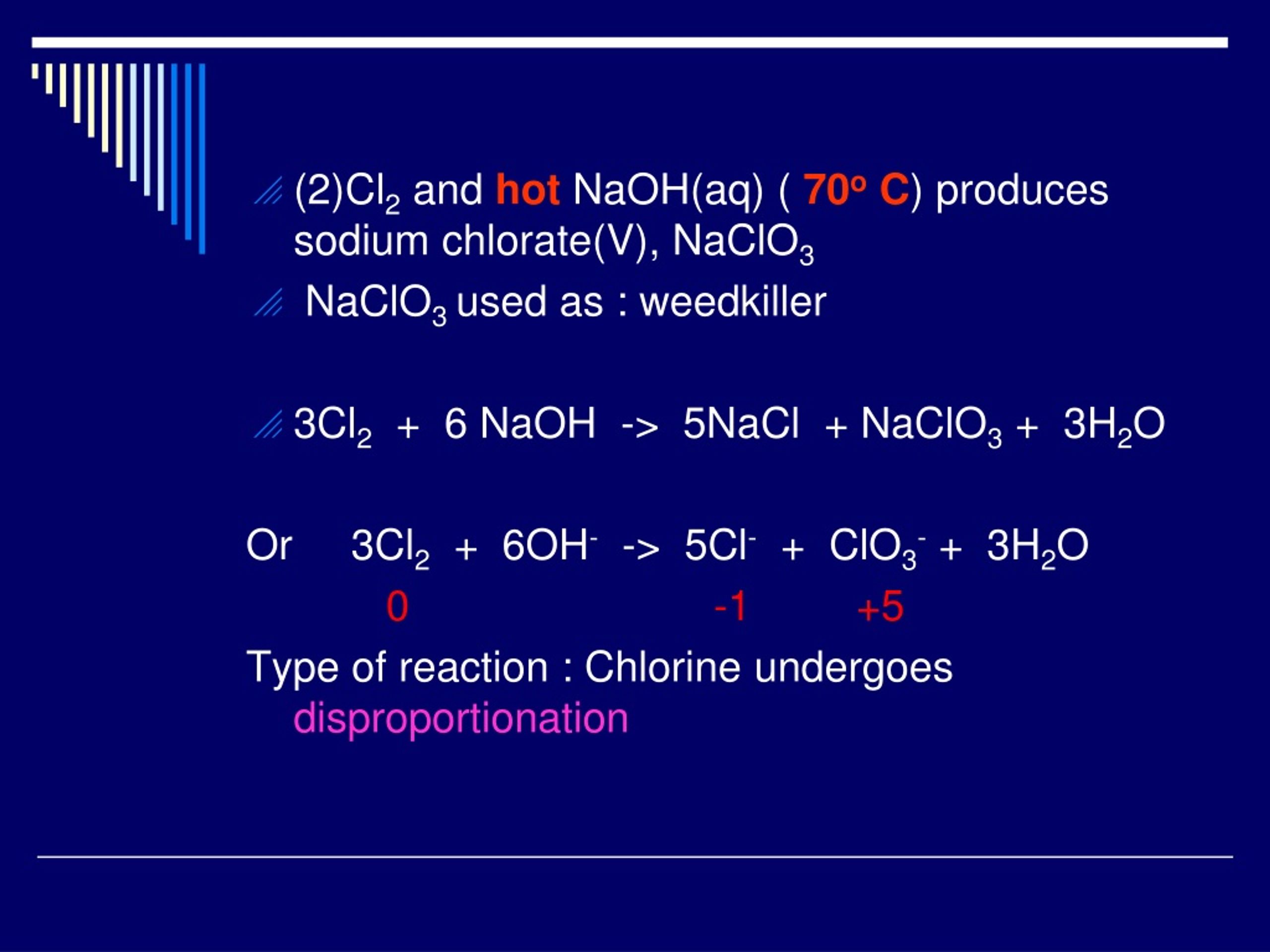
In a full sentence you can also say Cl2 chlorine reacts with NaOH sodium hydroxide and produce h3O water and NaCl sodium chloride and NaClO3 sodium chlorate Phenomenon. 3 Cl2 6 NAOH 5 NACl NAClO3. Click hereto get an answer to your question Balance the following equation.
Every course automatically has a Canvas page to support learning in any mode and to deliver classes that are fully online. See reviews photos directions phone numbers and more for Nacl Inc locations in Piscataway NJ. NaOHCl2NaClNaClOh3O Balanced EquationSodium hydroxideChlorineSodium chloride Sodium hypochloriteWater Balanced Equation How to Balance NaOH Cl2.
Cl2gNaOHaqNaClaqNaClO3aqh3Ol This problem has been solved. Расставьте коэффициенты в уравнениях окислительно-восстановительных реакций. ответ x — неизвестный газ из условия становится понятно что он содержит азот _x_o2 _n2 _h3o 2na 2h3o 2naoh h3 nh3o 003224 2000132000267 мол.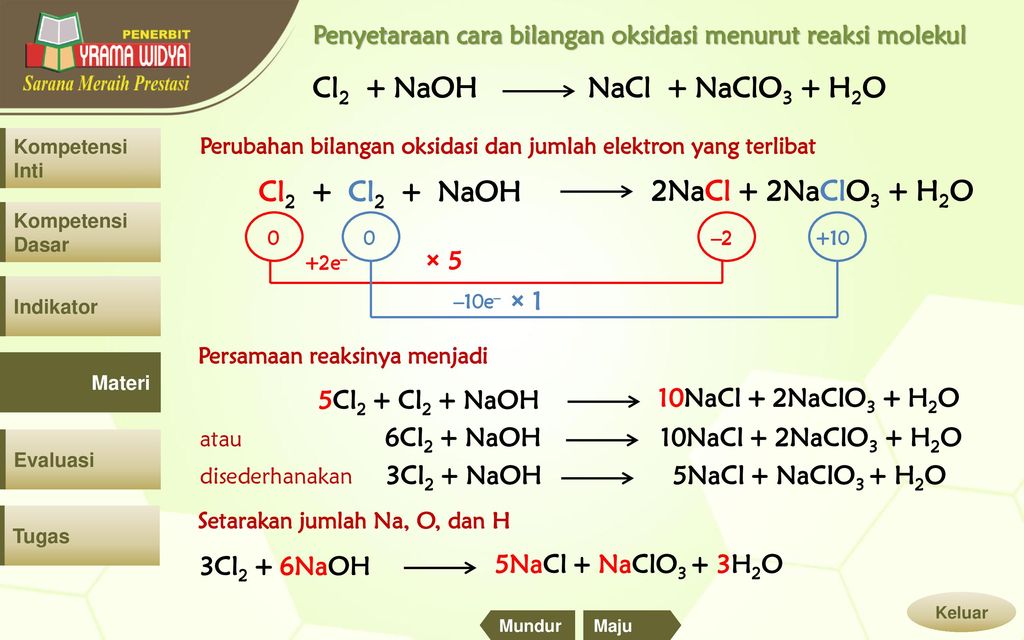
Check the balance Chlorine react with sodium hydroxide to produce sodium chlorate sodium chloride and water. Molar mass of amineptine. NaoH cl2-naclnaclo3h3o 2 See answers Advertisement Advertisement student8116 student8116 Explanation.
Descriptionh3O Associates is an elite. Name of hexachloroselenate IV anion vs hexaaquacobalt II cation. Trên đây THPT Sóc.
Alternate names of platinum IV ions. The solution placed on Al. Canvas is NJITs Learning Management System LMS.
Search for other No Internet Heading Assigned in Ewing on The Real Yellow Pages. Limiting reagent can be computed for a balanced equation by entering the number of moles or weight for all reagents. Cl2 NaOH NaCl NaClO3 h3O.
Khi cho Cl2 tác dụng với dung dịch NaOH ở nhiệt độ thường. See the answer See the answer See the answer done loading. 3Cl 2 6NaOH NaClO 3 5NaCl 3H 2 O.
C Cu2O CO2 Cu.
Balance The Following Equation By Oxidation Number Method Naoh Cl 2 Rarr Nacl Naclo 3 H 2 O
In The Reaction Cl2 Naoh Nacl Naclo3 h3o The Equivalent Weight Of Cl2 Is
How To Balance Naoh Cl2 Nacl Naclo h3o Dilute Sodium Hydroxide Chlorine Gas Youtube
Fqs5gjrkf Finm
You have just read the article entitled
Cl2 Naoh Nacl Naclo3 h3o. You can also bookmark this page with the URL : https://mariyahqiwright.blogspot.com/2022/09/cl2-naoh-nacl-naclo3-h3o.html
You can also bookmark this page with the URL : https://mariyahqiwright.blogspot.com/2022/09/cl2-naoh-nacl-naclo3-h3o.html
Share this post
«, numPosts: 8, titleLength: «auto», thumbnailWidth: 250, thumbnailHeight: 170, noImage: «//3.bp.blogspot.com/-ltyYh5ysBHI/U04MKlHc6pI/AAAAAAAADQo/PFxXaGZu9PQ/w255-h270-c/no-image.png», containerId: «related-post-7426008034102247264», newTabLink: false, moreText: «Read More», widgetStyle: 3, callBack: function() {} };
Удаление хлората натрия
Удаление хлората натрия Когда дело доходит до получения урожая хлората натрия из элемента, вы должны стремиться иметь не менее 600 г/л растворенного хлората в электролите. Эта концентрация хлората вместе с NaCl приведет к тому, что часть хлората натрия выйдет из электролита при его охлаждении до нуля и ниже.Однако вы не получите очень много, на самом деле вы не сможете получить ничего в первый раз, когда будете запускать свои ячейки, не выкипятив немного воды.
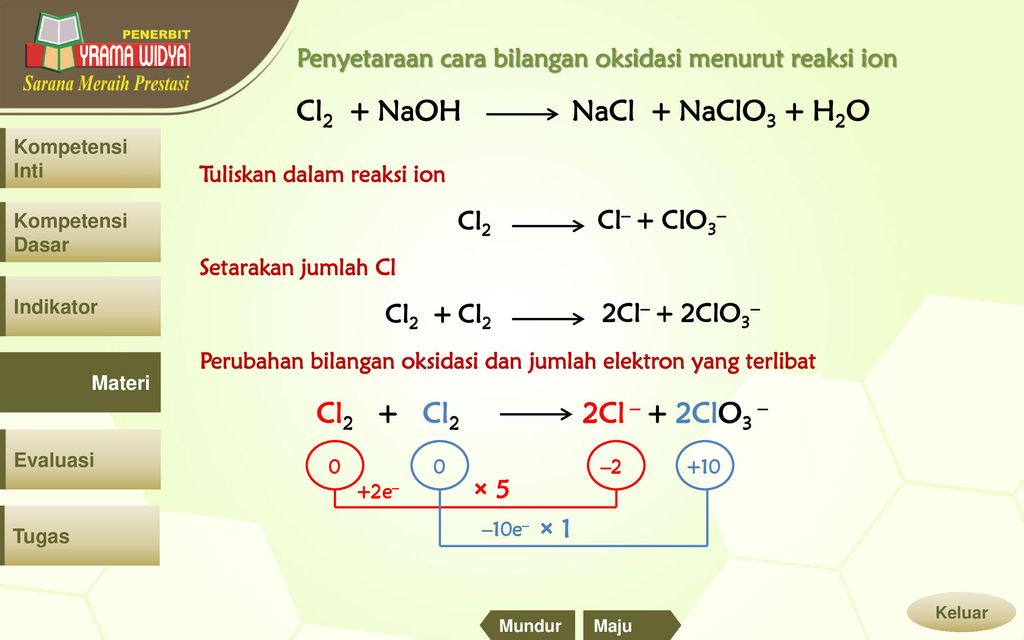 Проблема в том, что при первом запуске вашей ячейки с хлоратом концентрация хлората натрия не будет очень высокой, и вы не получите ни грамма хлората, он останется в растворе.
Проблема в том, что при первом запуске вашей ячейки с хлоратом концентрация хлората натрия не будет очень высокой, и вы не получите ни грамма хлората, он останется в растворе. Приведенная выше диаграмма получена отсюда с использованием исходного графика от EKA Chemicals. Ан
объяснение как интерпретировать
Диаграммы взаимной растворимости приведены в разделе «Как разработать процессы фракционной кристаллизации».
Также книга «Водные растворы и фазовая диаграмма» ФРЕДЕРИКА ФИЛДА ПУРДОНА. и ВИКТОР УОЛЛЕС СЛЕЙТЕР, очень полезное чтение. Он доступен в Google Книгах.
Когда вы впервые запустите свою камеру, на графике будет 26% NaCl. Если вы не добавляете раствор хлорида во время работы ячейки и запускаете ячейку в течение рекомендуемого времени, указанного формулой времени работы, в ячейке останется около 10 г/л00 мл (100 г/л) хлорида. а остальная часть хлорида (25 г/100 мл) будет преобразована в 106,5/58,5 * 25 г = 45,5 г хлората на 100 мл раствора. Это примерно в точке А на графике, 64,7% воды, 6,3% NaCl и 29% NaClO3. Как видите, при охлаждении вы не уберете хлорат. Если вы испарите около 14,8% воды, вы доберетесь до точки С на графике. Если теперь вы охладите свой раствор до нуля (точка B), вы получите около 11% хлората на ppt.
Если вы добавляете хлорид натрия в ячейку во время ее работы, вы можете увеличить концентрацию хлората, чтобы получить хлорат на ppt. когда ячейка закончена.
Еще один хороший способ получить хлорат натрия из раствора — добавить в раствор немного концентрированного NaCl. В промышленности это называется «высаливанием». Растворимость хлората заметно снижается по мере увеличения концентрации хлорида. NaCl будет использоваться, когда вы снова запустите ячейку. Запишите количество хлорида, которое вы добавили. Вы можете понизить температуру электролита ниже нуля, чтобы получить больший урожай хлората. Высаливание описано ниже с использованием информации из Энциклопедии химической обработки и дизайна (см. книги Google).
Диаграмма взаимной растворимости ниже представлена в граммах растворенных веществ на 100 мл воды.
 Эти ценности,
при удельном весе около 1,38 можно интерпретировать как 82 г хлорида натрия на 100 г воды и 14,5 г хлорида натрия на 100 г воды (соответствует 51,1% воды, 7,2% хлорида и 41,7% хлората). Эта композиция
показан точкой А выше. Хлорат натрия только начнет кристаллизоваться, когда температура поднимется до 25°С. При добавлении твердого хлорида натрия
и растворяются, это перемещает систему в точку B при кристаллизации хлората натрия. В точке B хлорид натрия больше не растворяется, и при дальнейшем охлаждении выпадает смесь хлората и хлорида.
Эти ценности,
при удельном весе около 1,38 можно интерпретировать как 82 г хлорида натрия на 100 г воды и 14,5 г хлорида натрия на 100 г воды (соответствует 51,1% воды, 7,2% хлорида и 41,7% хлората). Эта композиция
показан точкой А выше. Хлорат натрия только начнет кристаллизоваться, когда температура поднимется до 25°С. При добавлении твердого хлорида натрия
и растворяются, это перемещает систему в точку B при кристаллизации хлората натрия. В точке B хлорид натрия больше не растворяется, и при дальнейшем охлаждении выпадает смесь хлората и хлорида. Более распространенной практикой является выпаривание некоторого количества воды при температуре 25°C (с использованием вакуума), что имеет тот же эффект, что и перемещение системы из точки A в точку B, в то время как Кристаллизация хлората натрия. В таблице ниже приведены количества с цифрами в граммах.
| Твердый | Клеточный раствор состава А | Маточный раствор | Кристаллизация | с добавлением соли NaClO3 кристаллизованный | Маточный раствор | Кристаллизация по water evaporation | NaClO3 crystalized |
| NaClO3 | 82 | 68 | — | 14 | 45 | — | 37 |
| NaCl | 14. 5 5 | 22 | 7.5 (added) | — | 14.5 | — | — |
| h3O | 100 | 100 | — | — | 66 | 34 (evaporated) | — |
Обратите внимание, что алюминиевые контейнеры не подходят для кипячения раствора хлората, так как он почернеет от продуктов коррозии.
Твердый хлорат можно промыть очень холодной водой и поместить в ячейку для перхлората.
Когда ваша хлоратная ячейка остановится, в ней будет некоторое количество гипохлорита (промежуточный продукт). Рекомендуется уничтожить этот гипохлорит, прежде чем приступать к восстановлению твердого хлората натрия или получению хлората калия. Это можно сделать, кипячая ваш раствор в течение примерно 15 минут при нейтральном pH (вам, возможно, придется сделать это в любом случае, чтобы сконцентрировать раствор, если вы отделяете твердый хлорат натрия) или добавив около 1 г мочевины на литр раствора (кипятите ). Перекись водорода также разрушает гипохлорит, как и сульфит натрия и аммиак.
Перекись водорода также разрушает гипохлорит, как и сульфит натрия и аммиак.
Ячейковый раствор (маточный раствор, как его называют в промышленности) теперь будет возвращаться в ячейку для хлората. Высушите извлеченный хлорат и взвесьте, это даст вам представление о том, какое количество хлорида и хлората содержится в жидкости.
Следует отметить, что хлорат натрия очень растворим, и вы можете быть разочарованы выходом хлората натрия, который получается, когда вы берете продукт из своих клеток в первый раз.
В маточном растворе все еще будет оставаться большое количество хлората натрия, и когда он рециркулируется в ячейки, вы получите гораздо больший выход хлората натрия при последующих запусках ячейки. Если вы не дозаправляли свои ячейки хлоридом натрия, когда они работали в первый раз, вы не сможете вывести хлорат из раствора только путем охлаждения, вам придется выкипятить немного воды, чтобы получить хлорат ppt из. При последующих экстракциях (при условии, что вы повторно использовали маточный раствор в клетках) концентрация хлората натрия будет намного выше, и из него выйдет больше. Вы все еще можете выкипятить немного воды, как описано выше.
При последующих экстракциях (при условии, что вы повторно использовали маточный раствор в клетках) концентрация хлората натрия будет намного выше, и из него выйдет больше. Вы все еще можете выкипятить немного воды, как описано выше.
Удаление добавок
Если хроматы были добавлены в вашу ячейку по соображениям эффективности или для защиты железных или стальных катодов, их следует удалить. Хроматы можно удалить из ячейки, добавив необходимое количество хлорида бария. Хроматы будут осаждаться в виде нерастворимого хромата бария. Избыток хлорида бария можно осадить добавлением карбоната натрия.Я не знаю, как удалить персульфаты или фториды из электролита, а также не знаю, какое влияние окажут небольшие количества персульфатов или фторидов на пиротехнические составы.
НАЖМИТЕ КНОПКУ «НАЗАД» В ВАШЕМ ВЕБ-БРАУЗЕРЕ
NaClO () => ? | Калькулятор химических реакций
| Поиск |
Результаты поиска по химическому уравнению
Новости Только 5% НАСЕЛЕНИЯ знают
Реклама
1 результатов найдено
Отображение уравнения от 1 до 1 Страница 1 — Пожалуйста, прокрутите до конца, чтобы увидеть больше результатов
Уравнение Результат #1
Нажмите, чтобы увидеть более подробную информацию и рассчитать вес/моль >>
| jpg» substance-weight=»74.4422″> 3NaClO | → | 2NaCl | + | NaClO 3 | |
| sodium chloride | sodium chlorate | ||||
| 3 | 2 | 1 | Hệ số | ||
| Nguyên — Phân tử khối (g/mol) | |||||
| Số MOL | |||||
| KHốI LượNG (G) | KHốI LượNG (G) | 669KHốI LượNG (G) | . 0103 0103 Реклама Дополнительная информация об уравнении 3NaClO → 2NaCl + NaClO3Каковы условия реакции NaClO () ?Для этого химического уравнения не найдено информации Объяснение: идеальные условия окружающей среды для реакции, такие как температура, давление, катализаторы и растворитель. Катализаторы — это вещества, которые ускоряют темп (скорость) химической реакции, не потребляясь и не становясь частью конечного продукта. Катализаторы не влияют на равновесные ситуации. Как могут происходить реакции с образованием NaCl (хлорид натрия) и NaClO3 (хлорат натрия)?Явление после NaClO ()Это уравнение не несет никакой конкретной информации о явлении. В этом случае вам просто нужно наблюдать, чтобы убедиться, что вещество продукта NaClO3 (хлорат натрия), появляющийся в конце реакции. Или если какое-либо из следующих реагентов NaClO , исчезает Какую другую важную информацию вы должны знать о реакции У нас нет дополнительной информации об этой химической реакции. Категории уравненийНажмите, чтобы увидеть более подробную информацию и рассчитать вес/моль >> Дополнительные вопросы, связанные с химическими реакциями 3NaClO → 2NaCl + NaClO3Вопросы, связанные с реагентом NaClO ()Каковы химические и физические характеристики NaClO ()? реагент? Вопросы, связанные с продуктом NaCl (хлорид натрия)Каковы химические и физические характеристики NaCl ()? Какие химические реакции имеют NaCl (хлорид натрия) в качестве продукта? Вопросы, связанные с продуктом NaClO3 (хлорат натрия)Каковы химические и физические характеристики NaClO3 ()? Какие химические реакции происходят с NaClO3 (хлорат натрия) в качестве продукта? 1 результатов найдено Дополнительная информация о веществах, которые используют уравнениепродукт NaCl (Natri Clorua) Реакция, в результате которой образуется вещество NaClO (гипохлорит натрия) ()Cl 2 + 2NaOH → H 2 O + NaCl + NaClO H 2 O + NaCl → H 2 + NaClO 4NaOH + 4NH → 7 H 7 7 2 O + N 2 + 3NaCl + NaClO + 2NH 4 OH Реакция, в результате которой образуется вещество NaCl (Natri Clorua) (хлорид натрия) HCl + NaOH → H 2 O + NaCl CL 2 + 2NA → 2NACL BACL 2 + NA 2 SO 4 → 2NACL + BASO 4 4 → 2NACL + BASO 4 4 → 2NACL + BASO 4 → 2NACL + BASO 4 . |