Сполуки Нітрогену: Амоніак. Солі амонію.(підготовка до ЗНО).
Запитання 1
Амоніак можна отримати взаємодією:
1) NH4HCO3 і HCL
2) NH4NO3 і KCL
3) NH4CL і KOH
4) (NH4)2SO4 і Ca(OH)2
5) NH4NO3 і KOH
6) N2 і H2O
варіанти відповідей
Запитання 2
Амоній сульфат можна отримати взаємодією:
1) (NH4)2CO3 і H2SO4
2) NH4NO3 і K2SO4
3) NH3 і H2SO4
4 )NH3 і SO3
5) NH4CL і K2SO4
6) NH4H SO4 і NH3
варіанти відповідей
1,2,6
1,3,6
Запитання 3
Невідома сіль під час нагрівання розкладається, виділяючи газ, який зараховують до несолетворних оксидів. Під час дії розчину лугу на цю ж сіль виділяється газ із різким специфічним запахом. Невідома речовина — це
Під час дії розчину лугу на цю ж сіль виділяється газ із різким специфічним запахом. Невідома речовина — це
варіанти відповідей
NH4CL
(NH4)2SO4
NH4NO3
(NH4)2CO3
Запитання 4
Укажіть назви речовин, які взаємодіють з амоніаком:
1) Нітратна кислота
2) Кисень
3) Водень
4) Калій гідроксид
5) Гідроген сульфід
6) Натрій оксид
варіанти відповідей
1,2,5
1, 2,4
4,5,6
Запитання 5
Укажіть формули речовин, під час нагрівання яких виділяється амоніак:
1) NH4NO3
2) NH4CL
3) NH4HCO3
4) HNO3
5) (NH4)2CO3
6) NH4NO2
варіанти відповідей
2,3,4
3,5,6
Запитання 6
Установіть послідовність утворення сполук під час отримання амоній нітрату
1) NO2
2) NO
3) NH3
4) HNO3
варіанти відповідей
3,2,1,4
2,1. 3,4
3,4
1,2,3,4
3,4,2,1
Запитання 7
Унаслідок термічного розкладання солі Х , яка є мінеральним добривом,одержали газ У,який використовують у медицині. Укажіть речовини Х і У.
варіанти відповідей
NH4CL , HCl
(NH4)2SO4, NH3
NH4NO3 , N2O
(NH4)2CO3 , CO2
Запитання 8
Укажіть, яку геометричну форму має молекула амоніаку
варіанти відповідей
лінійну
октаедра
піраміди
трикутника
Запитання 9
Укажіть, яку геометричну форму має йон амонію
варіанти відповідей
трикутника
тетраедра
октаедра
лінійну структуру
Запитання 10
У кажіть групу речовин, з якими реагує амоніак
Запитання 11
У кажіть групу речовин, з якими реагує амоніак
варіанти відповідей
H2O, KOH, K2O
H2O, HCl, HNO3
CuO, H2O, NaOH
H2SO4 , Ag, KOH
Запитання 12
У разі збільшення тиску в системі: N2(Г) + 3H2(Г) ⇄ 2NH3(Г)
варіанти відповідей
Збільшується вихід амоніаку
Утворюється більше азоту та водню
Збільшується вміст азоту в реакційній суміші
Зменшується вміст амоніаку в реакційній суміші
Запитання 13
Укажіть формули речовин, які утворюються під час каталітичного окиснення амоніаку в кисні
варіанти відповідей
NO2 і H2O
N2 і H2O
N2O і H2O
NO і H2O
Запитання 14
Якщо амоніак пропустити крізь воду, то реакція середовища зміниться
варіанти відповідей
З нейтральної на кислу
З нейтральної на лужну
З кислої на нейтральну
З лужної на кислу
Запитання 15
Реакція синтезу амоніаку є
варіанти відповідей
необоротною, екзотермічною, каталітичною
оборотною, екзотермічною, каталітичною
оборотною, ендотермічною, некаталітичною
необоротною, ендотермічною, некаталітичною
Запитання 16
Укажіть фізичні властивості амоніаку
варіанти відповідей
безбарвний газ із характерним різким запахом, майже в два рази легший за повітря, дуже добре розчиняється у воді
безбарвний газ, без запаху і смаку; трохи легший за повітря, малорозчинний у воді
безбарвний газ із солодкуватим запахом; підтримує горіння
газ бурого кольору, з характерним гострим запахом, важчий за повітря, добре розчиняється у воді, дуже отруйний
Запитання 17
Розчин амоніаку у воді називають
варіанти відповідей
вапняковою водою
баритовою водою
аміачною водою
жавелевою водою
Запитання 18
Якими методами можна зібрати амоніак
варіанти відповідей
Методом витіснення води з пробірки
Методом витіснення вуглекислого газу з пробірки
Методом витіснення кисню з пробірки
Методом витіснення повітря з пробірки
Запитання 19
Амоніак використовують для:
варіанти відповідей
наповнення електролампочок
виведення плям, чищення ювелірних виробів, килимів та як рідке азотне добриво
для виробництва нітратної кислоти, нітратних добрив, вибухових речовин, барвників, лікарських речовин
створення інертного середовища при зварюванні металів, у вакуумних установках
Запитання 20
Укажіть формулу нашатирю
варіанти відповідей
NH4CL
NH3 x H2O
Запитання 21
Які реакції підтверджують наявність амоніаку в пробірці:
1) NH3 + HCl =NH4Cl
2) NH3 + H2SO4 = NH4HSO4
3)3CuO + 2NH3= N2↑+ 3Cu + 3H2O
4)СuSO4 + 5H2O = СuSO4 ∙ 5H2O
5)2NH3 + H2SO4 = (NH4)2 SO4
6)Nh4 + H2O ⇄ NH4 OH
варіанти відповідей
1,3,5
Запитання 22
Амоніак горить
варіанти відповідей
Червоним полум’ям
Блакитним полум’ям
Зеленуватим полум’ям
Жовтим полум’ям
Запитання 23
В одному об’ємі води розчиняється близько
варіанти відповідей
300 об’ємів амоніаку
400 об’ємів амоніаку
600 об’ємів амоніаку
700 об’ємів амоніаку
Запитання 24
Укажіть тип кристалічної гратки для солей амонію
варіанти відповідей
Молекулярні
Атомні
Металічні
Запитання 25
Укажіть якісну реакцію на йон амонію
варіанти відповідей
2NH4Cl+H2SO4=(NH4)2SO4+2HCl↑
2NH4Cl + Ca(OH)2 = CaCl2 + 2NH3↑+ 2H2O
(NH4)2SO4+BaCl2=2NH4Cl+BaSO4↓
(NH4)2СO3 →2NH3 ↑+ Н2О + СO2↑
Запитання 26
Амоній гідрогенкарбонат ( амоняк) використовують
варіанти відповідей
як добрива
у медицині, як дезинфікуючий засіб
розпушувач тіста у кондитерському виробництві ( Е -503)
для визначення присутності аміаку у повітрі
Запитання 27
Перша допомога при отруєнні амоніаком:
варіанти відповідей
уражене місце обробляють етиловим спиртом, після чого накладають суху стерильну пов’язку
очі промивають великою кількістю води
негайно змити їх залишки зі шкіри водою та нейтралізувати слабким розчином борної кислоти
свіже повітря, промити шлунок водою підкисленою оцтом або лимонним соком, випити склянку молока
Запитання 28
Укажіть твердження правильні щодо фізіологічної дії амоніаку:
1) Токсичний, викликає подразнення слизових оболонок дихальних шляхів. При потраплянні на шкіру викликає тяжкі опіки.
При потраплянні на шкіру викликає тяжкі опіки.
2) Вдихання малих кількостей амоніаку стимулює роботу серця і нервової системи, тому нашатирний спирт дають нюхати при втраті свідомості та отруєнні чадним газом.
3) Тривала дія навіть малих концентрацій призводить до виникнення бронхіту, гастриту, викликає загальне ослаблення організму.
4) Вдихання великих кількостей подразнює слизову оболонку очей і дихальних шляхів.
5) Забезпечує необхідну для перетравлення їжі кислотність, запобігає розвитку в шлунку процесів гниття та бродіння, впливу хвороботворних бактерій.
6) При попаданні в організм викликає нудоту, пронос, смерть від набряку гортані. При потраплянні в очі викликає сліпоту.
варіанти відповідей
1,3,5
2,3,6
Створюйте онлайн-тести
для контролю знань і залучення учнів
до активної роботи у класі та вдома
Створити тест
Натисніть «Подобається», щоб слідкувати за оновленнями на Facebook
сравните и сопоставьте, как Nh4 и Ca(OH)2 образуют ионы OH- в воде.

Физические науки
Пейси Д.
спросил 20.03.18Nh4 и Ca(OH)2 образуют в воде ионы ОН-
Подписаться І 3
Подробнее
Отчет
2 ответа от опытных наставников
Лучший Новейшие Самый старыйАвтор: Лучшие новыеСамые старые
Дж. Р. С. ответил 20.03.18
Репетитор
5,0 (136)
к.т.н. кандидат биохимии — профессор университета — преподаватель химии
Об этом репетиторе ›
Об этом репетиторе ›
Я бы немного не согласился с предыдущим ответом только потому, что Ca(OH)2 изначально классифицировался бы как основание Аррениуса, поскольку он «отдает» группу OH-.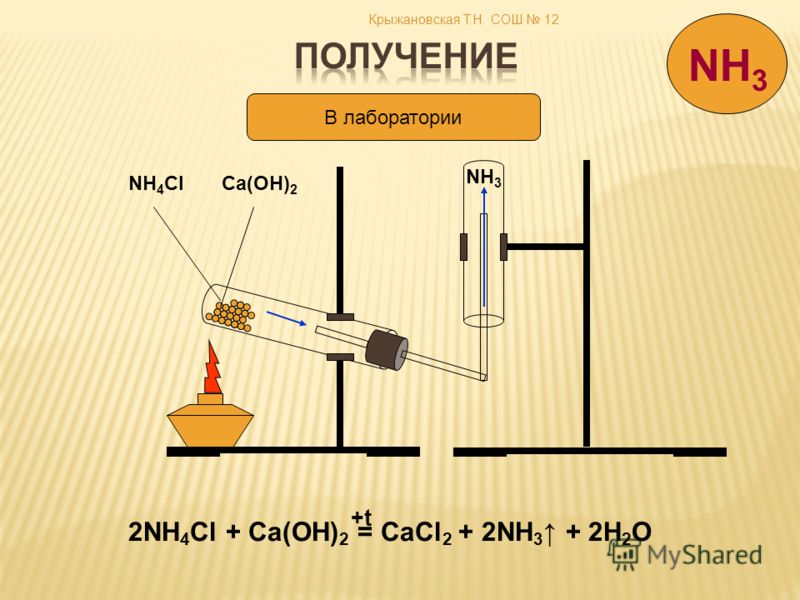
Голосовать за 0 голос против
Подробнее
Отчет
Кан Чит Л. ответил 20.03.18
Репетитор
Новое в Византе
Опытный репетитор по подготовке к экзаменам и колледжу
См. таких репетиторов
Смотрите таких репетиторов
Вы должны знать, что оба они являются основаниями, однако Nh4 является основанием Льюиса, а Ca(OH)2 — скорее основанием Бренстеда.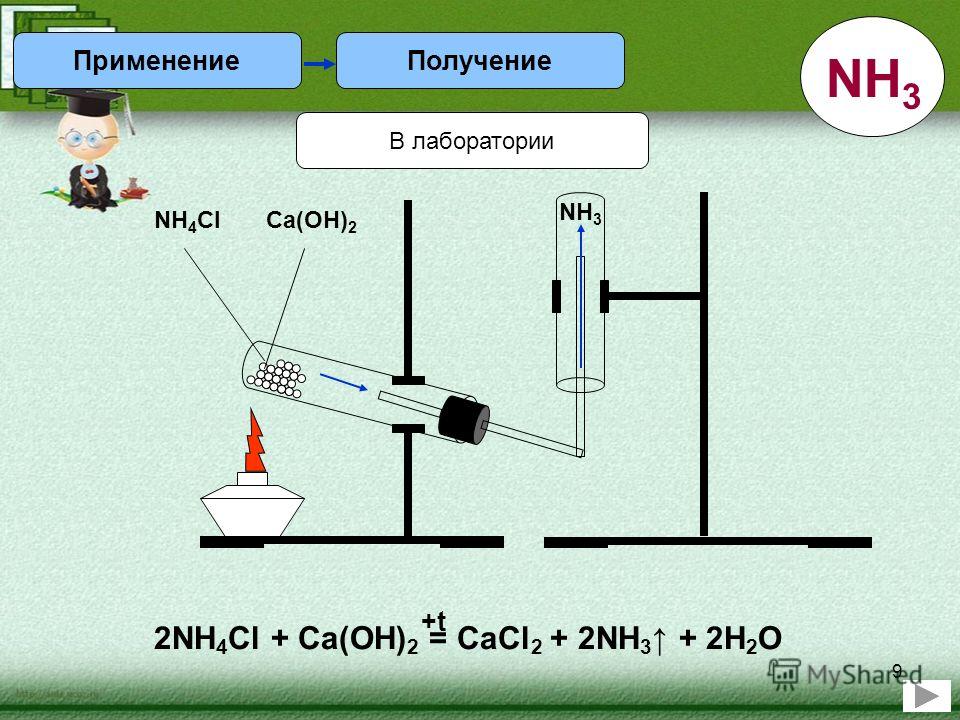
В качестве основания Льюиса Nh4 имеет неподеленную электронную пару, которая может притягивать ион водорода в воде, поэтому Nh4 + h3O—->(Nh5) + + (OH) — .
С другой стороны, Ca(OH)2 является основанием Бренстеда, поэтому он может сам диссоциировать (OH) — . Для Ca(OH)2 имеем Ca(OH) 2 -> Ca 2+ + 2(OH) —
Голосовать за 0 голос против
Подробнее
Отчет
Все еще ищете помощь? Получите правильный ответ, быстро.
Задайте вопрос бесплатно
Получите бесплатный ответ на быстрый вопрос.
ИЛИ
Найдите онлайн-репетитора сейчас
Выберите эксперта и встретьтесь онлайн. Никаких пакетов или подписок, платите только за то время, которое вам нужно.
Никаких пакетов или подписок, платите только за то время, которое вам нужно.
Является ли Ca(OH)2 кислотой или основанием? Strong or Weak
Главная > Химия > Является ли Ca(OH)2 кислотой или основанием?
Гидроксид кальция белого цвета, выглядит как гранулированное твердое вещество без запаха с химической формулой Ca(OH) 2 . Его также называют гашеной известью. Он образуется при смешивании оксида кальция с водой. Он плохо растворяется в воде.
В этой статье мы обсудим, является ли гидроксид кальция (CaOH 2 ) кислотой или основанием? Он сильный или слабый и т.д.?
Итак, Является ли Ca(OH) 2 кислотой или основанием? Ca(OH) 2 является основанием. В водном растворе диссоциирует на два иона (Са 2+ и 2ОН – ), наличие ионов ОН – в водном растворе Са(ОН) 2 делает его основным по своей природе.
| Name of Molecule | Calcium hydroxide |
| Chemical formula | Ca(OH) 2 |
| pH value | Around 12 |
| Натуральный | Сильное основание |
| Основность (pK b ) | 1,37 (первая ОН – ), 2,43 (вторая ОН – ) |
Основание определяется как акцептор протона или донор неподеленной пары. Когда Ca(OH) 2 растворяется в воде, он распадается на два иона Ca 2 + и 2OH – .
Поскольку Ca(OH) 2 диссоциирует на Ca 2 + и 2OH-, этот ион OH – принимает протон (H + ) с образованием воды.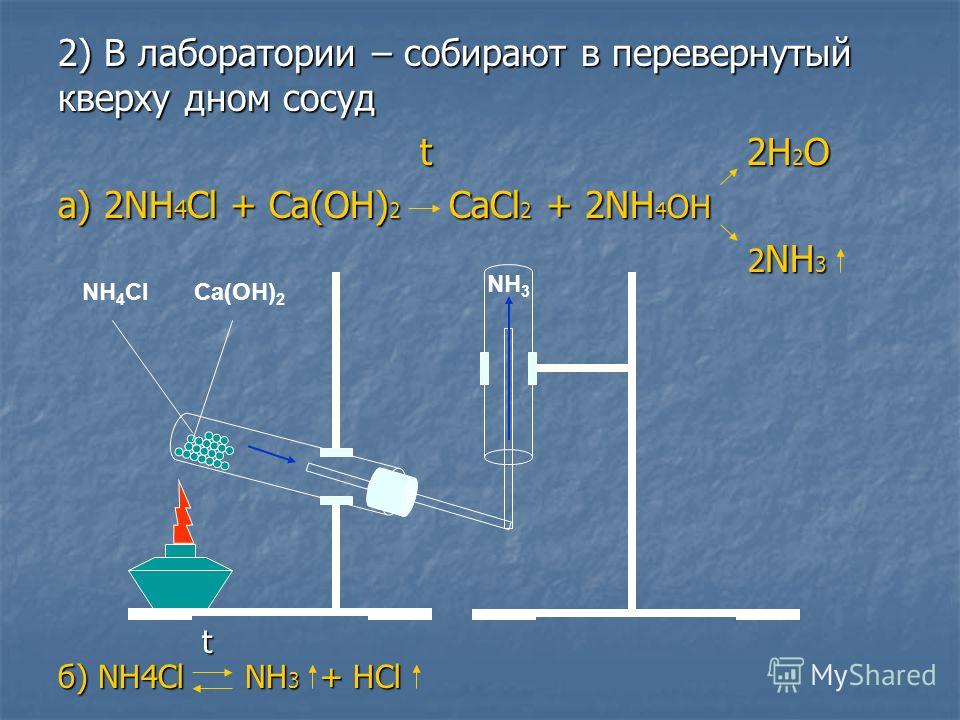
⇒ Ca(OH) 2 + (водн.) → Ca 2 + (водн.) + 2OH – (водн.)
Согласно теории Аррениуса, соединение также является основанием быть основанием, когда он образует ион ОН- в результате ионизации или диссоциации в воде.
Очевидно, что когда Ca(OH) 2 растворяется в воде, образуется два иона гидроксида на молекулу. Следовательно, мы можем сказать, что Ca(OH) 2 является основанием или основанием Аррениуса в природе.
Является ли Ca(OH)2 сильным или слабым основанием?Чтобы узнать, является ли Ca(OH) 2 сильным или слабым основанием, вы должны знать основную разницу между сильным основанием и слабым основанием.
Сильное основание: Соединение является сильным основанием, если оно полностью диссоциирует в водном растворе и высвобождает большое количество гидроксид-ионов. Все моли сильного основания диссоциируют на гидроксид-ион (ОН – ), и в растворе не остается недиссоциированной части.
Пример: гидроксид натрия (NaOH), гидроксид бария (Ba(OH) 2 ), гидроксид лития (LiOH), гидроксид калия (KOH) и т. д. сильная или слабая база?
Слабое основание: Соединение является слабым основанием, если оно частично или не полностью диссоциирует в водном растворе. Это означает, что только некоторые части слабого основания диссоциируют в растворе с образованием ОН – , но некоторые части остаются в растворе недиссоциированными.
Пример- аммиак (NH 3 ), метиламин (CH 3 NH 2 ), NH 4 OH и т. Д.
также читайте :-
- — это NH4 A STILY BASE. ?
- Ch4Nh3 — сильная или слабая база?
- Является ли Nh5OH сильным или слабым основанием?
| Сильное основание | Слабое основание |
Полностью ионизируются. | Ионизируют не полностью. |
| Они очень реакционноспособны. | Они менее реактивны по сравнению с сильной основой. |
| Значение рН составляет от 10 до 14. | Значение рН составляет от 7 до 10. |
| Они имеют высокую константу равновесия. | У них меньше константа равновесия. |
| Это хорошие электролиты. | Они не такие хорошие электролиты по сравнению с сильным основанием. |
| Пример – NaOH, KOH, LiOH и т. д. | Пример – N2h5, Nh4, Nh5OH и т. д. ? Ca(OH) 2 — сильное основание. Потому что он полностью диссоциирует в водном растворе с образованием иона ОН – , и в растворе не остается ни одного его моля недиссоциированным. А количество ионов ОН – в водном растворе очень велико и мы знаем ОН 9Ионы 0067 – склонны принимать протон. Таким образом, большее количество акцепторов протонов, присутствующих в растворе, в конечном итоге делает Ca(OH) 2 сильным основанием. Как видно из приведенного выше водного раствора, когда Ca(OH) 2 растворяется в воде, он полностью ионизируется в ионы (Ca 2 + и 2OH – ). В растворе нет недиссоциированной молекулы (Ca(OH) 2 ), повсюду в растворе присутствуют только ионизированные ионы. Одиночная стрелка, используемая в приведенной выше реакции, показывает, что в равновесии происходит только прямая реакция, а в растворе не происходит обратной реакции. As Ca 2+ представляет собой очень слабую сопряженную кислоту Ca(OH) 2 , поэтому она не способна реагировать ни с ионами OH – , ни с ионами молекул воды. Таким образом, в растворе остаются только расщепляющие ионы (Ca 2+ и 2OH – ). Или вы также можете принять Ca 2+ как ион-спектор , поскольку он почти бесполезен в растворе, он не влияет на значение рН раствора.
Следовательно, большое количество гидроксид-ионов, присутствующих в водном растворе Ca(OH) 2 , неуклонно увеличивает значение pH и усиливает действие основания в растворе. Кроме того, значение константы диссоциации основания (K b ) для Ca(OH) 2 на больше 1. основания в растворе. ⇒ Если значение константы диссоциации основания больше 1 ( K > 1), то природа соединения является сильным основанием. ⇒ Если K b < 1, то природа соединения является слабым основанием. Итак, чем выше значение константы диссоциации основания, тем больше прочность основания в растворе. Вот список некоторых распространенных сильных/слабых кислот и оснований. Как практически узнать, является ли Ca(OH)2 кислотой или основанием? Чтобы узнать, является ли соединение кислотой или основанием на практике, один из самых простых способов использовать лакмусовую бумагу.
Примечание: Когда красная лакмусовая бумажка становится синей, соединение считается щелочным. А когда синяя лакмусовая бумажка становится красной, говорят, что соединение кислое. При контакте Ca(OH) 2 с красной лакмусовой бумажкой лакмусовая бумажка окрашивается в синий цвет. Таким образом, мы можем сказать, что Ca(OH) 2 является основанием . Является ли Ca(OH)2 щелочным или нет?Щелочь является сильным основанием, которое образует гидроксид-ионы при растворении в воде. Все растворимые гидроксиды, такие как литий, цезий, натрий, калий и т. д., являются щелочными металлами. Щелочь считается самой сильной, если она производит почти все ОН – ионов при растворении в воде.
|




 Поскольку молекула Ca(OH) 2 при растворении в воде образует почти все ионы OH – , что в конечном итоге делает ее сильной щелочью.
Поскольку молекула Ca(OH) 2 при растворении в воде образует почти все ионы OH – , что в конечном итоге делает ее сильной щелочью.