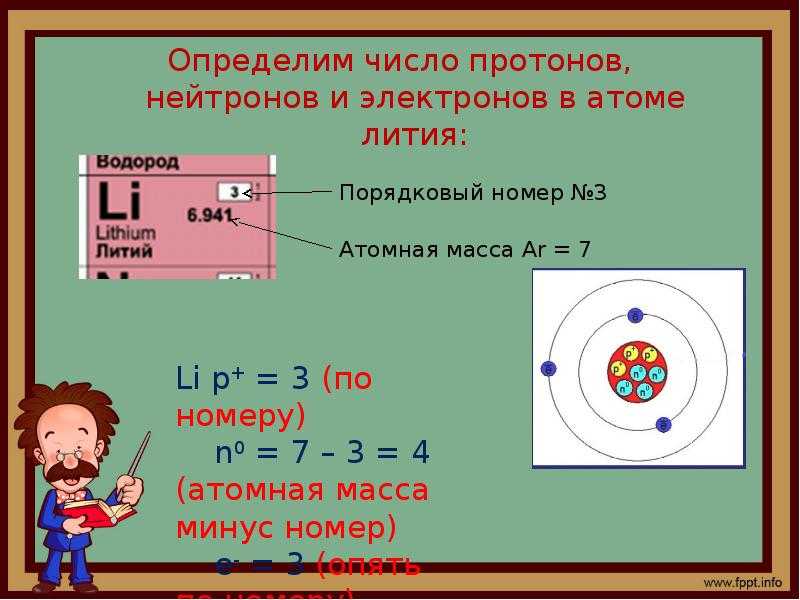
Кварковый конструктор. О протоне, его аддонах и спиноффах / Хабр
В одной из моих публикаций я затрагивал тему распада протона. Суть проблемы: до сих пор не зафиксировано ни одного самопроизвольного распада свободного протона, хотя искусственно «расколоть» протон не составляет труда. Более того, свободные нейтроны вне атома распадаются очень быстро (период полураспада – около 15 минут). Чрезвычайная стабильность протона – залог существования Вселенной и, в частности, залог горения звезд, состоящих в основном из водородной плазмы, то есть, из свободных протонов и свободных электронов (ни те, ни другие частицы в свободном виде не распадаются). При этом не менее интересно, что протон не является подлинно элементарной частицей, а состоит из кварков и глюонов. И здесь у физиков возникают большие вопросы о природе массы протона. С одной стороны, масса протона гораздо больше, чем суммарная масса входящих в него кварков и глюонов. С другой стороны, в 2022 году был поставлен эксперимент, указывающий, что некоторые свойства протона можно объяснить только присутствием в его составе очарованного кварка – а очарованный кварк сам по себе тяжелее протона. Наконец, я кратко остановлюсь на вкладе вещества и антивещества в массу протона, и расскажу о некоторых экзотических частицах, возникающих при этих взаимодействиях.
Наконец, я кратко остановлюсь на вкладе вещества и антивещества в массу протона, и расскажу о некоторых экзотических частицах, возникающих при этих взаимодействиях.
Представление об атомах как о подлинно неделимых частицах продержалось в течение почти всего XIX века. Античная атомистическая идея (сформулированная Левкиппом и развитая Демокритом) оставалась чисто философским конструктом, пока в 1803 году английский ученый Джон Дальтон не экстраполировал её на химическую почву. Он предположил, что сохранение массы при химических реакциях объясняется существованием атомов – элементарных частиц, которыми обмениваются химические элементы. Более того, он выдвинул гипотезу, что именно различия в атомном составе объясняют существование разных соединений между одними и теми же элементами. Атомный вес лежит в основе периодического закона, сформулированного Менделеевым в 1869 году. Правда, уже в 1890-е годы неделимость атома была фактически опровергнута: в 1892 году Хендрик Лоренц, изучая катодные лучи, предположил, что они могут состоять из частиц более мелких, чем атомы – «электронов». В 1894 году Анри Беккерель открыл радиоактивность, свидетельствующую о делимости атомов, а в 1897 году Уильям Томпсон доказал существование электронов.
В 1894 году Анри Беккерель открыл радиоактивность, свидетельствующую о делимости атомов, а в 1897 году Уильям Томпсон доказал существование электронов.
Электрон стал первой из известных элементарных частиц, история открытия которых выходит за рамки этой публикации. Однако, к началу 1940-х и к моменту получения первой управляемой ядерной реакции были сформулированы две фундаментальные модели атома – модель Резерфорда (не учитывавшая квантовую механику) и модель Бора (учитывавшая). Оказалось, что отрицательно заряженные частицы, электроны, находятся на периферии ядра атома, а в центре атома находится ядро, состоящее из положительно заряженных протонов и не имеющих заряда нейтронов. Ядерные реакции суть расщепление атома. Уже в 1940-е годы появилась возможность изучать продукты ядерных реакций, а значит – изучить, каков состав элементарных частиц, и каковы пределы делимости материи. Классическим аппаратом для описания такой делимости стали диаграммы Фейнмана.
Ричард Фейнман (1918 — 1988) широко известен как один из основателей квантовой электродинамики, популяризатор науки и балагур, заявлявший, что «никто не понимает квантовую механику». Но, на мой взгляд, Фейнман замечателен как один из самых молодых участников Манхэттенского проекта. Он на практике понимал, насколько «весомым, грубым зримым» является деление ядра, а также успел осмыслить и формализовать вероятностную природу и сложнейшую предсказуемость деления мельчайших частиц материи. Диаграммы Фейнмана – не столько физика, сколько математика, позволившая описать внутреннюю структуру элементарных частиц.
Но, на мой взгляд, Фейнман замечателен как один из самых молодых участников Манхэттенского проекта. Он на практике понимал, насколько «весомым, грубым зримым» является деление ядра, а также успел осмыслить и формализовать вероятностную природу и сложнейшую предсказуемость деления мельчайших частиц материи. Диаграммы Фейнмана – не столько физика, сколько математика, позволившая описать внутреннюю структуру элементарных частиц.
Итак, в 1940-е годы удалось не без труда разработать математический аппарат, описывающий, что происходит при соударениях элементарных частиц в ускорителях. По нынешним временам эти опыты были бы сочтены «низкоэнергетическими», но в середине прошлого века они буквально выплеснулись за передний край науки. Оказалось, что результат распада протона (например, при соударении с другим протоном) является вероятностным и зависит, например, от силы соударения. При этом и масса, и размер всех протонов совершенно одинаковы. Математических уравнений для описания этого парадокса не хватало, поэтому в качестве подспорья и появились «импровизированные» диаграммы Фейнмана, а также возник вопрос: из чего же состоят протоны и нейтроны?
В 1960-е годы поиск ответов на эти вопросы привел к открытию кварков и сильного взаимодействия – частиц и явлений, аналога которых в макромире просто не существует.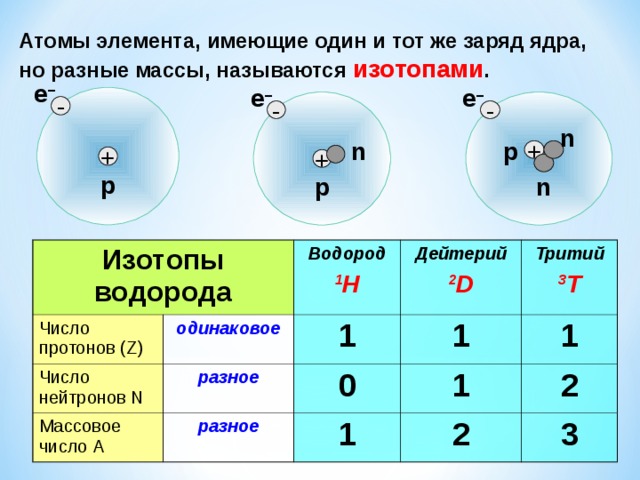 Кварки являются фермионами (как и электрон), но неразделимо связаны в протонах, нейтронах и других частицах сильным взаимодействием. Важнейшее отличие кварков от электрона заключается в дробности их электрического заряда.
Кварки являются фермионами (как и электрон), но неразделимо связаны в протонах, нейтронах и других частицах сильным взаимодействием. Важнейшее отличие кварков от электрона заключается в дробности их электрического заряда.
Поскольку электрический заряд протона выражается целым числом (+1), уточним, в чем суть этой дробности.
Заряды кварков складываются так: верхний кварк имеет заряд +2/3, нижний кварк имеет заряд -1/3. Соответственно, суммарный электрический заряд протона равен 2/3 + 2/3 — 1/3 = 3/3 = 1. При этом электрический заряд электрона равен -1. По умолчанию количество протонов и электронов в атоме является равным, поэтому цельный атом электрически нейтрален.
Что происходит внутри протона
Когда в 1960-е годы были открыты кварки, представления о микромире изменились раз и навсегда. Кварки оказались подобны электронам (фермионам) но в свободном виде они не существуют. При распаде крупной элементарной частицы (адрона) образуются не отдельные кварки, а новые элементарные частицы, каждая из которых состоит из целого количества кварков. Оказалось, что такая экзотическая межкварковая связь регулируется отсутствующей в макромире физической силой, которая получила название «сильное взаимодействие». Математически выразить суть сильного взаимодействия и связи кварков удалось только в 1973 году, но как теория кварковых взаимодействий (квантовая хромодинамика), так и деление частиц, с эмпирической точки зрения парадоксальны.
Оказалось, что такая экзотическая межкварковая связь регулируется отсутствующей в макромире физической силой, которая получила название «сильное взаимодействие». Математически выразить суть сильного взаимодействия и связи кварков удалось только в 1973 году, но как теория кварковых взаимодействий (квантовая хромодинамика), так и деление частиц, с эмпирической точки зрения парадоксальны.
Сильное взаимодействие принципиально отличается от электромагнитного в двух отношениях. Во-первых, в электромагнитном взаимодействии участвует всего один вид заряда (электрический), в сильном взаимодействии их три. Они условно обозначены цветами – «красный», «зеленый» и «синий».
Во-вторых, носителем сильного взаимодействия является глюон, обозначенный здесь желтой проволочкой – и также не встречающийся в свободном состоянии за пределами атома. Косвенные доказательства существования глюонов появились ещё в конце XX века. Взаимодействия кварков и глюонов описывает квантовая хромодинамика — теория, с вычислительной точки зрения чрезвычайно сложная даже для современных компьютеров. Дело в том, что явления, описываемые этой теорией, имеют вероятностный характер, а внутри элементарных частиц взаимодействуют как реально существующие, так и виртуальные кварки. Именно по причине этой виртуальной составляющей масса протона гораздо больше, чем общая масса входящих в него кварков. По умолчанию в состав протона входят три кварка: два верхних (up) и один нижний (down). Кварки участвуют как в электромагнитном взаимодействии (поскольку имеют электрический заряд), так и в сильном взаимодействии. Обратите внимание на их цветовые заряды.
Дело в том, что явления, описываемые этой теорией, имеют вероятностный характер, а внутри элементарных частиц взаимодействуют как реально существующие, так и виртуальные кварки. Именно по причине этой виртуальной составляющей масса протона гораздо больше, чем общая масса входящих в него кварков. По умолчанию в состав протона входят три кварка: два верхних (up) и один нижний (down). Кварки участвуют как в электромагнитном взаимодействии (поскольку имеют электрический заряд), так и в сильном взаимодействии. Обратите внимание на их цветовые заряды.
Но с учётом вероятностной природы состава протона оказывается, что наряду с этими видами кварков и с глюонами в протоне может содержаться и очарованный (charm) кварк. Более того, наряду с кварками в протонах существуют и антикварки, состоящие из антивещества; они образуют короткоживущие пары с соответствующими кварками. При изменении соотношения между кварками и антикварками возникают похожие на протон экзотические частицы, о которых будет рассказано в конце статьи.
Примерно так протон мог бы выглядеть «под лупой». Но все эти составляющие имеют вероятностный характер: если вслепую вытянуть из протона одну из его составляющих, то с большей вероятностью это окажется кварк (а не глюон), причём в 2/3 случаев будет вытянут верхний кварк, а в 1/3 случаев – нижний кварк.
Вероятностная составляющая протона и очарованный кварк
Именно такая квантовомеханическая вероятностная природа элементарной частицы допускает следующую возможность: в составе протона могут оказаться не только верхние и нижние кварки, но и другие кварки в паре с соответствующими им античастицами (антикварками). Состав протона может отличаться от базового, если протон обладает избыточной энергией (и, соответственно, массой), а это случается, когда протон движется в ускорителе высоких энергий. Эксперимент, призванный проверить, может ли в протоне присутствовать «лишний» очарованный кварк (заряд +2/3, как у верхнего кварка, но масса — 1,25 ГэВ, немногим больше, чем у целого протона – около 0,938 ГэВ). Такой эксперимент был впервые поставлен в Европейской мюонной коллаборации в институте ЦЕРН в 1980 году. Действительно, результаты можно было интерпретировать в пользу этой гипотезы: в протоне мог проявляться очарованный кварк, а вместе с ним — и эквивалентный ему антикварк. Впрочем, эти результаты оспаривались как очень сомнительные, поскольку сложно чётко разграничить состав самого протона и состав той высокоэнергетической среды, в которой он движется в ускорителе. Эксперимент сложен ещё и потому, что различные кварки и антикварки при движении протона в ускорителе рождаются и аннигилируют очень быстро.
Такой эксперимент был впервые поставлен в Европейской мюонной коллаборации в институте ЦЕРН в 1980 году. Действительно, результаты можно было интерпретировать в пользу этой гипотезы: в протоне мог проявляться очарованный кварк, а вместе с ним — и эквивалентный ему антикварк. Впрочем, эти результаты оспаривались как очень сомнительные, поскольку сложно чётко разграничить состав самого протона и состав той высокоэнергетической среды, в которой он движется в ускорителе. Эксперимент сложен ещё и потому, что различные кварки и антикварки при движении протона в ускорителе рождаются и аннигилируют очень быстро.
Однако в 2022 году Хуан Рохо из Свободного Университета в Амстердаме совместно с коллегами смог сформулировать и поставить новый эксперимент, результаты которого интерпретировались при помощи машинного обучения.
Модель, подготовленная для этого эксперимента, учитывала различные гипотетические структуры протона с учётом масс, зарядов и ароматов кварков. Затем результаты этой модели сравнивались с множеством данных, включавшим показатели более 500 000 реальных столкновений частиц, зафиксированных за много лет – в том числе, в Большом адронном коллайдере.
Использование машинного обучения в данном случае было особенно полезно потому, что компьютер сгенерировал и такие варианты, которые сами учёные просто не могли бы придумать – благодаря этому значительно повысилась объективность выборки.
Оказалось, что, если бы в протонах не встречалась пара из очарованного кварка и очарованного антикварка, то наблюдаемые результаты могли бы наблюдаться только с 0,3% вероятностью. Таким образом, внутри протонов происходят следующие явления, которые кажутся парадоксальными, поскольку не имеют аналогов в макромире:
Кроме реальных частиц внутри протона присутствуют виртуальные частицы и античастицы, которые попарно рождаются и аннигилируют (правда, есть мнение, что виртуальных частиц не существует)
Когда протоны движутся в ускорителях, возрастает их энергия, а значит и масса, поэтому и набор кварков в протоне с некоторой вероятностью может отличаться от обычной тройки «верхний, верхний, нижний»
Кварки не «запечатаны» внутри протона (хотя и не выходят за его пределы), поэтому в ускорителе они могут взаимодействовать как с кварками из других протонов, так и со свободными фотонами и электронами, свободно перемещающимися в ускорителе.

В квантовой теории поля электромагнитное взаимодействие возникает, когда электрически заряженные частицы обмениваются фотонами (фотон – переносчик электромагнитного взаимодействия). В свою очередь, сильное взаимодействие возникает на минимальных расстояниях, в основе этого взаимодействия лежит цветной заряд кварков, а переносчиком такого взаимодействия является глюон. Если электромагнитное взаимодействие между частицами сильнее всего при плотном контакте, а при удалении частиц друг от друга ослабевает, то сильное взаимодействие, напротив, усиливается даже при минимальном удалении кварков друг от друга – и поэтому прочно связывает их в протоне (нейтроне, других частицах). Поэтому размер протона составляет лишь около 0,85 фемтометров. При этом только 1-2% массы протона приходится на массу входящих в него верхних и нижних кварков и глюонов, а вся остальная масса протона возникает из энергии сильного взаимодействия. Именно поэтому в составе протона вполне могут возникать и более экзотические кварки и антикварки, при наличии высокой энергии столкновений, достижимой в ускорителях.
О протонах и некоторых экзотических атомах
Выше я изложил, каким образом, согласно современным представлениям, в протоне сочетается конкретная и вероятностная составляющая. При привычных нам низких энергиях в состав протона входит три кварка. Но в ускорителях, где энергия протона многократно возрастает, в нём могут на минимальное время возникать пары других кварков и антикварков. В том числе — очарованный кварк, более тяжелый, чем протон. Но сами кварки, существующие только внутри более крупных элементарных частиц, являются фермионами, поэтому сближаются по свойствам с электроном и позитроном (античастицей, противоположной электрону и имеющей заряд +1). Электрон и позитрон, в отличие от кварков, не входят в состав атомного ядра, а встречаются в свободном виде.
Но опыты с кварковым составом протона позволили не только уточнить природу и точную величину его массы, но и искусственно получить несколько экзотических атомов, напоминающих водород. Обычный атом водорода состоит из одного протона и одного электрона. Таким образом, в атом водорода-протия входят четыре фермиона: верхний, верхний и нижний кварк с суммарным зарядом +1 образуют ядро этого атома, а электрон с зарядом -1 находится в электронной оболочке. Но известно ещё несколько экзотических атомов, похожих на водород-протий, но отличающихся от него по кварковому составу.
Таким образом, в атом водорода-протия входят четыре фермиона: верхний, верхний и нижний кварк с суммарным зарядом +1 образуют ядро этого атома, а электрон с зарядом -1 находится в электронной оболочке. Но известно ещё несколько экзотических атомов, похожих на водород-протий, но отличающихся от него по кварковому составу.
Все эти совокупности частиц можно считать атомами, поскольку они электрически нейтральны, могут вступать в электромагнитные взаимодействия и химические реакции. Слева показан обычный водород, состоящий из протона (заряд +1) и электрона (заряд -1).
Сверху показан протоний. Это экзотический атом, впервые зафиксированный в опытах ЦЕРН в 1988 году. Представляет собой пару из протона (заряд +1) и антипротона (заряд -1), вращающихся вокруг друг друга. Кварковый состав антипротона – два верхних антикварка и нижний антикварк. Время жизни протония в зависимости от уровня энергии – от 10-11 до 10-6 с.
Справа показан антиводород. Это атом, состоящий из антипротона (заряд -1) и позитрона (заряд +1). Впервые получен в ЦЕРН в 1995 году группой Вальтера Олерта. Время жизни такого атома в лабораторных условиях доведено до 17 минут.
Впервые получен в ЦЕРН в 1995 году группой Вальтера Олерта. Время жизни такого атома в лабораторных условиях доведено до 17 минут.
Снизу показан позитроний. Это миниатюрный экзотический атом, состоящий из электрона и позитрона. Электрон и позитрон обладают спином (моментом вращения), и их спины могут быть сонаправленными или разнонаправленными. В первом случае образуется ортопозитроний, во втором – парапозитроний. Впервые позитроний был обнаружен в 1951 году Мартином Дойчем.
Ортопозитроний живет гораздо дольше, чем парапозитроний: 138,6 нс против 0,12 нс.
Масса водорода, антиводорода и протония отличается незначительно, а позитроний гораздо легче их всех. Но именно эти небольшие отличия в массе экзотических ядер позволяют с высокой точностью вычислять массы отдельных кварков, а также тот вклад в массу, который даёт сильное взаимодействие. Кроме того, эти опыты и частицы позволяют точнее понять природу сильного взаимодействия и готовят базу для попыток сымитировать или воспроизвести сильное взаимодействие в макромире (постепенно увеличивая искусственно получаемые совокупности разнообразных кварков). Возможно, такие опыты откроют путь к стабильному получению антивещества (эта тема заслуживает отдельной статьи), а также к контролируемому превращению вещества в антивещество и обратно – без аннигиляции. По-видимому, предел делимости материи, наконец, достигнут, но возможности её низкоуровневой пересборки перед нами только начинают открываться.
Возможно, такие опыты откроют путь к стабильному получению антивещества (эта тема заслуживает отдельной статьи), а также к контролируемому превращению вещества в антивещество и обратно – без аннигиляции. По-видимому, предел делимости материи, наконец, достигнут, но возможности её низкоуровневой пересборки перед нами только начинают открываться.
Внутри атомного ядра: сильное и слабое
Валерия Сирота
«Квантик» №8, 2019
Читавшие статью про устройство атомов в «Квантике» № 11 за 2018 год знают, что любое вещество состоит всего из трёх типов элементарных частиц — протонов, нейтронов и электронов. Протоны и нейтроны — тяжёлые, гораздо тяжелее электронов. Они образуют ядра атомов, а электроны летают вокруг этих ядер, совсем улететь им не даёт электрическое притяжение протонов: протоны имеют положительный заряд, а электроны — отрицательный, и все частицы с зарядами одного знака отталкиваются друг от друга, а с зарядами разных знаков — притягиваются.
Внутри атомного ядра протоны и нейтроны — они вместе называются нуклонами2 — «держатся» друг за дружку ядерными силами. Это совсем не то же самое, что электрические (точнее, электромагнитные) силы. Например, в ядерном взаимодействии протон и нейтрон участвуют «на равных» (в отличие от электромагнитного, ведь у нейтрона электрического заряда нет, а у протона есть). Ядерное взаимодействие иначе называют сильным, так что можно сказать: «В ядре действуют сильные силы» — и это не будет бессмысленным повтором.
Это совсем не то же самое, что электрические (точнее, электромагнитные) силы. Например, в ядерном взаимодействии протон и нейтрон участвуют «на равных» (в отличие от электромагнитного, ведь у нейтрона электрического заряда нет, а у протона есть). Ядерное взаимодействие иначе называют сильным, так что можно сказать: «В ядре действуют сильные силы» — и это не будет бессмысленным повтором.
Эти «сильные силы» действительно очень велики, иначе ядра не удерживались бы и разваливались. Ведь протоны в них все «отпихиваются» друг от друга электрическими силами. К тому же нуклоны в ядре не стоят на месте, а быстро движутся. Попробуйте втроём-вчетвером взяться за руки и начать беспорядочно прыгать и метаться туда-сюда. Удержать друг друга и не расцепить руки будет гораздо сложнее, чем если бы все спокойно водили хоровод.
Радиоактивность
И всё же иногда сильного взаимодействия не хватает, чтобы удержать ядро, и оно разваливается на части. Это называется распад ядра, или радиоактивный распад, а элементы, или изотопы (помните, что это?), которые норовят распасться, называются радиоактивными. В большинстве атомов вокруг нас ядра устойчивые и никогда не развалятся. Разве что по ядру очень сильно стукнет, например, ещё один протон или нейтрон (это будет вынужденный распад). Они такие стабильные потому, что в них правильное соотношение протонов и нейтронов: у лёгких ядер — протонов и нейтронов примерно поровну, а у тяжёлых — нейтронов чуть больше; чем тяжелее ядро, тем больше доля нейтронов (проверьте по таблице Менделеева). Но ядру вредно быть очень толстым: если протонов в нём совсем много (больше 82), то устойчивой конфигурации уже нет: сколько нейтронов ни клади, ядро развалится.
В большинстве атомов вокруг нас ядра устойчивые и никогда не развалятся. Разве что по ядру очень сильно стукнет, например, ещё один протон или нейтрон (это будет вынужденный распад). Они такие стабильные потому, что в них правильное соотношение протонов и нейтронов: у лёгких ядер — протонов и нейтронов примерно поровну, а у тяжёлых — нейтронов чуть больше; чем тяжелее ядро, тем больше доля нейтронов (проверьте по таблице Менделеева). Но ядру вредно быть очень толстым: если протонов в нём совсем много (больше 82), то устойчивой конфигурации уже нет: сколько нейтронов ни клади, ядро развалится.
Если соотношение протонов и нейтронов «неудачное», ядро рано или поздно распадётся. Некоторые, правда, могут перед этим прожить многие миллиарды лет, а другие не проживут и долю секунды. Ядро может развалиться на пару ядер поустойчивей и полегче, но чаще всего от него просто откалывается небольшой кусочек — обычно два протона и два нейтрона, то есть как раз ядро атома гелия. Ядро гелия \({}^{4}_{2}\mathrm{He}\) иначе называется альфа-частицей, а распад с испусканием этой частицы — альфа-распадом. {4}_{2}\mathrm{He}\).
{4}_{2}\mathrm{He}\).
Здесь ядро урана превращается в ядро тория.
Бета-распад
И вот — чудо. Представьте, берёте вы ядро радиоактивного изотопа — ну, например, цезий-137 — и ждёте, когда оно распадётся. А из него вместо альфа-частицы вылетает электрон! Откуда он взялся в ядре?! Там ведь только протоны и нейтроны!
Тут в игру вступает ещё одна новая сила, про которую мы пока не говорили. Чтобы подчеркнуть её отличие от сильного взаимодействия, её назвали слабой. И сама по себе она, действительно, куда слабее. Но слабые могут делать такое, чего не могут сильные.
С этой силой нейтрон в ядре действует… сам на себя и просто превращается в протон и электрон! И ещё в одну очень лёгкую частичку, антинейтрино.
Всё верно, и вас не обманывали: нейтрон — элементарная частица, то есть его нельзя разделить на части. Нет у него внутри протона с электроном. Он именно в них превращается. Слабые силы превращают одни частицы в другие!4 И в ядре им сделать это труднее. {137}_{56}\mathrm{Ba}\) + e− + \(\bar{ν}\).
{137}_{56}\mathrm{Ba}\) + e− + \(\bar{ν}\).
Обратите внимание, что масса ядра (число нуклонов в нём) остаётся прежней, а заряд его увеличивается на единицу; просто нейтрон в ядре заменяется на протон. Такие процессы называются бета-распадом5, а электрон, вылетевший из ядра, — бета-частицей.
Нейтрино и антинейтрино
Что же, все нейтроны распадутся когда-нибудь и их больше не будет? Нет. Во-первых, сильное взаимодействие мешает распаду, и в стабильных ядрах нейтроны надёжно защищены. Во-вторых, бывает, что протон в нестабильном ядре ухитряется «подцепить» слабыми силами электрон (например, из того же атома), и вдвоём они превращаются в нейтрон:
p+ + e− → n + ν.
Попутно образуется другая частица — нейтрино (уже без анти-, поэтому над её значком нет чёрточки). Она, как и антинейтрино, до того лёгкая, что её массу до сих пор не смогли измерить. Как и электрон, она не участвует в сильных взаимодействиях. Но и в электромагнитном взаимодействии она тоже не участвует! Только слабые да ещё гравитационные силы (которых никому не избежать) действуют на нейтрино. Из-за этого нейтрино очень мало взаимодействуют с остальным веществом. Огромное их количество каждую секунду протыкает Землю насквозь, не замечая её и ничего по дороге не нарушая. Их очень трудно изучать — поди поймай частицу, которая проходит незамеченной через любую ловушку…
Но и в электромагнитном взаимодействии она тоже не участвует! Только слабые да ещё гравитационные силы (которых никому не избежать) действуют на нейтрино. Из-за этого нейтрино очень мало взаимодействуют с остальным веществом. Огромное их количество каждую секунду протыкает Землю насквозь, не замечая её и ничего по дороге не нарушая. Их очень трудно изучать — поди поймай частицу, которая проходит незамеченной через любую ловушку…
Другие «анти-»
А протон может превратиться в нейтрон? Сам по себе — не может. Потому что нейтрон тяжелее протона. Как раз на массу электрона и ещё на маленькую чуточку. Более тяжёлая вещь в более лёгкие может превратиться, а наоборот — нет. Зато если протон в ядре, ему могут помочь соседи-нуклоны: вместо недостающей массы они отдают свою энергию, из-за чего просто будут помедленнее носиться по ядру да поближе прижмутся друг к дружке. Для прочности ядра это даже очень полезно. Но совсем не каждое ядро на такое способно, а только такое «рыхлое», у которого запас энергии достаточно большой. Обычно это как раз ядра с лишними протонами — или, говоря иначе, с недостатком нейтронов. Угадайте, почему…6
Обычно это как раз ядра с лишними протонами — или, говоря иначе, с недостатком нейтронов. Угадайте, почему…6
И на что же распадается протон, если ему помогают? Он, конечно, превратится в нейтрон, но ведь надо ещё деть куда-то положительный электрический заряд. И вот на сцене появляется ещё одна элементарная частица! Это «антиэлектрон», масса у него как у электрона, а электрический заряд — такой же по величине, но обратный по знаку — положительный. У всех элементарных частиц есть свои античастицы — и у протона, и даже у нейтрона. Каждая античастица участвует во всех тех же взаимодействиях и реакциях, что и её пара, но с приставкой «анти»: например, антинейтрон распадается на антипротон, антиэлектрон и анти-антинейтрино, то есть просто нейтрино:
\(\bar{n}\) → p− + e+ + ν,
а антипротон с антиэлектроном могут превратиться в антинейтрон. Могли бы быть антиатомы, антипланеты и антилюди на них, но, похоже, такого нигде нет. {121}_{53}\mathrm{I}\).
{121}_{53}\mathrm{I}\).
Теперь мы узнали более или менее всё, что может случиться с атомным ядром. А заодно обнаружили кучу новых элементарных частиц: только что было три — и вот их уже восемь… Но если такое изобилие вас пугает, можно утешаться тем, что всё, что мы видим вокруг себя, всё-таки состоит из атомов с вполне стабильными ядрами и только из трёх типов элементарных частиц — протонов, нейтронов и электронов.
Художник Мария Усеинова
1 Напомним: 10−15=11015=110…0 — в знаменателе число с 15 нулями.
2 От латинского слова nucleus — ‘ядро’.
3 Нам нужен основной изотоп радия, чаще всего встречающийся в природе.
4 Как именно происходит это превращение, понять с помощью наших обычных представлений невозможно, но физики умеют посчитать, что получается, написав определённые уравнения.
5 Альфа — первая буква греческого алфавита, а бета — вторая. Эти два вида распада — самые частые.
6 Ответ — в следующей статье, в следующем номере «Квантика».
7 От слова positive — ‘положительный’.
4.5: Элементы, определяемые количеством их протонов
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 47471
Цели обучения
- Дать определение атомному номеру.
- Определить массовое число.
- Определить количество протонов, нейтронов и электронов в атоме.
Важно уметь отличать атомы одного элемента от атомов другого элемента. Элементы — это чистые вещества, из которых состоит вся остальная материя, поэтому каждому из них дается уникальное имя.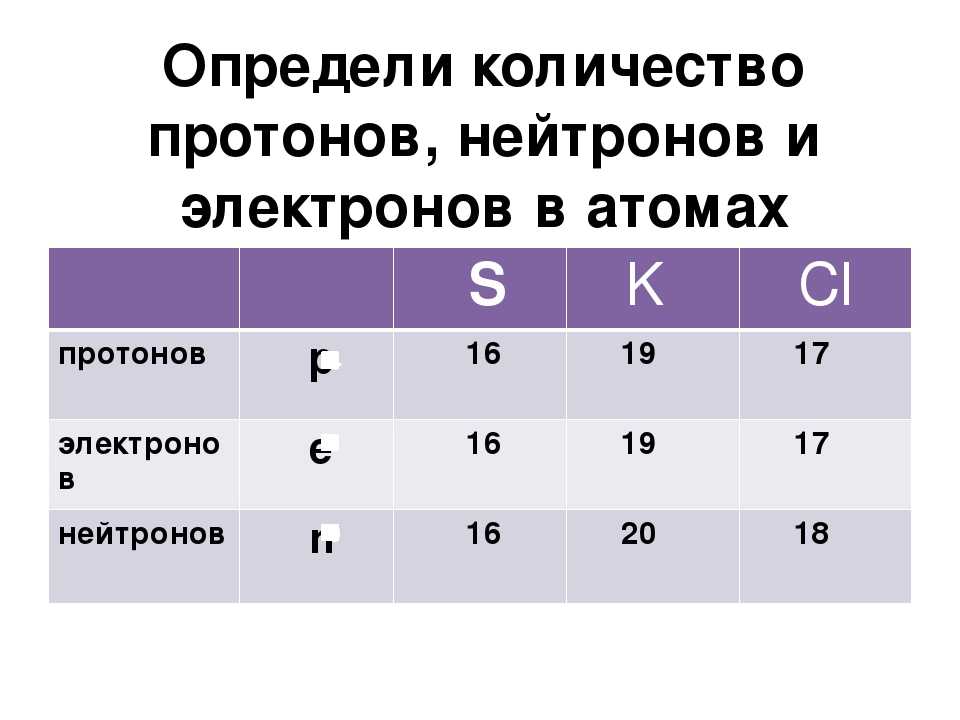 Названия элементов также представлены уникальными одно- или двухбуквенными символами, такими как \(\ce{H}\) для водорода, \(\ce{C}\) для углерода или \(\ce{He }\) для гелия. Однако было бы более убедительно, если бы эти имена можно было использовать для определения количества протонов и нейтронов в атомах. Вот где атомный номер и массовое число полезны.
Названия элементов также представлены уникальными одно- или двухбуквенными символами, такими как \(\ce{H}\) для водорода, \(\ce{C}\) для углерода или \(\ce{He }\) для гелия. Однако было бы более убедительно, если бы эти имена можно было использовать для определения количества протонов и нейтронов в атомах. Вот где атомный номер и массовое число полезны.
Атомный номер
Ученые различают разные элементы, подсчитывая количество протонов в ядре (таблица \(\PageIndex{1}\)). Если у атома есть только один протон, мы знаем, что это атом водорода. Атом с двумя протонами всегда является атомом гелия.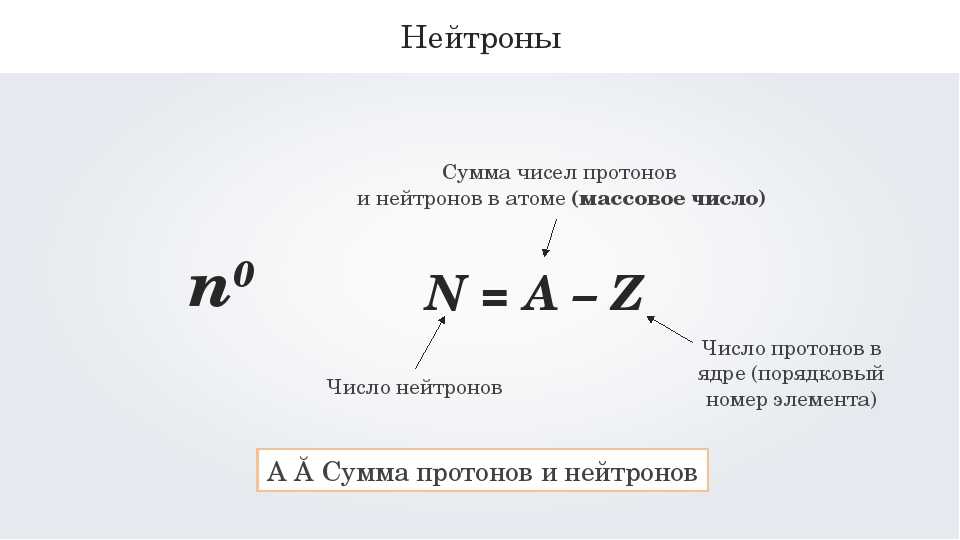
Поскольку атом одного элемента можно отличить от атома другого элемента по количеству протонов в его ядре, ученых всегда интересует это число и то, как это число отличается у разных элементов. Число протонов в атоме называется его атомным номером (\(Z\)). Это число очень важно, потому что оно уникально для атомов данного элемента. Все атомы элемента имеют одинаковое количество протонов, и каждый элемент имеет разное количество протонов в своих атомах. Например, все атомы гелия имеют два протона, и никакие другие элементы не имеют атомов с двумя протонами.
| Имя | | Нейтроны | Электроны | Атомный номер (Z) | Массовый номер (А) |
|---|---|---|---|---|---|
| Водород | 1 | 0 | 1 | 1 | 1 |
| Гелий | 2 | 2 | 2 | 2 | 4 |
| Литий | 3 | 4 | 3 | 3 | 7 |
| Бериллий | 4 | 5 | 4 | 4 | 9 |
| Бор | 5 | 6 | 5 | 5 | 11 |
| Углерод | 6 | 6 | 6 | 12 |
Конечно, поскольку нейтральные атомы должны иметь один электрон на каждый протон, атомный номер элемента также говорит вам, сколько электронов находится в нейтральном атоме этого элемента. {-27}\) килограммов, что является чрезвычайно малой массой. Масса нейтрона лишь чуть-чуть больше массы протона, но его массу также часто принимают равной одной атомной единице массы. Поскольку у электронов практически нет массы, практически вся масса атома приходится на его протоны и нейтроны. Следовательно, общее количество протонов и нейтронов в атоме определяет его массу в атомных единицах массы (таблица \(\PageIndex{1}\)).
{-27}\) килограммов, что является чрезвычайно малой массой. Масса нейтрона лишь чуть-чуть больше массы протона, но его массу также часто принимают равной одной атомной единице массы. Поскольку у электронов практически нет массы, практически вся масса атома приходится на его протоны и нейтроны. Следовательно, общее количество протонов и нейтронов в атоме определяет его массу в атомных единицах массы (таблица \(\PageIndex{1}\)).
Снова рассмотрим гелий. Большинство атомов гелия имеют два нейтрона в дополнение к двум протонам. Следовательно, масса большинства атомов гелия равна 4 атомным единицам массы (\(2 \: \text{аму}\) для протонов + \(2 \: \text{аму}\) для нейтронов). Однако некоторые атомы гелия имеют больше или меньше двух нейтронов. Атомы с одинаковым числом протонов, но разным числом нейтронов называются изотопами. Поскольку количество нейтронов может варьироваться для данного элемента, массовые числа различных атомов элемента также могут различаться. Например, некоторые атомы гелия имеют три нейтрона вместо двух (они называются изотопами и подробно обсуждаются позже).
Как вы думаете, почему в «массовое число» входят протоны и нейтроны, но не электроны? Вы знаете, что большая часть массы атома сосредоточена в его ядре. Масса атома зависит от количества протонов и нейтронов. Вы уже узнали, что масса электрона очень и очень мала по сравнению с массой протона или нейтрона (как масса пенни по сравнению с массой шара для боулинга). Подсчет количества протонов и нейтронов сообщает ученым об общей массе атома.
\[\text{массовое число} \: A = \left( \text{число протонов} \right) + \left( \text{количество нейтронов} \right) \nonumber \]
Масса атома число очень легко вычислить, при условии, что вы знаете количество протонов и нейтронов в атоме.
Пример 4.5.1
Каково массовое число атома гелия, содержащего 2 нейтрона?
Решение
\(\left( \text{число протонов} \right) = 2\) (Помните, что атом гелия всегда имеет 2 протона.)
\(\left( \text{количество нейтронов} \right) = 2\)
\(\text{массовое число} = \left( \text{количество протонов} \right) + \left( \ text{число нейтронов} \right)\)
\(\text{массовое число} = 2 + 2 = 4\)
Химический символ представляет собой одно- или двухбуквенное обозначение элемента .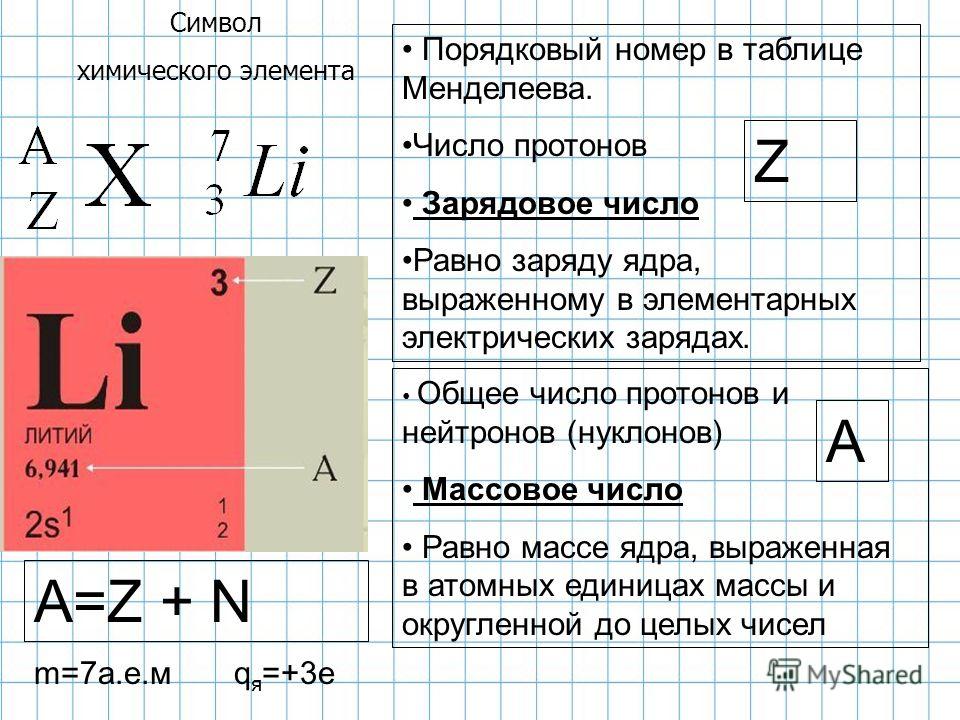
| Химический символ | Имя | Латинское название |
|---|---|---|
| \(\ce{Na}\) | Натрий | Натрий |
| \(\се{К}\) | Калий | Калиум |
| \(\ce{Fe}\) | Железо | Феррум |
| \(\ce{Cu}\) | Медь | Купрум |
| \(\ce{Ag}\) | Серебро | Аргентум |
| \(\ce{Sn}\) | Олово | Станнум |
| \(\ce{Sb}\) | Сурьма | Стибиум |
| \(\ce{Au}\) | Золото | Аурум |
| \(\ce{Pb}\) | Свинец | Пламбум |
Резюме
- Элементы — это чистые вещества, из которых состоит вся материя, поэтому каждому из них дается уникальное имя.

- Имена элементов также представлены уникальными одно- или двухбуквенными символами.
- Каждый элемент имеет уникальное количество протонов. Атомный номер элемента равен количеству протонов в ядрах любого из его атомов.
- Массовое число атома равно сумме протонов и нейтронов в атоме.
- Изотопы — это атомы одного и того же элемента (одинаковое количество протонов), имеющие разное количество нейтронов в атомных ядрах.
ПОД ЛИЦЕНЗИЕЙ
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Лицензия
- СК-12
- Показать страницу TOC
- № на стр.

- Теги
- автор@Генри Агнью
- автор@Мариса Альвиар-Агнью
- источник@https://www.ck12.org/c/chemistry/
‘Счет протонов, нейтронов и электронов A-P-E и M-A-N* Elament nana Mercury 80 Atomic Symbol Hg 200,59 Avq Масса Используя периодическую таблицу, определите атомный номер; массовое число; и количество протонов нейтронов и электронов в атоме каждого из следующих пятнадцати элементов Электроны Нейтроны;
Вопрос
‘Подсчет протонов, нейтронов и электронов
Введение: Информация, представленная в периодической таблице, позволяет вам определить количество протонов, нейтронов и электронов в любом заданном атоме элемента: Атомный номер всегда равен t0 количеству протонов.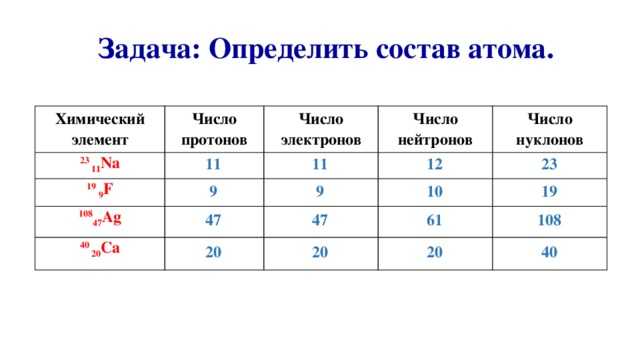 Количество электронов равно количеству протонов. А количество нейтронов равно t0 разнице между массовым числом и атомным номером: «Помни: А-Р-Е и М-А-Н* Эламент нана Меркурия 80 Атомный Символ Hg 200,59Средняя масса
Направления: Используя периодическую таблицу, определить атомный номер; массовое число; и количество протонов нейтронов и электронов в атоме каждого из следующих пятнадцати элементов
Атомный бор N:
Масса N:
Протоны:
Электроны:
Нейтроны:
Атомный азот меди:
Масса N:
Протоны:
Электроны:
Нейтроны:
Ведущий атомный азот:
Масса N:
Протоны:
Электроны:
Нейтроны:
Атомный азот водорода:
Масса N:
Протоны:
Электроны
Нейтроны;
Количество электронов равно количеству протонов. А количество нейтронов равно t0 разнице между массовым числом и атомным номером: «Помни: А-Р-Е и М-А-Н* Эламент нана Меркурия 80 Атомный Символ Hg 200,59Средняя масса
Направления: Используя периодическую таблицу, определить атомный номер; массовое число; и количество протонов нейтронов и электронов в атоме каждого из следующих пятнадцати элементов
Атомный бор N:
Масса N:
Протоны:
Электроны:
Нейтроны:
Атомный азот меди:
Масса N:
Протоны:
Электроны:
Нейтроны:
Ведущий атомный азот:
Масса N:
Протоны:
Электроны:
Нейтроны:
Атомный азот водорода:
Масса N:
Протоны:
Электроны
Нейтроны;
Мгновенный ответ:
Шаг 1/2
Бор Атомный N: 5
Масса N: 11
Протоны: 5
Электронов: 5
Нейтронов: 6
Атомная медь N: 29
Масса Н: 63,55
Протоны: 29
Электронов: 29
Нейтроны: 35
Рекомендация видео с лучшим совпадением:
Решено проверенным экспертом
У нас нет заданного вами вопроса, но вот рекомендуемое видео, которое может помочь.
Вопрос о лучшем совпадении
Пошаговые ответы
Субатомные частицы WS 1 Протоны, нейтроны и электроны Упражняться Вычисление числа каждой частицы в атом: # Протоны = Атомные Число # Электроны = Протоны # Нейтроны = массовое число – атомный номер Используйте периодическую таблицу, чтобы найти количество протонов, нейтроны и электроны для атомов следующих элементы. Имя элемента Элемент Символ масса Число атомный Число Протоны Нейтроны Электроны Бор Б 11 5 5 6 5 натрий 24 11 Д 8939 Медь 29 35 Тс 98 43 Pb 207 Таллий 204 81 ЧАС 0 Углерод 12 Н 7 Ба 56 Кальций Си 14 Аргон 18 мг 12 12
Рекомендуемые видеоролики
Расшифровка
Мы обсудим марсианское число, атомный номер, количество протонов, количество нейтронов, количество электронов в элементах, содержащих воду, атомный символ P после числа 11. Атомный номер пять. На этой картинке пять программ. Поскольку атомный номер равен количеству протонов, а количество протонов равно количеству электронов, поскольку это нейтральный атом, количество нейтронов можно найти по прошлому числу минус атомный номер. Остальные элементы нужно доработать. Количество протонов равно семи, а количество атомных символов равно 24. Даны количество электронов 11, количество нейтронов 24 и количество атомных символов. Поскольку это нейтрально, пункт 39электронам присвоен атомный номер 39. Спасибо, количество протонов Количество нейтронов 89 Атомный символ корпоративный и число 29. Массовое число 29, это 35 Это атомный номер 29. Число протонов 29. Число электронов 29 до н.э. 98. Итак, число 43. В этом числе 43 электрона. Количество нейтронов было -43. Ведущий элемент не имеет ни прошлого числа, ни числа дам, поэтому символ называется Фиби. Есть два числа: количество частиц и количество электронных частиц. Это 1 24, потому что количество нейтронов не равно 7. Итальянский символ элемента — это элемент. Маска номер 81 — это атомный номер mhm число протонов восемь. Количество электронов и количество нейтронов одинаковы. Когда водород будет равен нулю на вашем переводе в массовом числе, символ элемента будет для него.
Остальные элементы нужно доработать. Количество протонов равно семи, а количество атомных символов равно 24. Даны количество электронов 11, количество нейтронов 24 и количество атомных символов. Поскольку это нейтрально, пункт 39электронам присвоен атомный номер 39. Спасибо, количество протонов Количество нейтронов 89 Атомный символ корпоративный и число 29. Массовое число 29, это 35 Это атомный номер 29. Число протонов 29. Число электронов 29 до н.э. 98. Итак, число 43. В этом числе 43 электрона. Количество нейтронов было -43. Ведущий элемент не имеет ни прошлого числа, ни числа дам, поэтому символ называется Фиби. Есть два числа: количество частиц и количество электронных частиц. Это 1 24, потому что количество нейтронов не равно 7. Итальянский символ элемента — это элемент. Маска номер 81 — это атомный номер mhm число протонов восемь. Количество электронов и количество нейтронов одинаковы. Когда водород будет равен нулю на вашем переводе в массовом числе, символ элемента будет для него. Номер совпадает с атомным номером. Тогда это будет состояние с нулевым числом нейтронов. Атомный номер водорода равен 1. Последнее число также является числом. Это хорошо сделано. Количество электронов. Прошедшему числу присваивается углеродное число. Имеется атомный номер протонов Число нейтронов 6, 12-. Это символ Азота в 70-х годах. Есть ряд протонов и электронов. Число семь — это атомный номер. Семь — это прошлое # 1414 -7. Указано число нейтронов. Это варварская шестерка дается в США. Это количество электронов в числах. Количество протонов и количество пользователей — 137. Атомный номер — 20. 40-20 — это количество протонов, а 20 — это количество нейтронов. С этим связано количество электронов. Вчера количество протонов и количество электронов в элементе было таким же. Количество нейтронов было 28. Число 18 — это атомный номер, а полицейское — число 18. Было 18 электронов и 18 протонов. Количество радиоактивных частиц. Символ элемента – магний. Есть 12 программ, это то, что ему дали.
Номер совпадает с атомным номером. Тогда это будет состояние с нулевым числом нейтронов. Атомный номер водорода равен 1. Последнее число также является числом. Это хорошо сделано. Количество электронов. Прошедшему числу присваивается углеродное число. Имеется атомный номер протонов Число нейтронов 6, 12-. Это символ Азота в 70-х годах. Есть ряд протонов и электронов. Число семь — это атомный номер. Семь — это прошлое # 1414 -7. Указано число нейтронов. Это варварская шестерка дается в США. Это количество электронов в числах. Количество протонов и количество пользователей — 137. Атомный номер — 20. 40-20 — это количество протонов, а 20 — это количество нейтронов. С этим связано количество электронов. Вчера количество протонов и количество электронов в элементе было таким же. Количество нейтронов было 28. Число 18 — это атомный номер, а полицейское — число 18. Было 18 электронов и 18 протонов. Количество радиоактивных частиц. Символ элемента – магний. Есть 12 программ, это то, что ему дали.