Гидроксид стронция — хим. свойства и получение CHEMEGE.RU
Гидроксид стронция Sr(OH)2 — неорганическое соединение. Белый, плавится без разложения, при дальнейшем нагревании разлагается. Умеренно растворяется в воде. Проявляет основные свойства.
Относительная молекулярная масса Mr = 121,63; относительная плотность для тв. и ж. состояния d = 3,625; tпл = 460º C.
1. Гидроксид стронция получают в результате взаимодействия насыщенного нитрата стронция и насыщенного гидроксида натрия при комнатной температуре, на выходе образуется нитрат натрия и гидроксид стронция:
Sr(NO3)2 + 2NaOH = Sr(OH)2↓ + 2NaNO3
2. При взаимодействии стронция с
Sr + 2H2O = Sr(OH)2↓ + H2↑
3. Оксид стронция при взаимодействии с водой при комнатой температуре образует гидроксид стронция:
Оксид стронция при взаимодействии с водой при комнатой температуре образует гидроксид стронция:
SrO + H2O = Sr(OH)2
Качественная реакция на гидроксид стронция — окрашивание фенолфталеина в малиновый цвет.
1. Гидроксид стронция взаимодействует со сложными веществами:
1.1. Гидроксид стронция реагирует с кислотами:
1.1.1. В результате реакции между гидроксидом стронция и разбавленной соляной кислотой образуется хлорид стронция и вода:
Sr(OH)2 + 2HCl = SrCl2 + 2H2O
1.1.2. Гидроксид стронция взаимодействует с концентрированной серной кислотой, образуя сульфат стронция и воду:
Sr(OH)2 + H2SO4 = SrSO4↓ + 2H2O
1. 1.3. В результате взаимодействия гидроксида стронция и разбавленной фосфорной кислоты образуется фосфат стронция и вода:
1.3. В результате взаимодействия гидроксида стронция и разбавленной фосфорной кислоты образуется фосфат стронция и вода:
3Sr(OH)2 + 2H3PO4 = Sr3(PO4)2↓ + 6H2O,
1.1.4. С насыщенным и холодным гидроксидом стронция реагирует горячая сероводородная кислота, образуя сульфид стронция и воду:
Sr(OH)2 + H2S = SrS↓ + 2H2O
1.1.5. Гидроксид стронция вступает во взаимодействие с концентрированной плавиковой кислотой с образованием фторида стронция и воды:
Sr(OH)2 + 2HF = SrF2↓ + 2H2O
1. 2. Гидроксид стронция взаимодействует с оксидами:
2. Гидроксид стронция взаимодействует с оксидами:
1.2.1. В результате взаимодействия гидроксида стронция и углекислого газа образуется карбонат стронция и вода:
Sr(OH)2 + СO2 = SrСO3 + H2O,
если с углекислым газом реагирует карбонат стронция в виде суспензии, то образуется гидрокарбонат стронция в растворе:
Sr(OH)2 + 2СO2 = Sr(HСO3)2
1.2.2. Гидроксид стронция вступает в реакцию с оксидом серы (IV), образуя на выходе сульфит стронция и воду:
Sr(OH)2 + SO2 = SrSO3 + H2O,
если с оксидом серы (IV) взаимодействует гидроксид стронция в виде суспензии, то на выходе происходит образование гидросульфита стронция
Sr(OH)2 + 2SO2 = Sr(HSO3)2
2. Гидроксид стронция разлагается при температуре 520 — 580º С, образуя на выходе оксид стронция и воду:
Гидроксид стронция разлагается при температуре 520 — 580º С, образуя на выходе оксид стронция и воду:
Sr(OH)2 = SrO + H2O
404 — Документ не найден
Документ не найден.
Пожалуйста, воспользуйтесь поиском или нижним меню.
Обжимные фитинги муфты, штуцера, адаптеры, уголки, кресты, тройники Резьбовые фитинги ниппели, муфты, тройники.. Приварные фитинги VCR, VCO, БРС
Фитинги
Запорная арматура Игольчатые вентили Шаровые краны Мембранные клапаны Сильфонные вентили Манометрические вентили
Клапаны
Баллонные
Общепромышленные
Высокоточные
До себя
Для чистых сред
Двухступенчатые
Регуляторы давления
Фильтры и фильтрующие элементы
фильтры финишной очистки
Промышленные фильтры
Микронные фильтры
Фильтры
Калиброванные бесшовные трубки
Инструмент для труб
полимерные трубки
зажимы и крепления для труб
гибкие рукава
Зажимы, трубы, рукава и аксессуары
Изделия собственного производства газоразрядные рампы атмосферные испарители газовые шкафы устройства отбора пробы
Изделия
Поточные нагреватели жидкостей и газов
Нагреватели
Расходомеры Ротаметры
Средства контроля расхода
Уровнемеры Смотровые стёкла
Средства измерения уровня
Манометры
Преобразователи давления
Реле давления
Разделительные мембраны
Средства измерения давления
Средства измерения температуры
Анализаторы газов
Алюминиевые газовые баллоны:
— Одногорловые
— Двугорловые
Баллоны и Сосуды
Кабельные вводы
Тест на химические свойства оснований и амфотерных гидроксидов.

Задание №1
Из приведенного списка соединений выберите основные гидроксиды. Число верных ответов может быть любым.
- 1. Be(OH)2
- 2. Al(OH)3
- 3. Sr(OH)2
- 4. Zn(OH)2
- 5. Cr(OH)3
Задание №2
Из приведенного списка соединений выберите амфотерные гидроксиды. Число верных ответов может быть любым.
- 1. Cr(OH)2
- 2. Cr(OH)3
- 3. Be(OH)2
- 4. Fe(OH)3
- 5. Fe(OH)2
Задание №3
Из приведенного списка соединений выберите щелочи. Число верных ответов может быть любым.
- 1. Zn(OH)2
- 2. RbOH
- 3. CsOH
- 4. Sr(OH)2
- 5. KOH
Задание №4
Из приведенного списка соединений выберите основные гидроксиды. Число верных ответов может быть любым.
- 1.
 Mg(OH)2
Mg(OH)2 - 2. Be(OH)2
- 3. Cu(OH)2
- 4. Pb(OH)2
- 5. Sr(OH)2
Задание №5
Из приведенного списка соединений выберите амфотерные гидроксиды. Число верных ответов может быть любым.
- 1. CrO2(OH)2
- 2. Fe(OH)2
- 3. Cr(OH)3
- 4. Al(OH)3
- 5. Ca(OH)2
Задание №6
Из приведенного списка соединений выберите щелочи. Число верных ответов может быть любым.
- 1. Pb(OH)2
- 2. Mn(OH)2
- 3. Ca(OH)2
- 4. Fe(OH)2
- 5. Sr(OH)2
Задание №7
Из приведенного списка соединений выберите основные гидроксиды. Число верных ответов может быть любым.
- 1. NaOH
- 2. CsOH
- 3. Cr(OH)2
- 4. Zn(OH)2
- 5.
 Cu(OH)2
Cu(OH)2
Задание №8
Из приведенного списка гидроксидов выберите два таких, которые разлагаются при нагревании
- 1. RbOH
- 2. Sr(OH)2
- 3. Cr(OH)2
- 4. Ba(OH)2
- 5. Cu(OH)2
Задание №9
Из приведенного списка гидроксидов выберите два таких, которые не разлагаются при нагревании
- 1. Fe(OH)2
- 2. Be(OH)2
- 3. RbOH
- 4. CsOH
- 5. Zn(OH)2
Задание №10
Из приведенного списка гидроксидов выберите два таких, которые разлагаются при нагревании
- 1. NaOH
- 2. Cr(OH)3
- 3. Sr(OH)2
- 4. Ba(OH)2
- 5. Al(OH)3
Задание №11
Из приведенного списка гидроксидов выберите два таких, которые не разлагаются при нагревании
- 1. Zn(OH)2
- 2.
 Ba(OH)2
Ba(OH)2 - 3. Mn(OH)2
- 4. Sr(OH)2
- 5. Be(OH)2
Задание №12
Из приведенного списка гидроксидов выберите два таких, которые разлагаются при нагревании
- 1. NaOH
- 2. Fe(OH)2
- 3. Ba(OH)2
- 4. Mg(OH)2
- 5. Sr(OH)2
Задание №13
Из приведенного списка гидроксидов выберите два таких, которые не разлагаются при нагревании
- 1. KOH
- 2. Cr(OH)2
- 3. Ba(OH)2
- 4. Cu(OH)2
- 5. Fe(OH)3
Задание №14
Из приведенного списка гидроксидов выберите два таких, которые разлагаются при нагревании
- 1. Sr(OH)2
- 2. Ba(OH)2
- 3. Al(OH)3
- 4. CsOH
- 5. Fe(OH)3
Задание №15
Из приведенного списка гидроксидов выберите такой, который разлагается при нагревании
- 1.
 RbOH
RbOH - 2. Ba(OH)2
- 3. CsOH
- 4. Sr(OH)2
- 5. Zn(OH)2
В поле ответа введите уравнение реакции, используя в качестве разделителя левой и правой частей знак равенства.
РешениеОтвет: Zn(OH)2 = ZnO + H2O
Задание №16
Из приведенного списка гидроксидов выберите такой, который разлагается при нагревании
- 1. CsOH
- 2. Ba(OH)2
- 3. KOH
- 4. Sr(OH)2
- 5. Al(OH)3
В поле ответа введите уравнение реакции, используя в качестве разделителя левой и правой частей знак равенства.
РешениеОтвет: 2Al(OH)3 = Al2O3 + 3H2O
Задание №17
Из приведенного списка солей выберите две таких, с которыми будет взаимодействовать гидроксид лития.
1) нитрат свинца
2) бромид калия
3) фосфат натрия
4) хлорид натрия
5) йодид рубидия
РешениеЗадание №18
Из приведенного списка солей выберите две таких, с которыми будет взаимодействовать гидроксид натрия.
1) фторид калия
2) сульфат цинка
3) нитрат аммония
4) сульфат бария
5) хлорид серебра
РешениеЗадание №19
Из приведенного списка солей выберите две таких, с которыми будет взаимодействовать гидроксид кальция.
1) карбонат цезия
2) нитрат бария
3) бромид натрия
4) сульфат аммония
5) йодид свинца
РешениеЗадание №20
Из приведенного списка солей выберите две таких, с которыми будет взаимодействовать гидроксид бария.
1) хлорид аммония
2) карбонат калия
3) сульфат стронция
4) нитрат калия
5) бромид лития
РешениеЗадание №21
Из приведенного списка солей выберите две таких, с которыми будет взаимодействовать гидроксид цезия.
1) нитрат железа(II)
2) хлорид рубидия
3) карбонат калия
4) карбонат аммония
5) нитрат натрия
РешениеЗадание №22
Из приведенного списка солей выберите две таких, с которыми не будет взаимодействовать гидроксид рубидия.
1) нитрат калия
2) нитрат бария
3) нитрат магния
4) нитрат аммония
5) нитрат свинца
РешениеЗадание №23
Из приведенного списка солей выберите две таких, с которыми не будет взаимодействовать гидроксид стронция.
1) сульфат натрия
2) фосфат калия
3) фторид натрия
4) хлорид натрия
5) йодид цезия
РешениеЗадание №24
Из приведенного списка солей выберите две таких, с которыми не будет взаимодействовать гидроксид натрия.
1) бромид аммония
2) фторид кальция
3) нитрат аммония
4) силикат цинка
5) хлорид магния
РешениеЗадание №25
Из приведенного списка солей выберите две таких, с которыми не будет взаимодействовать гидроксид бария.
1) сульфат меди
2) карбонат свинца
3) сульфат аммония
4) карбонат натрия
5) сульфат стронция
РешениеЗадание №26
Из приведенного списка солей выберите две такие, с которыми не будет взаимодействовать гидроксид калия.
1) силикат натрия
2) сульфид железа(II)
3) сульфид аммония
4) нитрат свинца
5) нитрат цинка
РешениеЗадание №27
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с углекислым газом.
1) едкий натр
2) гидроксид железа(III)
3) гидроксид алюминия(III)
4) гашеная известь
5) гидроксид хрома(III)
РешениеЗадание №28
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с оксидом натрия.
1) гидроксид лития
2) едкое кали
3) гидроксид алюминия
4) гидроксид стронция
5) гидроксид цинка
РешениеЗадание №29
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с оксидом алюминия.
1) гидроксид цезия
2) гидроксид бериллия
3) гидроксид свинца
4) гидроксид бария
5) гидроксид цинка
РешениеЗадание №30
Из приведенного списка гидроксидов выберите два таких, которые не взаимодействуют с оксидом кремния.
1) гидроксид железа (II)
2) гидроксид рубидия
3) едкий натр
4) гидроксид хрома(III)
5) гашеная известь
РешениеЗадание №31
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с оксидом кальция.
1) гидроксид хрома(II)
2) гидроксид хрома(III)
3) гидроксид железа(II)
4) гидроксид железа(III)
5) гидроксид натрия
РешениеЗадание №32
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с оксидом цинка.
- 1. NaOH
- 2. Pb(OH)2
- 3. RbOH
- 4. Mn(OH)2
- 5. Cu(OH)2
Задание №33
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с оксидом углерода (IV).
- 1. NaOH
- 2. CsOH
- 3. Cr(OH)3
- 4. Al(OH)3
- 5. Fe(OH)3
Задание №34
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с оксидом бария.
- 1. Ba(OH)2
- 2. Al(OH)3
- 3. Sr(OH)2
- 4. Mn(OH)2
- 5. Cr(OH)3
Задание №35
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с оксидом хрома(III).
- 1. Fe(OH)2
- 2. Be(OH)2
- 3. RbOH
- 4. CsOH
- 5. Zn(OH)2
Задание №36
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с оксидом кремния.
- 1. Ca(OH)2
- 2. Cr(OH)2
- 3. Sr(OH)2
- 4. Be(OH)2
- 5. Cu(OH)2
Задание №37
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с едким кали.
- 1. Pb(OH)2
- 2. KOH
- 3. Cr(OH)3
- 4. Ca(OH)2
- 5. Sr(OH)2
Задание №38
Из приведенного списка гидроксидов выберите два таких, которые не взаимодействуют с едким натром.
- 1. Cr(OH)2
- 2. Fe(OH)2
- 3. Cr(OH)3
- 4. Al(OH)3
- 5. Be(OH)2
Задание №39
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с гашеной известью.
- 1. Cr(OH)2
- 2. Cr(OH)3
- 3. Be(OH)2
- 4. Cu(OH)2
- 5. Fe(OH)2
Задание №40
Из приведенного списка гидроксидов выберите два таких, которые не взаимодействуют с гидроксидом стронция.
- 1. Be(OH)2
- 2. Al(OH)3
- 3. Sr(OH)2
- 4. Zn(OH)2
- 5. Cr(OH)2
Задание №41
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с гидроксидом рубидия.
- 1. Pb(OH)2
- 2. Mn(OH)2
- 3. Ca(OH)2
- 4.
 Fe(OH)3
Fe(OH)3 - 5. Sr(OH)2
Задание №42
Из приведенного списка гидроксидов выберите два таких, которые не взаимодействуют с гидроксидом алюминия.
- 1. Mn(OH)2
- 2. Be(OH)2
- 3. Ca(OH)2
- 4. Ba(OH)2
- 5. Sr(OH)2
Задание №43
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с гидроксидом цинка.
- 1. Zn(OH)2
- 2. Be(OH)2
- 3. CsOH
- 4. Pb(OH)2
- 5. KOH
Задание №44
Из приведенного списка гидроксидов выберите два таких, которые не взаимодействуют с гидроксидом хрома(III).
- 1. Fe(OH)2
- 2. KOH
- 3. Cr(OH)3
- 4. Ca(OH)2
- 5. Sr(OH)2
Задание №45
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с гидроксидом железа(III).
- 1. Pb(OH)2
- 2. Mn(OH)2
- 3. Ca(OH)2
- 4. Fe(OH)2
- 5. Sr(OH)2
Задание №46
Из приведенного списка гидроксидов выберите два таких, которые не взаимодействуют с гидроксидом свинца.
- 1. Cr(OH)2
- 2. Ca(OH)2
- 3. Ba(OH)2
- 4. Al(OH)3
- 5. LiOH
Задание №47
Из приведенного списка гидроксидов выберите два таких, которые не взаимодействуют с кремниевой кислотой.
- 1. LiOH
- 2. Sr(OH)2
- 3. Cr(OH)2
- 4. Ba(OH)2
- 5. Cu(OH)2
Задание №48
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с сернистой кислотой.
- 1. Fe(OH)2
- 2. Be(OH)2
- 3. RbOH
- 4. CsOH
- 5.
 Zn(OH)2
Zn(OH)2
Задание №49
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с кремниевой кислотой.
- 1. LiOH
- 2. Cr(OH)3
- 3. Sr(OH)2
- 4. Be(OH)2
- 5. Al(OH)3
Задание №50
Из приведенного списка гидроксидов выберите два таких, которые не взаимодействуют с сероводородной кислотой.
- 1. NaOH
- 2. Al(OH)3
- 3. Ba(OH)2
- 4. Cr(OH)3
- 5. Sr(OH)2
Задание №51
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с кремнием.
- 1. Sr(OH)2
- 2. Be(OH)2
- 3. Al(OH)3
- 4. CsOH
- 5. Fe(OH)3
Задание №52
Из приведенного списка гидроксидов выберите два таких, которые не взаимодействуют с серой.
- 1. NaOH
- 2. Mn(OH)2
- 3. RbOH
- 4. Cr(OH)3
- 5. Ca(OH)2
Задание №53
Из приведенного списка гидроксидов выберите два таких, которые не взаимодействуют с кремнием.
- 1. RbOH
- 2. Ba(OH)2
- 3. Be(OH)2
- 4. Sr(OH)2
- 5. Zn(OH)2
Задание №54
Из приведенного списка гидроксидов выберите два таких, которые взаимодействуют с фосфором.
- 1. Mg(OH)2
- 2. Ba(OH)2
- 3. Cu(OH)2
- 4. Sr(OH)2
- 5. Be(OH)2
Задание №55
Из приведенного списка гидроксидов выберите два таких, которые не взаимодействуют с фосфором.
- 1. Ca(OH)2
- 2. Cu(OH)2
- 3. Ba(OH)2
- 4. Al(OH)3
- 5. LiOH
Задание №56
Из приведенного перечня выберите две пары реагентов, между которыми возможна реакция
- 1.
 Cr + NaOH
Cr + NaOH - 2. Si + CsOH
- 3. Fe + NaOH
- 4. I2 + Ba(OH)2
- 5. C + KOH
Задание №57
Из приведенного списка гидроксидов выберите два таких, которые не взаимодействуют с йодом.
- 1. NaOH
- 2. Pb(OH)2
- 3. RbOH
- 4. Fe(OH)3
- 5. CsOH
Задание №58
Из предложенного перечня выберите две пары реагентов, между которыми возможна реакция
- 1. Al + Zn(OH)2
- 2. Cl2 + Al(OH)3
- 3. P + NaOH
- 4. S + Ba(OH)2
- 5. Br2 + Cu(OH)2
Задание №59
Из приведенного перечня простых веществ выберите два таких, которые могут реагировать с концентрированным водным раствором гидроксида бария:
- 1. H2
- 2. Cl2
- 3. N2
- 4. O2
- 5.
 I2
I2
Задание №60
Из приведенного перечня простых веществ выберите два таких, которые могут реагировать с концентрированным водным раствором гидроксида калия:
- 1. Al
- 2. Cu
- 3. P
- 4. Cr
- 5. C
Задание №61
Из приведенного перечня простых веществ выберите два таких, которые могут реагировать с концентрированным водным раствором гидроксида натрия:
- 1. Fe
- 2. Cu
- 3. S
- 4. C
- 5. Zn
Задание №62
Из предложенного перечня выберите две пары реагентов, между которыми возможна реакция:
- 1. Cu + NaOH
- 2. Cl2 + Cu(OH)2
- 3. C + KOH
- 4. Si + Ba(OH)2
- 5. Zn + Sr(OH)2
Задание №63
Из предложенного перечня выберите две пары реагентов, между которыми возможна реакция:
- 1. Al + Fe(OH)2
- 2.
 I2 + RbOH
I2 + RbOH - 3. Cr + NaOH
- 4. N2 + KOH
- 5. P + CsOH
Задание №64
Из приведенного списка гидроксидов выберите такой, который взаимодействует с цинком.
- 1. NaOH
- 2. Fe(OH)2
- 3. Cr(OH)2
- 4. Zn(OH)2
- 5. Cu(OH)2
В поле ответа введите уравнение реакции водного раствора данного гидроксида с цинком. В качестве разделителя левой и правой частей используйте знак равенства (=).
РешениеОтвет: Zn + 2NaOH + 2H2O = Na2[Zn(OH)4] + H2
Задание №65
Установите соответствие между формулой/названием гидроксида и набором реагентов, с каждым из которых он может взаимодействовать.
| ГИДРОКСИД | РЕАГЕНТЫ |
А) гидроксид цинка Б) едкий натр В) гидроксид хрома(III) | 1) алюминий, хлор, серная кислота 2) гидроксид цезия, соляная кислота, оксид натрия 3) вода, кислород, сера 4) азотная кислота, оксид серы(VI), вода |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Задание №66
Установите соответствие между формулой гидроксида и набором реагентов, с каждым из которых он может взаимодействовать.
| ГИДРОКСИД | РЕАГЕНТЫ |
А) KOH Б) Al(OH)3 В) Ba(OH)2 | 1) Na2CO3, Br2, H2O 2) HNO3, P, HI 3) NaOH, HBr, K2O 4) HNO3, Fe(OH)2, KOH |
Запишите в таблицу выбранные цифры под соответствующими буквами.
РешениеЗадание №67
Установите соответствие между формулой гидроксида и набором реагентов, с каждым из которых он может взаимодействовать.
| ГИДРОКСИД | РЕАГЕНТЫ |
А) гидроксид меди Б) гашеная известь В) гидроксид цинка | 1) сульфат бария, нитрат аммония, карбонат свинца 2) серная кислота, сера, хлорид натрия 3) вода, кислород, кремний 4) азотная кислота, соляная кислота, оксид серы(VI) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Задание №68
Установите соответствие между формулой гидроксида и набором реагентов, с каждым из которых он может взаимодействовать.
| ГИДРОКСИД | РЕАГЕНТЫ |
А) LiOH Б) Al(OH)3 В) Fe(OH)3 | 1) фторид натрия, бром, кремний 2) гидроксид натрия, гашеная известь, вода 3) оксид бария, гидроксид калия, серная кислота 4) цинк, фосфор, нитрат калия |
Запишите в таблицу выбранные цифры под соответствующими буквами.
РешениеЗадание №69
Цинк сплавили со гидроксидом натрия. Впишите в поле ответа уравнение проведенной реакции, используя в качестве разделителя левой и правой частей знак равенства.
РешениеОтвет: Zn + 2NaOH = Na2ZnO2 + H2
Задание №70
Хлор пропустили через холодный раствор гидроксида калия. В случае если реакция протекает запишите ее уравнение. Если реакция не протекает введите в поле ответа знак минус (-).
В случае если реакция протекает запишите ее уравнение. Если реакция не протекает введите в поле ответа знак минус (-).
Ответ: Cl2 + 2KOH = KClO + KCl + H2O
Задание №71
Серу подвергли совместному нагреванию с избытком концентрированного водного раствора гидроксида натрия. В случае если реакция протекает впишите в поле ответа уравнение проведенной реакции, используя в качестве разделителя левой и правой частей знак равенства. Если реакция не протекает введите в поле ответа знак минус (-).
РешениеОтвет: 3S + 6NaOH = 2Na2S + Na2SO3 + 3H2O
Задание №72
Кремний растворили в водном растворе гидроксида натрия. В случае если реакция протекает впишите в поле ответа уравнение проведенной реакции, используя в качестве разделителя левой и правой частей знак равенства. Если реакция не протекает введите в поле ответа знак минус (-).
РешениеОтвет: Si + 2NaOH + H2O = 2H2 + Na2SiO3
Задание №73
Алюминий растворили при нагревании в растворе гидроксида рубидия. Впишите в поле ответа уравнение проведенной реакции, используя в качестве разделителя левой и правой частей знак равенства.
Впишите в поле ответа уравнение проведенной реакции, используя в качестве разделителя левой и правой частей знак равенства.
Ответ: 2Al + 2RbOH + 6H2O = 2Rb[Al(OH)4] + 3H2
Задание №74
Хлор пропустили через горячий раствор гидроксида натрия. В случае если реакция протекает впишите в поле ответа уравнение проведенной реакции, используя в качестве разделителя левой и правой частей знак равенства. Если реакция не протекает введите в поле ответа знак минус (-).
РешениеОтвет: 3Cl2 + 6NaOH = NaClO3 + 5NaCl + 3H2O
Задание №75
Через известковую воду пропустили углекислый газ в результате чего наблюдали ее помутнение. Впишите в поле ответа уравнение проведенной реакции, используя в качестве разделителя левой и правой частей знак равенства.
РешениеОтвет: Ca(OH)2 + CO2 = CaCO3 + H2O
Задание №76
Через известковую воду пропустили некоторое количество углекислого газа, в результате чего был получен прозрачный раствор. Впишите в поле ответа уравнение проведенной реакции, используя в качестве разделителя левой и правой частей знак равенства.
Впишите в поле ответа уравнение проведенной реакции, используя в качестве разделителя левой и правой частей знак равенства.
Ответ: Ca(OH)2 + 2CO2 = Ca(HCO3)2
Задание №77
Определите, протекает ли между данными веществами обменная реакция. Если нет, то запишите в ответ символ (-), если да, то целое уравнение с коэффициентами. Сульфат калия + гидроксид бария
РешениеОтвет: K2SO4 + Ba(OH)2 = BaSO4 + 2KOH
Задание №78
Определите, протекает ли между данными веществами обменная реакция. Если нет, то запишите в ответ символ (-), если да, то целое уравнение с коэффициентами. Гидроксид свинца + кремниевая кислота
РешениеЗадание №79
Определите, протекает ли между данными веществами обменная реакция. Если нет, то запишите в ответ символ (-), если да, то целое уравнение с коэффициентами. Гидроксид натрия + нитрат железа(III)
РешениеОтвет: 3NaOH + Fe(NO3)3 = Fe(OH)3 + 3NaNO3
Задание №80
К смеси порошкообразных гидроксида бария и хлорида аммония добавили каплю воды. Впишите в поле ответа уравнение проведенной реакции, используя в качестве разделителя левой и правой частей знак равенства.
Впишите в поле ответа уравнение проведенной реакции, используя в качестве разделителя левой и правой частей знак равенства.
Ответ: Ba(OH)2 + 2NH4Cl = BaCl2 + 2NH3 + 2H2O
Задание №81
Оксид алюминия прокалили совместно с твердым гидроксидом натрия. Если реакция протекает, впишите ее в поле ответа, используя в качестве разделителя левой и правой частей знак равенства. Если реакция не протекает введите в поле ответа знак минус (-)
РешениеОтвет: 2NaOH + Al2O3 = 2NaAlO2 + H2O
Задание №82
Оксид алюминия поместили в концентрированный водный раствор гидроксида калия и подвергли нагреванию. Если реакция протекает, впишите ее в поле ответа, используя в качестве разделителя левой и правой частей знак равенства. Если реакция не протекает введите в поле ответа знак минус (-)
РешениеОтвет: 2KOH + Al2O3 + 3H2O = 2K[Al(OH)4]
Задание №83
Твердый гидроксид калия сплавили с гидроксидом цинка. Если реакция протекает впишите ее уравнение в поле ответа, используя в качестве разделителя левой и правой частей знак равенства. Если реакция не протекает введите в поле ответа знак минус (-)
Если реакция протекает впишите ее уравнение в поле ответа, используя в качестве разделителя левой и правой частей знак равенства. Если реакция не протекает введите в поле ответа знак минус (-)
Ответ: 2KOH + Zn(OH)2 = K2ZnO2 + 2H2O
Задание №84
Сероводород пропустили через водную взвесь гидроксида алюминия. Если реакция протекает впишите ее уравнение в поле ответа, используя в качестве разделителя левой и правой частей знак равенства. Если реакция не протекает введите в поле ответа знак минус (-)
РешениеЗадание №85
Углекислый газ пропустили через водную взвесь гидроксида алюминия. Если реакция протекает впишите ее уравнение в поле ответа, используя в качестве разделителя левой и правой частей знак равенства. Если реакция не протекает введите в поле ответа знак минус (-)
РешениеЗадание №86
Вычислите массу осадка, полученную при взаимодействии избытка серной кислоты и 30 мл 10% раствора гидроксида бария (плотность 1,1 г/мл). Ответ укажите в граммах и округлите с точностью до десятых.
Ответ укажите в граммах и округлите с точностью до десятых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №87
Рассчитайте объем 5% раствора соляной кислоты (плотность 1,05 г/см3), необходимый для полной нейтрализации 14 г едкого кали. Ответ укажите в миллилитрах и округлите до десятых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №88
Определите массу воды, полученную при термическом разложении смеси 1,5 моль гидроксида алюминия и 49 г гидроксида меди. Ответ укажите в граммах округлите с точностью до десятых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №89
Вычислите массу твердого остатка, полученного при прокаливании 214 г гидроксида железа(III). Ответ укажите в граммах и округлите с точностью до целых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №90
Рассчитайте массовую долю бромата калия в растворе, полученном при полном растворении 8 г брома в 92 г горячего концентрированного раствора гидроксида калия. Ответ укажите в процентах и округлите до сотых.
Ответ укажите в процентах и округлите до сотых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №91
Навеску порошка кремния массой 3,5 г растворили при нагревании в избытке гидроксида натрия. Определите массу осадка, который можно получить при подкислении данного раствора соляной кислотой. Ответ укажите в граммах и округлите до сотых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №92
Смесь гидроксидов алюминия и магния имеет массу 100 г. Определите массовую долю гидроксида магния в исходной смеси, если для растворения гидроксида алюминия потребовалось 140 г 10% раствора гидроксида калия. Ответ укажите в процентах и округлите до десятых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №93
Навеску гидроксида магния прокалили до постоянной массы. Определите массу азотной кислоты, необходимой для растворения твердого остатка, если при прокаливании выделилось 4,5 г паров воды. Ответ укажите в граммах и округлите до десятых.
Ответ укажите в граммах и округлите до десятых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №94
При растворении навески кремния в избытке гидроксида натрия выделился водород. Определите массу исходной навески, если выделившимся газом можно восстановить 20 г оксида меди(II). Ответ укажите в граммах и округлите до десятых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №95
Рассчитайте объем хлора, который может поглотить горячий раствор, содержащий 10 г гидроксида натрия и 7 г гидроксида калия. Ответ укажите в литрах и округлите до десятых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №96
Вычислите массу хлорида аммония, необходимую для получения 112 л аммиака по реакции с гидроксидом бария. Ответ укажите в граммах и округлите до десятых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №97
Определите массу осадка, оставшегося после реакции 39 г гидроксида алюминия и 100 мл 10% раствора гидроксида натрия (плотность 1,1 г/мл). Ответ укажите в граммах и округлите до сотых.
Ответ укажите в граммах и округлите до сотых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №98
Рассчитайте объем углекислого газа, необходимого для полного осаждения карбоната бария из 0,2 л 15% раствора его гидроксида (плотность 1,12 г/см3). Ответ укажите в литрах и округлите до десятых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №99
Какую массу воды можно получить при прокаливании образца гидроксида железа(III) массой 59,5 г, содержащего 10% песка. Ответ укажите в литрах и округлите до десятых.
В поле ответа введите только число (без единиц измерения).
РешениеЗадание №100
При полном растворении навески серы массой 9,6 г в избытке раствора гидроксида калия получено 100 г раствора. Рассчитайте массовую долю сульфида калия в получившемся растворе. Ответ укажите в процентах и округлите до целых.
В поле ответа введите только число (без единиц измерения).
Молекулярная масса Sr (OH) 2
Молярная масса of Sr (OH) 2 = 121,63468 г / моль
Это соединение также известно как гидроксид стронция.
Перевести граммы Sr (OH) 2 в моль или моль Sr (OH) 2 в граммы
Расчет молекулярной массы:
87,62 + (15,9994 + 1,00794) * 2
| Элемент | Условное обозначение | Атомная масса | Количество атомов | Массовый процент |
| Стронций | Sr | 87.62 | 1 | 72,035% |
| Водород | H | 1,00794 | 2 | 1,657% |
| Кислород | O | 15,9994 | 2 | 26,307% |
В химии вес формулы — это величина, вычисляемая путем умножения атомного веса (в единицах атомной массы) каждого элемента в химической формуле на количество атомов этого элемента, присутствующего в формуле, с последующим сложением всех этих продуктов вместе.
Определение молярной массы начинается с единиц граммов на моль (г / моль). При расчете молекулярной массы химического соединения он говорит нам, сколько граммов содержится в одном моль этого вещества. Вес формулы — это просто вес в атомных единицах массы всех атомов в данной формуле.
Если формула, используемая при расчете молярной массы, является молекулярной формулой, вычисленная формула веса является молекулярной массой. Весовой процент любого атома или группы атомов в соединении можно вычислить, разделив общий вес атома (или группы атомов) в формуле на вес формулы и умножив на 100.
Атомные веса, используемые на этом сайте, получены от NIST, Национального института стандартов и технологий. Мы используем самые распространенные изотопы. Вот как рассчитать молярную массу (среднюю молекулярную массу), которая основана на изотропно взвешенных средних. Это не то же самое, что молекулярная масса, которая представляет собой массу одной молекулы четко определенных изотопов.
Формула веса особенно полезна при определении относительного веса реагентов и продуктов в химической реакции. Эти относительные веса, вычисленные по химическому уравнению, иногда называют весами по уравнениям.
Используя химическую формулу соединения и периодическую таблицу элементов, мы можем сложить атомные веса и вычислить молекулярную массу вещества.
Часто на этом сайте просят перевести граммы в моль. Чтобы выполнить этот расчет, вы должны знать, какое вещество вы пытаетесь преобразовать.Причина в том, что на конверсию влияет молярная масса вещества. Этот сайт объясняет, как найти молярную массу.
Синтез в однородной фазе при низкой температуре и применение для артефактов культурного наследия
CILIBERTO et al. Наночастицы Sr (OH)
2
: синтез и применение для культурного наследия 141
проникновения наночастиц внутрь штукатурного слоя и
оценивают как консолидирующие, так и защитные характеристики.
5 Выводы
Гидроксид стронция, растворимое неорганическое соединение
фунта, был синтезирован в форме наночастиц.
Это было достигнуто путем гомогенного осаждения с помощью метода солевого раствора
, синтетического пути, который начинается с
дешевого сырья, работает при низкой температуре и в водной среде
. В процессе не используются органические растворители
, специализированное оборудование, длительное время обработки или специальные химические вещества ex-
.Условия эксперимента для достижения высокой степени пересыщения
были установлены на уровне
60
◦
C с использованием
Sr (NO
3
)
2
и растворов NaOH 0,7 и 0,3 М соответственно.
Полученные наноразмеры состоят из гомо-
генных и почти округлых частиц правильной формы, которые имеют узкое распределение
и средний диаметр частиц около
30 нм.
Собранные экспериментальные данные и результаты, представленные в
этой работе, показывают, что нанокристаллы
Sr (OH)
2
могут представлять собой
хорошей альтернативой другим более традиционным методам защиты и консолидации культурных ценностей. артефакты наследия. На самом деле
артефакты наследия. На самом деле
опыты in vitro показали, что
Sr (OH)
2
способен реагировать как с атмосферным диоксидом углерода, так и с ионами сульфата
, возникающими из гипса.Таким образом, в качестве нового жертвенного материала его
можно использовать для окраски стен и реставрации штукатурки без проблем с токсичностью
, типичных для растворов гидроксида бария. Этот синтетический метод
, вероятно, может быть применен для получения
других наноразмерных частиц умеренно
/ хорошо растворимых
неорганических соединений и представляет собой инновационный технологический путь в химии наноматериалов.
ССЫЛКИ
1 X.Дуан, Ю. Хуанг, Р. Агарвал, К.М. Либер, Nature 421, 241
(2003)
2 M.S. Фюрер, Дж. Найгард, Л. Ши, М. Фореро, Ю.Г. Юн, M.S.C. Mazzoni,
H.J. Choi, Science 288, 494 (2000)
3 J.A. Стросчо, Д. Eigler, Science 254, 1319 (1991)
4 C.M. Либер, Дж. Лю, П. Шихан, Энджью. Chem. Int. Редактировать. Англ. 35, 687
Либер, Дж. Лю, П. Шихан, Энджью. Chem. Int. Редактировать. Англ. 35, 687
(1996)
5 A.I.Y. Ток, F.Y.C. Бой, X.L. Zhao, J. Mater. Процесс. Technol. 178, 270
(2006)
6 г.Scherer, Mezinarodni Konference o Naterovych Hmotach, 36th, Sec,
Czech Republic (2005), стр. 459
7 Т. Ватанабэ, Earozoru Kenkyu 21, 201 (2006)
8 С. Хамада, Ю. Кудо, К. Минигава, Bull. Chem. Soc. Япония. 63, 102
(1990)
9 E. Matijevic, P. Scheiner, J. Colloid Interf. Sci. 63, 509 (1978)
10 S. Hamada, E. Matijevic, J. Chem. Soc. Faraday Trans. 1 78, 2147
(1982)
11 Э. Матиевич, Acc. Chem. Res. 14, 22 (1981)
12 E.Матиевич, С. Чимас, Colloid Polym. Sci. 265, 155 (1987)
13 G.D. Rees, R. Evans-Gowing, S.J. Хаммонд, Б. Robinson, Langmuir
15, 1993 (1999)
14 Л. Перес-Македа, Л. Ван, Э. Матиевич, Лангмур 14, 4397 (1998)
15 Б. Сальвадори, Л. Дей, Лангмюр 17, 2371 (2001)
16 A. Nanni, L. Dei, Langmuir 19, 933 (2003)
Dei, Langmuir 19, 933 (2003)
17 B. Salvadori, G. Capitani, M. Mellini, L. Dei, J. Colloid Interf. Sci. 298,
487 (2006)
18 стр.Баглиони, М. Чеккато, Л. Деи, Р. Джорджи, К.В. Schettino, Langmuir 18,
8198 (2002)
19 R. Giorgi, C. Bozzi, L. Dei, C. Gabbiani, B. Ninham, P. Baglioni, Lang-
muir 21, 8495 (2005)
20 R. Giorgi, L. Dei, P. Baglioni, Stud. Консерв. 45, 154 (2000)
21 M. Ambrosi, L. Dei, R. Giorgi, C. Neto, P. Baglioni, Langmuir 17, 4251
(2001)
22 S. Li, H. Zhang, J Сюй Д. Ян, Матер. Lett. 59, 420 (2005)
23 Р. Дженкинс, Р.Л. Снайдер, Введение в порошковую рентгеновскую дифрактометрию
(Wiley, New York, 1996)
24 X. Wang, L. Andrews, J. Phys. Chem. A 109, 2782 (2005)
| Список растворимых веществ | |
| (Nh5) 2CO3 (КАРБОНАТ АММОНИЯ) | Растворимый |
| (Nh5) 2S (сульфид аммония) | Растворимый |
| (Nh5) 2SO4 (СУЛЬФАТ АММОНИЯ) | Растворимый |
| (Nh5) 3PO4 (фосфат аммония) | Растворимый |
| AgC2h4O2 (ацетат серебра) | Растворимый |
| AgClO3 (хлорат серебра) | Растворимый |
| AgClO4 (перхлорат серебра) | Растворимый |
| AgNO3 (нитрат серебра) | Растворимый |
| Al (NO3) 3 (нитрат алюминия) | Растворимый |
| Al2 (SO4) 3 (сульфат алюминия) | Растворимый |
| AlBr3 (бромид алюминия) | Растворимый |
| AlCl3 (хлорид алюминия) | Растворимый |
| AlCl3 (хлорид алюминия) | Растворимый |
| ацетат алюминия | Растворимый |
| Ba (C2h4O2) 2 | Растворимый |
| Ba (ClO4) 2 (ПЕРХЛОРАТ БАРИЯ) | Растворимый |
| Ba (NO3) 2 (нитрат бария) | Растворимый |
| Ba (OH) 2 (гидроксид бария) | Растворимый |
| BaBr2 (бромид бария) | Растворимый |
| BaCl2 (хлорид бария) | Растворимый |
| BaF2 (фторид бария) | Растворимый |
| BaI2 (йодид бария) | Растворимый |
| BaS (сульфид бария) | Растворимый |
| C12h32O11 (сахароза) | Растворимый |
| C2H7NO2 (ацетат аммония) | Растворимый |
| C4H6O4Ba (ацетат бария) | Растворимый |
| C4H6O4Ca (ацетат кальция) | Растворимый |
| Ca (C2h4O2) 2 | Растворимый |
| Ca (ClO4) 2 | Растворимый |
| Ca (NO3) 2 (нитрат кальция) | Растворимый |
| CaBr2 (бромид кальция) | Растворимый |
| CaCl2 (хлорид кальция) | Растворимый |
| CaCrO4 (ХРОМАТ КАЛЬЦИЯ) | Растворимый |
| CaI2 (йодид кальция) | Растворимый |
| CaSO4 (сульфат кальция) | Растворимый |
| Ch4OH (метанол) | Растворимый |
| Co (NO3) 2 (нитрат кобальта (II)) | Растворимый |
| CoBr2 (бромид кобальта) | Растворимый |
| CoCl2 (хлорид кобальта (II)) | Растворимый |
| CoSO4 | Растворимый |
| Cr (NO3) 2 | Растворимый |
| CsCl | Растворимый |
| CsOH (гидроксид цезия) | Растворимый |
| Cu (C2h4O2) 2 | Растворимый |
| Cu (Ch4COO) 2 (Ацетат меди (II)) | Растворимый |
| Cu (NO3) 2 (Нитрат меди (II)) | Растворимый |
| CuBr2 (бромид меди (II)) | Растворимый |
| CuCl (Хлорид меди (I)) | Растворимый |
| CuCl2 (хлорид меди) | Растворимый |
| CuSO4 (сульфат меди) | Растворимый |
| Fe (NO3) 2 (Нитрат железа (II)) | Растворимый |
| Fe (NO3) 3 (нитрат железа (III)) | Растворимый |
| FeCl2 (дихлорид железа) | Растворимый |
| FeCl3 (хлорид железа (III)) | Растворимый |
| FeSO4 (сульфат железа (II)) | Растворимый |
| h3SO3 (сернистая кислота) | Растворимый |
| h3SO4 (серная кислота) | Растворимый |
| h4PO4 (фосфорная кислота) | Растворимый |
| HBr (бромоводород) | Растворимый |
| HCl (соляная кислота) | Растворимый |
| HClO4 (хлорная кислота) | Растворимый |
| HCN (цианистый водород) | Растворимый |
| Hg2SO4 (сульфат ртути) | Растворимый |
| HgCl2 (хлорид ртути) | Растворимый |
| HgCl2 (хлорид ртути (II)) | Растворимый |
| HgSO4 (сульфат ртути (II)) | Растворимый |
| HNO3 (азотная кислота) | Растворимый |
| Ацетат железа (III) | Растворимый |
| K2CO3 (карбонат калия) | Растворимый |
| K2O (оксид калия) | Растворимый |
| K2S (сульфид калия) | Растворимый |
| K2SO3 (сульфит калия) | Растворимый |
| K2SO4 (СУЛЬФАТ КАЛИЯ) | Растворимый |
| K3PO4 (фосфат калия) | Растворимый |
| KBr (бромид калия) | Растворимый |
| KC2h4O2 (ацетат калия) | Растворимый |
| KCl (хлорид калия) | Растворимый |
| KClO3 (хлорат калия) | Растворимый |
| kclo4 (перхлорат калия) | Растворимый |
| KI (йодид калия) | Растворимый |
| KNO3 (нитрат калия) | Растворимый |
| КОН (гидроксид калия) | Растворимый |
| КСО4 | Растворимый |
| Li2CO3 (карбонат лития) | Растворимый |
| Li2S (сульфид лития) | Растворимый |
| Li2SO4 (сульфат лития) | Растворимый |
| Li3PO4 | Растворимый |
| LiBr (бромид лития) | Растворимый |
| LiCl (хлорид лития) | Растворимый |
| LiNO3 (нитрат лития) | Растворимый |
| LiOH (гидроксид лития) | Растворимый |
| мг (NO3) 2 (НИТРАТ МАГНИЯ) | Растворимый |
| MgBr2 (бромид магния) | Растворимый |
| MgC2O4 (оксалат магния) | Растворимый |
| MgCl2 (хлорид магния) | Растворимый |
| MgI2 (йодид магния) | Растворимый |
| MgS (сульфид магния) | Растворимый |
| MgSO4 (сульфат магния) | Растворимый |
| Mn (NO3) 2 (нитрат марганца (II)) | Растворимый |
| MnCl2 (хлорид марганца) | Растворимый |
| MnI2 (иодид марганца (II)) | Растворимый |
| Na2CO3 (карбонат натрия) | Растворимый |
| Na2S (сульфид натрия) | Растворимый |
| Na2SO3 (сульфит натрия) | Растворимый |
| Na2SO4 (сульфат натрия) | Растворимый |
| Na3PO4 (фосфат натрия) | Растворимый |
| Na3PO4 (тринатрийфосфат) | Растворимый |
| NaBr (бромид натрия) | Растворимый |
| NaC2h4O2 (ацетат натрия) | Растворимый |
| NaCl (хлорид натрия) | Растворимый |
| NaClO (гипохлорит натрия) | Растворимый |
| NaClO3 (ХЛОРАТ НАТРИЯ) | Растворимый |
| NaClO4 (перхлорат натрия) | Растворимый |
| nahco3 (бикарбонат натрия) | Растворимый |
| NaI (йодид натрия) | Растворимый |
| NaNO3 (нитрат натрия) | Растворимый |
| NaOH (гидроксид натрия) | Растворимый |
| NaPO4 | Растворимый |
| NaSO4 (сульфат натрия) | Растворимый |
| Nh4 (аммиак) | Растворимый |
| Nh5Br (бромид аммония) | Растворимый |
| Nh5C2h4O2 | Растворимый |
| Nh5Cl (ХЛОРИД АММОНИЯ) | Растворимый |
| Nh5I (йодид аммония) | Растворимый |
| Nh5NO3 (Аммиачная селитра) | Растворимый |
| Nh5OH (гидроксид аммония) | Растворимый |
| Ni (NO3) 2 (нитрат никеля (II)) | Растворимый |
| NiBr2 (БРОМИД НИКЕЛЯ) | Растворимый |
| NiCl2 (ХЛОРИД НИКЕЛЯ) | Растворимый |
| NiI2 (иодид никеля (II)) | Растворимый |
| NiSO4 (сульфат никеля (II)) | Растворимый |
| pb (c2h4o2) 2 (Ацетат свинца (II)) | Растворимый |
| Pb (NO3) 2 (динитрат свинца) | Растворимый |
| RbCl (хлорид рубидия) | Растворимый |
| SO2 (диоксид серы) | Растворимый |
| Sr (NO3) 2 (нитрат стронция) | Растворимый |
| Sr (OH) 2 (гидроксид стронция) | Растворимый |
| SrS (сульфид стронция) | Растворимый |
| Zn (Ch4COO) 2 (ацетат цинка) | Растворимый |
| Zn (NO3) 2 (нитрат цинка) | Растворимый |
| ZnBr2 (бромид цинка) | Растворимый |
| ZnCl2 (хлорид цинка) | Растворимый |
| ZnI2 (йодид цинка) | Растворимый |
| ZnSO4 (сульфат цинка) | Растворимый |
| Нерастворимый список | |
| Ag2CO3 (карбонат серебра) | Нерастворимый |
| Ag2CrO4 (хромат серебра) | Нерастворимый |
| Ag2O (оксид серебра) | Нерастворимый |
| Ag2S (сульфид серебра) | Нерастворимый |
| Ag2SO4 (сульфат серебра) | Нерастворимый |
| Ag3PO4 (фосфат серебра) | Нерастворимый |
| AgBr (бромид серебра) | Нерастворимый |
| AgCl (хлорид серебра) | Нерастворимый |
| AgCl2 (хлорид серебра) | Нерастворимый |
| AgCO3 (карбонат серебра) | Нерастворимый |
| AgI (йодид серебра) | Нерастворимый |
| agl | Нерастворимый |
| AgOH (гидроксид серебра) | Нерастворимый |
| AgSO4 (сульфат серебра (II)) | Нерастворимый |
| Al (OH) 3 (гидроксид алюминия) | Нерастворимый |
| Al2S3 (сульфид алюминия) | Нерастворимый |
| AlPO4 (фосфат алюминия) | Нерастворимый |
| Ba3 (PO4) 2 (фосфат бария) | Нерастворимый |
| BaCO3 (карбонат бария) | Нерастворимый |
| BaCrO4 (хромат бария) | Нерастворимый |
| BaSO4 (сульфат бария) | Нерастворимый |
| Ca3 (PO4) 2 (фосфат кальция) | Нерастворимый |
| CaC2O4 | Нерастворимый |
| CaCO3 (карбонат кальция) | Нерастворимый |
| CaF2 (фторид кальция) | Нерастворимый |
| Cd (OH) 2 (гидроксид кадмия) | Нерастворимый |
| CdCO3 (КАРБОНАТ КАДМИЯ) | Нерастворимый |
| Co (OH) 2 (гидроксид кобальта (II)) | Нерастворимый |
| CoCO3 (карбонат кобальта (II)) | Нерастворимый |
| CoS (сульфид кобальта (ii)) | Нерастворимый |
| Cr2S3 | Нерастворимый |
| Cu (OH) 2 (гидроксид меди (II)) | Нерастворимый |
| Cu (OH) 2 (гидроксид меди (II)) | Нерастворимый |
| Cu3 (PO4) 2 (Фосфат меди (II)) | Нерастворимый |
| CuCO3 (карбонат меди) | Нерастворимый |
| CuCrO4 (Хромат меди (II)) | Нерастворимый |
| Cui2 (йодид меди) | Нерастворимый |
| CuS (сульфид меди (II)) | Нерастворимый |
| Fe (OH) 2 (гидроксид железа (II)) | Нерастворимый |
| Fe (OH) 3 (гидроксид железа) | Нерастворимый |
| Fe2O3 (оксид железа (III)) | Нерастворимый |
| Fe2S3 (сульфид железа (III)) | Нерастворимый |
| FeCO3 (карбонат железа (II)) | Нерастворимый |
| FeO (OH) (гидроксид железа (III)) | Нерастворимый |
| FePO4 (фосфат железа (III)) | Нерастворимый |
| FeS (сульфид железа (II)) | Нерастворимый |
| HC2h4O2 | Нерастворимый |
| Hg2Br2 (бромид ртути (I)) | Нерастворимый |
| Hg2Cl2 (хлорид ртути (I)) | Нерастворимый |
| Hg2I2 (йодид ртути (I)) | Нерастворимый |
| HgI2 (дииодид ртути) | Нерастворимый |
| hno2 (Азотистая кислота) | Нерастворимый |
| Li3PO4 (фосфат лития) | Нерастворимый |
| Мг (C2h4O2) 2 | Нерастворимый |
| Mg (OH) 2 (гидроксид магния) | Нерастворимый |
| Mg3 (PO4) 2 (фосфат магния) | Нерастворимый |
| MgCO3 (карбонат магния) | Нерастворимый |
| MgO (оксид магния) | Нерастворимый |
| Mn (OH) 2 (гидроксид марганца) | Нерастворимый |
| MnCO3 (карбонат марганца (II)) | Нерастворимый |
| Ni (OH) 2 (гидроксид никеля (II)) | Нерастворимый |
| NiCO3 (карбонат никеля (II)) | Нерастворимый |
| NiS (сульфид никеля) | Нерастворимый |
| Pb (OH) 2 (Гидроксид свинца (II)) | Нерастворимый |
| Pb3 (PO4) 2 | Нерастворимый |
| PbBr2 (бромид свинца (II)) | Нерастворимый |
| PbCl2 (дихлорид свинца) | Нерастворимый |
| PbCO3 (карбонат свинца) | Нерастворимый |
| pbcro4 (ХРОМАТ СВИНЦА) | Нерастворимый |
| PbF2 (фторид свинца) | Нерастворимый |
| PbI (иодид свинца (II)) | Нерастворимый |
| PbI2 (иодид свинца (II)) | Нерастворимый |
| PbS (Сульфид свинца (II)) | Нерастворимый |
| PbSO4 (сульфат свинца (II)) | Нерастворимый |
| SrCO3 (карбонат стронция) | Нерастворимый |
| SrSO4 (сульфат стронция) | Нерастворимый |
| Zn (OH) 2 (гидроксид цинка) | Нерастворимый |
| Zn3 (PO4) 2 (фосфат цинка) | Нерастворимый |
| ZnCO3 (КАРБОНАТ ЦИНКА) | Нерастворимый |
| ZnS (сульфид цинка) | Нерастворимый |
| низкая растворимость (слаборастворимая) | |
| Ca (OH) 2 (гидроксид кальция) | низкая растворимость (слаборастворимая) |
| CaS (сульфид кальция) | низкая растворимость (слаборастворимая) |
| h3CO3 (угольная кислота) | низкая растворимость (слаборастворимая) |
| h3S (сероводород) | низкая растворимость (слаборастворимая) |
| PbCl2 (дихлорид свинца) | низкая растворимость (слаборастворимая) |
Влияние Sr (OH) 2 на водородные свойства системы Mg (Nh3) 2–2LiH
rsc.org/schema/rscart38″> Влияние легирования Sr (OH) 2 на систему Mg (NH 2 ) 2 –2LiH исследовано с учетом различных количеств добавленного Sr (OH) 2 в диапазон 0.05 до 0,2 мол. Экспериментальные результаты показывают, что как термодинамические, так и кинетические свойства Mg (NH 2 ) 2 –2LiH зависят от присутствия Sr (OH) 2 . Добавление 0,1 моль Sr (OH) 2 приводит к снижению как начала дегидрирования, так и пиковых температур на ок. 70 и 13 ° C, соответственно, и ускорение скорости де / повторного гидрирования за один раз при 150 ° C по сравнению с Mg (NH 2 ) 2 –2LiH.На основе анализа методом дифференциальной сканирующей калориметрии (ДСК) общая энтальпия реакции для образца, легированного 0,1 Sr (OH) 2 , рассчитана как 44 кДж на моль-H 2 , и есть два события поглощения. возникает в легированном образце вместо одного в исходном образце. Для применяемых экспериментальных условий, в соответствии с данными анализа порошковой рентгеновской дифракции (SR-PXD) и инфракрасной спектроскопии с преобразованием Фурье (FT-IR) in situ синхротронного излучения, механизм реакции был окончательно определен: Sr (OH) 2 , Mg (NH 2 ) 2 и LiH реагируют друг с другом с образованием SrO, MgO и LiNH 2 во время шаровой мельницы.После нагревания SrO взаимодействует с Mg (NH 2 ) 2 с образованием MgO и Sr (NH 2 ) 2 . Затем Mg (NH 2 ) 2 , LiNH 2 и Sr (NH 2 ) 2 реагируют с LiH с образованием Li 2 9 SrNH, Li 2 Mg (NH) 2 и Li 2 Mg 2 (NH) 3 в следах.
возникает в легированном образце вместо одного в исходном образце. Для применяемых экспериментальных условий, в соответствии с данными анализа порошковой рентгеновской дифракции (SR-PXD) и инфракрасной спектроскопии с преобразованием Фурье (FT-IR) in situ синхротронного излучения, механизм реакции был окончательно определен: Sr (OH) 2 , Mg (NH 2 ) 2 и LiH реагируют друг с другом с образованием SrO, MgO и LiNH 2 во время шаровой мельницы.После нагревания SrO взаимодействует с Mg (NH 2 ) 2 с образованием MgO и Sr (NH 2 ) 2 . Затем Mg (NH 2 ) 2 , LiNH 2 и Sr (NH 2 ) 2 реагируют с LiH с образованием Li 2 9 SrNH, Li 2 Mg (NH) 2 и Li 2 Mg 2 (NH) 3 в следах. После повторного гидрирования образуются LiSrH 3 , LiH и LiNH 2 вместе с аморфным Mg (NH 2 ) 2 . Причины улучшенной кинетики: (а) во время дегидрирования образование in situ SrNH, по-видимому, увеличивает межфазные контакты между Mg (NH 2 ) 2 и LiH, а также ослабляет N –H связь Mg (NH 2 ) 2 ; (b) во время абсорбции образование LiSrH 3 при температуре около 150 ° C может быть ключевым фактором для улучшения свойств гидрирования.
После повторного гидрирования образуются LiSrH 3 , LiH и LiNH 2 вместе с аморфным Mg (NH 2 ) 2 . Причины улучшенной кинетики: (а) во время дегидрирования образование in situ SrNH, по-видимому, увеличивает межфазные контакты между Mg (NH 2 ) 2 и LiH, а также ослабляет N –H связь Mg (NH 2 ) 2 ; (b) во время абсорбции образование LiSrH 3 при температуре около 150 ° C может быть ключевым фактором для улучшения свойств гидрирования.У вас есть доступ к этой статье
Подождите, пока мы загрузим ваш контент. ..
Что-то пошло не так. Попробуй еще раз?
..
Что-то пошло не так. Попробуй еще раз?sr (oh) 2 — Перевод на английский
Sr (OH) 2
естественные и прикладные науки — iate.europa.eu
▷▷
О механизме термического разложения при дегидроксилировании щелочноземельного гидроксида с … Экспериментальные результаты Mg (OH) 2 Ca (OH) 2 и Sr (OH) 2 согласуются с мономолекулярный закон распада и их энергии активации аналогичны значениям энтальпий разложения … ▷▷
Исследования газовых характеристик чистых и поверхностно модифицированных толстопленочных резисторов srtio3 Был подготовлен титанат стронция (SrTiO3 (ST)) механохимически из Sr (OH) 2 и TiO2. .. ▷
.. ▷▷
Аэробное окисление бензилового спирта на золотом материале на основе стронция : замечательная собственная основность и многоразовый катализатор … Наночастицы золота, стабилизированные наноразмерным ПВА, иммобилизованные на Sr (OH) 2 путем коллоидного осаждения продемонстрировали высокую каталитическую активность для окисления бензилового спирта … ▷▷
Термодинамическая стабильность и энтальпия гидратации церата стронция , легированного иттрием … 975 с образованием воды Sr (OH) 2 , CeO2, Y2O3 (DrH (298 … ▷▷
Стабильность материалов на основе srfeo3 в атмосфере, содержащей h3o / co2, при высоких температурах и давлениях … Ei-ther карбонат стронция или Sr (OH) 2 …природный и прикладной Sciences — iate.europa.eu
▷▷
Вычислительные исследования видообразования sr2 + в водном растворе и его взаимодействия с поверхностью гидратированного брусита (0001) … В третьей главе рассматриваются возможные комплексы гидроксида стронция в водная среда была исследована, чтобы установить вероятные виды-кандидаты для взаимодействия образующегося при ядерном делении стронция с гидратированными поверхностями брусита в прудах для хранения отработавшего ядерного топлива с высоким pH. .. ▷
.. ▷▷
Количественные исследования по очистке антител; диссоциация преципитатов, образованных полисахаридами, специфичными для пневмококков, и гомологичными … С тех пор Фелтон заявил, что осадки, специфичные для пневмококков типов I и II, растворенные с помощью кальция или гидроксида стронция и обработанные фосфатом для осаждения полисахарида, дают антитела, которые являются преципитатами. — осаждается гомологичным специфическим полисахаридом в пределах от 80 до 85 процентов (6) … ▷▷
Пористые нанокомпозиты бария стронция титанат-диоксид титана для фотокаталитических применений… Анодированный диоксид титана затем использовался в качестве темплата и подвергался гидротермальной обработке в смеси растворов гидроксида бария и гидроксида стронция с различными молярными соотношениями … ▷▷
Синтез серебра- Гибридные наночастицы титаната стронция золь-гель-гидротермальным методом … Мы приготовили гели-предшественники оксида титана, содержащие ионы Ag + и Sr2 + с различным молярным соотношением, и они были успешно преобразованы в гибридные наночастицы Ag-SrTiO3 гидротермальной обработкой 230 ° C в водных растворах гидроксида стронция . .. ▷
.. ▷▷
Количественные исследования по очистке антител. я. диссоциация преципитатов, образованных полисахаридами, специфичными для пневмококков, и гомологичными … С тех пор Фелтон заявил, что осадки, специфичные для пневмококков типов I и II, растворенные с помощью кальция или гидроксида стронция и обработанные фосфатом для осаждения полисахарида, дают антитела, которые осаждаются гомологичный специфический полисахарид в пределах от 80 до 85 процентов (6) … ▷▷
Легкий синтез нанокомпозита srco3- sr (oh) 2 / ppy с повышенной фотокаталитической активностью в видимом свете Мономер пиррола был химически полимеризован на Порошки SrCO3- Sr (OH) 2 для получения нанокомпозита SrCO3- Sr (OH) 2 / полипиррол, который будет использоваться в качестве кандидата для фотокаталитического разложения красителя метиленового синего (МБ)… ▷▷
Скорость растворения алюминия высокой чистоты в различных основаниях 1 … 998%) в KOH, Ba (OH) 2, Sr (OH) 2 , Ca (OH) s, Mg (OH) ) 2 и растворов Nh50H различных концентраций . .. ▷
.. ▷▷
Получение и характеристика стронция -содержащего гапсоля и исследования его воздействия на раковые и нормальные клетки … Использовался гидроксид стронция as strontium nitrition … ▷▷
Низкотемпературный гидротермальный синтез и определение характеристик фотокатализаторов srtio 3 на отсутствие разложения… В качестве исходных материалов использовали раствор бис (лактато аммония) ди гидроксида титана (IV) (TALH) и гидроксида стронция октагидрата [ Sr (OH) 2 · 8h3O] … ▷▷
Аналитическая методика алифатических органических кислот с плохим запахом в атмосфере … Метод заключается в следующем: образец адсорбируется через трубку гидроксид стронция и разлагается другими кислотами на муравьиную кислоту … ▷▷
Нанокристаллический мезопористый титанат стронция в качестве фотоэлектродного материала для фотосенсибилизированных солнечных устройств: увеличение фотоэдс за счет проектирования потенциалов с плоской полосой Нанокристаллический SrTiO3 синтезируется гидротермальной обработкой нанокристаллического диоксида титана в присутствии гидроксида стронция . ..
..1 миллиард переводов с разбивкой по видам деятельности на 28 языках
Наиболее частые запросы датский: 1-200, -1k, -2k, -3k, -4k, -5k, -7k, -10k, -20k, — 40k, -100k, -200k, -500k,
Наиболее частые запросы Английский: 1-200, -1k, -2k, -3k, -4k, -5k, -7k, -10k, -20k, -40k, — 100k, -200k, -500k,
Traduction Перевод Traducción Übersetzung Tradução Traduzione Traducere Vertaling Tłumaczenie Mετάφραση Oversættelse Översättning Käännös Aistriúchán Traduzzjoni Prevajanje Vertimas Tõlge Preklad Fordítás Tulkojumi Превод Překlad Prijevod 翻 訳 번역 翻译 Перевод
Разработано для TechDico
Издатель Условия и условия
Политика конфиденциальности
© techdico
Основанная в 1913 году как небольшой продуктовый магазин, за более чем 100 лет своей деятельности ECSA Chemicals стала одним из самых важных швейцарских дистрибьюторов che музыкальные продукты.Компания, занимающаяся международной дистрибуцией и торговлей, разделена на промышленные сегменты, которыми управляют команды специалистов и экспертов. Они гарантируют профессиональные и индивидуальные консультации и услуги. Благодаря нашему опыту мы можем быстро и безопасно связать вас с лучшими поставщиками на рынке, предоставив вам полный комплекс услуг по поиску, консультациям и поддержке. В центре нашего подхода и операций вы, наши клиенты. Каждый день мы стремимся найти лучшие продукты, которые максимально быстро удовлетворят ваши потребности.Ваше удовлетворение — наш самый большой успех. ПОЧЕМУ ECSA?
ОПЫТ
Работаем 100 лет. КАЧЕСТВО
Мы получили множество сертификатов (ISO, SQAS, GDP, Responsible Care, Bio-Inspecta, RSPO и т. Д.). Мы гарантируем полное соблюдение действующего законодательства и постоянное обучение наших сотрудников. БЕЗОПАСНОСТЬ
Мы постоянно проводим анализ рисков для каждой инфраструктуры, определяя уровни безопасности и оперативно внедряя корректирующие меры везде, где они необходимы.ШИРОКОЕ РАСПРОСТРАНЕНИЕ
У нас есть склады в стратегически важных местах для поставок товаров в Швейцарию и остальной мир. Они гарантируют профессиональные и индивидуальные консультации и услуги. Благодаря нашему опыту мы можем быстро и безопасно связать вас с лучшими поставщиками на рынке, предоставив вам полный комплекс услуг по поиску, консультациям и поддержке. В центре нашего подхода и операций вы, наши клиенты. Каждый день мы стремимся найти лучшие продукты, которые максимально быстро удовлетворят ваши потребности.Ваше удовлетворение — наш самый большой успех. ПОЧЕМУ ECSA?
ОПЫТ
Работаем 100 лет. КАЧЕСТВО
Мы получили множество сертификатов (ISO, SQAS, GDP, Responsible Care, Bio-Inspecta, RSPO и т. Д.). Мы гарантируем полное соблюдение действующего законодательства и постоянное обучение наших сотрудников. БЕЗОПАСНОСТЬ
Мы постоянно проводим анализ рисков для каждой инфраструктуры, определяя уровни безопасности и оперативно внедряя корректирующие меры везде, где они необходимы.ШИРОКОЕ РАСПРОСТРАНЕНИЕ
У нас есть склады в стратегически важных местах для поставок товаров в Швейцарию и остальной мир. ЕМКОСТЬ НАКОПИТЕЛЯ
Три склада, принадлежащие ECSA, гарантируют значительную площадь и вместимость каждого склада с полной доступностью продукции (базовые химикаты и специальные химикаты). СКОРОСТЬ
Присутствие по всей стране, персонал, занятый поиском сырья, и значительные складские мощности гарантируют быстрое получение и поставку товаров.КОНСУЛЬТИРОВАНИЕ
Наши специалисты — глубокое знание рынка и продуктов позволяет нам оказывать комплексные консультационные услуги, от закупки до поставки сырья. ЕМКОСТЬ НАКОПИТЕЛЯ
Три склада, принадлежащие ECSA, гарантируют значительную площадь и вместимость каждого склада с полной доступностью продукции (базовые химикаты и специальные химикаты). СКОРОСТЬ
Присутствие по всей стране, персонал, занятый поиском сырья, и значительные складские мощности гарантируют быстрое получение и поставку товаров.КОНСУЛЬТИРОВАНИЕ
Наши специалисты — глубокое знание рынка и продуктов позволяет нам оказывать комплексные консультационные услуги, от закупки до поставки сырья. |
Гидроксид стронция | 18480-07-4
Гидроксид стронция Химические свойства, использование, производство
использует
Гидроксид стронция используется для извлечения сахара из сахарной патоки из свеклы, а также для производства мыла и смазок.Токсичность
Сухой состав или водный раствор вызывают коррозию. Попадание на кожу или в глаза может вызвать раздражение.
Описание
Гидроксид стронция представляет собой ангидрат, призматический бесцветный кристаллы расплываются. Моногидрат и октагидрат также известны. Гидроксид стронция мало растворим в воде, но, как ни удивительно, октагидрат гораздо более растворим. Это последний из них коммерчески поставляется для большинства приложений.Когда октагидрат нагревается, семь вод гидратация теряется с образованием моногидрата и, наконец, оксида.Химические свойства
бесцветные расплывающиеся кристаллыФизические свойства
Белый расплывающийся кристалл; плотность 3,625 г / см 3 ; плавится при 375 ° C в атмосфере водорода; превращается в оксид при 710 ° C; слабо растворим в воде при 0 ° C, 0,41 г / 100 мл, растворим в кипящей воде при 100 ° C, 21,83 г / 100 мл; растворим в кислотах и растворе хлорида аммония.Октагидрат состоит из бесцветных тетрагональных расплывающихся кристаллов; плотность 1,90 г / см 3 ; теряет все молекулы воды при 100 ° C; трудно растворим в воде при низких температурах, 0,90 г / 100 мл при 0 ° C; растворим в кипящей воде, 47,7 г / 100 мл при 100 ° C; водный раствор сильнощелочной; растворим в кислотах и растворе хлорида аммония; не растворим в ацетоне.

использует
Гидроксид стронция используется в основном при рафинировании свекольный сахар и как стабилизатор в пластике.Его можно использовать в качестве источника ионов стронция, когда ион Cl — нежелателен. Гидроксид стронция поглощает углекислый газ из воздух с образованием карбоната стронция. Эта соль доступна в больших количествах. количества.использует
Извлечение сахара из патоки свекловичного сахара, мыла и смазки, стабилизаторы пластмасс, стекло, клеи.использует
Гидроксид стронция [Sr (OH) 2] используется для извлечения сахара из патоки сахарной свеклы.Он также используется в производстве мыла, клеев, пластиков, стекла и смазок, которые могут использоваться в среде с очень высокими или низкими температурами.Препарат
Приготовление Гидроксид стронция получают путем обработки оксида стронция водой: SrO + H 2 O → Sr (OH) 2В качестве альтернативы Sr (OH) 2 получают путем нагревания карбоната стронция или сульфида стронция паром при температуре около 500 ° С.
 до 600 ° C: SrCO 3 + H 2 O → Sr (OH) 2 + CO 2 SrS + 2H 2 O → Sr (OH) 2 + H 2 S.
до 600 ° C: SrCO 3 + H 2 O → Sr (OH) 2 + CO 2 SrS + 2H 2 O → Sr (OH) 2 + H 2 S.Методы очистки
Кристаллизовать гидроксид из горячей воды (2,2 мл / г) путем охлаждения до 0o.Продукты и сырье для получения гидроксида стронция
Сырье
Препараты
.

 Mg(OH)2
Mg(OH)2 Cu(OH)2
Cu(OH)2 Ba(OH)2
Ba(OH)2 RbOH
RbOH Fe(OH)3
Fe(OH)3 Zn(OH)2
Zn(OH)2 Cr + NaOH
Cr + NaOH I2
I2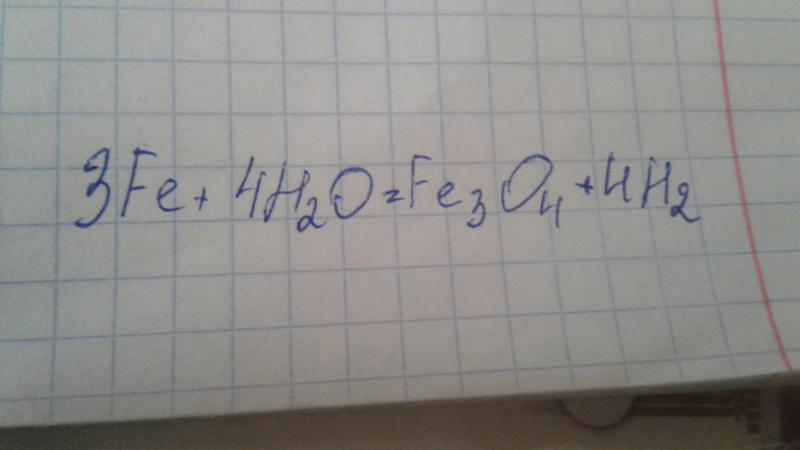 I2 + RbOH
I2 + RbOH