Тема 15. Молярный объём газов.
Часть I
1. 1 моль любого газа при н. у. занимает одинаковый объём, равный 22,4 л. Этот объём называется молярный и обозначается Vm.
2. Количество вещества (n) — отношение объёма газа при н. у. к молярному объёму:
n = V/Vm=> Vm измеряется в л/моль.
3. Следовательно, количество вещества
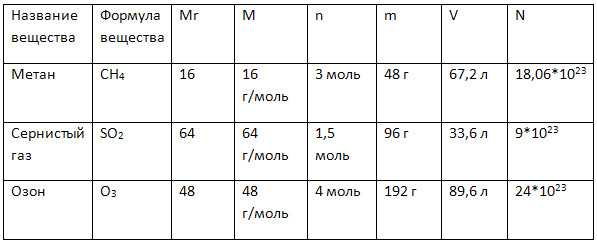
4. Дополните таблицу «Количественные характеристики веществ», делая необходимые вычисления.
Часть II
1. Установите соотношение между названием и размерностью величины.
2. Укажите формулы, которые являются производными от основной формулы n = V/Vm.
2) V=n•Vm
3) Vm=V/n
3. Сколько молекул содержат 44,8 л (н. у.) углекислого газа? Решите задачу двумя способами.
4. Придумайте условие задачи, в которой нужно найти число молекул N, если известен объём V.
Найти число частиц оксида азота(II), если его объём равен 67,2 л.
Решите задачу любым способом.
5. Вычислите массу 78,4 л (н. у.) хлора.
6. Найдите объём 297 г фосгена (COCl2).
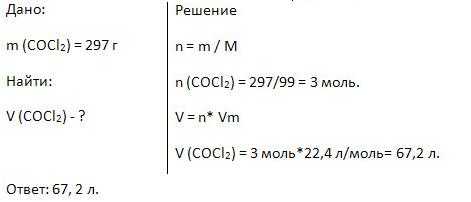
7. Вычислите массу 56 л аммиака, 10% -й водный раствор которого в медицине известен под названием «нашатырный спирт».
8. Придумайте задачу с использованием изученных понятий. С помощью компьютера создайте рисунок, иллюстрирующий данную задачу. Предложите способ её решения. Верно ли, что 22,4 л азота или 22,4 л водорода одинаковы по массе? Ответ подтвердите вычислениями.

superhimik.ru
Молярный объем газа — Techemy
Из положений о том, что один моль любого вещества включает число частиц этого вещества, равное числу Авогадро, и что равные числа частиц различных газов при одинаковых физических условиях содержатся в равных объемах этих газов, вытекает следствие:
равные количества любых газообразных веществ при одинаковых физических условиях занимают равные объемы
Например, объем одного моль любого газа имеет (при p, T = const) одно и то же значение. Следовательно, уравнение реакции, протекающей с участием газов, задает не только соотношение их количеств и масс, но и объемов.
молярный объем газа (VM) — это объем газа в котором содержится 1 моль частиц этого газа
VM = V / n
Единица молярного объема газа в СИ — кубический метр на моль (м3/моль), но чаще используют дольные единицы — литр (кубический дециметр) на моль (л/моль, дм3/моль) и мллилитр (кубический сантиметр) на моль (см3/моль).
В соответствии с определением молярного объема дял любого газа отношение его объема
При нормальных условиях (н.у.) — 101,3 кПа, 0°С — молярный объем идеального газа равен
VM = 2,241381·10-2 м3/моль ≈ 22.4 л/моль
В химических расчетах используется округленное значение 22,4 л/моль, поскольку точное значение относится к идеальному газу, а большинство реальных газов по свойствам отличаются от него. Реальные газы с очень низкой температурой равновесной конденсации (H2, O2, N2) при нормальных условиях имеют объем, почти равный 22,4 л/моль, а газы, конденсирующиеся при высоких температурах, имеют несколько меньшее значение молярного объема при н.у.: для CO2 — 22.26 л/моль, для NH3 — 22,08 л/моль.
Зная объем некоторого газа при заданных условиях, можно определить количество веществ в этом объеме, и наоборот, по количеству вещества в данной порции газа можно найти объем этой порции:
n = V / VM; V = VM * n
Молярный объем газа при н.у. — фундаментальная физическая постоянная, которая широко используется в химических расчетах. Она позволяет применять объем газа вместо его массы, что очень удобно в аналитической химии (газоанализаторы основанные на измерении объема), поскольку легче измерить объем газа, чем его массу.Значение молярного объема газа при н.у. является коэффициентом пропорциональности между постоянными Авогадро и Лошмидта:
VM = NA / NL = 6.022·1023 (моль-1) / 2,24·104 (см3/моль) = 2.69·1019 (см-3)
Используя значения молярного объема и молярную массу газа можно определить плотность газа:
ρ = M / VM
В расчетах, основанных на законе эквивалентов для газообразных веществ (реагентов, продуктов) вместо эквивалентной массы удобнее применятьэквивалентный объем, который предстваляет собой отношение объема порции данного газа к эквивалентному количеству вещества в этой порции:
Veq = V / neq = V / zn = VM / z; (p, T = const)
Единица эквивалентного объема совпадает с единицей молярного объема. Значение эквивалентного объема газа является константой данного газа только в конкретной реакции, так как зависит от фактора эквивалентности feq.
techemy.com
2.6. Закон Авогадро
2.6. Закон Авогадро2.6. Закон Авогадро (А. Авогадро, 1811)
В равных объемах газов (V) при одинаковых условиях (температуре Т и давлении Р) содержится одинаковое число молекул.
Следствие из закона Авогадро: один моль любого газа при одинаковых условиях занимает одинаковый объем.
В частности, при нормальных условиях, т.е. при 0°
С (273 К) и
101,3 кПа, объем 1 моля газа, равен 22,4 л. Этот объем называют
молярным объемом газа Vm.
Таким образом, при нормальных условиях (н.у.) молярный объем любого газа
Закон Авогадро используется в расчетах для газообразных веществ. При пересчете объема газа от нормальных условий к любым иным применяют объединенный газовый закон Бойля-Мариотта и Гей-Люссака:
где Рo, Vo, Тo – давление, объем газа и температура при нормальных условиях (Рo = 101,3 кПа, Тo = 273К).
Если известна масса (m) или количество (ν) газа и требуется вычислить его объем, или наоборот, используют уравнение Менделеева-Клапейрона:
где ν = m/M – отношение массы вещества к его молярной массе,
R – универсальная газовая постоянная, равная 8,31 Дж/(моль•К).
Из закона Авогадро вытекает еще одно важное следствие: отношение масс одинаковых объемов двух газов есть величина постоянная для данных газов. Эта постоянная величина называется относительной плотностью газа и обозначается D. Так как молярные объемы всех газов одинаковы (1-е следствие закона Авогадро), то отношение молярных масс любой пары газов также равна этой постоянной:
где М1 и М2 – молярные массы двух газообразных веществ.
Величина D определяется экспериментально как отношение масс одинаковых объемов исследуемого газа (М1) и эталонного газа с известной молекулярной массой (М2). По величинам D и М2 можно найти молярную массу исследуемого газа:
M1 = D • M2.orgchem.ru
Основные формулы для решения задач по химии
05-Авг-2012 | комментариев 413 | Лолита Окольнова
Все, все основные задачи по химии решаются с помощью
нескольких основных понятий и формул.
У всех веществ разная масса, плотность и объем. Кусочек металла одного элемента может весить во много раз больше, чем точно такого же размера кусочек другого металла.
Моль (количество моль)
обозначение: моль, международное: mol — единица измерения количества вещества. Соответствует количеству вещества, в котором содержится NA частиц (молекул, атомов, ионов)Поэтому была введена универсальная величина — количество моль. Часто встречающаяся фраза в задачах — «было получено…
NA = 6,02 · 1023
NA — число Авогадро. Тоже «число по договоренности». Сколько атомов содержится в стержне кончика карандаша? Порядка тысячи. Оперировать такими величинами не удобно. Поэтому химики и физики всего мира договорились — обозначим 6,02 · 1023 частиц (атомов, молекул, ионов) как 1 моль вещества.
1 моль = 6,02 · 1023 частиц
Это была первая из основных формул для решения задач.
Молярная масса вещества
Молярная масса вещества — это масса одного моль вещества.
Обозначается как Mr. Находится по таблице Менделеева — это просто сумма атомных масс вещества.
Например, нам дана серная кислота — H 2SO4. Давайте посчитаем молярную массу вещества: атомная масса H =1, S-32, O-16.
Mr(H2SO4)=1•2+32+16•4=98 г\моль.
Вторая необходимая формула для решения задач —
формула массы вещества:
Т.е., чтобы найти массу вещества, необходимо знать количество моль (n), а молярную массу мы находим из Периодической системы.
Закон сохранения массы — масса веществ, вступивших в химическую реакцию, всегда равна массе образовавшихся веществ.
Если мы знаем массу (массы) веществ, вступивших в реакцию, мы можем найти массу (массы) продуктов этой реакции. И наоборот.
Третья формула для решения задач по химии —
объем вещества:
Откуда взялось число 22.4? Из закона Авогадро:
в равных объёмах различных газов, взятых при одинаковых температуре и давлении, содержится одно и то же число молекул.
Согласно закону Авогадро, 1 моль идеального газа при нормальных условиях (н.у.) имеет один и тот же объём Vm = 22,413 996(39) л
Т.е., если в задаче нам даны нормальные условия, то, зная количество моль (n), мы можем найти объем вещества.
Итак, основные формулы для решения задач по химии
Число Авогадро NA
6,02 · 1023 частиц
Количество вещества n (моль)
n=m\Mr
n=V\22.4 (л\моль)
Масса веществаm (г)
m=n•Mr
Объем вещества V(л)
V=n•22.4 (л\моль)
или вот еще удобная табличка:

Это формулы. Часто для решения задач нужно сначала написать уравнение реакции и (обязательно!) расставить коэффициенты — их соотношение определяет соотношение молей в процессе.
_________________________________________________________________________________________________
Еще вам могут понадобиться:
- в ЕГЭ это вопрос А27
- А28
- задачи части С — 4 и 5
Категории: |
Обсуждение: «Основные формулы для решения задач по химии»
distant-lessons.ru
