co2, al4c3, khco3, ccl2, co
Химия, 08.06.2019 06:30, alesaastudinap0dbun
Показать ответы
Другие вопросы по: Химия
.(Для ремонтных работ купили краску, цемент и песок. песка купили в 4 раза больше, чем цемента, а краски-в 3 раза меньше, чем песка. сколько купили краски, цемента и песка отдельно…
Опубликовано: 28.02.2019 13:00
Ответов: 2
Автомобиль который движется равномерно и прямолинейно со скоростью 54км/ч прошел за время 10сек такой же путь как и мотоциклист за время 12сек. чему равна скорость мотоциклиста есл…
Опубликовано: 28.02.2019 13:30
Ответов: 2
Лаборатория представляет собой комнату длиной 5 м, шириной 4 м, высотой 3,5 м. во время ремонта из лаборатории вынесли все оборудование и мебель, кроме тумбочки, в которой стояла б. ..
..
Опубликовано: 01.03.2019 02:00
Ответов: 3
Наличие пигмента в волосах у человека доминирует над альбинизмом(отсутствие пигмента).муж и жена гетерозиготны по пигментации волос. возможно ли рождение у них ребенка альбиноса?…
Опубликовано: 01.03.2019 18:30
Ответов: 2
Отцу 45 лет. сын на 36 лет моложе отца. во сколько раз сын моложе отца? сохранится ли это соотношение возрастов через год?…
Опубликовано: 02.03.2019 02:10
Ответов: 3
Собственная скорость катера 15 1\2 км\ч. скорость течения реки 2 1\4км\ч. 1 за какое время проплывет катер расстояние 71км, если будет плыть по течению? 2 за какое время проплывет…
Опубликовано: 02.03.2019 21:40
Ответов: 1
Знаешь правильный ответ?
Определите степень окисления: co2, al4c3, khco3, ccl2, co. ..
..
Популярные вопросы
Даны два одинаковых по объёму шарика из свинца и олова . какой из них легче ? и почему ?…
Опубликовано: 07.03.2019 19:22
Ответов: 2
Решите неравенство 17-(х+2)> 12х-11…
Опубликовано: 27.02.2019 21:30
Ответов: 3
Собственная скорость катера 25,5 км/ч, скорость течения реки 2,5 км/ч. какой путь пройдёт катер за 1,5по течению? против течения?…
Опубликовано: 01.03.2019 15:50
Ответов: 3
Решение столбиком: а) 6,144: 12+1,62= б) 0,07-0,1001: 1,43= в) (62,1-61,44): 1,2= г) 48: (73,29+46,71)=…
Опубликовано: 01.03.2019 17:10
Ответов: 3
На сколько больше страниц прочитала оля вечером , чем утром , если она прочитала 9 страниц , а вечером 12 страниц.
Опубликовано: 01.03.2019 18:30
Ответов: 2
Периметр равнобедренного треугольника равна 42 см. найдите длины сторон треугольника, если основание на 3 см меньше, чем боковая сторона….
Опубликовано: 02.03.2019 09:10
Ответов: 2
Плоскость α и β параллельны причем плоскость α пересекает прямую а. докажите, что и плоскость β пересекает прямую а….
Опубликовано: 02.03.2019 23:10
Ответов: 3
Обозначить состав слов оттеснён бесстрашных расстелив поддавалась подал поддерживал преддверие расчёты рассчитанной мировоззрение расстёгнутой…
Опубликовано: 03.03.2019 16:00
Ответов: 3
Al + hcl, na2o+h4po4, zno+h3so4, mg+h3so4, fe2o3+hcl, bao+hno3…
Опубликовано: 03. 03.2019 17:50
03.2019 17:50
Ответов: 2
Никелевую пластину массой 25.9 г опустили в 555 г раствора сульфата железа(iii) с массовой долей соли 0.1. после некоторого выдерживания пластинки в растворе ее вынули, при этом ок…
Опубликовано: 03.03.2019 22:30
Ответов: 1
Больше вопросов по предмету: Химия Случайные вопросы
Популярные вопросы
Однажды летним солнечным утром мальчик решил измерить длину тени, от своегодома. Длина тени оказалась равна 5,6
Ответы
kmullagalieva 12.10.2020 12:52
123см
Объяснение:
5,6/5,9=0,95
130*0.95=123
ПОКАЗАТЬ ОТВЕТЫ
Другие вопросы по теме Химия
мпрьььоппааамт
11. 11.2019 13:15
11.2019 13:15
Hcl(al, k, ba) h4po4 (zn, fe валентность 3 , na) все расчеты по формулам и составление формул кислот …
0689433382 14.08.2019 05:20
Вкакой реакции при повышение давлении происходит смещение вправо ? 2no=n2+o2 4fes2+11o2=2fe2o3+8so2…
lera5471 14.06.2019 17:40
Какой объем кислорода требуется для сгорания 7.4 г бутанола по уравнению: c4h9oh+6o2 — 4со2+5н2о…
veronikamihailova37 01.06.2019 01:00
Определите массовую долю соли в растворе,если 350мл воды растворили 50 г хлорида натрия. ..
..
sooooooyeees 07.06.2019 12:30
Спо , нужно! : вычислите количество вещества и объем (н.у.) этилена, который может быть получен если 260г ацетилена вступит в реакцию с водородом….
Сколько граммов сульфида железа 2 образуется при взаимодействии 14 г железа с 6,4 г серы….
катя4799 12.03.2021 10:08
3.Запишите галогены и щелочные металлы. Где в периодической системе расположены. …
…
Medina20161102 20.03.2019 21:52
1. написать структурную формулу 2,4-диметилгексановои кислоты 2. написать уравнение реакции, отражающие свойства пентановой кислоты 3. написать реакцию образования мителпантаноату…
YuLia120620 25.11.2021 07:36
Расставьте коофиценты…
Дженитка 01.02.2021 19:19
1)Досліди, за до яких можна встановити: 1.Тимчасову жорсткість води; 2.Наявність домішок магній сульфату в порції натрій сульфату; 3. Що в розчині міститься ферум(3)хлорид,…
Що в розчині міститься ферум(3)хлорид,…
Алкинаи, алканаи, алкенаи, алкадиенаи, бензонаи, алкохолии, ….
Alkanus galima Laboratorijoje tik sudeginti
Alkenai, alkinai, alkadieniai dalyvauja
prisijungimo reakcijose visi iðblukina bromo
vandená ir kalioka parmanganatà be.
Бензины, содержащие бромистый тик,
Катализаторы и соединения бромсодержащих соединений
C6H6+Br2=C6H5Br+HBr (FeBr2)
Толуены и соединения Kalio parmanganatà
C6H5Ch4+(ið KMnO4)O=C6H5COOH+h3O
Toluenas reaguoja su azoto rûgðtim
Glicerolis su vario baze susidaro tamsiai
mëlynos spalvos skystis
CH-OH Ch3-OH
CH-OH +Cu(OH) 2 = CH-O+2HOH
CH-OH CH3-O CU
FENOLIS SU BROMO VANDENIU Iðkrenta Baltos
Nuosëdos
C6H5OH+3BR2 = C6H3BR3OH+3HBR
FENOLIS SUGELIES SUSELIES 3BLIDIIS 3BLIDIIS 3BLIDIIS 3.0002 C6H5OH+3BR2 = C6H3BR3OH+3HBR
ALKANAI:
CHEMINES SAVYBES:
• DEGA
• Kaitinant Skyla: CH5спешный.
• 2С+2ч32Ч5; Ch4COONa+NaOHCh5+Na2CO3; AL4C3+2H3O+3CH5+AL (OH) 3
Cikloalkanai:
Cheminë savybës:
• Pavadavimo reakcijos C6H22+Cl2спешный
Cheminës savybës:
• Dega
• Prisijungimas: Ch3=Ch3+h3Ch4-Ch4; Ch3=Ch3+Br2C2h5Br2
• Халоген ванденилиния дариний: C2h5+HClC2H5Cl
• Вандена: CC2h5+h3OCh4-Ch3-OH
• Ið5CHO)2HO4: C2h5O4+[[h5] 2
• Oksiduojasi: 2C2h5+O22C2h5O
• Polimerizuojasi:
n(Ch3=Ch3) (-Ch3-Ch3-)n
Gavimas:
• Dechidrinant alkanus: C2H6C2h5+h3
• Гидринант алкин: C2h3+h3C2h5
• Ið дихлорорганические соединения: C3H6Cl2+ZnZnCl2+Ch4-CH=Ch3
• Ið монохологенные соединения: Ch4-Ch3-Cl+KOH(спирт.)Ch3=Ch3+KCl+h3O
• Dechilktuuso: achilktuuso: achilktuuso: C2H5OHC2h5+h3O
ALKADIENAI:
Cheminës savybës:
• Применяется: Ch3=CH-CH-Ch3+h3Ch4-CH=CH-Ch4
• Полимеризация(Ch=CH3: n ) (-Ch3-CH=CH-Ch3-)n
АЛКИН(этилен):
Cheminës savybës:
• Дега
• Применяется: CHCH+Br2C2h3Cl; CHCH+HClC2h4Cl; CHCH+2HClC2h5Cl2
• Prisijungia HOH: CHCH+HOHC2h5O
• Iðblukina KMnO4
• Polimerizuojasi: n(CHCH) (-CH=CH-)n (KUPRENAS)
200002 Gavimas:2 De IR Alkenus
• Ið DichogogeniniO Dariniø: C3H6CL2+2KOH (Spirit) ϩ2Kcl+2H3O+C3H5
• Ið CAC2 UþPilant HOH:
CACO3 выполни. Ca(OH)2+C2h3
Ca(OH)2+C2h3
БЕНЗЕНАЙ:
Cheminës savybes:
• Дега
• Приведенные значения: C6H6+3Cl2C6H6Cl6; C6H6+3H3C6H22
• Pavadavimo (Vienoje Vietoje): C6H6+CL2C6H5CL+HCL
GAVIMAS:
• 3C2H3mC6H6H6
• DEHIDRINANT CIKLOALKANISUSIRSISIRSH6H6H6H6H6H6H6
• DEHIDRINANT CIKLOALKANISUSIS. C6H6+4h3
ALKOHOLIAI:
Cheminës savybës:
• Dega
• Активированный металл: 2C2H5OH+2Na2C2H5ONa+h3
Suø. dariniais: C2H5OH+HClC2H5Cl+HOH
• Дегидратация: C2H5OHC2h5+HOH
• Oksiduojasi: C3H7OH+[O] َSC3H6O+H3O
• DEHIDRINASI IR DEHIDRATUOJASI: 2C2H5OH. 2H3O+H3+C4H6
GAVIMAS:
• HIDRATUHHHH69
GAVIMAS:
H3O+H3+C4H6
GAVIMAS:
H3O+H3+C4H6
GAVIMAS:
H3O+H3+C4H6
GAVIMAS:
H3O+H3+C4H6
. dariniø: C4H9Cl+KOHKCl+C4H9OH
metanolio Pramonëje: CO+h3Ch4OH
etanolio RRauginant gliukozæ: C6h22O62C2H5OH+2CO2
Polihidroksiliai alkoholiai
Cheminës savybës:
• Gali reaguoti su kai kuriomis bazëmis
Ch3-OH Ch3-OH
Cu(OH)2 +CH-OH → CH-O +HOH
Ch3-OH Ch3-O Cu
• panaðios kaip monohidroksliø
Glicerolis gali reaguoti 9003 su azoto r -OH Ch3-ONO2
CH-OH +3HONO2CH-ONO2 +3HOH
Ch3-OH Ch3-ONO2
Gavimas:
Ið alkenø ir halogeniniø dariniø:
1.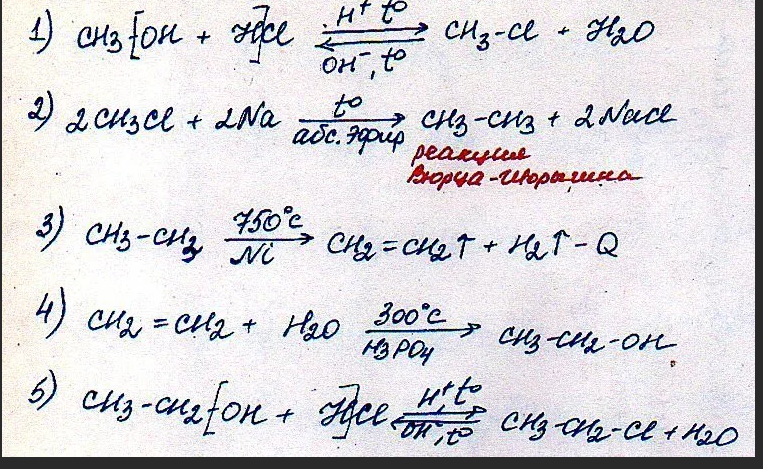 [++ Ch=
[++ Ch=
1. +HOH Ch3= Ch3
OH OH
2. Ch3= Ch3 +2KOH Ch3= Ch3 +2KCl
Cl Cl OH OH
Fenoliai CNH (2n-6) O
Cheminës savybës:
• Dega
• Su aktyviais metalais ir ðarmais:
C6H5 OH+Naíc6h5ona+H3
C6H5 OH+NAOH+3
C6H5 OH+NAOH. (Natrio Fenoletas)
• Su Halogenø vandeniliniais dariniais
• Dehidrinasi ir dehidratuojasi
• Oksiduojasi (Dël To Gauna Raudonà Spalvà)
• Su Brom OH+HONO2C6 h3(NO2)3OH+3h3 O
• Galima Hidrinti
C6H5 OH+3H3C C6H21 OH (Ciklo Heksanolis)
• SU FECL3 Susidaro Violetine Spalva
C6H5 OH+FECL3C C6H5 O FECL2+HCL
9000 29000 2
9000 2
9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000 2 9000.
C6H5ONa + h3 SO4 C6H5OH +NaHSO4
• CH+CH=CH-CHCh4 -CH-Ch4
C6H5
Ch4 -CH-Ch4 +O2 C6H5OH + Ch4 -CH-Ch3 9000
• Ið C6H6 галогеносодержащие вещества от перорального до сухого KOH
АЛЬДЕГИДЫ
Cheminës savybës:
• Dega
• Oksidacijos ir prisijungimo reakcijose
A) Sudabro Amoniakiniu Tirpalu
RCOH+Ag2OCCOOH+Ag
B) Su Cu (OH) 2 RCOH+2COHOH+AG
B) Su Cu (OH) 2 RCOH+2. RCOOH+2CuOH+h3O
• Содержит спирт RCOH+h3RCHHOH
• Сухие фенолы. Поликоденсация nC6H5OH+nCHHO(- C6H5 OH-Ch3)n+nh3O
Gavimas:
• Пираминоспирты: RCh3OH+[O]RCOH+HOH
• C2H5OH=CuOOCu4-CH
• METANALIUI Ið метанооксидант по кат.
Ch5+O2H-CH=O+h3
• ETANALIUI iið alkinø Ch3=Ch3+HOHCh4-CH=O Ch3=Ch3+O2 Ch4-CH=O
[Hoá 11] Phương pháp điều Чо ХК | Cộng đồng Học shin Вьетнам
кингвип
- #1
Chắc suất Đại học top — Giữ chỗ ngay!! ĐĂNG BÀI NGAY để cùng trao đổi với cac thành viên siêu nhiệt tình & dễ thương trên diễn đàn.
MỘT SỐ PHƯƠNG PHÁP ĐIỀU CHẾ HIĐROCACBON
I) ANKAN
- Đi từ hiđrocacbon không no
_ Hiđro hoá hiđrocacbon không no sẽ được ankan tương ứng:
RCH = CHR’ + h3 => RCh3 — Ch3R’
RC ≡ CR’ + h3 => RCh3 – Ch3R’
- Đi từ dẫn xuất halogen
_ Tổng hợp giữ nguyên mạch cacbon:
R – X + Mg => RMgX + HOH =>
Vd:
Ch4Ch3I + Mg => Ch4Ch3MgI+ HOH => Ch4Ch4 + Mg(OH)I
_ Tổng hợp tăng mạch cacbon:
2RX + 2 Na => Ch4Ch3 – Ch3Ch4 + 2NaI
Vd:
2Ch4Ch3I + 2Na => Ch4Ch3 – Ch3Ch4 + 2NaI
_ phản ứng điện phân:
2rcoona + 2 H3O => R — R + 2CO2 + 2NAOH + H3
VD:
2CH4COONA + 2H3O => CH4CH4 + 2CO2 + 2NAOH + H3
13o => ch4CH4 + 2CO2 + 2NAOH + H3
1313131313131313131313131313131313131313 гг.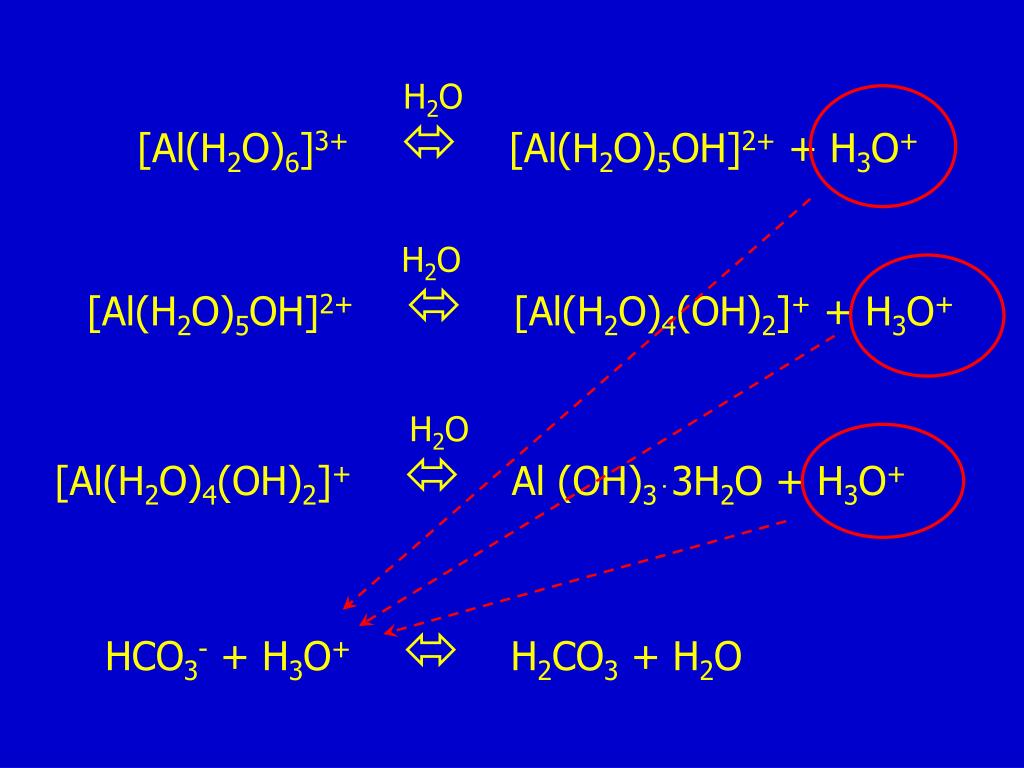 0313 RCOONa + NaOH => RH + Na2CO3
0313 RCOONa + NaOH => RH + Na2CO3
(хан) (rắn)
_ Xúc tác phản ứng này la CaO nhiệt đô cao. CaO ở đây đóng vai trò là giảm lượng nhiệt của pư an toàn khi điều chế trong Phòng thí nghiệm. Còn mêtan có thể điều chế riêng băng cách thuỷ phân nhôm cacbua
al4c3 + 12h3o => 3ch5 + 4al (OH) 3
II) Anken
1.CHI Từ Dẫn xuất mono halogen: phả. CHX — => — CH = CH- + HX ( điều kiện phản ứng trong môi trường ancol và KOH )
2.Đi từ dẫn xuất 1,2-галоген: phản ứng tách галоген
— CHX – CHX — + Zn => — C =C- + ZnX2 => Ch3 = Ch3 + ZnBr2
3.Đi từ ancol: phản ứng tách HOH (đêhiđrat hoá)
— Ch3–CH-OH ==> Ch3 = Ch3 + h3O
(Xúc tác 1 phản ản ứ3ng lĐng 180 độ)
4.Đi từ ankin phản ứng hiđro hoá
R – C ≡ C – R’ + h3 ==> R – CH = CH – R’ ( xúc tác Pd hay Ni , nhiệt đô )
0002 III) АНКИН
- Đi từ dẫn xuất đihalogen và dẫn xuất тетрагалоген.
 Tổng hợp giữ nguyên mạch cacbon
Tổng hợp giữ nguyên mạch cacbon
_ Tách hiđro halogenua từ dẫn xuất đihalogen:
Ch4Ch3CHCl2 ==> Ch4CH = CHCl ==> Ch4C ≡ CH
_ Tách hiđro halogenua từ dẫn xuất tetrahalogen
Ch4-CBr2 – CHBr2 + Zn => Ch4C ≡ CH + 2ZnBr2
- Đi từ axetilen v à dẫn xuất моногалоген. Tổng hợp tăng mạch cacbon
CH ≡ CH => CH ≡ CNa => CH ≡ C – C3H7
- Đi t ừ canxicacbua và từ mêtan. điều chế аксетилен
_ Thuỷ phân canxicacbua :
CaC2 + 2h3O => CH ≡ CH + Ca(OH)2
Последний раз редактировалось модератором:
Реакции:
Кьянхдосюаньхуй2711
- #2
R – C ≡ C – R’ + h3 ==> R – CH = CH – R’ ( xúc tác Pd hay Ni , nhiệt đô )
Chỗ ni sai này, ko xài Ni đc, xài Ni nếu h3 dư là ra ankan luôn, đc xài Pd/Pb(CO3)2 thui
Với trên nớ tùm lum thứ khó hiểu
- #3
_ Phản ứng điện phân:
2RCOONa + 2 h3O => R – R + 2CO2 + 2NaOH + h3 . ………… Phương pháp này gọi là phương Điều chế ankan còn có phương pháp như: phương pháp взламывание.
………… Phương pháp này gọi là phương Điều chế ankan còn có phương pháp như: phương pháp взламывание.
Trong công nghiep: người ta chưng cất phân đoạn dầu mỏ để tách được ankan.
— Ch3 — CHX — => — CH = CH- + HX ( điều kiện phản ứng trong môi trường ancol và KOH )
_ Hướng của phản ứng tách HHal tuân theo quy tắc Zaixep.
Điều kiện không nhất thiet phải la KOH, chỉ cần bazơ mạnh la được. Và chú ý : X = Cl hoặc Br.
2.Đi từ dẫn xuất 1,2-галоген: phản ứng tách галоген
— CHX – CHX — + Zn => — C =C- + ZnX2
Có th axeton)
Còn nhiều phương pháp điều chế anken các bạn có thể tham khảo như:
+ tách amin bậc III và nước từ tetraankyl amoni hidroxit
+ ngưng tụ hợp chất cacbonyl với photphoylit ( còn gọi là phản ứng Wittig)
TUY NHIEN 2 PHươNG PHAP Này Không Phổ Biến (mình chỉ post ể mọi người cùng tham khảo)
ankin : nhiệt ộ ộ ộ ầ ầ ầ ầ ầ ầ ầ ầ ầ ầ ầ ầ ộ ộ ộ ộ ộ ộ nhiệt ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ ộ hả hả ghả ộu
казу_96
- #4
mọi người giúp viết phương trình điều chế này với
* điều chế propen từ
a, từ 2-cloropropan b, từ propan
* từ propan-1-điều chế:
. 3 10002 * từ propan-1-điều chế:
3 10002 * từ propan-1-điều chế:
. б, 1-бром-2-хлор-3-иодпропан
танхнимен
- #5
bai 1
a,
thuc hien phan ung tach SN2 trong kiem manh nhu NaOH hoac EtONa…..
ung ung can nhiet do
2-клопропан + NaOH -> пропен + NaCl + h3O
b,
phan nay co 2 cach
cach 1; hidrat hoa ankan
кэш 2; cho propan + Cl2
bai 2
a,
_thuc hien phan ung tach nuoc
_ cho sp tac dung voi Cl2 < nhiet do khoang 500>
_ cho sp cong Cl2
b,
_ cho td voi dung dich NaI
_ cho sp td voi Br2 trong dung dich NaCl
Вы должны войти или зарегистрироваться, чтобы ответить здесь.

 Tổng hợp giữ nguyên mạch cacbon
Tổng hợp giữ nguyên mạch cacbon