Periodic Table — Ptable
Periodic Table — Ptable Menu Wide Top bar Side bar Dark SearchEnable JavaScript for a plethora of interactivity including property trend visualization, thousands of isotopes, compound mixing, and 3D orbital diagrams. Don’t like ads? No problem! Ptable will always be free for everyone. Find yourself here daily? Consider either unblocking the single ad banner, donating $1 a month (log in after donating), or buying a poster or wallet card, order numberTemperature
°C °F K
YearCE
- Search for:
- Atomic number
- Property values
- Linear
- Logarithmic
- s
- block
- p
- block
- d
- block
- f
- block
- α
- Alpha decay
- p
- Proton emission
- n
- Neutron emission
- SF
- Spontaneous fission
- β⁻
- Beta decay
- β⁺
- Positron emission
- ϵ
- Electron capture
- Stable
- 1 H Hydrogen 1.
 008
008 - 2 He Helium 4.0026
- 3 Li Lithium 6.94
- 4 Be Beryllium 9.0122
- 5 B Boron 10.81
- 6 C Carbon 12.011
- 7 N Nitrogen 14.007
- 8 O Oxygen 15.999
- 9 F Fluorine 18.998
- 10 Ne Neon 20.180
- 11 Na Sodium 22.990
- 12 Mg Magnesium 24.305
- 13 Al Aluminium 26.982
- 14 Si Silicon 28.085
- 15 P Phosphorus 30.974
- 16 S Sulfur 32.06
- 17 Cl Chlorine 35.
 45
45 - 18 Ar Argon 39.948
- 20 Ca Calcium 40.078
- 21 Sc Scandium 44.956
- 22 Ti Titanium 47.867
- 23 V Vanadium 50.942
- 24 Cr Chromium 51.996
- 25 Mn Manganese 54.938
- 26 Fe Iron 55.845
- 27 Co Cobalt 58.933
- 28 Ni Nickel 58.693
- 29 Cu Copper 63.546
- 30 Zn Zinc 65.38
- 31 Ga Gallium 69.723
- 32 Ge Germanium 72.630
- 33 As Arsenic 74.
 922
922 - 34 Se Selenium 78.971
- 35 Br Bromine 79.904
- 36 Kr Krypton 83.798
- 37 Rb Rubidium 85.468
- 38 Sr Strontium 87.62
- 39 Y Yttrium 88.906
- 40 Zr Zirconium 91.224
- 41 Nb Niobium 92.906
- 42 Mo Molybdenum 95.95
- 43 Tc Technetium (98)
- 44 Ru Ruthenium 101.07
- 45 Rh Rhodium 102.91
- 46 Pd Palladium 106.42
- 47 Ag Silver 107.87
- 48 Cd
- 49 In Indium 114.
 82
82 - 50 Sn Tin 118.71
- 51 Sb Antimony 121.76
- 52 Te Tellurium 127.60
- 53 I Iodine 126.90
- 54 Xe Xenon 131.29
- 55 Cs Caesium 132.91
- 56 Ba Barium 137.33
- 57 La Lanthanum 138.91
- 58 Ce Cerium 140.12
- 59 Pr Praseodymium 140.91
- 60 Nd Neodymium 144.24
- 61 Pm Promethium (145)
- 62 Sm Samarium 150.36
- 63 Eu Europium 151.96
- 64 Gd Gadolinium 157.25
- 65 Tb Terbium 158.
 93
93 - 66 Dy Dysprosium 162.50
- 67 Ho Holmium 164.93
- 68 Er Erbium 167.26
- 69 Tm Thulium 168.93
- 70 Yb Ytterbium 173.05
- 71 Lu Lutetium 174.97
- 72 Hf Hafnium 178.49
- 73 Ta Tantalum 180.95
- 74 W Tungsten 183.84
- 75 Re Rhenium 186.21
- 76 Os Osmium 190.23
- 77 Ir Iridium 192.22
- 78 Pt Platinum 195.08
- 79 Au Gold 196.97
- 80 Hg Mercury 200.59
- 81 Tl Thallium 204.
 38
38 - 82 Pb Lead 207.2
- 83 Bi Bismuth 208.98
- 84 Po Polonium (209)
- 85 At Astatine (210)
- 86 Rn Radon (222)
- 87 Fr Francium (223)
- 88 Ra Radium (226)
- 89 Ac Actinium (227)
- 90 Th Thorium 232.04
- 91 Pa Protactinium 231.04
- 92 U Uranium 238.03
- 93 Np Neptunium (237)
- 94 Pu Plutonium (244)
- 95 Am Americium (243)
- 96 Cm Curium (247)
- 97 Bk Berkelium (247)
- 98 Cf Californium (251)
- 99 Es Einsteinium (252)
- 100 Fm Fermium (257)
- 101 Md Mendelevium (258)
- 102 No Nobelium (259)
- 103 Lr Lawrencium (266)
- 104 Rf Rutherfordium (267)
- 105 Db Dubnium (268)
- 106 Sg Seaborgium (269)
- 107 Bh Bohrium (270)
- 108 Hs Hassium (277)
- 109 Mt Meitnerium (278)
- 110 Ds Darmstadtium (281)
- 111 Rg Roentgenium (282)
- 112 Cn Copernicium (285)
- 113 Nh Nihonium (286)
- 114 Fl Flerovium (289)
- 115 Mc Moscovium (290)
- 116 Lv Livermorium (293)
- 117 Ts Tennessine (294)
- 118 Og Oganesson (294)
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15Pnictogens
16Chalcogens
17Halogens
18
- Color
Minimum
Zero
Maximum
Unknown
- Scale
Atomic Symbol Name Weight
1
2
3
4
5
6
57–71
6
7
89–103
7
For elements with no stable isotopes, the mass number of the isotope with the longest half-life is in parentheses.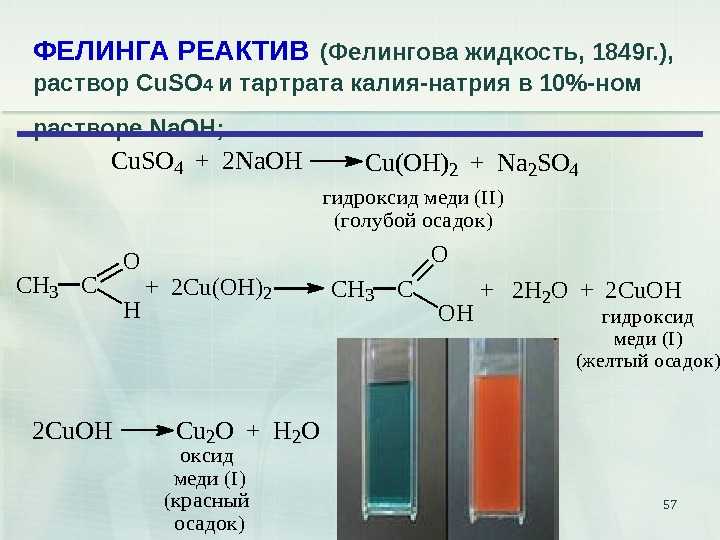
- View
- Wide
- Dark
- About
- Feature demo
- Questions
- PrivacyPrivacy
- Products
- Posters & cards
- ACSLesson plans
- Remove ads
- Editions
- Print PDF
- Image (Wide)
- LanguageAfrikaansالعربيةБългарскиবাংলাCatalàČeštinaCymraegDanskDeutschΕλληνικάEnglishEsperantoEspañolEestiفارسیSuomiFrançaisעבריתहिन्दीHrvatskiMagyarBahasaÍslenskaItaliano日本語한국어LatinaLietuviųLatviešuNederlandsNorskPolskiPortuguêsRomânăРусскийSlovenčinaSlovenščinaСрпскиSvenskaKiswahiliไทยTürkçeУкраїнськаTiếng Việt中文 (简)中文 (繁)
- Engage
- Discord Twitter Instagram
- Share
- Contact
Тренировочная работа ЕГЭ по химии-2023 №3
Тренировочная работа МИОО Статград в формате ЕГЭ по химии №3 06. 02.2023 года.
02.2023 года.
Вариант ХИ2210301. Тренировочный вариант ЕГЭ по химии №3 2023 года с ответами и решениями.
Часть 1
| Для выполнения заданий 1–3 используйте следующий ряд химических элементов: 1) Ca, 2) N, 3) Mn, 4) Br, 5) B Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду. |
1. Какие из указанных элементов имеют в основном состоянии наполовину заполненный подуровень?
Запишите номера выбранных элементов.
2. Из указанного ряда выберите три элемента, принадлежащих одному периоду Периодической системы, и расположите их в порядке увеличения электроотрицательности.
Запишите в поле ответа номера выбранных элементов в нужной последовательности.
3. Из указанного ряда выберите два элемента, которые в соединениях могут проявлять степень окисления +7.
Запишите в поле ответа номера выбранных элементов.
4. Из предложенного перечня выберите два вещества ионного строения, в которых нет ковалентных связей.
Запишите номера выбранных ответов.
1) Li2O
2) NH4NO3
3) BaO2
4) BaF2
5) CuSO4
5. Среди предложенных формул/названий веществ, расположенных в пронумерованных ячейках, выберите формулы/названия:
А) основного оксида; Б) кислой соли; В) двухосновной кислоты.
Запишите в таблицу номера ячеек, в которых расположены вещества, под соответствующими буквами.
6. В двух пробирках находился водный раствор хлорида хрома(III). В одну пробирку добавили водный раствор вещества X и наблюдали образование серо-зелёного осадка и выделение газа, а в другую – избыток водного раствора вещества Y, в результате чего сначала образовался серо-зелёный осадок, который затем растворился.
Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции.
1) NaOH
2) Na2CO3
3) NH3
4) HF
5) H2S
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
7. Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | РЕАГЕНТЫ |
| А) NH3 Б) NO В) HNO3 Г) Ca(NO3)2 | 1) S, NaCl, CO2 2) KOH, Al, P4 3) KMnO4, O2, H2 4) Na2CO3, NH4F, MgSO4 5) H2SO4, CO2, O2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
8. Установите соответствие между исходными веществами, вступающими в реакцию, и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТЫ РЕАКЦИИ |
| А) PCl3 + H2O Б) PCl3 + Cl2 + H2O В) PH3 + O2 Г) H3PO3(нагревание) | 1) H3PO2 + O2 2) HPO3 + H2O 3) H3PO4 + PH3 4) H3PO3 + HCl 5) H3PO4 + HCl 6) P + HCl |
Запишите в таблицу выбранные цифры под соответствующими буквами.
9. Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1) KOH
2) KMnO4
3) BaO2
4) SO2
5) NO
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
10. Установите соответствие между общей формулой и названием класса/группы органических соединений: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ОБЩАЯ ФОРМУЛА РЯДА | НАЗВАНИЕ КЛАССА/ГРУППЫ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ |
| А) CnH2n–6 Б) CnH2n–6O В) CnH2nO | 1) одноатомные спирты с одной двойной связью 2) фенолы 3) арены 4) алкатриены |
Запишите в таблицу выбранные цифры под соответствующими буквами.
11. Из предложенного перечня выберите два вещества, у которых есть геометрические изомеры.
Запишите номера выбранных ответов.
1) бутин-2
2) пентен-1
3) бутен-2-овая кислота
4) молочная кислота
5) 1,2-дихлорциклопропан
12. Из предложенного перечня выберите все вещества, реагирующие с альдегидами, но не реагирующие с кетонами.
Запишите номера выбранных ответов.
1) H2
2) H2O
3) Br2(H2O)
4) KMnO4
5) Cu(OH)2
13. Из предложенного перечня выберите два вещества, из которых в одну стадию можно получить этиламин.
Запишите номера выбранных ответов.
1) N2
2) CH3NH2
3) (CH3)2NH
4) CH3CH2NO2
5) CH3C≡N
14. Установите соответствие между реагирующими веществами и органическим продуктом, который преимущественно образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТ ВЗАИМОДЕЙСТВИЯ |
| А) бутен-1 и вода (H+) Б) бензол и ацетилхлорид (AlCl3) В) 1,6-дибромгексан и натрий Г) винилацетилен и хлороводород |
Запишите в таблицу выбранные цифры под соответствующими буквами.
15. Установите соответствие между схемой реакции и веществом Х, принимающим в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА РЕАКЦИИ | ВЕЩЕСТВО X |
3) CH3OH 4) CH3Cl 5) CH3CH=O 6) CH3OC2H5 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
16. Задана следующая схема превращений веществ:
циклопропан → X → HO(CH2)3OH Y
Определите, какие из указанных веществ являются веществами X и Y.
1) пропен
2) 1-хлорпропан
3) 1,3-дибромпропан
4) пропандиол-1,2
5) пропандиовая кислота
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
17. Из предложенного перечня типов реакций выберите все, которые характеризуют реакцию бензола с хлором в присутствии хлорида алюминия.
Запишите номера выбранных ответов.
1) гетерогенная
2) реакция замещения
3) каталитическая
4) реакция обмена
5) реакция нейтрализации
18. Укажите все факторы, от которых зависит скорость реакции нейтрализации в водном растворе.
Запишите номера выбранных ответов.
1) температура
2) объём раствора
3) давление над раствором
4) концентрация кислоты
5) концентрация щёлочи
19. Установите соответствие между схемой реакции и свойством, которое проявляет элемент азот в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА РЕАКЦИИ | СВОЙСТВО АЗОТА |
| А) NO2 + O3 → N2O5 + O2 Б) NO2 + CO → NO + CO2 В) NO2 + Ba(OH)2 → Ba(NO3)2 + Ba(NO2)2 + H2O | 1) является окислителем 2) является восстановителем 3) является и окислителем, и восстановителем 4) не изменяет степень окисления |
Запишите в таблицу выбранные цифры под соответствующими буквами.
20. Установите соответствие между формулой вещества и продуктом(ами) электролиза водного раствора этого вещества, образовавшим(и)ся на инертном аноде: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | ПРОДУКТ(Ы) НА АНОДЕ |
| А) KCl Б) HCOOK В) KClO4 | 1) кислород 2) галоген 3) галогеноводород 4) углекислый газ и водород |
Запишите в таблицу выбранные цифры под соответствующими буквами.
| Для выполнения задания 21 используйте следующие справочные данные. Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V). pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики |
21. Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую молярную концентрацию.
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
1) NaCl
2) NaClO2
3) HClO4
4) HClO
22. Установите соответствие между способом воздействия на равновесную систему
и направлением смещения равновесия при этом воздействии: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СПОСОБ ВОЗДЕЙСТВИЯ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ РАВНОВЕСИЯ |
| А) нагревание Б) увеличение давления В) добавление твёрдого AgCl Г) добавление твёрдого AgNO3 | 1) смещается в сторону прямой реакции 2) смещается в сторону обратной реакции 3) практически не смещается |
Запишите в таблицу выбранные цифры под соответствующими буквами.
23. В реактор постоянного объёма ввели циклогексан и сильно нагрели.
В реакторе установилось равновесие:
C6H12(г) ↔ C6H6(г) + 3H2(г)
(Температуру в ходе реакции поддерживали постоянной. Другие процессы в системе не протекают.)
Исходная концентрация циклогексана была равна 25 ммоль/л, а равновесная концентрация паров бензола составила 10 ммоль/л. Найдите равновесные концентрации циклогексана (X) и водорода (Y).
Выберите из списка номера правильных ответов.
1) 10 ммоль/л
2) 15 ммоль/л
3) 20 ммоль/л
4) 25 ммоль/л
5) 30 ммоль/л
6) 50 ммоль/л
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
24. Установите соответствие между названием вещества и признаком реакции, который наблюдается при взаимодействии вещества с аммиачным раствором оксида серебра: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВЕЩЕСТВО | ПРИЗНАК РЕАКЦИИ |
| А) пропаналь Б) пероксид водорода В) соляная кислота Г) иодид натрия | 1) видимые признаки отсутствуют 2) образование белого осадка 3) образование жёлтого осадка 4) образование тёмного осадка 5) выделение газа |
Запишите в таблицу выбранные цифры под соответствующими буквами.
25. Установите соответствие между названием материала и способом его получения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| МАТЕРИАЛ | СПОСОБ ПОЛУЧЕНИЯ |
| А) силиконовый каучук Б) резина В) политетрафторэтилен | 1) полимеризация 2) гидролиз 3) поликонденсация 4) вулканизация |
Запишите в таблицу выбранные цифры под соответствующими буквами.
26. В 207,8 г воды растворили 57,2 г кристаллической соды (декагидрата карбоната натрия). Рассчитайте массовую долю (в %) карбоната натрия в полученном растворе.
(Запишите число с точностью до целых.)
27. Дано термохимическое уравнение:
3MnO2 + 4Al = 3Mn + 2Al2O3 + 1785 кДж
Сколько теплоты (в кДж) выделилось, если в результате реакции образовалось 22 г марганца? (Запишите число с точностью до целых.)
28. При пиролизе 56 л метана образовалось 16,8 л ацетилена. Объёмы газов измерены при одинаковых условиях. Вычислите выход продукта реакции (в %). Ответ запишите с точностью до целых.
Вычислите выход продукта реакции (в %). Ответ запишите с точностью до целых.
| Для записи ответов на задания 29–34 используйте чистый лист бумаги. Запишите сначала номер задания (29, 30 и т.д.), а затем его подробное решение. Ответы записывайте чётко и разборчиво. |
| Для выполнения заданий 29 и 30 используйте следующий перечень веществ: хлорид бария, иодид аммония, разбавленная серная кислота, карбонат натрия, фосфат магния, диоксид марганца. Допустимо использование воды в качестве среды для протекания реакции. |
29. Из предложенного перечня выберите вещества, между которыми окислительно-восстановительная реакция протекает с изменением цвета раствора.
В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30. Из предложенного перечня выберите вещества, которые вступают в реакцию ионного обмена без образования осадка и выделения газа. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
31. К твёрдому нитрату натрия добавили концентрированную серную кислоту и нагрели смесь. Выделившиеся пары сконденсировали, полученную жидкость прилили к иоду и нагрели до растворения последнего. Твёрдое вещество, полученное при выпаривании раствора, поместили в две пробирки. В одну добавили иодоводородную кислоту, в другую – подкисленный раствор сульфата железа(II). В обеих пробирках наблюдали изменение цвета раствора.
Напишите молекулярные уравнения четырёх описанных реакций.
32. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
ацетат калия → X1 → C2H5Cl → C6H5C2H5 → X2 → полимер.
При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
33. Органическое вещество X содержит 30,0 % кислорода, 17,5 % азота, 7,5 % водорода по массе. При нагревании 1 моль вещества с избытком концентрированного раствора гидроксида калия образуются 1 моль этанола и 2 моль органической соли.
На основании данных условий задачи:
1) проведите необходимые вычисления (указывайте единицы измерения и обозначения искомых физических величин) и установите молекулярную формулу вещества X;
2) составьте возможную структурную формулу вещества X, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции X с избытком гидроксида калия (в уравнении используйте структурные формулы органических веществ).
34. Навеску нитрата натрия прокалили в течение непродолжительного времени и получили твёрдый остаток массой 18,53 г, который растворили в воде. При взаимодействии раствора с избытком алюминия в щелочной среде образуется 5,60 л аммиака (в пересчёте на н. у.). Определите, сколько процентов нитрата натрия разложилось, и найдите массу исходной навески.
При взаимодействии раствора с избытком алюминия в щелочной среде образуется 5,60 л аммиака (в пересчёте на н. у.). Определите, сколько процентов нитрата натрия разложилось, и найдите массу исходной навески.
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения и обозначения искомых физических величин).
Понравилось это:
Нравится Загрузка…
Дозиметрия гамма-излучения с использованием термолюминесцентного люминофора NaCl:Ba(T) (Журнальная статья)
Дозиметрия гамма-излучения с использованием термолюминесцентного люминофора NaCl:Ba(T) (Журнальная статья) | ОСТИ.GOVперейти к основному содержанию
- Полная запись
- Другое связанное исследование
Представлено подробное исследование термолюминесцентных (ТЛ) характеристик необработанного и термообработанного чистого NaCl и NaCl, легированного Ba, при воздействии гамма-излучения при комнатной температуре. Было обнаружено, что люминофор NaCl:Ba (молярная доля 10(-2)), закаленный от 750°C, обозначенный как NaCl:Ba(T), дает ярко выраженный выход TL с четко определенным пиком свечения около 220°C (пик III) вместе с другими пиками при более низких температурах. Предполагается, что центр ТЛ, связанный с пиком свечения III, состоит из примесно-вакансионного диполя с отрицательной ионной вакансией в его окрестности. Предполагается, что центры ТЛ расположены в дислокационной области. Также были исследованы дозиметрические свойства пика III после гамма-облучения. Замечено, что люминофор удовлетворяет большинству основных требований к эффективному материалу TLD.
Было обнаружено, что люминофор NaCl:Ba (молярная доля 10(-2)), закаленный от 750°C, обозначенный как NaCl:Ba(T), дает ярко выраженный выход TL с четко определенным пиком свечения около 220°C (пик III) вместе с другими пиками при более низких температурах. Предполагается, что центр ТЛ, связанный с пиком свечения III, состоит из примесно-вакансионного диполя с отрицательной ионной вакансией в его окрестности. Предполагается, что центры ТЛ расположены в дислокационной области. Также были исследованы дозиметрические свойства пика III после гамма-облучения. Замечено, что люминофор удовлетворяет большинству основных требований к эффективному материалу TLD.
- Авторов:
- Махаджан, О.
 Х.; Джоши, Т. Р.; Намби, К. С.; Джоши, Р.В.
Х.; Джоши, Т. Р.; Намби, К. С.; Джоши, Р.В.
- Дата публикации:
- Исследовательская организация:
- Унив. Барода (Индия)
- Идентификатор ОСТИ:
- 6985449
- Тип ресурса:
- Журнальная статья
- Название журнала:
- Физика здоровья; (США)
- Дополнительная информация журнала:
- Объем журнала: 51:1
- Страна публикации:
- США
- Язык:
- Английский
- Тема:
- 61 РАДИАЦИОННАЯ ЗАЩИТА И ДОЗИМЕТРИЯ; БАРИЙ; КОЛИЧЕСТВЕННОЕ СООТНОШЕНИЕ; НАТРИЯ ХЛОРИДА; ТЕРМОЛЮМИНЕСЦЕНТНАЯ ДОЗИМЕТРИЯ; ГАММА-ИЗЛУЧЕНИЕ; ФОСФОРЫ; СОЕДИНЕНИЯ ЩЕЛОЧНЫХ МЕТАЛЛОВ; ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ; ХЛОРИДЫ; СОЕДИНЕНИЯ ХЛОРА; ДОЗИМЕТРИЯ; ЭЛЕКТРОМАГНИТНОЕ ИЗЛУЧЕНИЕ; ЭЛЕМЕНТЫ; ГАЛИДЫ; ГАЛОГЕННЫЕ СОЕДИНЕНИЯ; ИОНИЗИРУЮЩЕЕ ИЗЛУЧЕНИЕ; МЕТАЛЛЫ; ИЗЛУЧЕНИЕ; СОЕДИНЕНИЯ НАТРИЯ; 655003* — Медицинская физика- Дозиметрия
Форматы цитирования
- MLA
- АПА
- Чикаго
- БибТекс
Махаджан О. Х., Джоши Т.Р., Намби К.С. и Джоши Р.В. Дозиметрия гамма-излучения с использованием термолюминофора NaCl:Ba(T) . США: Н. П., 1986.
Веб. дои: 10.1097/00004032-198607000-00011.
Х., Джоши Т.Р., Намби К.С. и Джоши Р.В. Дозиметрия гамма-излучения с использованием термолюминофора NaCl:Ba(T) . США: Н. П., 1986.
Веб. дои: 10.1097/00004032-198607000-00011.
Копировать в буфер обмена
Махаджан О.Х., Джоши Т.Р., Намби К.С. и Джоши Р.В. Дозиметрия гамма-излучения с использованием термолюминофора NaCl:Ba(T) . Соединенные Штаты. https://doi.org/10.1097/00004032-198607000-00011
Копировать в буфер обмена
Махаджан, О. Х., Джоши, Т. Р., Намби, К. С., и Джоши, Р. В. 1986.
«Дозиметрия гамма-излучения с использованием термолюминофора NaCl: Ba (T)». Соединенные Штаты. https://doi.org/10.1097/00004032-198607000-00011.
Копировать в буфер обмена
@статья{osti_6985449,
title = {Дозиметрия гамма-излучения с использованием термолюминесцентного люминофора NaCl:Ba(T)},
автор = {Махаджан, О. Х., и Джоши, Т. Р., и Намби, К. С., и Джоши, Р. В.},
Х., и Джоши, Т. Р., и Намби, К. С., и Джоши, Р. В.},
abstractNote = {Представлено подробное исследование термолюминесцентных (TL) характеристик необработанного и термообработанного чистого NaCl и NaCl, легированного Ba, под воздействием гамма-излучения при комнатной температуре. Было обнаружено, что люминофор NaCl:Ba (молярная доля 10(-2)), закаленный от 750°C, обозначенный как NaCl:Ba(T), дает ярко выраженный выход TL с четко определенным пиком свечения около 220°C (пик III) вместе с другими пиками при более низких температурах. Предполагается, что центр ТЛ, связанный с пиком свечения III, состоит из примесно-вакансионного диполя с отрицательной ионной вакансией в его окрестности. Предполагается, что центры ТЛ расположены в дислокационной области. Также были исследованы дозиметрические свойства пика III после гамма-облучения. Отмечено, что люминофор удовлетворяет большинству основных требований к эффективному материалу TLD.},
дои = {10.1097/00004032-198607000-00011},
URL-адрес = {https://www. osti.gov/biblio/6985449},
журнал = {Физика здоровья; (США)},
osti.gov/biblio/6985449},
журнал = {Физика здоровья; (США)},
номер = ,
объем = 51:1,
место = {США},
год = {1986},
месяц = {7}
}
Копировать в буфер обмена
https://doi.org/10.1097/00004032-198607000-00011
Найти в Google Scholar
Поиск в WorldCat, чтобы найти библиотеки, в которых может храниться этот журнал Вы должны войти в систему или создать учетную запись, чтобы сохранять документы в своей библиотеке.
Аналогичных записей в сборниках OSTI.GOV:
- Аналогичные записи
Что такое хлорид натрия и как он используется?
Что такое хлорид натрия и как он используется?- Заболевания
- Избранные
- Рак груди
- ВЗК
- Мигрень
- Рассеянный склероз (РС)
- Ревматоидный артрит
- Диабет 5 6 90 9009 Тип 2 009
- Статьи
- Кислотный рефлюкс
- СДВГ
- Аллергия
- Болезнь Альцгеймера и деменция
- Биполярное расстройство
- Рак
- Болезнь Крона
- Хроническая боль
- Простуда и грипп
- ХОБЛ
6
Депрессия
- Болезнь сердца
- Высокий уровень холестерина
- ВИЧ
- Гипертония
- IPF
- Остеоартрит
- Псориаз
- Кожные заболевания и уход
- ЗППП
- Discover
- Темы о здоровье
- Питание
- Фитнес
- Уход за кожей
- Сексуальное здоровье
- Женское здоровье
- Психическое благополучие
- Обзор продуктов
- Темы о здоровье
- Витамины и добавки
- Сон
- Психическое здоровье
- Питание
- Домашнее тестирование
- CBD
- Men’s Health
- Избранные
- Оригинальная серия
- Fresh Food Fast
- Дневники диагностики
- Ты не одинок
- Настоящее время
- Серия видео
- Молодежь в фокусе
- Здоровый урожай
- Больше нет 90 Тишина 6
- 6 90 90 9
- План
- Проблемы со здоровьем
- Внимательное питание
- Разбор сладкого
- Двигайтесь своим телом
- Здоровье кишечника
- Продукты для настроения
- Выровняйте позвоночник
- Find Care
- Первичная медико-санитарная помощь
- Психическое здоровье
- Акушер-гинеколог
- Дерматологи
- Неврологи
- Кардиологи
- Ортопеды
- 6 Lifestyle Quizzes
- Управление весом
- У меня депрессия? Викторина для подростков
- Вы трудоголик?
- Как хорошо ты спишь?
9
- Инструменты и ресурсы
- Новости здравоохранения
- Найдите диету
- Найдите полезные закуски
- Лекарства от A до Z
- Здоровье от A до Z
- Проблемы со здоровьем
- Connect
- Рак молочной железы
- Воспалительные заболевания кишечника
6 Псориатический артрит
6
- 5 Мигрень
- Рассеянный склероз
- Псориаз
Медицинское обследование Джудит Марчин, доктор медицинских наук — Джулия Хаскинс — Обновлено 29 сентября 2018 г.
Что такое хлорид натрия?
Хлорид натрия (NaCl), также известный как соль, является важным соединением, которое наш организм использует для:
- поглощать и транспортировать питательные вещества
- поддерживать кровяное давление
- поддерживать правильный баланс жидкости
- передавать нервные сигналы
- сокращать и расслаблять мышцы
Соль является неорганическим соединением, то есть она не происходит из живой материи. Он образуется, когда Na (натрий) и Cl (хлорид) объединяются, образуя белые кристаллические кубики.
Ваше тело нуждается в соли, чтобы функционировать, но слишком мало или слишком много соли может быть вредным для вашего здоровья.
Хотя соль часто используется для приготовления пищи, ее также можно найти в качестве ингредиента в пищевых продуктах или очищающих растворах. В медицинских случаях ваш врач или медсестра обычно вводят хлорид натрия в виде инъекции. Читайте дальше, чтобы узнать, почему и как соль играет важную роль в вашем организме.
Несмотря на то, что многие люди используют слова натрий и соль как синонимы, они разные. Натрий — это минерал и питательное вещество, встречающееся в природе. Необработанные продукты, такие как свежие овощи, бобовые и фрукты, могут естественным образом содержать натрий. В пищевой соде тоже есть натрий.
Но от 75 до 90 процентов натрия мы получаем из соли, уже добавленной в наши продукты. Вес соли обычно представляет собой комбинацию 40 процентов натрия и 60 процентов хлорида.
Чаще всего соль используется в пищевых продуктах. Его применение включает:
- пищевую приправу
- действие в качестве натурального консерванта
- усиление естественного цвета пищевых продуктов
- вяление или консервирование мяса
- создание рассола для маринования пищевых продуктов
Существует также широкий спектр бытовых применений, таких как:
- очистка кастрюль и сковородок
- предотвращение образования плесени
- удаление пятен и жира
- соление дорог зимой для предотвращения образования льда
когда врач прописывает лечение с солью они будут использовать термин хлорид натрия. Хлорид натрия, смешанный с водой, образует солевой раствор, который используется в различных медицинских целях.
Хлорид натрия, смешанный с водой, образует солевой раствор, который используется в различных медицинских целях.
Медицинское применение солевого раствора включает:
Хотя соль и натрий разные, соль на 40 процентов состоит из натрия, и мы получаем большую часть потребляемого нами натрия из соли. Многие компании и рестораны используют соль для консервации, приправы и придания вкуса еде. Поскольку в одной чайной ложке соли содержится около 2300 миллиграммов (мг) натрия, дневную норму легко превысить.
По данным CDC, средний американец съедает более 3400 мг каждый день. Вы можете ограничить потребление натрия, употребляя в пищу необработанные продукты. Вам также может быть легче контролировать потребление натрия, если вы готовите больше еды дома.
Американские рекомендации по питанию рекомендуют американцам потреблять менее 2300 мг натрия в день.
Диета с низким содержанием натрия
Ваш врач может порекомендовать придерживаться диеты с низким содержанием натрия, если вы подвержены риску высокого кровяного давления или сердечных заболеваний. Если у вас есть сердечные заболевания, вы должны потреблять менее 2000 мг натрия в день, хотя Американская кардиологическая ассоциация (AHA) рекомендует не превышать 1500 мг. Устранение обработанных пищевых продуктов, таких как колбасы и готовые блюда, может облегчить поддержание этого числа.
Если у вас есть сердечные заболевания, вы должны потреблять менее 2000 мг натрия в день, хотя Американская кардиологическая ассоциация (AHA) рекомендует не превышать 1500 мг. Устранение обработанных пищевых продуктов, таких как колбасы и готовые блюда, может облегчить поддержание этого числа.
Десять лучших замороженных блюд с низким содержанием натрия »
Всасывание и транспортировка питательных веществ
Натрий и хлориды играют важную роль в тонком кишечнике. Натрий помогает вашему организму усваивать:
- хлорид
- сахар
- воду
- аминокислоты (строительные блоки белка)
хлорид в форме соляной кислоты (водород и хлорид) также является компонентом желудочного сока. сок. Это помогает вашему телу переваривать и усваивать питательные вещества.
Поддержание энергии покоя
Натрий и калий являются электролитами в жидкости снаружи и внутри ваших клеток. Баланс между этими частицами влияет на то, как ваши клетки поддерживают энергию вашего тела.
Это также то, как нервы посылают сигналы в мозг, ваши мышцы сокращаются и ваше сердце работает.
Поддержание артериального давления и гидратации
Ваши почки, мозг и надпочечники совместно регулируют количество натрия в организме. Химические сигналы стимулируют почки либо удерживать воду, чтобы она могла повторно всасываться в кровоток, либо избавляться от лишней воды с мочой.
Когда в крови слишком много натрия, мозг дает сигнал почкам выпустить больше воды в кровоток. Это приводит к увеличению объема крови и артериального давления. Уменьшение потребления натрия может привести к тому, что меньше воды будет всасываться в кровоток. В результате снижается кровяное давление.
По большей части хлорид натрия не представляет опасности для здоровья, но в чрезмерных количествах он может раздражать:
- глаза
- кожу
- дыхательные пути
- желудок
Вы можете лечить раздражение, в зависимости от области, промывая место чистой водой или выходя на свежий воздух. Обратитесь за медицинской помощью, если раздражение не прекращается.
Обратитесь за медицинской помощью, если раздражение не прекращается.
Избыток соли
Хотя натрий необходим, он также содержится в больших количествах практически во всем, что мы едим. Употребление слишком большого количества соли связано с:
- высоким кровяным давлением
- повышенным риском заболеваний сердца и почек
- повышенным удержанием воды, что может привести к отекам в теле
- обезвоживание
Побочные эффекты солевых растворов
Солевые растворы обычно вводят внутривенно или через вену. Высокие концентрации солевых растворов могут вызывать побочные эффекты в виде покраснения или отека в месте инъекции.
Слишком мало натрия
Дефицит натрия обычно является признаком основного заболевания. Название этого состояния — гипонатриемия. Это может быть связано с:
- неадекватной секрецией антидиуретического гормона (АДГ), вызванной нарушениями, влияющими на гормональный баланс, некоторыми лекарствами и некоторыми заболеваниями
- чрезмерное потребление воды
- длительная рвота или диарея
- употребление некоторых диуретиков
- некоторые заболевания почек марафоны и триатлоны.

От 75 до 90 процентов нашего потребления натрия поступает из соли или хлорида натрия. Соль содержит важный минерал (натрий), который наш организм использует для таких функций, как поддержание артериального давления и усвоение питательных веществ. Вы также можете использовать соль для приправы к пище, чистки предметов домашнего обихода и решения определенных медицинских проблем.
Американские рекомендации по питанию рекомендуют употреблять менее 2300 мг натрия в день. Вы можете сделать это, употребляя меньше продуктов, подвергшихся технологической обработке, таких как мясное ассорти и полуфабрикаты, а также готовя еду дома.
В каких продуктах содержится наименьшее количество натрия? »
Слишком много соли может привести к более серьезным проблемам со здоровьем, таким как высокое кровяное давление, болезни сердца и почек. Снижение потребления соли при одновременном увеличении количества получаемого калия может помочь снизить риск возникновения этих состояний.

Перед добавлением в рацион большего количества хлорида натрия следует проконсультироваться с врачом. Большинство людей превышают рекомендуемое количество, но люди, которые пьют чрезмерное количество воды, страдают постоянной диареей или участвуют в длительных соревнованиях на выносливость, могут иметь дефицит натрия. В этих случаях может помочь хорошая оральная гидратация. В более тяжелых случаях медицинскому работнику может потребоваться введение физиологического раствора внутривенно (в/в) для восстановления гидратации и электролитов.
Последний медицинский осмотр 18 августа 2016 г.
Как мы рецензировали эту статью:
Healthline придерживается строгих правил выбора поставщиков и опирается на рецензируемые исследования, академические исследовательские институты и медицинские ассоциации. Мы избегаем использования третичных ссылок. Вы можете узнать больше о том, как мы обеспечиваем точность и актуальность нашего контента, прочитав нашу редакционную политику.

- О натрии (соли). (2015, 8 декабря)
heart.org/HEARTORG/HealthyLiving/HealthyEating/Nutrition/About-Sodium-Salt_UCM_463416_Article.jsp#.V6o8NLQye20 - Риск для здоровья и заболевания, связанные с солью и натрием. (без даты)
hsph.harvard.edu/nutritionsource/salt-and-sodium/sodium-health-risks-and-disease/ - Хигдон, Дж. (2008 г., ноябрь). Натрий (хлорид)
lpi.oregonstate.edu/mic/minerals/sodium — источники - Безопасность с солью: Информация о безопасности хлорида натрия. (2015, 10 апреля)
msdsonline.com/blog/health-safety/2015/04/10/safety-with-salt-sodium-chloride-safety-information - Раствор хлорида натрия для ингаляций. (2014, сентябрь)
dailymed.nlm.nih.gov/dailymed/fda/fdaDrugXsl.cfm?setid=34375b61-0af7-4ed9-8bdb-0538ecc9068c - Натрий: факты. (2016, апрель)
cdc.gov/salt/pdfs/sodium_fact_sheet.pdf
Поделиться этой статьей
Медицинский обзор Джудит Марцин, доктора медицины — Джулия Хаскинс — Обновлено 29 сентября 2018 г.

Читать далее
6 Малоизвестные опасности чрезмерного ограничения натрия
Автор: Hrefna Palsdottir, MS
Для снижения артериального давления часто рекомендуется уменьшить потребление натрия. Вот 6 причин, по которым слишком сильное ограничение натрия может быть вредным.
ПОДРОБНЕЕ
Полезны ли соленья?
Медицинское заключение Натали Батлер, доктор медицинских наук, доктор медицинских наук.
Люди говорят о пользе соленых огурцов для здоровья, ссылаясь на потерю веса, лечение диабета и даже противораковые свойства. Здесь узнайте, что…
ПОДРОБНЕЕ
Питание при высоком кровяном давлении: продукты и напитки, которых следует избегать
Диета может оказать большое влияние на ваше кровяное давление. Мы рассмотрим основные продукты, повышающие артериальное давление, а также продукты, которые следует есть и которых следует избегать, чтобы…
ПОДРОБНЕЕ
6 продуктов с низким содержанием натрия для улучшения здоровья сердца
Медицинский обзор Натали Олсен, доктор медицинских наук, L.
 D., ACSM EP-C
D., ACSM EP-CСлишком много соли в вашем рационе может привести к высокому кровяному давлению, которое человеку трудно обнаружить, особенно поначалу. Узнайте о продуктах с низким…
ПОДРОБНЕЕ
Гипонатриемия: понимание низкого уровня натрия в крови
Медицинское заключение Мередит Гудвин, доктора медицинских наук, FAAFP
Низкий уровень натрия в крови или гипонатриемия возникает, когда в организме нарушается баланс воды и натрия. Это может вызвать слабость, головную боль, тошноту и мышечные…
ПОДРОБНЕЕ
Бикарбонат натрия и эффективность упражнений
Алина Петре, MS, RD (NL) и Katey Davidson, MScFN, RD, CPT
Бикарбонат натрия (пищевая сода) полезен для физической работоспособности. Она может повысить силу, координацию и повысить интенсивность упражнений…
ПОДРОБНЕЕ
Кошерная соль: что это такое, в сравнении с кошерной солью.

- О натрии (соли). (2015, 8 декабря)

 008
008 45
45 922
922 82
82 93
93 38
38 Х.; Джоши, Т. Р.; Намби, К. С.; Джоши, Р.В.
Х.; Джоши, Т. Р.; Намби, К. С.; Джоши, Р.В.



 D., ACSM EP-C
D., ACSM EP-C