Ca + O2 → CaO2 | Химические Уравнения oнлайн! — Orașul Löbau
Ca + O2 → CaO2 | Химические Уравнения oнлайн! — Orașul Löbau — document PDFliblib.ro
Ca + O 2 → CaO · Названия: Кальций, Кальций (порошок), Ca · Внешность (состояние): От серебристо-белого до серого цвета порошок …
Ca + O2 → CaO2 | Химические Уравнения oнлайн!
Ca + O 2 → CaO · Названия: Кальций, Кальций (порошок), Ca · Внешность (состояние): От серебристо-белого до серого цвета порошок …
2 Ca + O2 → 2 CaO | Химические Уравнения oнлайн!
Ca. Названия: Кальций, Кальций (порошок), Ca Внешность (состояние): От серебристо-белого до серого цвета порошок · O Названия: Молекулярный кислород, …
2 K2O → 4 K + O2 | Химические Уравнения oнлайн!
Решенное и коэффициентами уравнение реакции 2 K2O → 4 K + O2 с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
Al(OH)3 → Al + 3 OH | Химические Уравнения oнлайн!
Решенное и коэффициентами уравнение реакции Al(OH)3 → Al + 3 OH с дополненными продуктами.
2 KClO3 → 2 KCl + 3 O2 | Химические Уравнения oнлайн!
Решенное и коэффициентами уравнение реакции 2 KClO3 → 2 KCl + 3 O2 с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
2 AlCl3 → 2 Al + 3 Cl2 | Химические Уравнения oнлайн!
Решенное и коэффициентами уравнение реакции 2 AlCl3 → 2 Al + 3 Cl2 с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
2 NaCl → 2 Na + Cl2 | Химические Уравнения oнлайн!
Решенное и коэффициентами уравнение реакции 2 NaCl → 2 Na + Cl2 с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
2 Na + Cl2 → 2 NaCl | Химические Уравнения oнлайн!
2 Na + Cl 2 → 2 NaCl · Названия: Хлор · Внешность (состояние): От зеленоватого до желтого цвета сжатый сжиженный газ с резким запахом …
2 C2H5OH → 2 h3O + h3 + C4H6 | Химические Уравнения oнлайн!
Решенное и коэффициентами уравнение реакции 2 C2H5OH → 2 h3O + h3 + C4H6 с дополненными продуктами. Приложение для вычисления и дополнения продуктов …
Приложение для вычисления и дополнения продуктов …
AlCl3 + 3 Na → 3 NaCl + Al | Химические Уравнения oнлайн!
Решенное и коэффициентами уравнение реакции AlCl3 + 3 Na → 3 NaCl + Al с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
4 h4PO3 → 3 h4PO4 + Ph4 | Химические Уравнения oнлайн!
Решенное и коэффициентами уравнение реакции 4 h4PO3 → 3 h4PO4 + Ph4 с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
3 HNO2 → HNO3 + 2 NO + h3O | Химические Уравнения oнлайн!
Решенное и коэффициентами уравнение реакции 3 HNO2 → HNO3 + 2 NO + h3O с дополненными продуктами. Приложение для вычисления и дополнения продуктов реакции.
h3SO4 + h3O → HSO4:- + h4O:+ | Химические Уравнения oнлайн!
Решенное и коэффициентами уравнение реакции h3SO4 + h3O → HSO4:- + h4O:+ с дополненными продуктами. Приложение для вычисления и дополнения продуктов …
Ch4COOH → Ch3CO + h3O | Химические Уравнения oнлайн!
Решенное и коэффициентами уравнение реакции Ch4COOH → Ch3CO + h3O с дополненными продуктами.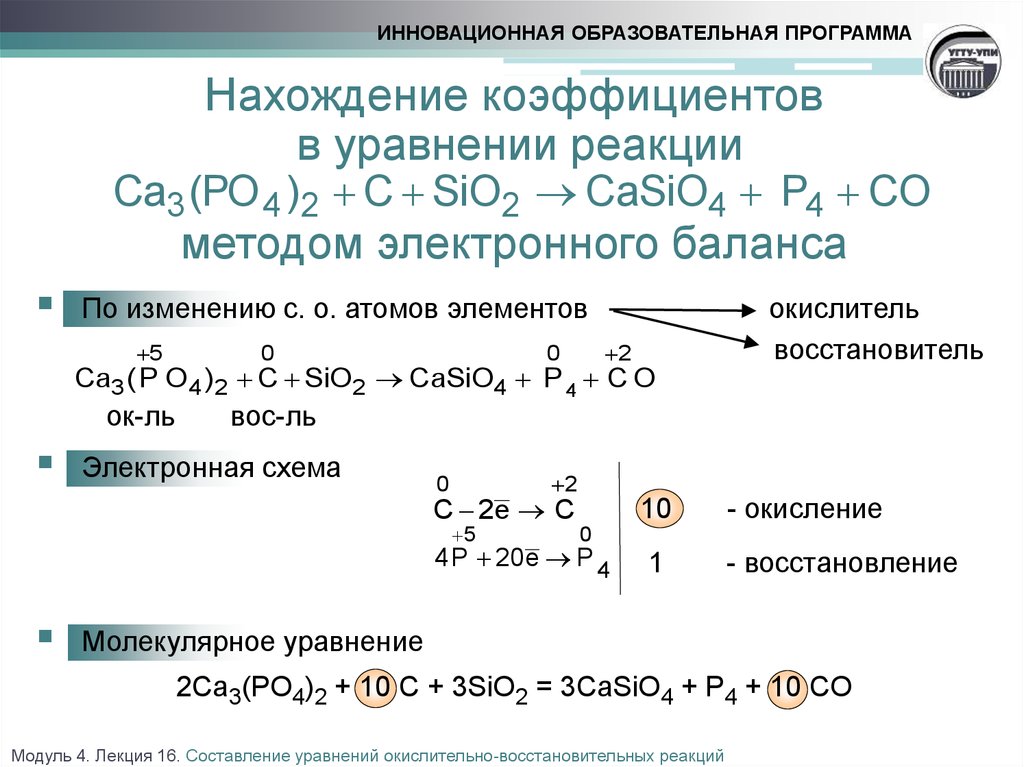 Приложение для вычисления и дополнения продуктов реакции.
Приложение для вычисления и дополнения продуктов реакции.
Cu + Ca(OH)2 = Cu(OH) + Ca — Решённые химические уравнения
Как уравнять химическую реакцию. Прочитайте нашу статью на Как уравнивать уравнения либо попросите помощи в нашем чате. You can also ask for help in our …
K2O + h3O = KOH — Решённые химические уравнения
Уравняйте K2O + h3O = KOH химическое уравнение или реакцию с помощью этого калькулятора!
Fe + CuSO4 = Fe(SO4)3 + Cu — Решённые химические уравнения
Уравняйте Fe + CuSO4 = Fe(SO4)3 + Cu химическое уравнение или реакцию с помощью этого калькулятора!
Ca + O2 = CaO — Решённые химические уравнения — ChemicalAid
Уравняйте Ca + O2 = CaO химическое уравнение или реакцию с помощью этого калькулятора!
Al(OH)3 = Al2O3 + h3O — Решённые химические уравнения
Al(OH)3 = Al2O3 + h3O — Решённые химические уравнения · Решённые химические уравнения · Reaction Information · Инструкции · Как уравнять химическую реакцию · Примеры.
h3P = H + P — Решённые химические уравнения — ChemicalAid
Уравняйте h3P = H + P химическое уравнение или реакцию с помощью этого калькулятора!
SiO3 + C = Si + CO — Решённые химические уравнения
Уравняйте SiO3 + C = Si + CO химическое уравнение или реакцию с помощью этого калькулятора!
CaI2 = Ca + I — Решённые химические уравнения — ChemicalAid
Уравняйте CaI2 = Ca + I химическое уравнение или реакцию с помощью этого калькулятора!
HSO4 + h3 = h3SO4 — Решённые химические уравнения
CuCi + Ci2 = CuCi2 — Решённые химические уравнения
Уравняйте CuCi + Ci2 = CuCi2 химическое уравнение или реакцию с помощью этого калькулятора!
Cu + Ci2 = CuCi — Решённые химические уравнения — ChemicalAid
Уравняйте Cu + Ci2 = CuCi химическое уравнение или реакцию с помощью этого калькулятора!
P2O5 + h3O = HPO4 + h3 — Решённые химические уравнения
Уравняйте P2O5 + h3O = HPO4 + h3 химическое уравнение или реакцию с помощью этого калькулятора!
Na + Cl = NaCl — Решённые химические уравнения — ChemicalAid
Уравняйте Na + Cl = NaCl химическое уравнение или реакцию с помощью этого калькулятора!
HPO4 + H = h4PO4 — Решённые химические уравнения
Уравняйте HPO4 + H = h4PO4 химическое уравнение или реакцию с помощью этого калькулятора!
AlCl3 = Al + Cl2 — Решённые химические уравнения — ChemicalAid
AlCl3 = Al + Cl2 — Решённые химические уравнения.
KClO3 = O2 + KCl — Решённые химические уравнения — ChemicalAid
Уравняйте KClO3 = O2 + KCl химическое уравнение или реакцию с помощью этого калькулятора!
HCl + NaOH = NaCl + h3O — Решённые химические уравнения
Уравняйте HCl + NaOH = NaCl + h3O химическое уравнение или реакцию с помощью этого калькулятора!
Si + C = SiC4 — Решённые химические уравнения — ChemicalAid
Уравняйте Si + C = SiC4 химическое уравнение или реакцию с помощью этого калькулятора!
AlCl3 = Al + Cl — Решённые химические уравнения — ChemicalAid
Уравняйте AlCl3 = Al + Cl химическое уравнение или реакцию с помощью этого калькулятора!
Cu + S = Cu2S — Решённые химические уравнения — ChemicalAid
Уравняйте Cu + S = Cu2S химическое уравнение или реакцию с помощью этого калькулятора!
KClO3 + O2 = K2O + ClO3 — Решённые химические уравнения
Уравняйте KClO3 + O2 = K2O + ClO3 химическое уравнение или реакцию с помощью этого калькулятора!
Молярная и молекулярная масса CaO2 — Ваш онлайн
Расчёт молярной и относительной молекулярной массы CaO2. Mr[CaO2] = Ar[Ca] + Ar[O] * 2 = 40.078 + 15.9994 * 2 = 72.0768; Молярная масса (в кг/моль) …
Mr[CaO2] = Ar[Ca] + Ar[O] * 2 = 40.078 + 15.9994 * 2 = 72.0768; Молярная масса (в кг/моль) …
Уравнения плоскостей
Координатная плоскость XOY имеет уравнение z = 0. Аналогично, x = 0 — уравнение координатной плоскости YOZ; x = а — уравнение плоскости, параллельной YOZ; …
Изотермы уравнения Ван–дер–Ваальса
Проанализируем изотермы уравнения Ван–дер–Ваальса – зависимости Р от V для реального газа при постоянной температуре. Умножив уравнение Ван-дер-Ваальса на V …
реши уравнения 16+x=16, x-35=0. — Школьные Знания.com
Реши уравнения 16+x=16, x-35=0. 2. Посмотреть ответы. Разблокированный значок показывает как сапог космонавта касается поверхности Луны.
I. Химические факторы КонсультантПлюс
Оксиды органические и перекиси: эпоксиэтанКР (этилена оксид), 1,2-эпоксипропанК (пропилена оксид), (хлорметил) оксиранАК (эпихлоргидрин).
Prin utilizarea site-ului nostru, sunteți de acord cu utilizarea cookie-urilor pentru o experiență mai bună.
Liblib.ro © 2022
Ошибка 404 — Страница не найдена
К сожалению мы не можем показать то, что вы искали. Может быть, попробуете поиск по сайту или одну из приведенных ниже ссылок?
Поиск для:Архивы
Архивы Выберите месяц Сентябрь 2022 Август 2022 Июль 2022 Июнь 2022 Май 2022 Апрель 2022 Март 2022 Февраль 2022 Январь 2022 Декабрь 2021 Ноябрь 2021 Октябрь 2021 Сентябрь 2021 Август 2021 Июль 2021 Июнь 2021 Май 2021 Апрель 2021 Март 2021 Февраль 2021 Январь 2021 Декабрь 2020 Ноябрь 2020 Октябрь 2020 Сентябрь 2020 Август 2020 Июль 2020 Июнь 2020 Май 2020 Апрель 2020 Март 2020 Февраль 2020 Январь 2020 Декабрь 2019 Ноябрь 2019 Октябрь 2019 Сентябрь 2019 Август 2019 Июль 2019 Июнь 2019 Май 2019 Апрель 2019 Март 2019 Февраль 2019 Январь 2019 Декабрь 2018 Ноябрь 2018 Октябрь 2018 Сентябрь 2018 Август 2018 Июль 2018 Июнь 2018 Февраль 2018 Январь 2018 Ноябрь 2017 Сентябрь 2017 Август 2017 Июль 2017 Апрель 2017 Март 2017 Февраль 2017 Январь 2017Рубрики
РубрикиВыберите рубрикуbritish bulldogАстраБез рубрикиВидеоурокивоспитательная работаВПРВСОШвысшая пробадвидиктантЕГЭЕГЭ 2022 информатикаЕГЭ 2022 математикаЕГЭ по химиизолотое руноизложениеитоговое сочинениеитоговое устное собеседованиеКенгуруКИТконкурс Пегасконтрольная работактпматематический праздникмежрегиональный химический турнирМОШмцкоОВИООГЭОГЭ 2022 математикаолимпиада звездаолимпиада курчатоволимпиада ЛомоносовОПКРаботы статградрабочая программарабочая тетрадьРДРРешу ЕГЭРешу ОГЭрусский медвежонокСочинениеСтатьитексты егэтесттурнир ЛомоносоваУчебные пособияЧИПЮМШСтраницы
- 04.
 10.2020 XLIII Турнир Ломоносова задания и ответы
10.2020 XLIII Турнир Ломоносова задания и ответы - 05.12.17 Ответы и задания по математике 10 класс СтатГрад варианты МА00201-МА00208
- 05.12.17 Ответы и задания по математике 7 класс «СтатГрад» варианты МА70101-МА70106
- 06.11.2017 Олимпиада «Звезда» естественные науки задания и ответы 6-11 класс отборочный этап
- 06.12.17 Официальные темы итогового сочинения 2017 для Камчатского края и Чукотского автономного округа
- 06.12.17 Официальные темы итогового сочинения 2017 для Республика Алтай, Алтайский край, Республика Тыва, Респ. Хакасия, Красноярский край, Кемеровская, Томская и Новосибирская область
- 06.12.17 Официальные темы итогового сочинения 2017 зона 8 Республика Саха (Якутия), город Якутск, Амурская область, Забайкальский край
- 06.12.17 Официальные темы итогового сочинения для Республика Бурятия, Иркутская область зона 7
- 06.12.2017 5 зона Омск MSK+3 (UTC+6) официальные темы
- 06.12.2017 Ответы и задания по обществознанию 9 класс «СтатГрад» варианты ОБ90201-ОБ90204
- 07.
 12.17 Ответы и задания по русскому языку 11 класс СтатГрад варианты РЯ10701-РЯ10702
12.17 Ответы и задания по русскому языку 11 класс СтатГрад варианты РЯ10701-РЯ10702 - 07.12.2017 Ответы и задания по биологии 9 класс пробное ОГЭ 4 варианта
- 08.12.2017 Ответы и задания по географии 9 класс контрольная работа ОГЭ 56 регион
- 08.12.2017 Ответы и задания по физике 9 класс работа СтатГрад ОГЭ ФИ90201-ФИ90204
- 10.04.2020 Решать впр тренировочные варианты по математике 6 класс с ответами
- 10.10.17 Математика 9 класс контрольная работа 4 варианта ФГОС 56 регион задания и ответы
- 10.10.17 Русский язык 9 класс задания и ответы «СтатГрад» варианты РЯ90101-РЯ90102
- 10.11.2017 История 9 класс задания и ответы статград варианты ИС90201-ИС90204
- 100balnik мы в ВКОНТАКТЕ
- 100balnik отзывы пользователей
- 11 апреля 10-11 класс география ответы и задания
- 11 апреля 6 класс история ответы и задания
- 11 апреля 7 класс биология ответы и задания
- 11.04.2020 Решать ВПР тренировочные варианты по математике 5 класс с ответами
- 11.
 10.17 Физика 11 класс СтатГрад задания и ответы варианты ФИ10101-ФИ10104
10.17 Физика 11 класс СтатГрад задания и ответы варианты ФИ10101-ФИ10104 - 11.12.2017 — 16.12.2017 Олимпиада по дискретной математике и теоретической информатике
- 11.12.2017 Зимняя олимпиада по окружающему миру для 4 класса задания и ответы
- 11.12.2017 Ответы и задания по английскому языку 11 класс СтатГрад вариант АЯ10101
- 11.12.2017 Соревнование для 5-6 классов интернет-карусель по математике задания и ответы
- 12.04.2020 Решать тренировочные варианты ВПР по математике 4 класс + ответы
- 12.10 Русский язык 10 класс диагностическая работа ФГОС для 11 региона задания и ответы
- 12.10.17 Русский 2 класс ВПР официальные варианты задания и ответы
- 12.10.17 Химия 9 класс «СтатГрад» задания и ответы варианты ХИ90101-ХИ90104
- 12.12.2017 Ответы и задания по географии 9 класс работа СтатГрад варианты ГГ90101-ГГ90102
- 13.09.2017 Биология 11 класс СтатГрад задания и ответы все варианты
- 13.10.17 Математика 9 класс задания и ответы для 11 региона
- 13.
 10.2017 Обществознание 11 класс работа СтатГрад задания и ответы ОБ10101-ОБ10104
10.2017 Обществознание 11 класс работа СтатГрад задания и ответы ОБ10101-ОБ10104 - 13.12.2017 Ответы по физике 11 класс статград задания варианты ФИ10201-ФИ10204
- 13.12.2017 Письмо говорение по английскому языку 7-9 класс работа 56 регион
- 14.09.2017 Информатика 11 класс тренировочная работа статград ответы и задания
- 14.12 Геометрия 9 класс задания и ответы «СтатГрад»
- 14.12.2017 КДР ответы по русскому языку 8 класс задания все варианты
- 14.12.2017 Контрольная работа по математике 8 класс за 1 полугодие 2 варианта заданий с ответами
- 14.12.2017 Литература 11 класс ответы и задания СтатГрад вариант ЛИ10101
- 14.12.2017 Ответы КДР по математике 10 класс задания 6 вариантов
- 14.12.2017 Ответы по геометрии 9 класс СтатГрад задания варианты МА90301-МА90304
- 14.12.2017 Ответы по математике 11 класс КДР задания 6 вариантов
- 15.09 Математика 10 класс контрольная работа 3 варианта 56 регион задания и ответы
- 15.
 09.2017 Биология 9 класс тренировочная работа «СтатГрад» БИ90101-БИ90104 ответы и задания
09.2017 Биология 9 класс тренировочная работа «СтатГрад» БИ90101-БИ90104 ответы и задания - 15.11.2017 Задания и ответы 2-11 класс по Русскому медвежонку 2017 год
- 15.12.2017 Обществознание 11 класс ответы и задания СтатГрад варианты ОБ10201-ОБ10204
- 16 апреля 11 класс английский язык ответы и задания
- 16 апреля 5 класс история ответы и задания
- 16 апреля 6 класс биология ответы и задания
- 16 апреля 7 класс география ответы и задания
- 16.01.2018 Контрольная работа по русскому языку 9 класс в формате ОГЭ с ответами
- 16.01.2018 Ответы и задания КДР по русскому языку 11 класс 23 регион
- 16.10.2017 Ответы и задания всероссийской олимпиады школьников по математике 4-11 класс ВОШ
- 16.11.2017 МЦКО 10 класс русский язык ответы и задания
- 17.01.2018 Ответы и задания по информатике 11 класс работа статград варианты ИН10301-ИН10304
- 17.10.17 Физика 9 класс «СтатГрад» задания и ответы варианты ФИ90101-ФИ90104
- 18 апреля 11 класс химия ответы и задания
- 18 апреля 5 класс биология ответы и задания
- 18 апреля 6 класс обществознание ответы и задания
- 18 апреля 7 класс математика ответы и задания
- 18.
 09. Математика 10 класс задания и ответы
09. Математика 10 класс задания и ответы - 18.10.17 Математика 9 класс РПР 64 регион задания и ответы 1 этап
- 18.10.2017 Задания и ответы по математике 9 класс 50 регион Московская область
- 18.12.2017 Биология 11 класс Статград задания и ответы варианты БИ10201-БИ10204
- 19.09 Диагностическая работа по русскому языку 5 класс задания и ответы за 1 четверть
- 19.09 Контрольная работа по русскому языку 11 класс для 56 региона задания и ответы 1 четверть
- 19.09.2017 школьный этап всероссийской олимпиады по ОБЖ 5-11 класс задания и ответы
- 19.10.17 Русский язык 11 класс (ЕГЭ) задания и ответы статград варианты РЯ10601-РЯ10602
- 19.12.2017 КДР геометрия 8 класс краевая диагностическая работа задания и ответы
- 19.12.2017 КДР математика 9 класс краевая диагностическая работа задания и ответы
- 19.12.2017 Математика 10 класс тригонометрия база и профиль ответы и задания СтатГрад
- 2 апреля 11 класс история ВПР
- 2 апреля 7 класс английский язык ВПР
- 20.
 09 Входная контрольная работа русский язык 7 класс для 56 региона задания и ответы
09 Входная контрольная работа русский язык 7 класс для 56 региона задания и ответы - 20.09.2017 История 9 класс варианты ИС90101-ИС90102 ОГЭ задания и ответы
- 20.11.2017 Русский язык 9 класс «СтатГрад» ОГЭ задания и ответы РЯ90701-РЯ90702
- 20.12.2017 Химия 9 класс ответы и задания работа Статград варианты ХИ90201-ХИ90202
- 21.09.17 Математика 11 класс варианты МА10101-МА10108 задания и ответы
- 21.10.17 ОБЖ 7-11 класс муниципальный этап ВОШ для Москвы ответы и задания
- 21.11.17 Биология 9 класс СтатГрад задания и ответы варианты БИ90201-БИ90204
- 21.12.2017 Математика 9 класс РПР для 64 региона задания и ответы 2 этап
- 21.12.2017 Ответы и задания по математике 11 класс «СтатГрад» база и профиль
- 21.12.2017 Ответы и задания по русскому языку 10-11 класс варианты КДР 23 регион
- 22.09.17 Обществознание 9 класс работа статград ОГЭ варианты ОБ90101-ОБ90102 задания и ответы
- 22.09.17 Русский язык 10 класс входная контрольная работа ФГОС задания и ответы
- 22.
 10 Задания и ответы олимпиады по литературе 7-11 класс муниципальный этап 2017
10 Задания и ответы олимпиады по литературе 7-11 класс муниципальный этап 2017 - 23 апреля математика 5 класс ВПР 2019
- 23 апреля русский язык 6 класс ВПР 2019
- 23 апреля ФИЗИКА 7 класс ВПР 2019
- 23.11.2017 Задания и ответы по информатике 9 класс для вариантов статград ИН90201-ИН90204
- 24.10.17 Изложение 9 класс русский язык СтатГрад варианты РЯ90601-РЯ90602
- 24.10.17 КДР 8 класс математика алгебра задания и ответы 23 регион
- 24.10.17 Контрольная работа английский язык 7-9 класс для 56 региона письмо
- 25.09.17 Информатика 9 класс задания и ответы СтатГрад варианты ИН90101-ИН90102
- 25.10.17 Английский язык 7-9 класс контрольная работа для 56 региона чтение варианты
- 25.10.17 История 11 класс МЦКО варианты задания и ответы
- 25.10.17 Русский язык 9 класс МЦКО задания и ответы
- 26.09 Английский язык 7,8,9 класс контрольная работа для 56 региона задания и ответы ФГОС
- 26.09.17 История 11 класс задания и ответы «СтатГрад» варианты ИС10101-ИС10102
- 26.
 09.17 Математика 11 класс мониторинговая работа ЕГЭ 3 варианта задания и ответы
09.17 Математика 11 класс мониторинговая работа ЕГЭ 3 варианта задания и ответы - 26.10 ВПР Русский язык 5 класс ответы и задания все реальные варианты
- 26.10.17 Химия 11 класс «СтатГрад» задания и ответы варианты ХИ10101-ХИ10104
- 27.09.2017 Математика 9 класс работа статград варианты МА90101-МА90104 задания и ответы
- 27.10 Задания и ответы для олимпиады по биологии муниципальный этап 2017
- 28.09.17 Русский язык 11 класс задания и ответы «СтатГрад» варианты РЯ10101-РЯ10102
- 29.09.17 Математика 10 класс задания и ответы «СтатГрад» варианты МА00101-МА00104
- 30.11.2017 МЦКО математика 11 класс ответы и задания
- 4 апреля 11 класс биология ВПР
- 4 апреля 7 класс обществознание ВПР
- 4 класс диктант 2019 год
- 4 класс диктант платно
- 4 класс математика 22.04.2019-26.04.2019
- 4 класс математика платно ответы и задания
- 4 класс окр. мир платно
- 4 класс окружающий мир 22.04.2019-26.
 04.2019
04.2019 - 4 класс русский тест 2019 год
- 4 класса тест платно
- 5 класс биология платно
- 5 класс история платно
- 5 класс русский язык впр 25 апреля
- 5 класс русский язык платно
- 6 класс история платно
- 6 класс математика впр 25 апреля
- 6 класс математика платно
- 6 класс общество платно
- 6 класс платно гео ответы и задания
- 6 класс платно ответы и задания
- 7 класс ВПР 2019 по географии ответы и задания 16 апреля 2019
- 7 класс история впр 25 апреля
- 7 класс русский язык 56 регион ответы и задания 21.12.2018
- 7.11.17 Английский язык 9 класс от СтатГрад задания и ответы варианты АЯ90101-АЯ90102
- 8.11.2017 Русский язык 11 класс СтатГрад задания и ответы варианты РЯ10201-РЯ10202
- 9 апреля география 6 класс ВПР 2019
- 9 апреля русский язык 7 класс ВПР 2019
- 9 апреля физика 11 класс ВПР 2019
- 9 класс английский язык ОГЭ 24 25 мая
- 9 класс БИОЛОГИЯ ЭКЗАМЕН огэ 2019 год
- 9 класс информатика огэ 2019 год
- 9 класс математика огэ 2019 год
- 9 класс обществознание ОГЭ 2019
- 9 класс ОГЭ 2019
- 9 класс русский язык ОГЭ 2019
- 9 класс ФИЗИКА огэ 2019 год
- 9 класс ФИЗИКА ЭКЗАМЕН огэ 2019 год
- 9 класс экзамен по истории огэ 2019 год
- 9.
 11.17 Математика 9 класс работа «СтатГрад» задания и ответы варианты МА90201-МА90204
11.17 Математика 9 класс работа «СтатГрад» задания и ответы варианты МА90201-МА90204 - British Bulldog 2019 ответы и задания 3-4 класс 10-11 декабря 2019
- British Bulldog 3-4 класс ответы и задания 2018-2019
- British Bulldog 5-6 класс ответы и задания 2018-2019
- British Bulldog 9-11 класс ответы и задания 2018-2019
- FAQ
- My Calendar
- Алгебра 7 класс статград 4 декабря 2019 ответы и задания МА1970101-106
- Алгебра и начала анализа статград 10 класс 4 декабря 2019 ответы и задания
- Английский 9 класс СтатГрад задания и ответы
- Английский язык 11 класс АЯ10301 ответы и задания 23 апреля 2019 год
- Английский язык 11 класс СтатГрад 17.04
- Английский язык 11 класс статград 5 декабря 2019 ответы и задания АЯ1910101
- Английский язык 7 класс ВПР 2020 тренировочные варианты задания и ответы
- Английский язык 7 класс ВПР ответы и задания 2 апреля 2019 год
- Английский язык 7-9 класс ответы и задания 56 регион
- Английский язык 7,8,9 класс мониторинговая работа чтение 2019
- Английский язык 9 класс ответы и задания АЯ1990101 АЯ1990102 статград 6 ноября 2019
- Английский язык 9 класс платно
- Английский язык 9 класс статград ответы и задания 2018-2019 06.
 11
11 - Английский язык аудирование ответы 7 8 9 класс 56 регион 2018-2019
- Английский язык говорение 56 регион ответы 7 8 9 класс 2018-2019
- Английский язык задания и ответы школьного этапа олимпиады ВОШ 2019-2020
- Английский язык ответы 7 8 класс 56 регион чтение 2018-2019
- Английский язык письмо 7 8 класс ответы и задания 2018-2019
- Аргументы для тем итогового сочинения 2019-2020 регион МСК+8
- Архив работ
- 01.04.2020 Английский язык 9 класс ответы и задания для АЯ1990201-АЯ1990202
- 05.03.2020 Физика 11 класс статград ответы и задания ФИ1910401-ФИ1910404
- 06.03.2020 История 11 класс ИС1910401-ИС1910404 статград ответы и задания
- 12.02.2020 Математика 10 класс МА1900401-МА1900404 ответы и задания
- 12.05.2020 Математика 9 класс МА1990701-МА1990704 ответы и задания статград
- 13.05.2020 Русский язык 11 класс варианты РУ1910501-РУ1910502 ответы и задания
- 14.05.2020 Химия 11 класс варианты ХИ1910501-ХИ1910504 ответы и задания
- 14.
 09.2017 Варианты и ответы контрольной работы математика 8 класс для 56 региона
09.2017 Варианты и ответы контрольной работы математика 8 класс для 56 региона - 15.05.2020 Математика 10-11 класс варианты МА1900701-МА1900710 ответы и задания
- 18.05.2020 Физика 11 класс варианты ФИ1910501-ФИ1910504 ответы и задания
- 19.03.2020 Русский язык 10-11 класс РЯ1910901-РЯ1910902 ответы и задания
- 19.05.2020 История 11 класс варианты ИС1910501-ИС1910504 статград ответы и задания
- 21.05.2020 ОБ1910501-ОБ1910504 ответы и задания обществознание 11 класс статград
- 24.03.2020 Химия 11 класс ХИ1910401-ХИ1910404 ответы и задания статград
- Биология 11 класс контрольная работа в формате ЕГЭ 2020 ответы и задания
- Вариант № 33006760 тренировочный ЕГЭ по математике профильный уровень с ответами
- Варианты с ответами пробного экзамена ЕГЭ 2020 по математике в Санкт-Петербурге
- ВПР 2020 по математике 8 класс новые варианты с ответами
- ВПР 2020 тренировочная работа по обществознанию 8 класс задания и ответы
- ВПР 2020 тренировочные варианты БИ1980201-БИ1980202 по биологии 8 класс задания с ответами
- ВПР 2020 тренировочные варианты по биологии 6 класс задания с ответами
- ВПР 2020 тренировочные варианты по географии 7 класс задания с ответами
- ВПР 2020 тренировочные варианты по математике 7 класс
- ВПР 2020 физика 7 класс варианты ФИ1970101, ФИ1970102 с ответами
- ВПР по математике 4 класс задания и ответы 2018
- ВПР по математике 5 класс задания и ответы 2018 год
- ВПР по обществознанию 7 класс 2020 тренировочные варианты с ответами
- ЕГЭ 2020 тренировочный вариант 200622 с ответами по литературе 11 класс
- ЕГЭ 2020 тренировочный вариант 200622 с ответами по математике ПРОФИЛЬ 11 класс
- ЕГЭ 2020 тренировочный вариант 200622 с ответами по русскому языку 11 класс
- Задания и ответы для всероссийской олимпиады школьников по праву 5-11 класс 2017-2018
- Задания и ответы регионального этапа 2019 по экономике ВСОШ
- История 5 класс ИС1950101-ИС1950102 ВПР 2020 ответы и задания
- Контрольная работа в формате ОГЭ 2020 по истории 9 класс 3 четверть
- Контрольная работа ЕГЭ 2020 по химии 11 класс задания и ответы
- Контрольная работа по истории 11 класс в формате ЕГЭ 2020 задания и ответы
- Математика 7 класс ответы и задания по диагностической работе 09.
 10.2018
10.2018 - МЦКО русский язык 11 класс задания и ответы варианты 14 января 2020
- Новые задачи с ответами по химии 9-10 класс Сириус
- Новый тренировочный вариант 200622 по информатике и ИКТ 11 класс ЕГЭ 2020 с ответами
- Новый тренировочный вариант 33006755 по математике профильный ЕГЭ с ответами
- Обществознание 9 класс ответы ОБ90301 и ОБ90302 25.01.2019
- Олимпиада по английскому языку 4-7 класс ответы и задания для пригласительного этапа 16 апреля 2020
- Ответы Биология 11 класс тренировочная работа 18 января 2019
- Ответы пробное ОГЭ география 9 класс 22 января 2019
- Ответы работа статград история 11 класс 22 января 2019
- Пробные варианты ВПР 2020 по окружающему миру 4 класс с ответами
- Пробный ЕГЭ по математике 11 класс задания и ответы апрель 2020 год
- РДР 2020 5 класс реальные 2 варианта задания и ответы
- РДР 2020 6 класс реальные задания и ответы 12 марта 2020 год
- Решать новые тренировочные варианты впр по обществознанию 6 класс 2020
- Решу ЕГЭ 2020 по информатике 11 класс тренировочный вариант задания №200106
- Тренировочная работа Обществознание 11 класс ответы 1 февраля 2019
- Тренировочная работа по математике 9 класс ответы 12 февраля 2019
- Тренировочная работа по физике 9 класс ответы статград 29 января 2019
- Тренировочная работа по химии 9 класс ответы статград 14 февраля 2019
- Тренировочная работа русский язык 11 класс ответы 5 февраля 2019
- Тренировочная работа русский язык 9 класс ответы 7 февраля 2019
- Тренировочный вариант 200622 по английскому языку 11 класс ЕГЭ 2020 с ответами
- Тренировочный вариант 200622 по географии 11 класс ЕГЭ 2020 с ответами
- Тренировочный вариант 200622 по обществознанию 11 класс ЕГЭ 2020 с ответами
- Тренировочный вариант 200622 по химии 11 класс ЕГЭ 2020 с ответами
- Тренировочный вариант 29382872 по математике профильный ЕГЭ с ответами
- Тренировочный вариант 29382873 по математике профильный ЕГЭ задания с ответами
- Тренировочный вариант 29382874 по математике профильный ЕГЭ задания с ответами
- Тренировочный вариант 29527679 по математике профильный ЕГЭ с ответами
- Тренировочный вариант 29527683 по математике профильный ЕГЭ задания с ответами
- Тренировочный вариант 29527684 по математике профильный ЕГЭ задания с ответами
- Тренировочный вариант 29527685 по математике профильный ЕГЭ задания с ответами
- Тренировочный вариант 29527686 по математике профильный ЕГЭ задания с ответами
- Тренировочный вариант 29527687 по математике 11 класс профильный ЕГЭ задания с ответами
- Тренировочный вариант 33006750 по математике профильный ЕГЭ с ответами
- Тренировочный вариант 33006751 по математике профильный ЕГЭ с ответами
- Тренировочный вариант 33006752 по математике профильный ЕГЭ с ответами
- Тренировочный вариант 33006753 по математике профильный ЕГЭ с ответами
- Тренировочный вариант 33006754 по математике профильный ЕГЭ с ответами
- Тренировочный вариант 33006756 по математике профильный уровень ЕГЭ с ответами
- Тренировочный вариант ЕГЭ 200525 задания и ответы по математике профиль
- Тренировочный вариант ЕГЭ 29527688 по математике 11 класс профильный задания с ответами
- Тренировочный вариант ЕГЭ 29527689 по математике 11 класс профильный задания с ответами
- Тренировочный вариант ЕГЭ 29527690 по математике 11 класс профильный задания с ответами
- Тренировочный вариант ЕГЭ 33006763 задания и ответы по математике профиль
- Тренировочный вариант ЕГЭ 33006764 задания и ответы по математике профиль
- Физика 9 класс ФИ1990401- ФИ1990404 ответы и задания статград 3 марта 2020
- Химия 11 класс ХИ1910601-ХИ1910602 ВПР 2020 тренировочная работа
- Экзаменационная контрольная работа по литературе 9 класс ОГЭ 2020
- Астра 2019 ответы и задания 3-4 класс 20 ноября 2019
- Банк заданий ФИПИ по русскому языку ЕГЭ 2019 морфемика и словообразование
- Биология 10 класс РДР задания и ответы 14 ноября 2019-2020
- Биология 11 класс 5 ноября 2019 статград ответы и задания БИ1910201-204
- Биология 11 класс ВПР 2019 ответы и задания 4 апреля 2019 год
- Биология 11 класс ВПР ответы и задания 11.
 05
05 - Биология 11 класс ответы и задания тренировочная №5 26 апреля 2019
- Биология 5 класс ВПР 2018 ответы и задания
- Биология 5 класс ВПР 2019 ответы и задания 18 апреля 2019 год
- Биология 5 класс ВПР 2020 вариант демоверсии ответы и задания
- Биология 6 класс ВПР 2018 ответы и задания
- Биология 6 класс ВПР 2019 ответы и задания 16 апреля 2019
- Биология 6 класс платно
- Биология 7 класс ВПР 2019 ответы и задания 11 апреля 2019
- Биология 7 класс впр статград ответы и задания 11 сентября 2019
- Биология 9 класс 15 ноября ответы и задания статград 2018
- Биология 9 класс БИ90501 БИ90502 ответы и задания 23 апреля 2019
- Биология 9 класс ответы БИ90401 и БИ90402 статград 01.2019
- Биология 9 класс ответы и задания 25 ноября работа статград БИ1990201-БИ1990204
- Биология 9-10 класс ответы КДР 24 января 2019
- Биология ОГЭ 2018 платно
- Благодарим за ваш заказ!
- Британский бульдог 7-8 класс ответы и задания 2018-2019
- Вариант 322 КИМы с реального ЕГЭ 2018 по математике
- Вариант № 33006761 тренировочный ЕГЭ по математике профильный уровень с ответами
- Вариант № 33006762 тренировочный ЕГЭ по математике профильный уровень с ответами
- Вариант №1 морфемика и словообразование банк заданий ФИПИ ЕГЭ 2018-2019
- Вариант №2 морфемика и словообразование банк заданий ФИПИ ЕГЭ 2018-2019
- Вариант №3 морфемика и словообразование банк заданий ФИПИ ЕГЭ 2018-2019
- Вариант №4 морфемика и словообразование банк заданий с ответами ФИПИ ЕГЭ
- Вариант №5 банк заданий с ответами ФИПИ ЕГЭ 2019 по русскому языку морфемика
- Вариант №6 банк заданий с ответами ФИПИ ЕГЭ 2019 по русскому языку морфемика
- Вариант №7 банк заданий с ответами ФИПИ ЕГЭ 2019 по русскому языку морфемика
- Вариант по биологии с реального ЕГЭ 2020 задания и ответы
- Варианты БИ1910301-БИ1910304 по биологии 11 класс ответы и задания 14 января 2020
- Варианты ВПР по физике 11 класс задания и ответы за 2018 год
- Варианты для проведения ВПР 2020 по математике 6 класс с ответами
- Ваши отзывы — пожелания
- Вероятность и статистика 7 класс ответы 16.
 05
05 - Вероятность и статистика 8 класс ответы 16.05
- Витрина
- ВКР английский язык 7,8,9 класс задания и ответы говорение 2019-2020
- ВКР по геометрии 8 класс ответы и задания
- Возможные варианты для устного собеседования 9 класс ОГЭ 13 марта 2019
- Вот что с восторгом воскликнул Иван Васильевич готовые сочинения
- ВОШ всероссийская олимпиада школьников задания и ответы
- ВОШ ВСЕРОССИЙСКИЕ школьные олимпиады 2017-2018 задания и ответы
- ВОШ муниципальный этап по обществознанию ответы и задания 2018-2019
- ВОШ по ОБЩЕСТВОЗНАНИЮ 2017-2018
- ВОШ Школьный этап 2017-2018 задания и ответы для Республики Коми
- ВОШ школьный этап по экономике ответы и задания 2018-2019
- ВПР 11 класс английский язык ответы и задания 20 марта 2018
- ВПР 11 класс география
- ВПР 11 класс история ответы и задания 21 марта 2018
- ВПР 2019 6 класс обществознание ответы и задания 18 апреля 2019 год
- ВПР 2019 по математике 7 класс ответы и задания 18 апреля 2019 год
- ВПР 2019 по химии 11 класс ответы и задания 18 апреля 2019 год
- ВПР 2019 физика 11 класс ответы и задания 9 апреля 2019 год
- ВПР 2020 6 класс задание №10 по математике с ответами которые будут
- ВПР 2020 6 класс задание №11 по математике с ответами которые будут
- ВПР 2020 6 класс задание №6 по математике с ответами
- ВПР 2020 6 класс задание №7 по математике с ответами
- ВПР 2020 6 класс задание №8 по математике с ответами
- ВПР 2020 6 класс задание №9 по математике с ответами которые будут
- ВПР 2020 английский язык варианты АЯ1910201-АЯ1910202 задания и ответы
- ВПР 2020 биология 11 класс варианты БИ1910601-БИ1910602 ответы и задания
- ВПР 2020 биология 5 класс новые варианты с ответами
- ВПР 2020 вариант демоверсии по биологии 7 класс задания и ответы
- ВПР 2020 география 10-11 класс варианты ГГ1910401-ГГ1910402 ответы и задания
- ВПР 2020 география 6 класс варианты ГГ1960101, ГГ1960102 задания и ответы
- ВПР 2020 год 6 класс задание №12 по математике с ответами которые будут
- ВПР 2020 год 6 класс задание №12 по русскому языку с ответами
- ВПР 2020 год 6 класс задание №13 по математике с ответами которые будут
- ВПР 2020 год 6 класс задание №13 по русскому языку с ответами
- ВПР 2020 год 6 класс задание №14 по русскому языку с реальными ответами
- ВПР 2020 демоверсия по биологии 8 класс задания и ответы
- ВПР 2020 демоверсия по географии 7 класс задания и ответы
- ВПР 2020 демоверсия по географии 8 класс задания и ответы
- ВПР 2020 демоверсия по иностранным языкам 7 класс задания и ответы
- ВПР 2020 демоверсия по истории 7 класс задания и ответы
- ВПР 2020 демоверсия по истории 8 класс задания и ответы
- ВПР 2020 демоверсия по математике 7 класс задания и ответы
- ВПР 2020 демоверсия по математике 8 класс задания и ответы
- ВПР 2020 демоверсия по обществознанию 7 класс задания и ответы
- ВПР 2020 демоверсия по обществознанию 8 класс задания и ответы
- ВПР 2020 демоверсия по русскому языку 7 класс задания и ответы
- ВПР 2020 демоверсия по русскому языку 8 класс задания и ответы
- ВПР 2020 задание 6 по русскому языку 6 класс с ответами
- ВПР 2020 задание №1 по математике 6 класс с ответами
- ВПР 2020 задание №1 по русскому языку 6 класс с ответами
- ВПР 2020 задание №10 по русскому языку 6 класс ответы которые будут
- ВПР 2020 задание №11 по русскому языку 6 класс ответы которые будут
- ВПР 2020 задание №2 по математике 6 класс с ответами
- ВПР 2020 задание №2 по русскому языку 6 класс с ответами
- ВПР 2020 задание №3 по математике 6 класс с ответами
- ВПР 2020 задание №3 по русскому языку 6 класс с ответами
- ВПР 2020 задание №4 по математике 6 класс с ответами
- ВПР 2020 задание №4 по русскому языку 6 класс с ответами
- ВПР 2020 задание №5 по математике 6 класс с ответами
- ВПР 2020 задание №5 по русскому языку 6 класс с ответами
- ВПР 2020 задание №7 по русскому языку 6 класс с реальными ответами
- ВПР 2020 задание №8 по русскому языку 6 класс с реальными ответами
- ВПР 2020 задание №9 по русскому языку 6 класс ответы которые будут
- ВПР 2020 математика 5 класс реальные задания с ответами
- ВПР 2020 новые варианты с ответами по русскому языку 7 класс
- ВПР 2020 ответы и задания всероссийские проверочные работы
- ВПР 2020 по биологии 6 класс задание №1 с ответами
- ВПР 2020 по биологии 6 класс задание №10 с реальными ответами
- ВПР 2020 по биологии 6 класс задание №2 с ответами
- ВПР 2020 по биологии 6 класс задание №3 с ответами
- ВПР 2020 по биологии 6 класс задание №4 с ответами
- ВПР 2020 по биологии 6 класс задание №6 с ответами
- ВПР 2020 по биологии 6 класс задание №7 с ответами
- ВПР 2020 по биологии 6 класс задание №8 с реальными ответами
- ВПР 2020 по биологии 6 класс задание №9 с реальными ответами
- ВПР 2020 по биологии 7 класс тренировочные варианты БИ1970201,БИ1970202
- ВПР 2020 по истории 6 класс задание 1 с ответами
- ВПР 2020 по истории 6 класс задание №10 с реальными ответами
- ВПР 2020 по истории 6 класс задание №2 с ответами
- ВПР 2020 по истории 6 класс задание №3 с ответами
- ВПР 2020 по истории 6 класс задание №4 с реальными ответами
- ВПР 2020 по истории 6 класс задание №5 с реальными ответами
- ВПР 2020 по истории 6 класс задание №6 с реальными ответами
- ВПР 2020 по истории 6 класс задание №7 с реальными ответами
- ВПР 2020 по истории 6 класс задание №8 с реальными ответами
- ВПР 2020 по истории 6 класс задание №9 с реальными ответами
- ВПР 2020 по математике 7 класс задание 11 реальное с ответами
- ВПР 2020 по математике 7 класс задание 12 реальное с ответами
- ВПР 2020 по математике 7 класс задание №1 реальное с ответами
- ВПР 2020 по математике 7 класс задание №13 реальное с ответами
- ВПР 2020 по математике 7 класс задание №2 реальное с ответами
- ВПР 2020 по математике 7 класс задание №8 реальное с ответами
- ВПР 2020 русский язык 8 класс варианты РУ1980201, РУ1980202 ответы
- ВПР 2020 тренировочные варианты по географии 8 класс задания с ответами
- ВПР 2020 тренировочные варианты по русскому языку 5 класс задания с ответами
- ВПР 2020 физика 11 класс варианты ФИ1910601-ФИ1910602 ответы и задания
- ВПР 2020 химия 8 класс демоверсия задания и ответы
- ВПР 2021 ответы и задания всероссийские проверочные работы
- ВПР 2022 ответы и задания всероссийские проверочные работы
- ВПР 4 класс математика 2020 год реальные официальные задания и ответы
- ВПР БИОЛОГИЯ 11 класс 2018 реальные ответы и задания
- ВПР география 10-11 класс
- ВПР математика 5 класс ответы и задания
- ВПР по истории 11 класс ответы и задания 18.
 05
05 - ВПР ФИЗИКА 11 класс 2018
- ВПР физика 11 класс резервный день ответы
- ВПР ХИМИЯ 11 05.04
- ВСЕРОССИЙСКАЯ олимпиада муниципальный этап 2018-2019 задания и ответы
- ВСЕРОССИЙСКАЯ олимпиада муниципальный этап 2019-2020 задания и ответы
- Всероссийская олимпиада по праву ответы и задания школьный этап 25-26 октября 2019
- Всероссийская олимпиада по химии ответы и задания школьный этап 21-22 октября 2019
- ВСЕРОССИЙСКАЯ олимпиада региональный этап 2018-2019 задания и ответы
- Всероссийская олимпиада школьников региональный этап 2019-2020 задания и ответы
- ВСЕРОССИЙСКАЯ олимпиада школьный этап 2019-2020 задания и ответы
- ВСЕРОССИЙСКИЕ олимпиады 2017-2018 муниципальный этап задания и ответы
- ВСЕРОССИЙСКИЕ олимпиады 2017-2018 муниципальный этап задания и ответы для Краснодарского края
- ВСЕРОССИЙСКИЕ олимпиады 2017-2018 муниципальный этап задания и ответы для Челябинской области
- ВСЕРОССИЙСКИЕ олимпиады 2017-2018 региональный этап задания и ответы
- ВСЕРОССИЙСКИЕ олимпиады 2017-2018 учебный год задания и ответы
- ВСЕРОССИЙСКИЕ олимпиады 2018-2019 учебный год задания и ответы
- ВСЕРОССИЙСКИЕ олимпиады 2018-2019 школьный этап задания и ответы
- ВСЕРОССИЙСКИЕ олимпиады 2019-2020 учебный год задания и ответы
- ВСЕРОССИЙСКИЕ олимпиады 2020-2021 муниципальный этап задания и ответы
- ВСЕРОССИЙСКИЕ олимпиады 2020-2021 региональный этап задания и ответы
- ВСЕРОССИЙСКИЕ олимпиады 2020-2021 школьный этап задания и ответы
- ВСЕРОССИЙСКИЕ олимпиады 2021 заключительный этап задания и ответы
- ВСЕРОССИЙСКИЕ олимпиады 2022-2023 задания и ответы
- Всероссийские проверочные работы 2017 задания и ответы
- Всероссийские проверочные работы 2017-2018 задания и ответы
- Всероссийские проверочные работы 2018-2019 задания и ответы
- Всесибирская олимпиада школьников задания и ответы по математике 2018-2019
- Входная контрольная работа по математике 11 класс ответы и задания 2019-2020
- Входная контрольная работа по математике 4 класс ответы и задания 2019-2020
- Входная контрольная работа по математике 5 класс ответы и задания 2019-2020
- Входная работа по русскому языку 11 класс ответы и задания ФГОС 2019-2020
- Входные контрольные работы ФГОС варианты и ответы с 1 по 11 класс
- Гарантия
- ГГ1910101 ответы и задания география 11 класс статград 4 октября 2019
- ГДЗ 5 классы решебники
- ГДЗ по Математике за 5 класс: Виленкин Н.
 Я
Я - ГДЗ решебники
- Гелиантус АСТРА 1-2 класс ответы и задания 2018-2019
- Гелиантус АСТРА 3-4 класс ответы и задания 2018-2019
- География 10-11 класс ВПР 2019 ответы и задания 11 апреля 2019
- География 11 класс ответы и задания 17 апреля 2019 тренировочная №4
- География 11 класс ответы и задания вариант ГГ10101 статград 2018-2019
- География 11 класс платно
- География 11 класс статград ЕГЭ ответы и задания
- География 6 класс ВПР 2019 ответы и задания 9 апреля 2019
- География 6 класс ВПР 2020 год задание 7 и официальные ответы
- География 6 класс ВПР 2020 год задание №8 и реальные ответы
- География 6 класс ВПР 2020 задание №2 официальное с ответами
- География 6 класс ВПР 2020 задание №3 с ответами официальные
- География 6 класс ВПР 2020 задание №4 с ответами официальные
- География 6 класс ВПР 2020 задание №5 с ответами официальные
- География 6 класс ВПР 2020 задание №6 и официальные ответы
- География 6 класс задание №1 реального ВПР 2020 с ответами
- География 9 класс ОГЭ 4 июня 2019 год
- География 9 класс ответы и задания ГГ90401 ГГ90402 22 апреля 2019
- География 9 класс ответы и задания тренировочная статград 18 марта 2019
- География 9 класс СтатГрад задания и ответы
- География 9 класс статград ответы и задания 13 марта 2018
- География задания и ответы школьный этап 2019-2020 всероссийской олимпиады
- География муниципальный этап 2019 задания и ответы всероссийской олимпиады
- Геометрия 9 класс ответы и задания 12 декабря 2019 работа статград
- Готовое итоговое сочинение 2018-2019 на тему может ли добрый человек проявлять жестокость?
- Готовые сочинения для варианта №1 из сборника ЕГЭ 2021 Цыбулько И.
 П
П - Готовые сочинения для варианта №2 из сборника ЕГЭ 2021 Цыбулько И.П
- Готовые сочинения для варианта №3 из сборника ЕГЭ 2021 Цыбулько И.П
- Готовые сочинения для варианта №4 из сборника ЕГЭ 2021 Цыбулько И.П
- Готовые сочинения для варианта №5 из сборника ЕГЭ 2021 Цыбулько И.П
- Готовые сочинения для варианта №6 из сборника ЕГЭ 2021 Цыбулько И.П
- Готовые сочинения для варианта №7 из сборника ЕГЭ 2021 Цыбулько И.П
- Готовые сочинения ЕГЭ в избушке у самого леса живёт старый охотник
- Готовые сочинения ЕГЭ несомненно Дюма останется ещё на многие
- Готовые сочинения ЕГЭ по тексту может быть самая трогательная и самая глубокая
- Готовые сочинения ЕГЭ по тексту Н. Тэффи нежность самый кроткий робкий божественный лик любви
- Готовые сочинения ЕГЭ по тексту отправь голову в отпуск Измайлов
- Готовые сочинения ЕГЭ ты часто жаловался мне, что тебя «не понимают!»
- Готовые сочинения как-то Анатолий Бочаров высказал по тексту В.
 В. Быкову
В. Быкову - Готовые сочинения на Невском, у Литейного постоянно толпились
- Готовые сочинения по тексту Ф. М. Достоевскому в эту ночь снились мне
- Готовые сочинения чего нам так не хватает а не хватает нам любви к детям по тексту А. А. Лиханову
- Готовые сочинения я очень плохо знаю деревенскую жизнь с проблемами и текстом
- ДВИ МГУ варианты ответы и программы вступительных испытаний
- Демоверсии ЕГЭ 2023 года ФИПИ по всем предметам
- Демоверсия ВПР 2020 география 6 класс задания и ответы фипи
- Демоверсия ВПР 2020 история 6 класс задания и ответы фипи
- Демоверсия ВПР 2020 по биологии 6 класс задания и ответы фипи
- Демоверсия ВПР 2020 по обществознанию 6 класс задания и ответы фипи
- Демоверсия ОГЭ 2019 по математике решение заданий
- Диктант по русскому языку 4 класс ВПР 2018 задания
- ДКР 2019 по географии 10 класс ответы и задания Свердловская область
- ДКР 2019 по географии 7 класс задания и ответы 11 декабря 2019-2020
- Добро пожаловать
- Доступ ко всем работам
- ЕГЭ 2020 тренировочный вариант 200622 с ответами по истории 11 класс
- Если хочешь понять душу леса найди лесной 9 готовых сочинений ЕГЭ
- Естественные науки ответы и задания олимпиада ЗВЕЗДА 25-29 ноября 2019-2020
- за эти месяцы тяжелой борьбы решающей 9 готовых сочинений ЕГЭ
- Задание № 15 неравенства ОГЭ по математике 9 класс 2020
- Задания ВПР 2017 для 11 класса по географии
- Задания ВПР 2017 для 4 класса по русскому языку
- Задания ВПР 2017 для 5 класса по математике
- Задания заключительного этапа ВСЕРОССИЙСКОЙ олимпиады по информатике 2017/2018
- Задания и ответы 2 варианта пробного экзамена ЕГЭ по математике 11 класс 4 апреля 2018
- Задания и ответы 56 регион на ФЕВРАЛЬ 2017
- Задания и ответы 6 класс XXX математический праздник 2019 год
- Задания и ответы Англ.
 яз 18.11
яз 18.11 - Задания и ответы Биология 14.11
- Задания и ответы Биология 9 класс 21.11.
- Задания и ответы всероссийской олимпиады по русскому языку Московской области 19 ноября 2017
- Задания и ответы ГЕОГРАФИЯ 21.11.2017
- Задания и ответы для комплексной работы КДР для 8 класса ФГОС 4 варианта
- Задания и ответы для Оренбургской области 56 регион декабрь 2017
- Задания и ответы для Оренбургской области ноябрь 2017
- Задания и ответы для Оренбургской области октябрь 2017
- Задания и ответы для Оренбургской области сентябрь 2017
- Задания и ответы для работ 11 регион Республика Коми 2018-2019
- Задания и ответы для работ 11 региона Республика Коми Декабрь 2018-2019
- Задания и ответы для работ 11 региона Республика Коми НОЯБРЬ 2018-2019
- Задания и ответы для работ 56 региона октябрь 2018
- Задания и ответы для работ Республики Коми
- Задания и ответы для регионального этапа по физической культуре 2018
- Задания и ответы для школьных работ Оренбургской области 56 регион декабрь 2018
- Задания и ответы для школьных работ Оренбургской области 56 регион февраль 2018
- Задания и ответы КДР 2019 математика 9 класс 20 февраля
- Задания и ответы Математика 03.
 12
12 - Задания и ответы Математика 17.11
- Задания и ответы муниципального этапа 2019-2020 по немецкому языку 7-11 класс ВСОШ
- Задания и ответы муниципального этапа по русскому языку 2019-2020 Москва
- Задания и ответы МХК 15.11
- Задания и ответы на Апрель 2017 для 56 региона
- Задания и ответы на Май 2017 для 56 региона
- Задания и ответы на Март 2017 для 56 региона
- Задания и ответы олимпиады по литературе региональный этап 2020
- Задания и ответы по информатике 11 класс 28 ноября 2017 СтатГрад варианты ИН10201-ИН10204
- Задания и ответы по истории для 11 классов (56 регион)
- Задания и ответы по математике 11 класс профиль вариант №22397963
- Задания и ответы по математике 11 класс профиль ЕГЭ вариант №22397967
- Задания и ответы по математике 6 класс ВПР 2018
- Задания и ответы по русскому языку 6 класс ВПР 2018
- Задания и ответы по русскому языку 9 класс СтатГрад 29 ноября 2017 варианты РЯ90201-РЯ90202
- Задания и ответы по физике муниципального этапа 2019 всероссийская олимпиада
- Задания и ответы по химии 11 класс СтатГрад 30 ноября 2017 года варианты ХИ10201-ХИ10204
- Задания и ответы ПРАВО 14.
 11
11 - Задания и ответы право региональный этап ВОШ 2019
- Задания и ответы регионального этапа 2019 по английскому языку
- Задания и ответы регионального этапа 2019 по испанскому языку
- Задания и ответы регионального этапа 2019 по китайскому языку
- Задания и ответы регионального этапа 2019 по химии ВОШ
- Задания и ответы региональный этап ВОШ 2019 по французскому
- Задания и ответы Русский язык 19.11
- Задания и ответы Русский язык ОГЭ 9 класс 20.11.
- Задания и ответы Физика 18.11
- Задания и ответы Химия 24.11
- Задания Московской математической олимпиады 8 класс 17 марта 2019 год
- Задания МОШ 2019 по физике 1 тур 7 8 9 10 класс
- Задания по истории муниципальный этап 11 ноября всероссийской олимпиады 2018-2019
- Задания, ответы и результаты олимпиады по биологии региональный этап 2020
- Задания, ответы и результаты олимпиады по химии региональный этап 2020
- Заключительный этап 2022 задания и ответы многопрофильной инженерной олимпиады звезда
- Заключительный этап всероссийской олимпиады школьников 2019-2020 задания и ответы
- Закрытый раздел
- Золотое руно 2018 ответы и задания 16 февраля конкурс по истории
- Изложение русский язык 9 класс статград ответы и задания 4 октября 2019
- Информатика 11 класс 15 ноября 2019 статград ответы и задания ИН1910201- ИН1910204
- Информатика 11 класс КДР ответы и задания 18 декабря 2018
- Информатика 11 класс платно
- Информатика 11 класс СтатГрад задания и ответы
- Информатика 11 класс тренировочная №5 ответы и задания 15 апреля 2019 год
- Информатика 7 класс ответы РДР 21 февраля 2019
- Информатика 9 класс 06.
 03
03 - Информатика 9 класс ОГЭ 4 июня 2019 год
- Информатика 9 класс ответы и задания тренировочная №5 25 апреля 2019
- Информатика 9 класс ответы статград 13 ноября 2018
- Информатика 9 класс ответы статград 31 января 2019
- Информатика ВОШ школьный этап ответы и задания 2018-2019
- Информатика ОГЭ 2018
- Информатика ОГЭ 2018 платно
- Информатика ответы и задания школьный этап 2019 всероссийской олимпиады школьников
- История 10 класс РДР 2019 официальные задания и ответы все варианты
- История 11 класс 13 ноября 2019 ответы и задания статград вариант ИС1910201- ИС1910204
- История 11 класс ВПР 2018 год задания и ответы все варианты
- История 11 класс ВПР 2019 ответы и задания 2 апреля 2019 год
- История 11 класс ВПР 2020 тренировочные варианты с ответами
- История 11 класс задания и ответы СтатГрад
- История 11 класс ИС10201 и ИС10202 ответы и задания статград 23.11.2018
- История 11 класс ответы и задания СтатГрад 24.
 04
04 - История 11 класс ответы ИС10401 и ИС10402 11 марта 2019 год
- История 11 класс СтатГрад 24 ноября 2017 задания и ответы варианты ИС10201-ИС10204
- История 5 класс ВПР 2018 ответы и задания
- История 5 класс ВПР 2019 ответы и задания 16 апреля 2019
- История 5 класс ВПР 2020 вариант демоверсии ответы и задания
- История 5 класс ВПР 25.04
- История 6 класс ВПР 2018 ответы и задания
- История 6 класс ВПР 2019 ответы и задания 11 апреля 2019
- История 6 класс тренировочные варианты ВПР 2020 задания и ответы
- История 7 класс ВПР 2019 ответы и задания варианты 25 апреля
- История 7 класс платно 24 апреля
- История 9 класс входная контрольная работа ФГОС задания и ответы 2019-2020
- История 9 класс ответы и задания тренировочная №5 26 апреля 2019 год
- История 9 класс СтатГрад 27 февраля ответы и задания
- История 9 класс статград ответы и задания 2018-2019
- История 9 класс статград ответы и задания 30 марта 2018
- История всероссийская олимпиада школьный этап 2019-2020 задания и ответы московская область
- Итоговая контрольная работа по математике 8 класс за 2018-2019 учебный год
- Итоговая контрольная работа по русскому языку 7 класс за 2018-2019 учебный год
- Итоговая работа математика 10 класс ответы и задания 24 апреля 2019 год
- Итоговое собеседование варианты 12 февраля 2020
- Итоговое сочинение 05.
 12.2018
12.2018 - Итоговое сочинение 2017
- Итоговое устное собеседование ОГЭ 2022 по русскому языку 9 класс
- Как написать эссе по обществознанию ЕГЭ
- Как получить задания и ответы для ВПР 2019
- Как получить работу задания и ответы
- Как получить темы на итоговое сочинение 6 декабря 2017 года
- Как человеку воспитать в себе доброту? готовое итоговое сочинение 2018-2019
- КДР (задания+ответы) на Февраль 2017
- КДР (задания+ответы) на Январь 2017
- КДР 1 класс задания и ответы комплексная работа варианты 2018 год
- КДР 2 класс задания и ответы комплексная работа варианты 2018 год
- КДР 2019 23 регион ответы и задания май 2019 год
- КДР 2019 задания и ответы по английскому языку 8 класс 21 мая 2019 год
- КДР 2019 ответы и задания апрель 2019 год
- КДР 2019 ответы по географии 9 класс 15 февраля
- КДР 2019 химия 9 и 10 класс ответы 19 марта 2019 год
- КДР 2019-2020 декабрь 23 регион ответы и задания
- КДР 2020 23 регион ответы и задания Краснодарский край
- КДР 9 класс русский язык ответы и задания 14 декабря 2018
- КДР Английский язык 8 класс ответы и задания 2018-2019
- КДР апрель 2017 работы задания и ответы
- КДР апрель 2018 задания и ответы для Краснодарского края 23 регион
- КДР декабрь 2017 задания и ответы для Краснодарского края 23 регион
- КДР задания и ответы
- КДР задания и ответы комплексная работа 3 класс 2018 год
- КДР задания и ответы комплексная работа 4 класс варианты 2018 год
- КДР Май 2017 работы задания и ответы
- КДР Май 2018 задания и ответы для Краснодарского края 23 регион
- КДР математика 11 класс задания и ответы 28 февраля 2018 год
- КДР математика 7 класс ответы и задания 12.
 04
04 - КДР математика 9 класс 19.04
- КДР ответы и задания 23 регион Январь 2019
- КДР ответы и задания для Краснодарского края 23 регион ДЕКАБРЬ 2018
- КДР ответы и задания математика 10-11 класс 23 ноября 2018
- КДР ответы и задания НОЯБРЬ 2018 для Краснодарского края 23 регион
- КДР ответы и задания октябрь 2018 для Краснодарского края 23 регион
- КДР ответы и задания по английскому языку 9 10 11 класс 8 февраля 2018
- КДР ответы и задания по Биологии 10 класс 23 января 2018
- КДР ответы и задания по Биологии 11 класс 23 января 2018
- КДР ответы и задания по Биологии 9 класс 23 января 2018
- КДР ответы и задания по Географии 10 класс 25 января 2018
- КДР ответы и задания по Географии 9 класс 25 января 2018
- КДР ответы и задания по информатике 10 класс 18 января 2018
- КДР ответы и задания по информатике 9 класс 18 января 2018
- КДР ответы и задания по истории 9 10 11 класс 13 февраля 2018
- КДР ответы и задания по обществознанию 9 10 11 класс 1 февраля 2018
- КДР ответы и задания по русскому языку 9 класс 6 февраля 2018
- КДР ответы и задания по химии 10 11 класс 6 февраля 2018
- КДР ответы математика 7 класс 30 января 2019
- КДР ответы русский язык 9 класс 6 февраля 2019
- КДР ответы физика 9-10 класс 31 января 2019
- КДР по алгебре 8 класс ответы и задания 2018-2019
- КДР ПО ГЕОГРАФИИ 11 КЛАСС 23 регион ответы и задания 22 февраля
- КДР по литературе 10 11 класс 2018 ответы и задания
- КДР по литературе 10 класс ответы
- КДР по Математике 9 класс официальные ответы
- КДР по русскому языку для 9 классов
- КДР русский язык 7 8 класс ответы и задания
- КДР русский язык 7-8 класс ответы 17.
 05
05 - КДР февраль 2018 задания и ответы для Краснодарского края 23 регион
- КДР январь 2018 задания и ответы для Краснодарского края 23 регион
- Кенгуру 2017 9 класс ответы
- Кенгуру 2017 ответы и задания 2-10 класс
- Кенгуру 2019 ответы и задания 5-6 класс
- Кенгуру 2019 ответы и задания для 7-8 класса
- КИТ 2-3 класс ответы и задания 2018-2019
- КИТ 8-9 класс ответы и задания 2018-2019
- КИТ-2019 ответы и задания 10-11 класс 27 ноября 2019-2020
- Комплексная работа ФГОС 5 6 7 8 9 класс ответы и задания 30 ноября 2018
- Конкурс АСТРА 2019 ответы и задания 5-6 класс 20 ноября 2019
- Конкурс КИТ 2018 4-5 класс ответы и задания
- Конкурс КИТ 2019 ответы и задания 2-3 класс 27 ноября 2019
- Контакты
- Контрольная входная работа по русскому языку 10 класс ответы и задания 2019-2020
- Контрольная работа за 1 полугодие по русскому языку 7 класс ответы и задания
- Контрольная работа по математике 11 класс 2 четверть в формате ЕГЭ 3 варианта с ответами
- Контрольная работа по русскому языку 10 класс за 1 полугодие 2 варианта с ответами
- Контрольная работа по русскому языку 8 класс за 1 полугодие 2 четверть задания и ответы
- Контрольные работы ОГЭ 2021 задания и ответы для 9 класса
- Контрольные срезы 56 регион ответы и задания октябрь 2019-2020
- Корзина
- Критерии ответы и задания по физике 11 класс статград 23 марта 2018
- Критерии ответы по информатике 11 класс статград 16 марта 2018
- Критерии ответы по русскому языку 11 класс статград 2018
- Кружила январская метелица скрипели мерзлые готовые сочинения ЕГЭ
- Куда поступить после 11 класса в 2017 году
- Литература 11 класс ответы и задания ЕГЭ статград 22.
 03.2018
03.2018 - Литература 11 класс СтатГрад задания и ответы
- Литература 9 класс ОГЭ 2019 год
- Литература 9 класс ответы и задания статград 22 ноября 2018 год
- Литература 9 класс статград ОГЭ сочинение ответы 14 марта 2018
- Литература ОГЭ 2018 платно
- Литература олимпиада ВОШ задания муниципальный этап 2018-2019
- Литература ответы и задания школьный этап 2019 всероссийской олимпиады школьников
- Литература ответы и задания школьный этап всероссийской олимпиады школьников 2019-2020
- Литература школьный этап 2019-2020 задания и ответы олимпиады ВОШ
- Математика 7 классов 56 регион задания и ответы
- Математика 10 класс (вероятность и статистика)
- Математика 10 класс 56 регион ответы 16.05
- Математика 10 класс вероятность и статистика ответы и задания 4 апреля 2019
- Математика 10 класс задания и ответы мониторинговая работа ФГОС 2019-2020
- Математика 10 класс ответы и задания 18.05
- Математика 10 класс ответы и задания статград
- Математика 10 класс ответы и задания статград 2018-2019
- Математика 10 класс статград ответы и задания 29.
 03.2018
03.2018 - Математика 10 класс статград ответы и задания БАЗА и ПРОФИЛЬ
- Математика 10 класс тригонометрия ответы статград 18.12.2018
- Математика 10-11 класс ответы и задания варианты статград 17 мая 2019
- Математика 10-11 класс ответы и задания СтатГрад
- Математика 11 класс 17 декабря 2019 контрольная работа задания и ответы
- Математика 11 класс диагностическая работа ЕГЭ профиль задания и ответы для 11 региона
- Математика 11 класс КДР ответы и задания 28 февраля
- Математика 11 класс ответы база профиль статград 24 января 2019
- Математика 11 класс ответы и задания БАЗА ПРОФИЛЬ 20.09
- Математика 11 класс ответы и задания тренировочная работа №5 19 апреля 2019
- Математика 11 класс ответы статград БАЗА ПРОФИЛЬ 20.12.2018
- Математика 11 класс профиль 56 рег
- Математика 11 класс тренировочная №4 статград ответы и задания 13 марта 2019
- Математика 3 класс задания ВСОКО МЦКО итоговая работа 2019
- Математика 4 класс ВПР 2018 ответы и задания
- Математика 4 класс ВПР ответы 25.
 04
04 - Математика 4 класс демоверсия ВПР 2020 задания и ответы ФИПИ
- Математика 5 класс ВПР 2018 ответы и задания
- Математика 5 класс ВПР 2019 ответы и задания 23 апреля
- Математика 5 класс задания и ответы СтатГрад варианты 12 сентября 2017 год
- Математика 5 класс контрольная работа за 1 полугодие задания и ответы 2019-2020
- Математика 5 класс официальная демоверсия ВПР 2020 задания и ответы
- Математика 5 класс платно
- Математика 6 класс ВПР 2018 ответы и задания
- Математика 6 класс ВПР 2019 ответы и задания варианты 25 апреля
- Математика 6 класс ВПР 2020 демоверсия фипи задания и ответы
- Математика 6 класс ответы СтатГрад 15.05
- Математика 7 класс ответы и задания варианты МА70301 МА70302 14 мая 2019
- Математика 7 класс РДР ответы 2018-2019
- Математика 8 класс 56 регион 17.03
- Математика 8 класс 56 регион ответы и задания 15 марта 2018
- Математика 8 класс входная контрольная работа ответы и задания 2019-2020
- Математика 8 класс задания и ответы работа статград 12 сентября 2017
- Математика 8 класс ответы и задания варианты МА80201 МА80202 14 мая 2019
- Математика 8 класс ответы и задания по диагностической работе 11 регион 2018-2019
- Математика 8 класс статград ответы и задания
- Математика 9 класс — 64 регион ответы
- Математика 9 класс 12 ноября 2019 ответы и задания работа статград МА1990201-04
- Математика 9 класс 13.
 02
02 - Математика 9 класс 56 рег ответы
- Математика 9 класс контрольная работа в формате ОГЭ 4 варианта ответы и задания
- Математика 9 класс ОГЭ 2018 ответы и задания
- Математика 9 класс ответы 11 регион 18.12.2018
- Математика 9 класс ответы 15.05 СтатГрад
- Математика 9 класс ответы и задания 11 регион 4 октября 2018
- Математика 9 класс ответы и задания варианты 56 регион 10 октября 2019
- Математика 9 класс ответы и задания РПР 64 регион 20.12.2018
- Математика 9 класс ответы и задания статград 19 марта 2019
- Математика 9 класс ответы и задания статград варианты 15 мая 2019 год
- Математика 9 класс ответы РПР 64 регион 2019 3 этап 20 марта
- Математика 9 класс пробник статград ответы и задания 21 марта 2018
- Математика 9 класс статград ОГЭ ответы и задания
- Математика 9 класс статград ответы и задания 13 февраля 2018 года
- Математика 9 класс статград ответы и задания 27.09.2018
- Математика База платно
- Математика геометрия 9 класс КДР ответы и задания 20 февраля 2018
- Математика задания и ответы муниципальный этап ВОШ 2018-2019 для Москвы
- Математика олимпиада ВОШ 2018-2019 школьный этап задания и ответы
- Математика ответы и задания для школьного этапа всероссийской олимпиады 2019-2020
- Математика профиль 11 класс 56 регион контрольная работа 18.
 12.2018
12.2018 - Математика тренировочная работа 9 класс ответы статград 8 ноября 2018 года
- Математическая вертикаль 2021-2022 ответы и задания
- Математическая вертикаль ответы и задания 2020-2021 учебный год
- Материалы за 2016-2021 учебный год
- Международный молодёжный предметный чемпионат по правоведению для 10-11 классов.
- Многопрофильная инженерная олимпиада «Звезда» 2017-2018 задания и ответы
- Многопрофильная инженерная олимпиада «Звезда» 2018-2019 ответы и задания
- Многопрофильная инженерная олимпиада Звезда 2021-2022 ответы и задания
- Многопрофильная олимпиада Звезда 2019-2020 ответы и задания
- Многопрофильная олимпиада Звезда 2020-2021 ответы и задания
- Мой аккаунт
- Мониторинговая работа аудирование по английскому языку 7,8,9 класс задания и ответы 2019-2020
- Мониторинговая работа по английскому языку 7,8,9 класс задания и ответы 2019
- Мониторинговая работа по русскому языку 5 класс ответы и задания ФГОС 2019-2020
- Мониторинговая работа по русскому языку 8 класс ответы и задания ФГОС 2019-2020
- Мониторинговые работы 56 регион ответы и задания сентябрь 2019
- Московская олимпиада школьников 2020-2021 ответы и задания
- Московская олимпиада школьников 2021-2022 ответы и задания
- Московский турнир юных физиков задания 2019-2020 учебный год
- МПУ МЦКО 4 класс задания 31 января 2019 год
- Муниципальный этап 2019 олимпиады по испанскому языку задания и ответы ВОШ
- Муниципальный этап 2019 олимпиады по истории задания и ответы ВСОШ
- Муниципальный этап 2019-2020 олимпиада по ОБЖ ответы и задания для Москвы
- Муниципальный этап 2019-2020 олимпиады по химии задания и ответы Московская область
- Муниципальный этап 2019-2020 олимпиады по экологии ответы и задания ВсОШ Москва
- Муниципальный этап 2019-2020 по литературе ответы и задания ВсОШ Москва
- Муниципальный этап ВОШ 2018 по праву задания и ответы для Москвы
- Муниципальный этап ВОШ 2018-2019 задания по химии в Московской области
- Муниципальный этап ВОШ по астрономии ответы и задания 2018-2019 учебный год
- Муниципальный этап ВОШ по ОБЖ ответы и задания 2018-2019
- Муниципальный этап олимпиады 2019 по искусству МХК задания и ответы ВСОШ
- Муниципальный этап олимпиады 2019-2020 по астрономии задания и ответы Московская область
- Муниципальный этап олимпиады по биологии ответы и задания 19 октября 2019
- Муниципальный этап по астрономии всероссийской олимпиады задания 2018-2019
- Муниципальный этап по обществознанию 2019-2020 ответы и задания ВСОШ Москва
- Муниципальный этап по экономике всероссийская олимпиада 2018-2019
- МХК искусство задания и ответы муниципального этапа 2019-2020 учебный год
- МХК искусство школьный этап 2019 ответы и задания всероссийской олимпиады школьников
- МХК муниципальный этап 8 ноября задания всероссийской олимпиады 2018-2019
- МЦКО 2019-2020 расписание и демоверсии диагностических работ
- МЦКО 2020-2021 расписание и демоверсии диагностических работ с ответами
- МЦКО 2021-2022 расписание и демоверсии диагностических работ с ответами
- МЦКО 2022-2023 демоверсии, варианты и ответы диагностических работ
- МЦКО 7 класс математика ответы 13 февраля 2018
- МЦКО 8 класс метопредмет ответы и задания 27 февраля
- МЦКО 8 класс ответы 15.
 03
03 - МЦКО история 10 класс ответы 25.10.2018
- МЦКО математика 3 класс задания
- Мцко математика 7 класс 02.03.17
- МЦКО математика 9 класс варианты задания и ответы 2019-2020
- МЦКО математика 9 класс ответы и задания 3 октября 2018
- МЦКО ответы и задания по русскому языку 11 класс 18 января 2018
- МЦКО ответы и задания по русскому языку 7 8 класс 1 февраля 2018
- МЦКО по физике для 9 классов
- МЦКО русский язык 9 класс ответы 2018-2019
- МЦКО физика для 7 классов ответы и задания
- Направления тем итогового сочинения 2017-2018
- Наше наследие 1-11 класс муниципальный тур ответы и задания 2019-2020
- Наше наследие 1-11 класс школьный тур ответы и задания 2019-2020
- Наше наследие олимпиада задания и ответы 2017-2018
- Наше наследие ответы и задания 5-6 класс школьный тур 2019-2020
- Наше наследие ответы и задания 9-11 класс школьный тур 2019-2020
- Новый тренировочный вариант 200622 по биологии 11 класс ЕГЭ 2020 с ответами
- Новый тренировочный вариант 200622 по физике 11 класс ЕГЭ 2020 с ответами
- Новый тренировочный вариант 210201 по английскому языку 11 класс ЕГЭ 2021 с ответами
- Новый тренировочный вариант 210201 по истории 11 класс ЕГЭ 2021 с ответами
- Новый тренировочный вариант 210201 по литературе 11 класс ЕГЭ 2021 с ответами
- Новый тренировочный вариант 210201 по обществознанию 11 класс ЕГЭ 2021 с ответами
- Новый тренировочный вариант 210208 по химии 11 класс ЕГЭ 2021 с ответами
- Новый тренировочный вариант 34072997 по математике профиль 11 класс ЕГЭ с ответами
- Новый тренировочный вариант 34072998 по математике профиль 11 класс ЕГЭ с ответами
- Новый тренировочный вариант 34072999 по математике профиль 11 класс ЕГЭ 2021 с ответами
- Новый тренировочный вариант 34073000 по математике профиль 11 класс ЕГЭ 2021 с ответами
- Новый тренировочный вариант ЕГЭ 34073001 по математике профильный с ответами
- Новый тренировочный вариант КИМ 210208 по биологии 11 класс ЕГЭ 2021 с ответами
- Новый тренировочный вариант КИМ 210208 по физике 11 класс ЕГЭ 2021 с ответами
- О нас
- ОБ1910201-ОБ1910204 ответы и задания обществознание 11 класс 13 декабря 2019
- ОБЖ школьный этап задания и ответы олимпиады ВОШ 2019-2020
- Обществознание 10 класс КДР 2019 задания и ответы 01.
 03.2019
03.2019 - Обществознание 11 класс 04.05
- Обществознание 11 класс ответы тренировочная №4 статград 20 марта 2019
- Обществознание 11 класс статград ЕГЭ ответы и задания 19 марта 2018
- Обществознание 11 класс СтатГрад задания и ответы
- Обществознание 11 класс Статград ответы и задания
- Обществознание 6 класс ВПР 2018 ответы и задания
- Обществознание 7 класс ВПР 2019 ответы и задания 4 апреля 2019 год
- Обществознание 9 11 класс контрольная работа 56 регион 20 февраля 2018
- Обществознание 9 класс 19 декабря 2019 ответы и задания ОБ1990201-ОБ1990204
- Обществознание 9 класс КДР 2019 ответы 01.03.2019
- Обществознание 9 класс ответы и задания 29 апреля 2019 тренировочная №5
- Обществознание 9 класс СтатГрад задания и ответы
- Обществознание 9 класс тренировочная №4 статград ответы и задания 14 марта 2019
- Обществознание 9 класс тренировочная работа №1 ответы и задания 21.09
- ОБЩЕСТВОЗНАНИЕ для 9 классов Республика Коми, 11 регион
- Обществознание ОГЭ 2018 платно
- ОГЭ
- ОГЭ 2017 закрытый раздел
- ОГЭ 2018 Математика платно
- ОГЭ 2019 география 9 класс ответы для 24 региона
- ОГЭ 2019 география 9 класс ответы для 54 региона
- ОГЭ 2019 официальное расписание экзаменов 9 класс
- ОГЭ английский язык 2018 ответы и задания 9 класс
- Одно желание было у лейтенанта Бориса Костяева готовые сочинения ЕГЭ
- Окружающий мир 4 класс ВПР 2018 ответы и задания
- Окружающий мир 4 класс демоверсия ВПР 2020 задания и ответы ФИПИ
- Олимпиада Звезда заключительный тур 2017-2018 задания и ответы
- Олимпиада Ломоносов по математике 11 класс задания и ответы 2018-2019
- Олимпиада Наше Наследие 2019-2020 учебный год задания и ответы
- Школьный тур 5-11 класс наше наследие задания и ответы 2019-2020
- Олимпиада Наше Наследие 2020-2021 учебный год ОВИО задания и ответы
- Олимпиада Наше Наследие задания и ответы 2018-2019 учебный год
- Олимпиада основы православной культуры задания и ответы 2019-2020
- Олимпиада по английскому языку 8-10 класс ответы и задания для пригласительного этапа 17 апреля 2020
- Олимпиада по английскому языку задания и ответы муниципального этапа 2019
- Олимпиада по английскому языку школьный этап 2017 задания
- Олимпиада по астрономии муниципальный этап 2019 задания и ответы
- Олимпиада по биологии ответы и задания школьный этап 2019 ВОШ
- Олимпиада по биологии ответы и задания школьный этап ВсОШ 23-24 октября 2019
- Олимпиада по математике НТИ отборочный этап ответы и задания 2018-2019
- Олимпиада по МХК школьный этап 2017 задания
- Олимпиада по обществознанию школьный этап 2017 задания
- Олимпиада по праву школьный этап 2017 задания
- Олимпиада по русскому языку задания и ответы школьного этапа 2019
- Олимпиада по физической культуре муниципальный этапа 2019-2020 задания и ответы
- Олимпиада по экологии 4-10 класс ответы и задания для пригласительного этапа 15 апреля 2020
- Олимпиада по экологии ответы и задания школьный этап 2019-2020 Московская область
- Олимпиада по экологии школьный этап 2017 задания
- Олимпиада РОСАТОМ 2018-2019 задания и ответы
- Олимпиада ФИЗТЕХ 11 класс ответы и задания 2018-2019
- Олимпиада школьников САММАТ 2019-2020 ответы и задания
- Оплата заказа
- Оренбургская область 56 регион задания и ответы работы январь 2018
- Отборочные задания по математике для физико-математической школы 2019 год
- Отборочные задания по физике для физико-математической школы 2019 год
- Ответы 56 регион математика 8 класс 19 декабря 2018
- Ответы 7 8 класс золотое руно 2019 с заданиями
- Ответы 9-11 класс золотое руно задания 2019
- Ответы английский язык 7 8 9 класс говорение 56 регион 2018-2019
- Ответы английский язык для 9 классов 56 регион
- Ответы ВПР 2020 по биологии 6 класс задание №5
- Ответы для реального задания №10 ВПР 2020 по географии 6 класс
- Ответы для реального задания №9 ВПР 2020 по географии 6 класс
- Ответы задания и сочинения татарский язык ЕРТ
- Ответы задания изложение по русскому языку 9 класс СтатГрад 8 февраля 2018
- Ответы и задания 1-2 класс конкурс АСТРА 20 ноября 2019-2020
- Ответы и задания 10-11 класс КИТ 2018
- Ответы и задания 11 класс кенгуру выпускника 2019
- Ответы и задания 12.
 04.2018
04.2018 - Ответы и задания 2 класс пегас 2019
- Ответы и задания 2 класс чип 2019-2020 Австралия
- Ответы и задания 3-4 класс золотое руно 2019
- Ответы и задания 3-4 класс кенгуру 2019 год
- Ответы и задания 3-4 класс пегас 2019
- Ответы и задания 3-4 класс ЧИП 2019 год
- Ответы и задания 4-5 класс КИТ 2019 конкурс 27 ноября 2019-2020
- Ответы и задания 4-5 класс русский медвежонок 14 ноября 2019
- Ответы и задания 5-6 класс Гелиантус (астра) 2018-2019
- Ответы и задания 5-6 класс золотое руно 2019 год
- Ответы и задания 6-7 класс КИТ 2019 конкурс 27 ноября 2019-2020
- Ответы и задания 6-7 класс русский медвежонок 2018-2019
- Ответы и задания 8-9 класс русский медвежонок 2018-2019
- Ответы и задания 9 класс кенгуру выпускника 2019
- Ответы и задания 9-10 класс кенгуру 2019 год
- Ответы и задания английский язык 9 класс диагностика №2 22 марта 2019
- Ответы и задания БИ10401 и БИ10402 биология 11 класс 4 марта 2019
- Ответы и задания биология 11 класс статград
- Ответы и задания биология 11 класс статград 30 ноября 2018
- Ответы и задания ВПР по географии 10-11 класс 03.
 04.2018
04.2018 - Ответы и задания география 11 класс статград 9 декабря 2019 ГГ1910201
- Ответы и задания для конкурса Кенгуру 2020 11 класс
- Ответы и задания для конкурса по информатике КИТ 1-11 класс 29 ноября 2017 год
- Ответы и задания для Оренбургской области 56 регион март 2019
- Ответы и задания для пробных работ 56 региона 2018
- Ответы и задания для работ 15.02.2017
- Ответы и задания для работы статград по истории 9 класс
- Ответы и задания золотое руно 2019 1-2 класс
- Ответы и задания информатика 11 класс ИН1910101 ИН1910102 23 сентября 2019
- Ответы и задания история 9 класс статград 29 ноября 2018 год
- Ответы и задания КДР 23 регион март 2019 год
- Ответы и задания КДР геометрия 8 класс 16 ноября 2018 года
- Ответы и задания кенгуру 2 класс 2019 год
- Ответы и задания кенгуру выпускника 4 класс 2019
- Ответы и задания контрольная по математике 7 класс
- Ответы и задания контрольных работ для 56 региона декабрь 2019
- Ответы и задания МЦКО английский язык 9 класс 2018
- Ответы и задания ОГЭ 2018 по математике 9 класс
- Ответы и задания олимпиада звезда по обществознанию 2019-2020 отборочный этап
- Ответы и задания олимпиады по физкультуре 8,9,10 класс пригласительный этап 28 апреля 2020
- Ответы и задания по астрономии школьный этап всероссийской олимпиады 2019-2020
- Ответы и задания по биологии 11 класс 30 января 2018 СтатГрад
- Ответы и задания по биологии 11 класс статград 12.
 09
09 - Ответы и задания по биологии 9 класс 17.09 статград
- Ответы и задания по Биологии 9 класс 24 января 2018 СтатГрад
- Ответы и задания по биологии 9 класс БИ1990101-02 статград 14 октября 2019
- Ответы и задания по биология 9 класс СтатГрад 2018
- Ответы и задания по информатике 11 класс статград 14.09
- Ответы и задания по информатике 9 класс статград 19.09
- Ответы и задания по информатике 9 класс СтатГрад 31 января 2018
- Ответы и задания по Истории 11 класс 23 января 2018 СтатГрад
- Ответы и задания по истории 11 класс ИС1910101 ИС1910102 27 сентября 2019
- Ответы и задания по истории 9 класс 18 января 2018 СтатГрад
- Ответы и задания по истории школьный этап всероссийской олимпиады школьников 2019-2020
- Ответы и задания по итальянскому языку школьный этап всероссийской олимпиады 2019-2020
- Ответы и задания по китайскому языку олимпиада школьный этап 2019-2020
- Ответы и задания по литературе школьный этап всероссийской олимпиады 2019-2020 московская область
- Ответы и задания по математике 10 класс контрольная работа
- Ответы и задания по математике 11 класс 25 января 2018 СтатГрад
- Ответы и задания по математике 11 класс ЕГЭ база 56 регион 04.
 04.18
04.18 - Ответы и задания по математике 11 класс мониторинговая работа 2019-2020
- Ответы и задания по математике 8 класс статград 11.09
- Ответы и задания по математике 9 класс 12 декабря 2019 статград все варианты
- Ответы и задания по математике 9 класс 56 регион 4 декабря 2018
- Ответы и задания по математике 9 класс МА1990101-МА1990104 3 октября 2019
- Ответы и задания по математике школьный этап 2019-2020 всероссийская олимпиада
- Ответы и задания по математике школьный этап 2019-2020 всероссийской олимпиады
- Ответы и задания по МХК искусство всероссийская олимпиада школьный этап 2019-2020
- Ответы и задания по ОБЖ всероссийская олимпиада 2018-2019
- Ответы и задания по ОБЖ школьный этап всероссийской олимпиады школьников 2019-2020
- Ответы и задания по обществознанию 11 класс ОБ10101 ОБ10102 статград 2018-2019
- Ответы и задания по обществознанию 9 класс 26 января 2018 СтатГрад
- Ответы и задания по обществознанию ОГЭ 2018
- Ответы и задания по праву муниципальный этап 11 ноября всероссийской олимпиады 2018-2019
- Ответы и задания по русскому языку 11 класс 19 января 2018 СтатГрад
- Ответы и задания по русскому языку 11 класс 2 октября 2019 РУ1910101 РУ1910102
- Ответы и задания по Русскому языку 11 класс статград 28 марта 2018
- Ответы и задания по русскому языку 7 класс входная работа
- Ответы и задания по русскому языку 8 класс 56 регион
- Ответы и задания по русскому языку 9 класс МЦКО 1 октября 2019
- Ответы и задания по русскому языку 9 класс статград РУ1990101-02 16 октября 2019
- Ответы и задания по Русскому языку КДР 11 класс январь 2019
- Ответы и задания по русскому языку муниципальный этап 11 ноября всероссийской олимпиады 2018-2019
- Ответы и задания по русскому языку ОГЭ 2018
- Ответы и задания по русскому языку олимпиада школьный этап 22 октября 2019
- Ответы и задания по физике 10 класс КДР 30 января 2018
- Ответы и задания по физике 11 класс ВОШ 2018-2019
- Ответы и задания по физике 11 класс ВПР 2018 10.
 04.18
04.18 - Ответы и задания по физике 11 класс КДР 30 января 2018
- Ответы и задания по физике 9 класс 29 января 2018 СтатГрад
- Ответы и задания по физике 9 класс КДР 30 января 2018
- Ответы и задания по физике 9 класс статград
- Ответы и задания по физике школьный этап всероссийской олимпиады 2019-2020
- Ответы и задания по химии 11 класс 28 ноября 2018
- Ответы и задания по химии 11 класс ВПР 2018 05.04.18
- Ответы и задания по химии 11 класс статград ХИ1910101 и ХИ1910102 15 октября 2019
- Ответы и задания по химии 9 класс статград ХИ1990101-ХИ1990104 21 октября 2019
- Ответы и задания по химии 9 класс тренировочная работа статград
- Ответы и задания по экологии школьный этап всероссийской олимпиады школьников 2019-2020
- Ответы и задания русский язык 11 класс варианты 16 мая 2019 год
- Ответы и задания русский язык 7 класс ВПР 9 апреля 2019 год
- Ответы и задания русский язык 9 класс 56 регион 06.
 04.18
04.18 - Ответы и задания стартовая работа русский язык 8 класс 23 сентября 2019
- Ответы и задания статград обществознание 11 класс 14 декабря 2018
- Ответы и задания статград по физике 9 класс варианты 24 октября 2019
- Ответы и задания тренировочная №4 история 9 класс 21 марта 2019
- Ответы и задания ФИ90401 и ФИ90402 физика 9 класс 4 марта 2019
- Ответы и задания Физика ОГЭ 2018 9 класс
- Ответы и задания ЧИП 1-2 класс 2019
- Ответы и задания школьный этап по математике всероссийской олимпиады новосибирская область 2019-2020
- Ответы и задания школьный этап по физике всероссийской олимпиады в Московской области 2019-2020
- Ответы КДР 2019 по информатике 10 класс 15 марта 23 регион
- Ответы КДР 2019 по информатике 9 класс 15 марта 23 регион
- Ответы КДР 2019 по литературе 10 класс 15 марта 23 регион
- Ответы КДР 2019 по литературе 9 класс 15 марта 23 регион
- Ответы КДР 23 регион биология 11 класс 21.
 12.2018
12.2018 - Ответы КДР 23 регион история 11 класс 21.12.2018
- Ответы КДР задания 23 регион Февраль 2019 год
- Ответы КДР литература 11 класс 14 декабря 2018
- Ответы КДР физика 11 класс 14 декабря 2018
- Ответы МЦКО математика 10 класс 5 декабря 2018
- Ответы МЦКО математика 11 класс 28 ноября 2018
- Ответы МЦКО по истории 9 класс 19.09
- Ответы на тренировочная работа по химии 9 класс «СтатГрад»
- Ответы на тренировочную работу по русскому языку 11 класс
- Ответы обществознание 9 класс статград 5 декабря 2018
- Ответы обществознание для 10 классов 23 регион
- Ответы ОГЭ 2018 английский язык
- Ответы ОГЭ 2018 русский язык
- Ответы олимпиада по праву 9 класс школьный этап ВОШ 2018-2019
- Ответы олимпиада по физике 9 класс 2018-2019
- Ответы по английскому языку 7-9 класс 56 регион 10.12.2018 Аудирование
- Ответы по английскому языку олимпиада ВОШ школьный этап 2018-2019
- Ответы по астрономии школьный этап олимпиады ВОШ 2018-2019
- Ответы по биологии 9 10 11 класс вош 2018-2019 школьный этап
- Ответы по биологии для 9 классов (Оренбургская область, 56 регион)
- Ответы по географии ВОШ олимпиада школьный этап 2018-2019
- Ответы по географии для 9 классов 11 регион
- Ответы по информатике 11 класс 12.
 05
05 - Ответы по искусству МХК олимпиада ВОШ школьный этап 2018-2019
- Ответы по истории 11 класс статград тренировочная работа №1 26.09
- Ответы по истории 11 класс школьный этап олимпиады ВОШ 2018-2019
- Ответы по истории 9 класс статград
- Ответы по истории для 9 классов (Оренбургская область, 56 регион)
- Ответы по математике 7-8 класс КДР
- Ответы по математике 8 класс МЦКО 28 марта 2018
- Ответы по математике 9 класс 64 регион
- Ответы по математике 9 класс СтатГрад 15.02
- Ответы по немецкому языку 7-9 класс 56 регион 10.12.2018 Аудирование
- Ответы по русскому языку 11 класс 11 регион 13.02
- Ответы по русскому языку для 7 и 8 класс 12.05
- Ответы по русскому языку школьный этап олимпиады ВОШ 2018-2019
- Ответы по тренировочная работа по биологии 11 класс
- Ответы по тренировочная работа по обществознанию 9 класс
- Ответы по физике 9 класс ФИ90201 и ФИ90202 статград 7 декабря 2018
- Ответы по физике, биологии для 11 классов 56 регион 16.
 02
02 - Ответы по химии 11 класс пробное ЕГЭ статград 12 марта 2019
- Ответы по химии 9 класс статград 19 декабря 2018
- Ответы по химии, информатике, географии, обществознанию для 9 классов
- Ответы по экологии школьный этап ВОШ 2018-2019
- Ответы репетиционный экзамен по математике 9 класс пробное ОГЭ 9 февраля 2018
- Ответы РПР по математике 9 класс 64 регион 3 этап 2018
- Ответы русский язык 10 класс 56 регион 12.05
- Ответы русский язык 5-8 класс контрольная работа за 1 полугодие 56 регион 2018
- Ответы статград география 11 класс 11.12.2018
- Ответы СтатГрад по обществознанию 9 класс
- Ответы статград по обществознанию 9 класс варианты ОБ1990101-02 23 октября 2019
- Ответы тренировочная работа по истории 9 класс
- Ответы тренировочная работа по математике 10 класс 08.02.2017
- Ответы тренировочная работа по русскому языку 9 класс 09.02.2017
- Ответы тренировочная работа по химии 11 класс 14.
 02
02 - Ответы физике для 9 классов (Оренбургская область, 56 регион)
- Отзывы прошлых лет
- Отзывы с первого экзамена ОГЭ 2018 по английскому языку
- Отзывы с первых экзаменов ЕГЭ 2017
- Отзывы с прошедших экзаменов ОГЭ 2019
- Отзывы с экзамена по русскому языку ОГЭ 2018
- Открытый банк заданий и ответы ФИПИ ЕГЭ 2019 по русскому языку 11 класс
- Официальные работы РДР 2019-2020 для 78 региона
- РДР 2020 по математике 11 класс задания и ответы 2 варианта ИС «Знак»
- РДР 2020 по математике 9 класс задания, ответы и критерии
- Официальные работы РДР для 78 региона 2018-2019 учебный год
- Официальные РДР 2020 для Московской области задания и ответы
- Официальные РДР 2021 для Московской области задания и ответы
- Официальные РДР 2022 для Московской области задания и ответы
- Официальные темы для Республика Саха (Якутия) Сахалинская область итоговое сочинение 2018-2019
- Официальные темы итогового сочинения 2018-2019 11 класс для часового пояса MSK+1
- Официальные темы итогового сочинения 2018-2019 11 класс для часового пояса MSK+6
- Официальные темы итогового сочинения 2018-2019 11 класс для часового пояса МСК
- Официальные темы итогового сочинения 2018-2019 для часового пояса MSK +9
- Официальные темы итогового сочинения 2018-2019 для часового пояса MSK+7
- Оформление заказа
- Пегас 2018 задания и ответы 7 февраля конкурс по литературе
- Пегас 2019 5-6 класс ответы и задания
- Пегас 2019 7-8 класс ответы и задания
- Пегас 2019 ответы для 9-11 класса
- Письмо английский язык 7 8 9 класс 56 регион ответы и задания
- Платно русский язык 9 класс
- Поддержать проект
- Полугодовая контрольная работа по русскому языку 11 класс задания и ответы 2019-2020
- ПОЛЬЗОВАТЕЛЬСКОЕ СОГЛАШЕНИЕ
- Предэкзаменационная работа задания и ответы по информатике 9 класс ОГЭ 2019
- Предэкзаменационная работа задания и ответы по математике 11 класс ЕГЭ 2019
- Пригласительный школьный этап 2021 всероссийская олимпиада школьников задания и ответы
- Пробная (тренировочная) ВПР 2019 география 10-11 класс ответы и задания
- Пробное (тренировочное) ВПР 2019 биология 11 класс ответы и задания
- Пробное (тренировочное) ВПР 2019 география 6 класс ответы и задания
- Пробное (тренировочное) ВПР 2019 математика 7 класс ответы и задания
- Пробное (тренировочное) ВПР 2019 русский язык 4 класс ответы и задания
- Пробное (тренировочное) ВПР 2019 русский язык 5 класс ответы и задания
- Пробное (тренировочное) ВПР 2019 русский язык 6 класс ответы и задания
- Пробное ВПР 2019 ответы и задания по английскому языку 11 класс
- Пробное ВПР 2019 ответы и задания по биологии 5 класс
- Пробное ВПР 2019 ответы и задания по биологии 7 класс
- Пробное ВПР 2019 по истории 5 класс ответы и задания
- Пробное ВПР 2019 по истории 6 класс ответы и задания
- Пробное ВПР 2019 по химии 11 класс ответы и задания
- Пробное Итоговое собеседование 9 класс русский язык ОГЭ 2019 задания
- Пробный экзамен по обществознанию и литературе для 11 классов ответы
- Проект математическая вертикаль ответы и задания
- Работа по математике 11 класс статград ответы и задания 25 сентября 2019
- Работа статград по русскому языку 9 класс 3 декабря 2019 ответы и задания
- Работы (задания+ответы) для Республики Коми Март 2017
- Работы (задания+ответы) Март 2017 СтатГрад
- Работы (задания+ответы) Февраль 2017
- Работы (задания+ответы) Январь 2017
- Работы 56 регион ответы и задания май 2019 год
- Работы для 56 региона Май 2018 ответы и задания
- Работы для Оренбургской области
- Работы для Республики Коми Декабрь 2017 задания и ответы
- Работы для Республики Коми Ноябрь 2017 задания и ответы
- Работы для Республики Коми Октябрь 2017 задания и ответы
- Работы задания и ответы по регионам
- Работы МЦКО демоверсии задания и ответы
- Работы СтатГрад 2018 февраль задания и ответы
- Работы СтатГрад апрель 2018 задания и ответы
- Работы Статград ВПР задания и ответы февраль 2019
- Работы статград ВПР март 2019 задания и ответы
- Работы СтатГрад декабрь 2017 задания и ответы
- Работы статград декабрь 2018-2019 ответы и задания
- Работы статград декабрь 2019 задания и ответы 2019-2020 учебный год
- Работы статград задания и ответы ноябрь 2019-2020 учебный год
- Работы СтатГрад задания и ответы октябрь 2018
- Работы статград задания и ответы октябрь 2019-2020 учебный год
- Работы СтатГрад задания и ответы сентябрь 2018
- Работы СтатГрад март 2018 задания и ответы
- Работы СтатГрад ноябрь 2017 задания и ответы
- Работы СтатГрад октябрь 2017 задания и ответы
- Работы СтатГрад сентябрь 2017 задания и ответы
- Работы статград сентябрь 2019 год ответы и задания
- Работы СтатГрад январь 2018 задания и ответы
- Работы статград январь 2020 задания и ответы 2019-2020 учебный год
- Работы СтатГрад, КДР за апрель 2017
- Работы СтатГрад, КДР за май 2017
- Работы СтатГрад, КДР за март 2017
- Работы СтатГрад, КДР, тренировочные за февраль 2017
- Работы СтатГрад, КДР, тренировочные за январь 2017
- Рабочая программа по окружающему миру ФГОС с 1 по 4 класс на 2022-2023
- Рабочая программа по чтению ФГОС с 1 по 4 класс на 2022-2023
- Рабочие программы по английскому языку ФГОС с 2 по 11 класс на 2022-2023
- Рабочие программы ФГОС на 2022-2023 учебный год для 1-11 класса
- Рабочая программа по информатике ФГОС с 5 по 11 класс на 2022-2023
- Рабочие программы 7 класс по ФГОС на 2022-2023 год
- Рабочие программы для 10 класса ФГОС на 2022-2023
- Рабочие программы по ОБЖ ФГОС с 5 по 11 класс на 2022-2023
- Разговоры о важном цикл внеурочных занятий 2022-2023
- Расписание
- ЕГЭ 2021 официальное расписание проведения экзаменов от Рособрнадзора
- ЕГЭ и ОГЭ 2020 год официальное расписание экзаменов у 9 и 11 класса
- ОГЭ 2021 официальное расписание проведения экзаменов у 9 класса
- Официальное расписание ЕГЭ 2019 11 класс основной досрочный этап
- Расписание муниципального этапа всероссийской олимпиады школьников в Санкт-Петербурге 2018-2019
- Расписание работ КДР 2019
- Расписание РДР 2020-2021 для 58 региона задания и ответы Пензенская область
- Расписание РПР 2018-2019 для 26 региона
- Расписание ГИА ОГЭ 2017
- Расписание ЕГЭ 2018 досрочный основной резервный период
- Расписание итогового сочинения 2017-2018
- Расписание проведения экзаменов 9 класса ОГЭ 2018
- Расписание школьных олимпиад 2017-2018 задания и ответы
- Распределения реальных тем итогового сочинения 2017-2018 по зонам регионам
- РДР 2019-2020 по физике 10 класс ответы и задания
- РДР 8 класс ответы и задания по математике 15 ноября 2018
- РДР математика 10 класс 14 ноября 2019 ответы и задания
- РДР математика 6 класс ответы и задания 21 ноября 2019 78 регион
- РДР ответы и задания для Санкт-Петербурга
- Официальные работы РДР для 78 региона задания и ответы 2020-2021 учебный год
- РДР по русскому языку 9 класс ответы и задания вариант 1901 и 1902 17 октября 2019
- Реальное ВПР 2020 задание 1 по биологии 5 класс с ответами
- Реальное ВПР 2020 задание 2 по биологии 5 класс с ответами
- Реальное ВПР 2020 задание №1 по русскому языку 5 класс с ответами
- Реальное ВПР 2020 задание №10 по биологии 5 класс с ответами
- Реальное ВПР 2020 задание №10 по русскому языку 5 класс с ответами
- Реальное ВПР 2020 задание №11 по русскому языку 5 класс с ответами
- Реальное ВПР 2020 задание №12 по русскому языку 5 класс с ответами
- Реальное ВПР 2020 задание №2 по русскому языку 5 класс с ответами
- Реальное ВПР 2020 задание №3 по биологии 5 класс с ответами
- Реальное ВПР 2020 задание №3 по русскому языку 5 класс с ответами
- Реальное ВПР 2020 задание №4 по биологии 5 класс с ответами
- Реальное ВПР 2020 задание №4 по русскому языку 5 класс с ответами
- Реальное ВПР 2020 задание №5 по биологии 5 класс с ответами
- Реальное ВПР 2020 задание №5 по русскому языку 5 класс с ответами
- Реальное ВПР 2020 задание №6 по биологии 5 класс с ответами
- Реальное ВПР 2020 задание №6 по русскому языку 5 класс с ответами
- Реальное ВПР 2020 задание №7 по биологии 5 класс с ответами
- Реальное ВПР 2020 задание №7 по русскому языку 5 класс с ответами
- Реальное ВПР 2020 задание №8 по русскому языку 5 класс с ответами
- Реальное ВПР 2020 задание №9 по русскому языку 5 класс с ответами
- Реальные задания по математике ПРОФИЛЬ ЕГЭ 2018
- Реальные темы и готовые сочинения 4 декабря 2019 ФИПИ для региона МСК+9
- Реальные темы итогового сочинения 2018-2019 5 декабря
- Реальный вариант с ЕГЭ 2019 по математике 29 мая 2019 год
- Региональный экзамен по математике 7 класс
- Региональный экзамен по математике 7 класс 56 регион ответы и задания
- Региональный экзамен по русскому языку 8 класс 56 регион
- Региональный этап 2019 по астрономии задания и ответы всероссийская олимпиада
- Региональный этап 2019 по географии ответы и задания ВОШ
- Региональный этап 2019 по искусству МХК ответы и задания ВОШ
- Региональный этап 2019 по истории задания и ответы всероссийская олимпиада
- Региональный этап 2019 по немецкому языку задания и ответы
- Региональный этап по биологии задания всероссийская олимпиада 2018-2019
- Региональный этап по математике ответы и задания 2019
- Результаты ЕГЭ 2017 у школьников
- Решать реальное ВПР 2020 задание №8 по биологии 5 класс с ответами
- Решать реальное ВПР 2020 задание №9 по биологии 5 класс с ответами
- Решения и задания муниципального этапа 2019 олимпиады по математике
- РПР 2017-2021 задания и ответы для Саратовской области 64 регион
- РПР математика 9 класс 3 этап задания и ответы 2018-2019
- РПР по математике 9 класс 64 регион задания 2018-2019
- Русский медвежонок 10-11 класс ответы и задания 2018-2019
- Русский медвежонок 14 ноября 2019 ответы и задания 6-7 класс
- Русский медвежонок 2-3 класс ответы и задания 2018-2019
- Русский медвежонок 2019 ответы и задания для 10-11 класса 14 ноября
- Русский Медвежонок 2019 ответы и задания для 2-3 класса
- Русский медвежонок 2019-2020 ответы и задания 8-9 класс 14 ноября
- Русский медвежонок 4-5 класс ответы и задания 2018-2019
- Русский медвежонок для учителей 2020 год задания и ответы
- Русский язык 10 класс КДР ответы и задания
- Русский язык 10 класс КДР ответы и задания 19 декабря 2018
- Русский язык 10 класс ответы и задания 56 регион
- Русский язык 10 класс ответы МЦКО 8 ноября 2018 год
- Русский язык 10 класс СтатГрад ответы 12.
 05
05 - Русский язык 10-11 класс ответы и задания 22 апреля 2019 тренировочная №1
- Русский язык 10-11 класс ответы и задания СтатГрад
- Русский язык 10-11 класс ответы РЯ10901 и РЯ10902 6 марта 2019
- Русский язык 11 класс 03.06.2019
- Русский язык 11 класс 11 ноября 2019 ответы и задания работа статград
- Русский язык 11 класс 56 регион ответы
- Русский язык 11 класс диагностическая работа №5 ответы и задания 8 апреля 2019
- Русский язык 11 класс КДР ответы и задания 19 декабря 2018
- Русский язык 11 класс контрольная работа в формате ЕГЭ 2 варианта задания и ответы
- Русский язык 11 класс мониторинговая работа ответы и задания
- Русский язык 11 класс ответы и задания диагностика 2 статград 18 марта 2019
- Русский язык 11 класс ответы и задания СтатГрад 17.05
- Русский язык 11 класс ответы РЯ10601 и РЯ10602 статград 2018-2019
- Русский язык 11 класс ответы статград 30 января 2019
- Русский язык 11 класс РЯ1910701-РЯ1910702 статград ответы и задания 11 декабря 2019
- Русский язык 11 класс статград 24 октября 2019 ответы и задания РЯ1910601-02
- Русский язык 11 класс статград ЕГЭ ответы и задания
- Русский язык 11 класс СТАТГРАД ответы и задания 28 февраля
- Русский язык 11 класс статград ответы и задания вариант РЯ10201 и РЯ10202 07.
 11.2018
11.2018 - Русский язык 11 класс тренировочная работа №1 ответы статград 2018-2019
- Русский язык 3 класс МЦКО ВСОКО задания итоговая работа 2019
- Русский язык 4 класс ВПР 2020 демоверсия задания и ответы ФИПИ
- Русский язык 4 класс задания и ответы мониторинговая работа 2019-2020
- Русский язык 5 класс демоверсия ВПР 2020 ФИПИ задания и ответы
- Русский язык 5 класс ответы и задания 21.09
- Русский язык 6 класс ВПР 2018 ответы и задания
- Русский язык 6 класс ВПР 2019 ответы и задания 23 апреля
- Русский язык 6 класс ВПР 2020 демоверсия фипи задания и ответы
- Русский язык 6 класс статград ответы и задания 2018-2019
- Русский язык 7 класс 56 регион ответы
- Русский язык 7 класс 56 регион ответы и задания 15 марта 2018
- Русский язык 7 класс задания и ответы мониторинговая работа 10 сентября 2019
- Русский язык 7 класс ответы и задания РУ1970101 и РУ1970102 26 сентября 2019
- Русский язык 7 класс ответы и задания статград 2018-2019
- Русский язык 7 класс статград ответы и задания
- Русский язык 7-8 класс ответы КДР 23 января 2019
- Русский язык 8 класс 56 регион задания и ответы
- Русский язык 8 класс КДР ответы и задания 19 декабря 2018
- Русский язык 8 класс ответы и задания 56 регион
- Русский язык 8 класс ответы и задания 6 мая 2019 итоговая работа
- Русский язык 8 класс стартовая работа ответы и задания 24.
 09
09 - Русский язык 8 класс статград ответы и задания
- Русский язык 9 класс 11.05 ответы
- Русский язык 9 класс 74 регион ответы
- Русский язык 9 класс ответы и задания 19 апреля 2019 диагностическая работа №4
- Русский язык 9 класс ответы и задания варианты 13 мая 2019 год
- Русский язык 9 класс ответы и задания диагностика статград 15 марта 2019
- Русский язык 9 класс ответы и задания полугодовая работа 2018-2019
- Русский язык 9 класс ответы изложение статград 2018-2019
- Русский язык 9 класс СтатГрад 17.04
- Русский язык 9 класс СтатГрад задания и ответы
- Русский язык 9 класс статград ОГЭ ответы и задания 15 марта 2018
- Русский язык 9 класс СТАТГРАД ответы и задания
- Русский язык 9 класс статград РЯ90201-РЯ90202 ответы и задания 27.11.
- Русский язык платно
- Русский язык школьный этап 2018-2019 ответы и задания Санкт-Петербург
- Русский язык школьный этап 2019-2020 задания и ответы московская область
- РЭ по математике 7 класс 24.
 05 ответы
05 ответы - РЭ по русскому языку 7 класс ответы 19.05
- РЭ по русскому языку 8 класс ответы 24.05
- СтатГрад
- Задания и ответы работы СТАТГРАД ВПР март 2020
- Работы статград апрель 2021 год задания ответы и решения
- Работы статград апрель 2022 год варианты ответы и решения
- Работы статград декабрь 2020 год задания ответы и решения
- Работы статград декабрь 2021 год задания ответы и решения
- Работы статград задания и ответы апрель 2020 год
- Работы статград май 2020 год задания, ответы, решения
- Работы статград май 2021 год задания ответы и решения
- Работы статград май 2022 год варианты ответы и решения
- Работы статград март 2021 год задания ответы и решения
- Работы статград март 2022 год задания ответы и решения
- Работы статград ноябрь 2020 год задания, ответы и решения
- Работы статград ноябрь 2021 год задания ответы и решения
- Работы статград октябрь 2020 год задания, ответы и решения
- Работы статград октябрь 2021 год задания ответы и решения
- Работы статград сентябрь 2020 год задания, ответы и решения
- Работы статград сентябрь 2021 год задания ответы и решения
- Работы статград сентябрь 2022 год варианты ответы и решения
- Работы статград февраль 2021 год задания ответы и решения
- Работы статград февраль 2022 год задания ответы и решения
- Работы статград январь 2021 год задания ответы и решения
- Работы статград январь 2022 год задания ответы и решения
- Статград 9 класс русский язык ответы и задания 21.
 12.2018
12.2018 - СтатГрад апрель 2017 работы задания и ответы
- СтатГрад биология 11 класс 14.04.17
- Статград ВПР работы апрель 2019 ответы и задания
- СТАТГРАД ВПР февраль 2020 задания и ответы 2019-2020 учебный год
- Статград география 11 класс ответы и задания март 2018
- Статград география 9 класс ответы и задания 20 ноября 2018
- СтатГрад задания и ответы по обществознанию 11 класс 1 февраля 2018 года
- Статград задания и ответы январь 2018-2019
- Статград информатика 9 класс 27 ноября 2019 ответы и задания ИН1990201-ИН1990204
- СтатГрад информатика 9 класс ответы и задания 5 марта 2018
- Статград история 11 класс 2 варианта ответы и задания 12 марта 2018
- СтатГрад май 2017 работы задания и ответы
- СтатГрад математика 11 класс ответы и задания 6 марта 2018
- Статград Обществознание 11 класс ответы и задания
- Статград обществознание 9 класс ответы и задания 13 марта 2018
- СтатГрад обществознание 9 класс ответы и задания 17.
 05
05 - СтатГрад ответы и задания для работ ноябрь 2018
- СтатГрад ответы и задания по математике 10 класс База и Профиль 7 февраля 2018
- СтатГрад ответы и задания по русскому языку 11 класс 6 февраля 2018
- Статград ответы русский язык 11 класс 19.12.2018
- СтатГрад по математике для 11 классов
- Статград работы май 2018 ответы и задания
- Статград работы ответы и задания май 2019
- СтатГрад русский язык диагностические работы 2017 задания и ответы
- Темы итогового сочинения 2017
- Темы на пробное итоговое сочинение для 52 региона
- Темы по направлениям которые будут итоговое сочинение 2018 6 декабря
- Тест по русскому языку 4 класс ВПР 2018 ответы и задания
- Тренировочная работа по биологии 11 класс
- Тренировочная работа по биологии 9 класс ответы и задания 15 января 2019
- Тренировочная работа по информатике 11 класс
- Тренировочная работа по информатике 9 класс ответы
- Тренировочная работа по математике 10 класс ответы 6 февраля 2019
- Тренировочная работа по математике 11 класс ответы 06.
 03
03 - Тренировочная работа по химии 11 класс ответы 8 февраля 2019
- Тренировочная работа статград по географии 11 класс ответы 15.02.2019
- Тренировочное ВПР 2019 ответы и задания по английскому языку 7 класс
- Тренировочное ВПР 2019 ответы и задания по биологии 6 класс
- Тренировочное ВПР 2019 ответы и задания по истории 11 класс
- Тренировочное ВПР 2019 ответы и задания по математике 6 класс
- Тренировочное ВПР 2019 ответы и задания по физике 11 класс
- Тренировочные варианты 200203, 200217, 200302 по химии 11 класс с ответами 2020
- Тренировочные варианты ВПР 2020 по химии 8 класс ХИ1980101,ХИ1980102
- Тренировочные варианты ЕГЭ 2022 по биологии задания с ответами
- Тренировочные варианты ЕГЭ 2022 по обществознанию 11 класс задания с ответами
- Тренировочные варианты ЕГЭ 2022 по русскому языку задания с ответами
- Тренировочные варианты ЕГЭ 2023 по математике 11 класс задания с ответами
- Тренировочные варианты ЕГЭ по английскому языку 11 класс задания с ответами
- Тренировочные варианты ЕГЭ по географии 11 класс задания с ответами
- Тренировочные варианты ЕГЭ по информатике задания с ответами
- Тренировочные варианты ЕГЭ по истории 11 класс задания с ответами
- Тренировочные варианты ЕГЭ по литературе 11 класс задания с ответами
- Тренировочные варианты ЕГЭ по физике 11 класс задания с ответами
- Тренировочные варианты ЕГЭ по химии 11 класс задания с ответами
- Тренировочные варианты КДР 10 класс обществознание 2019
- Тренировочные варианты ОГЭ по английскому языку 9 класс задания с ответами
- Тренировочные варианты ОГЭ по биологии 9 класс задания с ответами
- Тренировочные варианты ОГЭ по географии 9 класс задания с ответами
- Тренировочные варианты ОГЭ по информатике 9 класс задания с ответами
- Тренировочные варианты ОГЭ по истории 9 класс задания с ответами
- Тренировочные варианты ОГЭ по математике 9 класс задания с ответами
- Тренировочные варианты ОГЭ по обществознанию 9 класс задания с ответами
- Тренировочные варианты ОГЭ по русскому языку 9 класс задания с ответами
- Тренировочные варианты ОГЭ по физике 9 класс задания с ответами
- Тренировочные варианты ОГЭ по химии 9 класс задания с ответами
- Тренировочные варианты по биологии 10 класс задания с ответами
- Тренировочные задания МЦКО ВСОКО математика 3 класс 2019
- Тренировочные работы для 56 региона задания и ответы сентябрь 2018
- Тренировочные работы для 56 региона Оренбургской области задания и ответы
- Тренировочные работы по математике статград 2017 задания и ответы
- Тренировочный вариант 33006757 ЕГЭ по математике профильный уровень с ответами
- Тренировочный вариант 33006758 ЕГЭ по математике профильный уровень с ответами
- Тренировочный вариант 33006759 ЕГЭ по математике профильный уровень с ответами
- Тренировочный вариант ЕГЭ 34073002 по математике профильный уровень с ответами
- Тренировочный вариант ЕГЭ 34073003 по математике профильный уровень с ответами
- Тренировочный вариант ЕГЭ 34073004 по математике профильный уровень с ответами
- Тренировочный вариант ЕГЭ 34073005 по математике профильный уровень с ответами
- Тренировочный вариант ЕГЭ 34073006 по математике профильный уровень с ответами
- Тренировочный вариант ЕГЭ 34073007 по математике профильный уровень с ответами
- Тренировочный вариант ЕГЭ 34073008 по математике профильный уровень с ответами
- Тренировочный вариант ЕГЭ 34073009 по математике профильный уровень с ответами
- Тренировочный вариант ЕГЭ 34073010 по математике профильный уровень с ответами
- Тренировочный вариант ЕГЭ 34073011 по математике профильный уровень с ответами
- Тренировочный вариант с ответами 200316 по физике 11 класс ЕГЭ 2020
- Тренировочный варианты №191223 и №191209 по химии 11 класс ЕГЭ 2020
- Тренировочный ЕГЭ 2020 математика 11 класс профиль задания и ответы
- Турнир ЛОМОНОСОВ задания и ответы 2018-2019
- Турнир Ломоносова задания и ответы 2019-2020 учебный год
- 09.
 03.2020 XLII Заключительный тур Ломоносова по биологии задания и ответы
03.2020 XLII Заключительный тур Ломоносова по биологии задания и ответы - 09.03.2020 Заключительный тур Ломоносова по астрономии задания и ответы
- 29.09.2019 Задания и ответы по астрономии 42 турнир М.В.Ломоносова
- 29.09.2019 Задания и ответы по биологии 42 турнир М.В. Ломоносова
- 29.09.2019 Задания и ответы по истории 42 турнир М.В. Ломоносова
- 29.09.2019 Задания и ответы по лингвистике 42 турнир М.В. Ломоносова
- 29.09.2019 Задания и ответы по литературе 42 турнир М.В. Ломоносова
- 29.09.2019 Задания и ответы по математике 42 турнир М.В. Ломоносова
- 29.09.2019 Задания и ответы по физике 42 турнир М.В. Ломоносова
- 29.09.2019 Задания и ответы по химии 42 турнир М.В. Ломоносова
- Ответы и задания по истории XLII заключительный тур Ломоносова 9 марта 2020
- Ответы и задания по лингвистике XLII заключительный турнир Ломоносова 9 марта 2020
- Ответы и задания по литературе XLII заключительный турнир Ломоносова 9 марта 2020
- Ответы и задания по математике XLII заключительный турнир Ломоносова 9 марта 2020
- Ответы и задания по физике XLII заключительный турнир Ломоносова 9 марта 2020
- Ответы и задания по химии XLII заключительный турнир Ломоносова 9 марта 2020
- 09.
- Условия перепечатки материалов | Правообладателям
- Устная часть английский язык 2018 платно
- Устное собеседование 2019 официальные варианты 13 февраля
- Устное собеседование 9 класс 2019
- Физика 11 класс 7 ноября 2019 статград ответы и задания варианты ФИ1910201-ФИ1910204
- Физика 11 класс ВПР ответы 25.
 04
04 - Физика 11 класс ответы и задания 6 мая 2019 тренировочная работа №5
- Физика 11 класс ответы и задания пробник статград 14 февраля 2018
- Физика 11 класс ответы и задания статград 2018
- Физика 11 класс ответы и задания ФИ1910101 ФИ1910102 19 сентября 2019
- Физика 11 класс СтатГрад ответы и задания
- Физика 11 класс тренировочная ЕГЭ №4 статград ответы и задания 14 марта 2019
- Физика 7 класс ВПР 2019 ответы и задания 23 апреля
- Физика 9 класс задания и ответы СтатГрад
- Физика 9 класс ответы и задания ФИ90101 и ФИ90102 статград 2018-2019
- Физика 9 класс ответы и задания ФИ90401 ФИ90402 статград
- Физика 9 класс СтатГрад 03.05 ответы
- Физика 9 класс статград ответы и задания 10 декабря 2019 варианты ФИ1990201-ФИ1990204
- Физика ОГЭ 2018 ответы и задания 2 июня
- Физика ОГЭ 2018 платно
- Физика турнир Ломоносова задания 2018-2019
- Физическая культура 10 ноября задания муниципальный этап всероссийская олимпиада 2018-2019
- ФИПИ открытый банк заданий ЕГЭ 2019 по русскому языку Лексика и фразеология
- Французский язык 7-11 класс муниципальный этап 2019-2020 ответы и задания Москва
- Химия 11 класс 10.
 05 СтатГрад ответы
05 СтатГрад ответы - Химия 11 класс ВПР 27.04 задания и ответы
- Химия 11 класс ЕГЭ статград ответы и задания 14 марта 2018
- Химия 11 класс ответы для ХИ10101 ХИ10102 статград 19.10
- Химия 11 класс ответы и задания 28 ноября 2019 статград ХИ1910201-ХИ1910204
- Химия 11 класс ответы и задания варианты статград 13 мая 2019 год
- Химия 11 класс ответы и задания СтатГрад 9 февраля 2018 года
- Химия 11 класс СтатГрад задания и ответы
- Химия 9 класс задания и ответы СтатГрад
- Химия 9 класс КДР ответы и задания 15 февраля 2018 года
- Химия 9 класс ОГЭ 4 июня 2019 год
- Химия 9 класс ОГЭ статград ответы и задания 15 февраля 2018
- Химия 9 класс ответы и задания 16.05
- Химия 9 класс ответы и задания ОГЭ статград 22.03.2018
- Химия 9 класс ответы тренировочная №4 статград 20 марта 2019
- Химия 9 класс статград ОГЭ ответы и задания
- Химия ВОШ школьный этап ответы и задания 2018-2019
- Химия ответы и задания для школьного этапа всероссийской олимпиады 2019-2020
- Частная группа
- ЧИП Австралия 23 октября 2019 ответы и задания 7-8 класс
- ЧИП Австралия 3-4 класс ответы и задания 23 октября 2019-2020
- ЧИП Австралия ответы и задания 5-6 класс 23 октября 2019-2020
- ЧИП мир сказок 2019 ответы и задания для 1 класса 5-7 лет
- Читательская грамотность 4 класс МЦКО 2019 тестирование
- Чтение читательская грамотность 3 класс МЦКО ВСОКО задания 2019
- Школьные конкурсы расписание 2017-2018
- Школьные олимпиады и конкурсы 2017-2018 задания и ответы
- Школьный тур наше наследие 7-8 класс ответы и задания 2019-2020
- Школьный этап 2019-2020 всероссийская олимпиада по астрономии ответы и задания
- Школьный этап 2019-2020 олимпиады ВОШ по физике ответы и задания
- Школьный этап 2019-2020 по биологии ответы и задания всероссийской олимпиады школьников
- Школьный этап 2019-2020 по испанскому языку ответы и задания всероссийской олимпиады
- Школьный этап 2019-2020 по праву задания и ответы для всероссийской олимпиады школьников
- Школьный этап 2019-2020 по праву ответы и задания всероссийской олимпиады школьников
- Школьный этап 2019-2020 по русскому языку ответы и задания всероссийская олимпиада школьников
- Школьный этап ВОШ 2019-2020 ответы и задания по французскому языку
- Школьный этап ВОШ по информатике ответы и задания 2018-2019
- Школьный этап ВОШ по испанскому языку ответы и задания 2018-2019
- Школьный этап ВОШ по математике задания и ответы 2018-2019
- Школьный этап ВСЕРОССИЙСКИХ олимпиад 2017-2018 задания
- Школьный этап всероссийской олимпиады задания и ответы по обществознанию 2019-2020 учебный год
- Школьный этап всероссийской олимпиады задания и ответы по физической культуре 2019-2020
- Школьный этап ВсОШ 2019-2020 ответы и задания по обществознанию
- Школьный этап олимпиады по информатике ответы и задания всероссийской олимпиады 2019
- Школьный этап олимпиады по математике ответы и задания всероссийской олимпиады 2019
- Школьный этап олимпиады по экономике ответы и задания всероссийской олимпиады 2019
- Школьный этап по английскому языку 2019-2020 задания и ответы московская область
- Школьный этап по ОБЖ задания и ответы всероссийская олимпиада 2019-2020
- Экзамен по географии ОГЭ 2019
- Экономика олимпиада муниципальный этап 2019 ВсОШ задания и ответы
Химические свойства кремния – окислительные и восстановительные
4. 6
6
Средняя оценка: 4.6
Всего получено оценок: 247.
4.6
Средняя оценка: 4.6
Всего получено оценок: 247.
Кремний – твёрдый неметалл, входящий в состав горных пород. При обычных условиях инертен, но при нагревании проявляет окислительные и восстановительные свойства. Химические свойства кремния использует силикатная промышленность для изготовления стекла, зеркал, электроники, строительного материала.
Общее описание элемента
Кремний расположен в четвёртой группе и третьем периоде таблицы Менделеева. Ядро атома кремния имеет положительный заряд +14. Вокруг ядра движется 14 отрицательно заряженных электронов.
Атом может переходить в возбуждённое состояние за счёт свободного d-подуровня. Поэтому элемент проявляет две положительные степени окисления (+2 и +4) и одну отрицательную (-4). Электронная конфигурация – 1s22s22p63s23p2.
Рис. 1. Строение атома кремния.Кремний – хрупкий полупроводник с высокими температурами правления и кипения. Относительно лёгкий неметалл: плотность составляет 2,33 г/см3.
Относительно лёгкий неметалл: плотность составляет 2,33 г/см3.
В чистом виде кремний не встречается. Входит в состав песка, кварца, агата, аметиста и других пород.
Рис. 2. Агат.Реакции с неметаллами
При взаимодействии с неметаллами кремний проявляет восстановительные свойства – отдаёт электроны. Реакции возможны только при сильном нагревании. При нормальных условиях кремний реагирует только с фтором. Реакции с основными неметаллами приведены в таблице.
Элемент | Описание | Реакция |
Фтор | При обычных условиях | Si + 2F2 → SiF4 |
Кислород | Взаимодействует при 600°C с образованием диоксида (песка) | Si + O2 → SiO2 |
Хлор | Реагирует при 400°C | Si + 2Cl2 → SiCl4 |
Углерод | Реагирует при 2000°C с образованием карборунда | Si + C → SiC |
Азот | Протекает при 1000°C | 3Si + 2N2 → Si3N4 |
Сера | Реагирует при 1000°C | Si + 2S → SiS2 |
Бор | Взаимодействует при 2000°C | Si + 3B → B3Si |
Гидрид кремния – силан (SiH4) – можно получить путём разложения силицидов кислотой. Например, Mg2Si + 2H2SO4 → SiH4 + 2MgSO4.
Например, Mg2Si + 2H2SO4 → SiH4 + 2MgSO4.
Взаимодействие с металлами
Окислительные свойства кремний проявляет только в реакциях с металлами. При сплавлении образуются соли – силициды:
- Si + 2Mg → Mg2Si;
- Si + 2Ca → Ca2Si;
- Si + Na → NaSi;
- 2Si + Fe → FeSi2.
Силициды используются в промышленности для производства сплавов и материалов. В качестве сверхпроводника используется силицид ванадия (V3Si), полупроводника – силицид рения (ReSi).
Реакции со сложными веществами
Помимо простых веществ кремний реагирует со сложными соединениями – кислотами и щелочами. Основные реакции описаны в таблице.
Реакция | Описание | Уравнение |
С галогеноводородами | Реагирует с плавиковой кислотой при обычных условиях, с соляной кислотой – при 300°С, с бромоводородом – при 500°С | – Si + 4HF → SiF4 + 2H2; – Si + 4HCl → SiCl4 + 2H2; – Si + 4HBr → SiBr4 + 2H2 |
С кислотами | Является устойчивым по отношению к кислотам, покрываясь оксидной плёнкой. | 3Si + 4HNO3 + 18HF → 3H2[SiF6] + 4NO + 8H2O |
Со щелочами | В водных растворах растворяется, образуя силикаты и водород | Si + 2KOH + H2O → K2SiO3 + H2 |
При 1200°C кремний реагирует с диоксидом, образуя монооксид: Si + SiO2 → SiO.
Рис. 3. Применение кремния.Что мы узнали?
Кремний – хрупкий неметалл, взаимодействующий с металлами, неметаллами и сложными веществами. В реакциях с металлами проявляет свойства окислителя, с неметаллами – восстановителя. Реагирует при нормальных условиях только с фтором, плавиковой кислотой (в том числе вместе с азотной кислотой), со щелочами. Остальные реакции протекают при повышенных температурах.
Тест по теме
Доска почёта
Чтобы попасть сюда — пройдите тест.
Пока никого нет. Будьте первым!
Оценка доклада
4.6
Средняя оценка: 4.6
Всего получено оценок: 247.
А какая ваша оценка?
КОС по химии 8 класс
РЕСПУБЛИКА КРЫМ
ДЖАНКОЙСКИЙ РАЙОН
МУНИЦИПАЛЬНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
«ИЗУМРУДНОВСКАЯ ШКОЛА»
РАССМОТРЕНО | «СОГЛАСОВАНО» | «УТВЕРЖДАЮ»
| |
на заседании ШМО учителей, естественно-математических дисциплин | Зам. | Директор школы | |
Протокол №______ | ___________ А.Н. Ошмарин | _______________ Л.И. Липеха | |
от «_____» ______ 2016 г. | «____» ___________ 2016 г. | Приказ от «___»______2016 г. № ____ |
|
КОНТРОЛЬНО-оценочныЕ средствА
по химии
класс: 8
на 2016-2017 учебный год
материалы подготовила:
Липеха Лариса Ивановна,
учитель химии, специалист
с. Изумрудное, 2016 г.
Изумрудное, 2016 г.
Паспорт
контрольно- оценочных средств
по химии 8 класс
(наименование дисциплины)
№ п/п | Контролируемые темы (разделы) дисциплины | Наименование оценочного средства |
1 | «Первоначальные химические понятия» | Контрольная работа № 1 |
2 | «Основные понятия химии» | Контрольная работа № 2 |
3 | «Важнейшие классы неорганических соединений» | Контрольная работа №3 |
4 | «Периодический закон и периодическая система химических элементов Д. | Контрольная работа №4 |
Контрольная работа № 1 по теме:
«Первоначальные химические понятия»
Вариант I
Тест:
1. В левом столбце под номерами 1—3 записаны известные вам понятия, в правом столбце буквами А—В обозначены их характеристики. Выпишите номер, которым обозначено понятие, и букву, соответствующую его характеристике.
A. состоит из атомов одного вида, обладает постоянными физическими свойствами
Б. состоит из атомов разных видов, имеет постоянные свойства
В. один вид атомов, физические свойства которого обычно не характеризуют!
1 | 2 | 3 |
|
|
|
2. Очистить
железные опилки от порошка серы можно
Очистить
железные опилки от порошка серы можно
1) фильтрованием 3) нагреванием
2) с помощью магнита 4) растиранием смеси в ступке
3. Правильно вложен фильтр в воронку для проведения опыта по разделению смеси на рисунке
4. Только сложные вещества перечислены в ряду
1) воздух, вода, кислород
2) серная кислота, водород, озон
3) кислород, азот, хлор
4) поваренная соль, вода, сероводород
5. Какая запись обозначает, что молекула азота состоит из двух атомов?
1) 2N 2) N2 3) N2О 4) N2О3
6. В соединении с водородом валентность II всегда имеют химические элементы
1) S, N 2) О, S 3) О, С 4) S, С1
7. Среди
приведённых схем химических реакций к реакциям соединения относится
Среди
приведённых схем химических реакций к реакциям соединения относится
1) Zn + HCI → H2↑ + ZnCl2
2) СН4 + О2 → CО2↑ + Н2О
3) H2SО4 + Na2О → Na2SО4 + H2О
4) K2О + H2О → КОН
8. Валентность серы в соединении H2S равна
а) II б) I в) IV г) VI
9. Химическая реакция N2 + O2 → 2NO относится к реакциям
а) замещения б) соединения
в) разложения в) обмена
10. Коэффициентом в записи 5Al2(SO4)3 является:
а) 2 б) 3 в) 4 г) 5
11. Вычислите относительную молекулярную массу Na3PO4
Задания со свободным ответом:
1.
Составьте
формулы веществ: сульфида железа(II),
хлорида кремния(IV), иодида меди(I), оксида натрия.
2. Вычислите массовую долю кислорода в железной окалине Fe304.
3. Расставьте коэффициенты в схемах химических реакций и укажите тип каждой реакции:
а) Н2О + Р2О5 — Н3РО4
ЭЛ. ток
б) Н2О → H2↑ + О2↑
t
в) СuО + Н2 → Н2О + Сu
Вариант II
Тест
1. Покажите стрелкой вертикальной (↑), горизонтальной (→) или диагональной (\) расположение в каждом из трёх квадратов названий: в первом квадрате — металлов, во втором — сложных веществ, в третьем — смесей.
I II
Серебро | Сера | Кислород |
| Вода | Сера | Кислород |
Железо | Хлор | Кремний | Воздух | Углекислый газ | Азот | |
Медь | Водород | Азот | Железо | Медь | Сульфид алюминия |
Ill
|
2. Фильтрованием
можно разделить смесь
Фильтрованием
можно разделить смесь
1) воды и сахара 3) воды и угольной пыли
2) воды и поваренной соли 4) воды и уксусной эссенции
3. Правильно погасить пламя спиртовки нужно,
1) подув на пламя
2) надев на пламя колпачок
3) накрыв пламя руками
4. Только простые вещества перечислены в ряду
1) воздух, вода, кислород 3) кислород, азот, хлор
2) серная кислота, водород, озон 4) поваренная соль, вода, сероводород
5. Запись 2О2 обозначает
1) четыре атома кислорода
2) два атома кислорода
3) две молекулы кислорода
4) четыре молекулы кислорода
6. Валентность V и II азот имеет в каждом из веществ, указанных в ряду
1) N2О5, NO 3) N2O5, NО2,
2) NH3, N2O5 4) NH3, NO
7. Среди
приведённых схем химических реакций к реакциям разложения относится
Среди
приведённых схем химических реакций к реакциям разложения относится
1) Сu + H2SО4(конц.) → CuSО4 + H2О + SО2
2) HgO → Hg + О2
3) H2 + О2 — H2О
4) FeO + HC1 — FeCl2 + H2О
8. Валентность серы в соединении SО3 равна
а) II б) I в) IV г) VI
9. Химическая реакция СаСО3 → СаО + СО2↑ относится к реакциям
а) замещения б) соединения
в) разложения в) обмена
10. Коэффициентом в записи 5Al2(SO4)3 является:
а) 2 б) 3 в) 4 г) 5
11. Вычислите относительную молекулярную массу Ca3(PO4)
2. Задания cо свободным ответом:
1.
Вещества,
обозначенные формулами Н2, СО2, СН4, СаС12,
Р2О5, С, разделите на две
группы: простые и сложные вещества. Определите значения валентности атомов
химических элементов в формулах сложных веществ.
Определите значения валентности атомов
химических элементов в формулах сложных веществ.
2. Вычислите массовую долю химических элементов в молекуле метана СН4.
3. Расставьте коэффициенты в схемах химических реакций и укажите тип каждой реакции:
а) NH3 → N2 + H2↑
б) Na + Cl2 → NaCl
в) А1 + НС1 → А1С13 + Н2↑
Ответы Критерии оценивания.
1 вариант:
Первое задание:
1) 1-в, 2а, 3б,
2) 2
3) 2
4) 4
5) 2
6) 2
7) 4
В первом вопросе за каждый правильный ответ 0,5 б (всего 1,5 балла), в последующих вопросах за каждый правильный ответ -1 балл. Всего – 7,5 баллов.
Второе задание:
1. формулы
веществ: FeS , SiCl4,
CuI, Na2O – за каждую правильную формулу 1 балл
формулы
веществ: FeS , SiCl4,
CuI, Na2O – за каждую правильную формулу 1 балл
Всего 4 балла;
2. Вычислите массовую долю кислорода в железной окалине Fe3O4
Мr (Fe3O4) = 56×3 + 16x 4 = 232 – 1 балл
W (Fe) = 168 : 232 x 100% = 72,4 % — 1 балл
W (O) = 64 : 232 x 100% = 27,6 % — 1 балл
Всего – 3 балла
3. Расставьте коэффициенты в схемах химических реакций и укажите тип каждой реакции:
а) 3Н2О + Р2О5 = 2 Н3РО4 — реакция соединения
ЭЛ. ток
б) 2Н2О = 2 H2↑ + О2↑ — реакция разложения
в) СuО + Н2 = Н2О + Сu – реакция замещения
За правильно расставленные коэффициенты в
каждом уравнении -1 балл, за определение типа реакции -1 балл. Всего – 6
баллов.
Всего – 6
баллов.
Всего за работу – 20,5 балла.
Критерии оценивания:
«2» — от 0 — 10 баллов, «3» — 10,5 до 15 баллов, «4» -от 15,5 до17 баллов, «5» от 17,5 баллов.
Контрольная работа № 2 по теме:
«Основные понятия химии»
Цель урока. Проконтролировать знания и умения по теме: «Основные понятия химии»
«Кислород», «Водород», «Вода. Растворы».
Предметные. Уметь применять полученные знания.
Метапредметные. Развивать умения соотносить свои действия с планируемыми результатами, осуществлять контроль своей деятельности в процессе достижения результата, определять способы действий в рамках предложенных условий и требований, корректировать свои действия в соответствии с изменяющейся ситуацией.
Личностные. Формировать ответственное
отношение к учению.
Формировать ответственное
отношение к учению.
Вариант I
Тест.
1. Элемент, наиболее распространенный на Земле, — это
1) кислород 2) азот
3) водород 4) кремний
2. В промышленности кислород получают из
1) хлората калия 2) воды
3) воздуха 4) перманганата калия
3. Катализатором разложения пероксида водорода является
1) оксид кальция 2) оксид серы(IV)
3) оксид магния 4) оксид марганца(IV)
4. Кислород выделяется в ходе
1) гниения 2) дыхания
3) горения 4) фотосинтеза
5. Укажите газ, который не относиться к благородным
1) азот 2) гелий
3) аргон 4)неон
6. Как переводиться с греческого приставка
«экзо»?
Как переводиться с греческого приставка
«экзо»?
1) направо 2)налево
3) наружу 4) внутрь
7.Укажите правильное суждение
1) водород очень мало растворяется в воде
2) водород имеет высокую температуру сжижения
3) водород может быть получен при взаимодействии серебра с водой
4) водород не реагирует с кислород
8. Взвеси, в которых мелкие частицы твердого вещества равномерно распределены между молекулами воды, называются
1) суспензиями 2)эмульсиями
3) дымами 4)аэрозолями
9.Вода реагирует с активными металлами, такими как натрий и кальций, с образованием
1) гидроксидов 2)оксидов и водорода
3)кислот 4)гидроксидов и водорода
10. Вода реагирует почти со всеми оксидами неметаллов с образованием
1) гидроксидов и водорода 2)оксидов и водорода
3)кислот 4)гидроксидов
2 Задания со свободным ответом
1. Закончите уравнения реакций горения,
расставьте коэффициенты, назовите получившиеся вещества.
Закончите уравнения реакций горения,
расставьте коэффициенты, назовите получившиеся вещества.
а) P + O2 → б) C + O2 →
в) Zn + O2 → г) C2H6 + O2 →
2.Допишите уравнения реакций, характеризующих химические свойства водорода:
а) Н2 + CI2 →
t
б) Н2 + FeО →
Укажите, окисляется или восстанавливается водород в этих реакциях.
3.Рассчитайте, какую массу сахара и воды нужно взять для приготовления 250г раствора с массовой долей сахара 15%.
4.Составьте уравнения реакций взаимодействия с водой следующих веществ: калия, кальция, оксида лития. Укажите названия веществ, образующихся в результате реакции.
Вариант II Тест.
1. Укажите объемную долю кислорода в воздухе
1) 0,009 2) 0,209
3) 0,409 4) 0,781
2. В лаборатории кислород можно получить при
разложении
В лаборатории кислород можно получить при
разложении
1) хлората калия 2) перманганата калия
3) пероксида водорода 4) любого из перечисленных веществ
3. Молекулярный кислород не реагирует с
1) алюминием 2) золотом
3) медью 4) цинком
4. Газ, который поддерживает горение, — это
1) кислород 2) водород
3) азот 4) углекислый газ
5. Известковая вода мутнеет при пропускании через нее
1) оксида углерода(IV) 2) аргона
3) азота 4) оксида углерода(II)
6. Как переводиться с греческого приставка «эндо»?
1) направо 2)налево
3) наружу 4) внутрь
7. При нагревании идет реакция: H2 + CuO = Cu +H2O. Окислителем и восстановителем являются
При нагревании идет реакция: H2 + CuO = Cu +H2O. Окислителем и восстановителем являются
1) H2 и CuO
2) H2 и Cu
3) CuO и H2
4) CuO и H2O
8. Взвеси, в которых мелкие капельки жидкого вещества равномерно распределены между молекулами воды, называются
1) суспензиями 2) эмульсиями
3) дымами 4) аэрозолями
9. При нагревании вода реагирует с менее активными металлами, такими как железо и цинк, с образованием
1) гидроксидов 2) оксидов и водорода
3) кислот 4) гидроксидов и водорода
10. Вода реагирует с оксидами активных металлов, таких как натрий и кальций, с образованием
1) гидроксидов и водорода 2) оксидов и водорода
3) кислот 4) гидроксидов
2 Задания со свободным ответом
1. Закончите уравнения реакций горения,
расставьте коэффициенты, назовите получившиеся вещества.
Закончите уравнения реакций горения,
расставьте коэффициенты, назовите получившиеся вещества.
а) Fe + O2 → б) Ca + O2 →
в) Li + O2 → г) C2H2 + O2 →
2.Допишите уравнения реакций, характеризующих химические свойства водорода:
а) Н2 + S →
б)WO3 + H2 →
Укажите, окисляется или восстанавливается водород в этих реакциях.
3. Рассчитайте, какую массу сахара и воды нужно взять для приготовления 500г раствора с массовой долей сахара 5%.
4.Составьте уравнения реакций взаимодействия с водой следующих веществ: бария, лития, оксида натрия. Укажите названия сложных веществ, образующихся в результате реакции.
Ответы Критерии оценивания.
1 вариант:
Первое задание:
1) 1
2) 3
3) 4
4) 4
5) 1
6) 3
7) 1
8) 1
9) 4
10)3
За
каждый правильный ответ 1 балл. Всего – 10 баллов.
Всего – 10 баллов.
Второе задание
1.
а) 4P + 5O2 → 2P2O5 — оксид фосфора(V) б) C + O2 → CO2 – оксид углерода(IV)
в) 2Zn + O2 → 2ZnO — оксид цинка г) 2C2H6 + 7O2 → 4CO2 +6 H2O – оксид углерода(IV), вода
За каждое правильно написанное уравнение 1балл, за каждое правильно названное вещество 0,5 балла. Всего 6 баллов.
2.
а) Н2 + CI2 → 2HCl
t
б) Н2 + FeО → Fe +H2O
Водород в этих реакциях окисляется.
За каждое правильно написанное уравнение 1балл. За определение процесса 1 балл. Всего 3 балла.
3.1) m(сахара) = m(раствора) x W(сахара) : 100% = (250х15% ): 100% =37,5г
2) m(воды) = m(раствора) — m(сахара) = 250 — 37,5 =212,5г
За каждое правильное действие 1 балл, всего 2 балла
4 2K + 2H2O = 2KOH + H2
Ca + 2H2O = Ca(OH)2 + H2
Li2O +H2O = 2LiOH
KOH – гидроксид калия
Ca(OH)2 – гидроксид кальция
LiOH– гидроксид лития
За каждое правильно написанное уравнение
1балл, за каждое правильно названное вещество 0,5 балла. Всего 4,5 балла.
Всего 4,5 балла.
Всего за работу – 25,5 баллов
Критерии оценивания:
«2» — от 0 — 13 баллов, «3» — от13,5 до 18,5 баллов, «4» -от 19 до 21 баллов, «5» от 21,5 баллов.
Ответы Критерии оценивания.
2 вариант:
Первое задание:
1) 2
2) 4
3) 2
4) 1
5) 1
6) 4
7) 3
8) 2
9) 2
10)1
За каждый правильный ответ 1 балл. Всего – 10 баллов.
Второе задание
1.
а) 3Fe + 2O2 → FeO Fe2O3 (Fe3O4) — железная окалина б) 2Ca + O2 →2CaO – оксид кальция
в) 4Li + O2 → 2Li2O — оксид лития г) 2C2H2 + 5O2 → 4CO2 + 2H2O – оксид углерода(IV), вода
За каждое правильно написанное уравнение
1балл, за каждое правильно названное вещество 0,5 балла. Всего 6 баллов.
Всего 6 баллов.
2.
а) Н2 + S → H2S
t
б) WO3 + 3H2 →W + 3H2O
Водород в этих реакциях окисляется.
За каждое правильно написанное уравнение 1балл. за определение процесса 1 балл. Всего 3 балла.
3.1) m(сахара) = m(раствора) x W(сахара) : 100% = (500х 5% ): 100% = 25г
2) m(воды) = m(раствора) — m(сахара) = 500 — 25 = 475г
За каждое правильное действие 1 балл, всего 2 балла
4 Вa + 2H2O = Вa(OH)2 + H2
2Li + 2H2O = 2LiOH + H2
Na2O +H2O = 2NaOH
Вa(OH)2 – гидроксид бария
LiOH– гидроксид лития
NaOH – гидроксид натрия
За каждое правильно написанное уравнение
1балл, за каждое правильно названное вещество 0,5 балла. Всего 4,5 балла.
Всего за работу – 25,5 баллов
Критерии оценивания:
«2» — от 0 — 13 баллов, «3» — от13,5 до 18,5 баллов, «4» -от 19 до 21 баллов, «5» от 21,5 баллов.
Контрольная работа №3 по теме: «Важнейшие классы неорганических соединений»
Вариант 1
1. К кислотам относится каждое из 2-х веществ:
а) H2S, Na2CO3 б) K2SO4, Na2SO4 в)
H3PO4, HNO3 г) KOH, HCl
2. Расставьте коэффициенты, определи тип каждой реакции – соединение, разложение, замещение, обмена:
1) Fe(OH)3 = Fe2O3 + H2O; 2)Mg(OH)2 + HCl = MgCl2 + H2O; 3)ZnO+ Н2 → Zn + H2O;
4)N2 + O2 = NO.
3.Составьте уравнение реакции
по описанию, не забудь поставить коэффициенты. Если один из продуктов реакции
выпадает в осадок поставь — , если выделяется в виде газа поставь :
Если один из продуктов реакции
выпадает в осадок поставь — , если выделяется в виде газа поставь :
1) Карбонат кальция взаимодействует с соляной кислотой, образуя хлорид кальция, воду и оксид углерода (IV).
2)Нитрат серебра взаимодействует с хлоридом калия, образуя хлорид серебра и нитрат калия.
4. Осуществите цепочку следующих превращений:
а) S → SO2 → SO3 → H2SO4 → ZnSO4
5. Какая масса сульфата калия образуется при взаимодействии 49 г серной кислоты с гидроксидом калия?
Контрольная работа №3 по теме «Важнейшие классы неорганических соединений» Вариант 2
1. К основаниям относится каждое из 2-х
веществ:
а) H2O, Na2O; б) KOH, NaOH; в) HPO3, HNO3 ; г) KOH, NaCl.
2. Расставьте коэффициенты, определи тип каждой
реакции – соединение, разложение, замещение, обмена. 1)NaOH + HI = NaI + H2O; 2)K +
O2 = K2O ;3)HgO→ Hg + O2 ; 4)Fe2O3 + H2 = Fe +H2O
1)NaOH + HI = NaI + H2O; 2)K +
O2 = K2O ;3)HgO→ Hg + O2 ; 4)Fe2O3 + H2 = Fe +H2O
3.Составьте уравнение реакции по описанию, не забудь поставить коэффициенты. Если один из продуктов реакции выпадает в осадок – поставь- если выделяется в виде газа — .
1) Карбонат натрия взаимодействует хлоридом кальция, при этом образуются карбонат кальция и хлорид натрия.
2) Железо взаимодействует с соляной кислотой, при этом выделяется водород и образуется хлорид железа (II).
4. Осуществите цепочку следующих превращений:
а) Mg → MgO→MgCl2→Mg(OH)2 → MgO
5. Какая масса сульфата бария образуется при взаимодействии 30,6 г оксида бария с достаточным количеством серной кислоты?
Таблица ответов.
1 вариант | 2 вариант |
1 в | 1б |
2 б | 2 г |
3 а | 3 в |
4 б | 4 в |
5 б | 5 г |
6 в | 6 а |
7 а | 7 г |
8 — 253 | 8 — 253 |
10- 87 г | 10 – 46,6 г |
Контрольная работа
№4 на тему: «Периодический
закон и периодическая система химических элементов Д. И. Менделеева. Строение
атома»
И. Менделеева. Строение
атома»
1 вариант
Часть А
При выполнении заданий с выбором ответа этой части (А1 – А16) выберите один правильный ответ
А1. Какое количество протонов содержит атом натрия:
1) 23 2) 11 3) 1 4) 3
27
А2. Какое количество нейтронов содержит ядро атома алюминия 13 Аl
1) 14 2) 13 3) 27 4) 3
А3. Для элементов главных подгрупп число электронов на внешнем энергетическом уровне равно:
1) числу нейтронов 2) номеру периода 3) заряду ядра атома 4) номеру группы
А4. Атомы лития и натрия имеют одинаковое:
Атомы лития и натрия имеют одинаковое:
1) число нейтронов в ядре атома
2) значение относительной атомной массы
3) число протонов в ядре
4) число валентных электронов
А5. В атоме серы распределение электронов по энергетическим уровням соответствует ряду чисел:
1) 2, 8, 6 2) 2, 8, 4 3) 2, 6 4) 6, 8, 2
А6. В каком ряду химические элементы расположены в порядке усиления неметаллических свойств:
1) С → N → O 2) N → P → As 3) O → S → Se 4) Cl → S → P
А7. В ряду оксидов SiO2 → Al2O3 → MgOсвойства изменяются от:
1) кислотных к амфотерным
2) амфотерных к основным
3) основных к кислотным
4) кислотных к основным
А8. Хлор в ПСХЭ Д.И.Менделеева находится:
Хлор в ПСХЭ Д.И.Менделеева находится:
1) в 3 периоде VII В-группе
2) в 3 периоде VII A-группе
3) в 7 периоде III A-группе
4) в 7 периоде III В-группе
А9. В периоде слева направо увеличиваются:
1) металлические свойства простых веществ
2) радиусы атомов элементов
3) число электронов на внешнем энергетическом уровне
4) число энергетических уровней
А10. В ряду элементов Li → Na → K электроотрицательность:
1) увеличивается
2) уменьшается
3) не изменяется
4) изменяется периодически
А11. Валентные возможности атома фосфора:
1) III, IV 2) III, V 3) III 4) III, V, VIII
А12. Ковалентная полярная связь характерна для
1) С12 2) O2 3) Na2О 4) NH3
А13. Веществами с ковалентной полярной и
ионной связью являются, соответственно:
Веществами с ковалентной полярной и
ионной связью являются, соответственно:
1) сероводород и водород
2) хлорид калия и кислород
3) вода и хлорид натрия
4) оксид калия и аммиак
А14. Кристаллическая решетка алмаза:
1) ионная 2) молекулярная 3) атомная 4) металлическая
А15. В каких соединениях атомы азота и фосфора имеют одинаковое значение степени окисления
1) NH3 и Р 2) NO2 и PH3 3) NO и Ca3P2 4) NaNO3 и H3PO4
А16. В процессе превращения по схеме N-3 → N+2:
1) отдает электроны, восстанавливается
2) отдает электроны, окисляется
3) принимает электроны, окисляется
4) принимает электроны, восстанавливается
Часть В
В задании В1 выберите верные ответы и запишите цифры в порядке возрастания
B1. В ряду химических элементов C – N – O:
В ряду химических элементов C – N – O:
1) не изменяется число протонов в ядре
2) ослабевают неметаллические свойства
3) возрастает число электронов во внешнем энергетическом уровне
4) уменьшается радиус атомов
5) возрастают неметаллические свойства
6) увеличивается число энергетических уровней в атоме
В заданиях В2, В3 установите соответствия
В2. Установите соответствие между формулой вещества и степенью окисления серы в них:
А) | SO3 | 1) | -2 |
Б) | CaS | 2) | 0 |
В) | Na2SO3 | 3) | +2 |
Г) | Н2SO4 | 4) | +4 |
|
| 5) | +6 |
В 3. Установите соответствие между названием вещества и типом химической
связи в нём:
Установите соответствие между названием вещества и типом химической
связи в нём:
ТИП ХИМИЧЕСКОЙ СВЯЗИ | НАЗВАНИЕ ВЕЩЕСТВА |
А) ионная Б) ковалентная неполярная В) ковалентная полярная
| 1) O2 |
2) H2S | |
3) NaCl | |
|
Часть С
При выполнении задания этой части дайте развернутый ответ
С1. Расставьте коэффициенты методом электронного баланса в схеме химической реакции, определите окислитель и восстановитель:
H2S + O2 → SO2 + H2O
2 вариант
Часть А
При выполнении заданий с выбором ответа этой части (А1 – А16) выберите один правильный ответ
А1. Какое количество электронов содержит атом хлора:
Какое количество электронов содержит атом хлора:
1) 17 2) 35 3) 7 4) 3
23
А2. Какое количество нейтронов содержит ядро атома натрия 11 Na
1) 11 2) 12 3) 23 4) 3
А3. Число энергетических уровней в атоме равно:
1) порядковому номеру 3) номеру периода
2) заряду ядра атома 4) номеру группы
А4. Атомы азота и фтора имеют одинаковое:
1) значение радиусов атомов
2) значение относительной атомной массы
3) число энергетических уровней
4) число электронов на внешнем энергетическом уровне
А5. Схема распределения электронов по энергетическим уровням 2 , 8 ,7 соответствует атому:
1) хлора 2) фтора 3) кислорода 4) серы
А6. В каком ряду химические элементы расположены в порядке усиления металлических свойств:
В каком ряду химические элементы расположены в порядке усиления металлических свойств:
1) Na → Mg →Al
2) K → Na → Li
3) Ca → Mg → Be
4) Ca → Sr → Ba
А7. В ряду оксидов Al2O3 → SiO2 → P2O5 свойства изменяются от:
1) кислотных к основным
2) амфотерных к основным
3) основных к кислотным
4) амфотерных к кислотным
А8. Натрий в ПСХЭ Д.И.Менделеева находится:
1) в 3 периоде I В-группе
2) в 3 периоде I A-группе
3) в 1 периоде III A-группе
4) в 1 периоде III В-группе
А9. В группе (главной подгруппе) сверху вниз увеличиваются:
1) неметаллические свойства простых веществ
2) радиусы атомов элементов
3) число электронов на внешнем энергетическом уровне
4) значение электроотрицательности
А10. В ряду элементов P → S → Cl электроотрицательность:
В ряду элементов P → S → Cl электроотрицательность:
1) увеличивается 2) уменьшается
3) не изменяется 4) изменяется периодически
А11. Валентные возможности атома углерода:
1) II 3) III, V
2) II, IV 4) II, IV, VI
А12. Ионная связь характерна для
1) Н2 2) Н2О 3) NaCl 4) NH3
А13. Веществами с ковалентной неполярной и ионной связью являются, соответственно:
1) сероводород и оксид натрия
2) вода и водород
3) кислород и оксид натрия
4) аммиак и хлорид калия
А14. Кристаллическая решетка поваренной соли:
1) ионная
2) молекулярная
3) металлическая
4) атомная
А15. В каких соединениях атомы углерода и серы имеют одинаковое
значение степени окисления:
В каких соединениях атомы углерода и серы имеют одинаковое
значение степени окисления:
1) СO2 и H2S 3) Na2CO3 и SO2
2) CO и H2SO4 4)H2CO3 и Na2S
А16. В процессе превращения по схеме N+5 → N+3:
1) отдает электроны, восстанавливается
2) отдает электроны, окисляется
3) принимает электроны, окисляется
4) принимает электроны, восстанавливается
Часть В
В задании В1 выберите верные ответы и запишите цифры в порядке возрастания
B1. В ряду химических элементов Be – Mg – Ca
1) уменьшается радиус атомов
2) возрастают металлические свойства
3) возрастает число электронов во внешнем энергетическом уровне
4) уменьшается заряды ядер атомов
5) уменьшается значение электроотрицательности
6) увеличивается число энергетических уровней в атоме
В заданиях В2, В3 установите соответствия
В2. Установите соответствие
между формулой вещества и степенью окисления азота в них
Установите соответствие
между формулой вещества и степенью окисления азота в них
ФОРМУЛА ВЕЩЕСТВА | СТЕПЕНЬ ОКИСЛЕНИЯ | ||
А) | N2O3 | 1) | -3 |
Б) | Ca3N2 | 2) | +1 |
В) | NaNO3 | 3) | +2 |
Г) | NO2 | 4) | +3 |
|
| 5) | +4 |
|
| 6) | +5 |
В 3. Установите соответствие между названием вещества и типом химической
связи в нём:
Установите соответствие между названием вещества и типом химической
связи в нём:
ТИП ХИМИЧЕСКОЙ СВЯЗИ | НАЗВАНИЕ ВЕЩЕСТВА |
А) ионная Б) ковалентная неполярная В) ковалентная полярная
| 1) HCl |
2) Cl2 | |
3) CaF2 | |
|
Часть С
При выполнении заданий этой части дайте развернутый ответ
С1. Расставьте коэффициенты методом электронного баланса в схеме химической реакции, определите окислитель и восстановитель:
Mg + HCl → MgCl2 + H2
Ответы:
ЧАСТЬ А
Задание с выбором ответа считается выполненным верно, если учащийся
указал код правильного ответа. Во всех остальных случаях (выбран другой ответ;
выбрано два или больше ответов, среди которых может быть и правильный; ответ на
вопрос отсутствует) задание считается невыполненным.
Во всех остальных случаях (выбран другой ответ;
выбрано два или больше ответов, среди которых может быть и правильный; ответ на
вопрос отсутствует) задание считается невыполненным.
I вариант II вариант
№ задания | Ответ |
А1 | 2 |
А2 | 1 |
А3 | 4 |
А4 | 4 |
А5 | 1 |
А6 | 1 |
А7 | 4 |
А8 | 2 |
А9 | 3 |
А10 | 2 |
A11 | 2 |
A12 | 4 |
A13 | 3 |
A14 | 3 |
A15 | 4 |
A16 | 2 |
№ задания | Ответ |
А1 | 1 |
А2 | 2 |
А3 | 3 |
А4 | 3 |
А5 | 1 |
А6 | 4 |
А7 | 4 |
А8 | 2 |
А9 | 2 |
А10 | 1 |
A11 | 2 |
A12 | 3 |
A13 | 3 |
A14 | 1 |
A15 | 3 |
A16 | 4 |
ЧАСТЬ В
Задание с кратким свободным ответом считается
выполненным верно, если правильно указана последовательность цифр.
За полный правильный ответ на задания В1 – В3 ставится 2 балла, за правильный неполный – 1 балл, за неверный ответ (или при его отсутствии) – 0 баллов.
I вариант II вариант
Ответ | |
345 | |
В2 | 5145 |
В3 | 312 |
Ответ | |
256 | |
В2 | 4165 |
В3 | 321 |
ЧАСТЬ С
За
выполнение задания С1ставится от 0 до 3 баллов.
I вариант
Содержание верного ответа и указания по оцениванию (допускаются иные формулировки ответа, не искажающие его смысла) | Баллы |
Элементы ответа: 1) Расставлена степень окисления элементов: +1 -2 0 +4 -2 +1 -2 H2S + O2 → SO2 + H2O 2) Написана схема окисления и восстановления: S0 — 6е → S+4 (окисление, восстановитель) O20 +4е → 2O-2(восстановление, окислитель) 3) Составлен электронный баланс, расставлены коэффициенты:
2 S0 — 6е → S+4 (окисление, восстановитель) 12 3 O20 +4е → 2O-2(восстановление, окислитель)
2H2S + 3O2 → 2SO2 + 2H2O |
|
Ответ правильный и полный, включает все названные выше элементы | 3 |
Правильно записаны только два из названных выше элементов ответа | 2 |
Правильно записан один из названных выше элементов ответа | 1 |
Все элементы ответа записаны неверно | 0 |
Максимальный балл | 3 |
II вариант
Содержание верного ответа и указания по оцениванию (допускаются иные формулировки ответа, не искажающие его смысла) | Баллы |
Элементы ответа: 1) Расставлена степень окисления элементов: 0 +1 -1 +2 -1 0 Mg + HCl → MgCl2 + H2 2) Написана схема окисления и восстановления: Mg0 — 2е → Mg+2 (окисление, восстановитель) 2H+1 +2е → H20 (восстановление, окислитель) 3) Составлен электронный баланс, расставлены коэффициенты:
1 Mg0 — 2е → Mg+2 (окисление, восстановитель) 2 1 2H+1 +2е → H20 (восстановление, окислитель)
Mg + 2HCl → MgCl2 + H2 |
|
Ответ правильный и полный, включает все названные выше элементы | 3 |
Правильно записаны только два из названных выше элементов ответа | 2 |
Правильно записан один из названных выше элементов ответа | 1 |
Все элементы ответа записаны неверно | 0 |
Максимальный балл | 3 |
Q12 Напишите сбалансированные молекулярные уравнения для словесных уравнений 1 Кальций Кислород Оксид кальция 2 Кал.
 ..
..Перейти к
- Упражнение
- Вопросы объективного типа
- Иметь значение
- Физические и химические изменения
- Элементы, соединения и смеси
- Атомная структура
- Язык химии
- Химические реакции
- Водород
- Вода
- Углерод и его соединения
Главная > Союзные решения Класс 8 Химия > Глава 5 — Язык химии > Упражнение > Вопрос 12
Вопрос 12 Упражнение
Q12) Напишите сбалансированные молекулярные уравнения для словесных уравнений:
Кальций + кислород → оксид кальция
Кальций + вода → гидроксид кальция + водород
Цинк + серная кислота → сульфат цинка + водород
Сульфат свинца + Гидроксид аммония → Сульфат аммония + Гидроксид свинца
Гидроксид меди + Азотная кислота → Нитрат меди + Вода
Нитрат свинца + хлорид натрия → Нитрат натрия + хлорид свинца
Ответ:
Решение:
(а) 2Ca+\ O_2\ →\ 2CaO
(б) Ca+2H_2O\ →\ Ca\левый(ОН\правый)_2+H_2
(в) Zn+H_2SO_4 \ →\ ZnSO_4+H_2
(г) PbSO_4+2NH_4OH\ →\ Pb\левый(ОН\правый)_2+\левый(NH_4\правый)_2SO_4
(д) Cu\левый(ОН\правый)_2+2HNO_3 →\ Cu\левый[NO_3\правый]_2+2H_2O
(е) Pb\левый[NO_3\правый]_2+2NaCl\ →\ 2NaNO_3+PbCl_2
youtube.com/embed/jfhaDIkSAhU?rel=0″ frameborder=»0″ allow=»autoplay; fullscreen» loading=»lazy» allowfullscreen=»»>Стенограмма видео
«Здравствуйте, добро пожаловать на обучение. Мы собираемся решить, как сбалансировать уравнение монстра. Давайте посмотрим, либо сбалансируем молекулярное уравнение для словесных уравнений, использующих кальций плюс кислород. Вы, оксид кальция, в больнице собирались посмотри сейчас. Кальций. CA плюс кислород O2 вы нарезаете инструмент кальций справа. CA о создании побочных квестов перенаправляются на буквы. И rhs Пастор, когда мы закончим с этим, проверьте, жара Осень здесь. Мы получили, можно оценить на записи один атом кальция в его жидком кислороде, атомы кислорода здесь попали в кислород, был одним из десяти, когда я умножаю на два года, вы можете проверить, отправляйтесь в тюрьму и поместите кальций, а также вы можете оставаться здесь, чтобы мы могли сигнализировать об условиях для Галатам 2 кислород для окисления
И это равно правому балансу, тогда работайте над вторым. Calcium CA также позволяет поливать его. Используют нах, чтобы гидроксид кальция СА o h взял дважды плюс водород h3. Проверьте часы здесь. Я получил один кальций один кальций сбалансированный. Два водорода и для поддержки водорода здесь, чтобы прийти сюда и отсюда, чтобы сказать нам, когда я умножил на 2 здесь, и вы можете видеть, что увеличение кислорода на 0,042 для более безопасного для кислорода кальция сбалансировало водородный баланс и кислородный баланс. Ну, это равно rhs, когда я держу два года. Это был сбалансированный компьютер, один цинк плюс альфа-кепка, это, думаю, определенный процент от commbuys h3so4.
Тот же размер, что и сульфат цинка с сульфатом хондроитина, — это день, так что 4 сульфат — это так 4. Поместите водород H, чтобы сообщить им, что у нас есть хлопок с цинковым кольцом, и мы всего лишь квартал One Wing для авторов 2002 года, а не один раз и платите 100. NS равен ро по умолчанию сам. Итак, первая вторая, и мы закончили, мы собираемся изучить четвертую. Сегодня сам 84 мы делаем, мы должны знать, что исполнитель тепла один.
Calcium CA также позволяет поливать его. Используют нах, чтобы гидроксид кальция СА o h взял дважды плюс водород h3. Проверьте часы здесь. Я получил один кальций один кальций сбалансированный. Два водорода и для поддержки водорода здесь, чтобы прийти сюда и отсюда, чтобы сказать нам, когда я умножил на 2 здесь, и вы можете видеть, что увеличение кислорода на 0,042 для более безопасного для кислорода кальция сбалансировало водородный баланс и кислородный баланс. Ну, это равно rhs, когда я держу два года. Это был сбалансированный компьютер, один цинк плюс альфа-кепка, это, думаю, определенный процент от commbuys h3so4.
Тот же размер, что и сульфат цинка с сульфатом хондроитина, — это день, так что 4 сульфат — это так 4. Поместите водород H, чтобы сообщить им, что у нас есть хлопок с цинковым кольцом, и мы всего лишь квартал One Wing для авторов 2002 года, а не один раз и платите 100. NS равен ро по умолчанию сам. Итак, первая вторая, и мы закончили, мы собираемся изучить четвертую. Сегодня сам 84 мы делаем, мы должны знать, что исполнитель тепла один. Это сама молекула. Это значит, что когда ТВ так за место. Гидроксид аммония компания аминов и чистой для водорода урологии просто ждать использования гидроксида аудио сульфат аммония аммиака то же самое, что аммиак означает и как для ОК. Что касается so4 Players, пусть гидроксид из 70 будет взят дважды, чтобы он обогатился на рекордной ноге. Можем ли мы поставить баланс одной ногой тогда? Мы пойдем сразу и встретимся здесь. Вы должны сконцентрировать баланс преступника здесь. У нас есть один общий здесь. Нас учат молекулам аммиака. Итак, чтобы увеличить еще один здесь. Итак, когда я увеличил молекулы аммиака до молекул аммиака, мы получили гидроксиды гидропса, и он также попал в топ-сайты.
Итак, помощник по управлению дачами. С Фотоном покончено? Итак, я думаю, это то, что мы движемся, чтобы удержать человека, которому вы должны следовать, чтобы сбалансировать химическое уравнение в первую очередь. Мы должны мы должны я беспокоиться о калориях Чанг. Что это за форма молекулы условий или это молекула из гидроксида аммония Лос-Анджелеса, это вы все должны знать, тогда вы можете сделать это легко.
Это сама молекула. Это значит, что когда ТВ так за место. Гидроксид аммония компания аминов и чистой для водорода урологии просто ждать использования гидроксида аудио сульфат аммония аммиака то же самое, что аммиак означает и как для ОК. Что касается so4 Players, пусть гидроксид из 70 будет взят дважды, чтобы он обогатился на рекордной ноге. Можем ли мы поставить баланс одной ногой тогда? Мы пойдем сразу и встретимся здесь. Вы должны сконцентрировать баланс преступника здесь. У нас есть один общий здесь. Нас учат молекулам аммиака. Итак, чтобы увеличить еще один здесь. Итак, когда я увеличил молекулы аммиака до молекул аммиака, мы получили гидроксиды гидропса, и он также попал в топ-сайты.
Итак, помощник по управлению дачами. С Фотоном покончено? Итак, я думаю, это то, что мы движемся, чтобы удержать человека, которому вы должны следовать, чтобы сбалансировать химическое уравнение в первую очередь. Мы должны мы должны я беспокоиться о калориях Чанг. Что это за форма молекулы условий или это молекула из гидроксида аммония Лос-Анджелеса, это вы все должны знать, тогда вы можете сделать это легко. Просто примите заезд или поворот, и тогда вы сможете легко следовать за ним. Я надеюсь, что вы понимаете это видео. Спасибо за просмотр этого видео.
Просто примите заезд или поворот, и тогда вы сможете легко следовать за ним. Я надеюсь, что вы понимаете это видео. Спасибо за просмотр этого видео.
Связанные вопросы
Q1) Объясните термин «символ». Объясните, почему символ кальция — «Ca», а меди — «Cu».
Q2) Дайте определение термину «валентность». Что касается воды и аммиака как соединений соответственно, укажите…
Q3) Объясните термин «переменная валентность». Медь, имеющая электронную конфигурацию [[2,8,18,1]], проявляет…
Q4) Укажите валентность следующих металлических элементов: (a) калий (b) натрий (c) кальций (d) M…
Q4) Некоторые металлы обладают переменной валентностью, включая валентность: 1+, 2+, 3+ и 4+. Укажите В…
Укажите В…
Q6) Укажите, какие из приведенных ниже ионов или радикалов неметаллических элементов проявляют ценность…
Фейсбук WhatsApp
Копировать ссылку
Было ли это полезно?
Упражнения
Упражнения
Вопросы объективного типа
Главы
Материя
Физические и химические изменения
Элементы, соединения и смеси
Атомная структура
Язык химии
Химические реакции
Водород
Вода
Углерод и его соединения
Курсы
Быстрые ссылки
Условия и политика
Условия и политика
2022 © Quality Tutorials Pvt Ltd Все права защищены реакции — Уравновешивание окислительно-восстановительных реакций
Во многих важных химических реакциях электроны передаются от атома к атому. Такие реакции называются либо окислительно-восстановительными реакциями , либо окислительно-восстановительными реакциями .
Многие важные химические реакции включают окисление и восстановление. Фактически, большинство реакций, используемых для производства энергии, являются окислительно-восстановительными реакциями. У живых организмов окисление сахаров, жиров и белков обеспечивает энергию, необходимую для жизни. Электрический ток от аккумуляторов, питающих компьютеры и сотовые телефоны, генерируется в результате окислительно-восстановительных реакций.
Одной из наиболее известных окислительно-восстановительных реакций является коррозия металла. Коррозия — это превращение металла в соединение металла в результате реакции между металлом и некоторым веществом в его среде. Когда металл подвергается коррозии, каждый атом металла теряет электроны и образуется катион, который может соединяться с анионом, образуя ионное соединение.
Такие реакции называются либо окислительно-восстановительными реакциями , либо окислительно-восстановительными реакциями .
Многие важные химические реакции включают окисление и восстановление. Фактически, большинство реакций, используемых для производства энергии, являются окислительно-восстановительными реакциями. У живых организмов окисление сахаров, жиров и белков обеспечивает энергию, необходимую для жизни. Электрический ток от аккумуляторов, питающих компьютеры и сотовые телефоны, генерируется в результате окислительно-восстановительных реакций.
Одной из наиболее известных окислительно-восстановительных реакций является коррозия металла. Коррозия — это превращение металла в соединение металла в результате реакции между металлом и некоторым веществом в его среде. Когда металл подвергается коррозии, каждый атом металла теряет электроны и образуется катион, который может соединяться с анионом, образуя ионное соединение.
Блестящая металлическая поверхность кальция тускнеет в виде форм CaO:
2Ca (т) + O2 (г) → 2 CaO (т)
В приведенной выше реакции Ca окисляется до Ca+2 и O2, которые становится нейтральным, становится О-2 восстанавливается.
На самом деле старое определение окисления и восстановления было следующим:
Окисление — это реакция элемента с кислородом (O2) с образованием кислородсодержащего соединения, а восстановление — это удаление кислорода из соединения
Например:
C + O2 → CO2 (окисление, в сочетании с O)
Zno + C → Zn + CO (снижение, потеря O)
Также
называется окисление. удаление водорода из соединения и восстановление реакции с (h3) с образованием водородсодержащего соединения
переход от одного атома к другому. Тот факт, что первыми окислительно-восстановительными реакциями, изученными химиками, были реакции с О2, дал этому процессу название окисление.
Однако существуют и другие реакции, в которых электрон(ы) переносится (реакция является окислительно-восстановительной), но в реагентах или продуктах нет O2 или h3 (рис. I.2).
Например,
Более общее определение для окисления и уменьшения было предложено включать реакции, такие как на фиг. И.2, где O2 OR OR или SUTE h3 не является реагентом или продуктом.
И.2, где O2 OR OR или SUTE h3 не является реагентом или продуктом.
Окислением называется потеря электронов элементом или соединением
Восстановлением называется приобретением электронов элементом или соединением
Однако существуют реакции, в которых не происходит полного переноса электрона s) от одного элемента к другому (как в случае Na и Cl, рис. I.2), а частичный перенос электронов на более электроотрицательный элемент. Такая реакция идет между Н2 и Вг2 (рис. I.1). Связь, образующаяся между атомами H и Br, представляет собой полярную связь с частичным отрицательным зарядом на атомах Br и частичным положительным зарядом на атомах H (рис. I.3)
Поскольку реакции Na(s) и Cl(g) и реакции h3(g) и Br2(g) очень похожи, химики расширили определение окислительно-восстановительных реакций, включив в них частичные реакции. а также полный перенос электронов.
Окисление определяется как полная или частичная потеря электронов элементом или соединением
Восстановление определяется как полное или частичное приобретение электронов элементом или соединением
Атом Na (рис. I.2) при взаимодействии с Cl2 окисляется до Na+, а атом Cl восстанавливается. Поскольку атом Na делает возможным восстановление атома Cl, он называется восстановителем .
I.2) при взаимодействии с Cl2 окисляется до Na+, а атом Cl восстанавливается. Поскольку атом Na делает возможным восстановление атома Cl, он называется восстановителем .
Атом Cl (рис. I.2) при взаимодействии с Na восстанавливается до Cl-1. а атом Na окисляется. Поскольку атом Cl делает возможным окисление атома Na, он называется окислителем .
Однако простое считывание результатов химической реакции не всегда говорит нам о том, произошло ли окисление или восстановление. Химики разработали числовую систему, помогающую идентифицировать реакцию как окислительно-восстановительную. Первым шагом в этой системе является присвоение числа, называемого 9.0081 степени окисления для каждого атома в реакции. Концепция степеней окисления (также называемых степенями окисления) была разработана как способ отслеживания электронов, полученных восстанавливаемым веществом, и электронов, потерянных окисляемым веществом.
Общие этапы присвоения степеней окисления атомам в молекуле или ионе следующие:
- Степень окисления для каждого атома в чистом элементе равна нулю
- Степень окисления одноатомного иона равна его заряду
- Когда атомы H объединяются с неметаллами, их степень окисления равна +1 (т.
 е. ΗCl, Nh4, h3O, Ch5…). Когда атомы H соединяются с металлами, их степень окисления равна -1 (т.е. NaH) .
е. ΗCl, Nh4, h3O, Ch5…). Когда атомы H соединяются с металлами, их степень окисления равна -1 (т.е. NaH) . - Степень окисления O обычно равна -2 (т.е. CO, CO2, SO2). Основное исключение составляют пероксиды со степенью окисления -1 (т.е. Н2О2) и OF2 со степенью окисления +2
- Когда атомы фтора соединяются с атомами других элементов, их степень окисления составляет -1
Если формула соединения содержит один элемент, для которого степень окисления не может быть присвоена с помощью вышеуказанных шагов, степень окисления рассчитывается следующим образом:
- Сумма степеней окисления всех атомов в нейтральном соединении равна нулю.
- Сумма степеней окисления атомов в многоатомном ионе равна общему заряду иона
Используя концепцию степени окисления, было предложено новое определение окисления и восстановления:
Окисление – это реакция, при которой происходит увеличение степени окисления элемента
Восстановление – это реакция, при которой происходит уменьшение степени окисления элемента Рассчитайте степень окисления атомов в: α) CO 2 b) SF 6 α) Шаг 1 : Найдите наиболее электроотрицательный атом Самый электроотрицательный атом в CO 2 — это атом O 2 и поэтому степень окисления равна -2 Этап 3 : Необходимо рассчитать неизвестные степени окисления. Степень окисления C в CO 2 неизвестна, предположим, что она равна x Тогда, поскольку CO 2 нейтрален, сумма степеней окисления должна быть равна 0 CO 2 x + 2 * (-2) = x – 4 = 0 x = 4 Следовательно, степень окисления C в CO 2 равна +4
Шаг 1 : Найдите самый электроотрицательный атом
Самый электроотрицательный атом в SF 6 это атом F
Стадия 2 : Степень окисления наиболее электроотрицательного атома равна заряду его иона Этап 3 : Необходимо рассчитать неизвестные степени окисления.
Степень окисления S в SF 6 неизвестна и предположим, что она равна x
Тогда, поскольку SF 6 является нейтральным, сумма степеней окисления должна быть равна 0
SF 6
x + 6 * (-1) = x – 6 = 0
x = 6
Relevant Posts — Relevant Videos
youtube.com/embed/ijn8_Mq1nPA?list=PLGEE3kLOMCp51SiThFCEIRr0Zlhpu7aU1″ frameborder=»0″ allowfullscreen=»»>
References
Key Terms
oxidation, reduction , redox , oxidation number , балансировка окислительно-восстановительных реакций,
Балансировка окислительно-восстановительных реакций
Цели обучения
- Научиться уравновешивать простые окислительно-восстановительные реакции путем проверки.
- Научитесь уравновешивать сложные окислительно-восстановительные реакции методом половинной реакции.
- Используйте растворитель или его части в качестве реагента или продукта для уравновешивания окислительно-восстановительной реакции.
Уравновешивание простых окислительно-восстановительных реакций может быть простым вопросом перехода от продуктов к реагентам. Например, в окислительно-восстановительной реакции Na и Cl 2 :
Например, в окислительно-восстановительной реакции Na и Cl 2 :
Na + Cl 2 → NaCl
сразу должно быть понятно, что атомы Cl не уравновешены. Мы можем это исправить, поставив перед произведением коэффициент 2:
Na + Cl 2 → 2NaCl
Однако теперь натрий несбалансирован. Это можно исправить, включив коэффициент 2 перед реагентом Na:
2Na + Cl 2 → 2NaCl
Теперь эта реакция уравновешена. Это было довольно просто; мы говорим, что мы в состоянии уравновесить реакцию по инспекции . Многие простые окислительно-восстановительные реакции можно сбалансировать путем проверки.
Пример 3
Сбалансируйте эту окислительно-восстановительную реакцию путем проверки.
SO 2 + O 2 → SO 3
Решение
В обеих частях уравнения имеется по одному атому S, поэтому содержание серы сбалансировано. Однако сторона реагента имеет четыре атома O, а сторона продукта — три. Очевидно, что нам нужно больше атомов O на стороне продукта, поэтому давайте начнем с включения коэффициента 2 в SO 3 :
Однако сторона реагента имеет четыре атома O, а сторона продукта — три. Очевидно, что нам нужно больше атомов O на стороне продукта, поэтому давайте начнем с включения коэффициента 2 в SO 3 :
SO 2 + O 2 → 2SO 3
Теперь это дает нам шесть атомов O на стороне продукта, а также вызывает дисбаланс атомов S. Мы можем сбалансировать оба элемента, добавив коэффициент 2 к SO 2 на стороне реагента:
2SO 2 + O 2 → 2SO 3
Это дает нам два атома S с обеих сторон и всего шесть атомов O с обеих сторон химического уравнения. Эта окислительно-восстановительная реакция теперь уравновешена.
Проверьте себя
Сбалансируйте эту окислительно-восстановительную реакцию путем проверки.
Al + O 2 → Al 2 O 3
Answer
4Al + 3O 2 → 2Al 2 O 3
The first thing you should do when encountering an unbalanced redox реакция состоит в том, чтобы попытаться сбалансировать его путем проверки.
Некоторые окислительно-восстановительные реакции нелегко сбалансировать путем проверки. Рассмотрим эту окислительно-восстановительную реакцию:
Al + Ag + → Al 3+ + Ag
На первый взгляд это уравнение кажется сбалансированным: с обеих сторон имеется по одному атому Ag и по одному атому Al с обеих сторон. Однако, если вы посмотрите на общий заряд с каждой стороны, вы увидите дисбаланс заряда: на стороне реагента общий заряд 1+, а на стороне продукта общий заряд 3+. Что-то не так с этим химическим уравнением; несмотря на равное количество атомов с каждой стороны, он не уравновешен.
Фундаментальным моментом окислительно-восстановительных реакций, который ранее не возникал, является то, что общее количество потерянных электронов должно равняться общему количеству приобретённых электронов , чтобы окислительно-восстановительная реакция была сбалансированной. Это не относится к реакции алюминия и серебра: атом Al теряет три электрона, чтобы стать ионом Al 3+ , в то время как ион Ag + получает только один электрон, чтобы стать элементарным серебром.
Чтобы сбалансировать это, мы запишем каждую реакцию окисления и восстановления отдельно, явно указав количество электронов в каждой. По отдельности реакции окисления и восстановления называются половинными реакциями. Отдельная реакция окисления или восстановления окислительно-восстановительной реакции. Затем мы будем брать кратные каждой реакции до тех пор, пока количество электронов на каждой стороне полностью не сократится, и объединять половинные реакции в общую реакцию, который затем должен быть уравновешен. Этот метод уравновешивания окислительно-восстановительных реакций называется методом половинных реакций. Метод уравновешивания окислительно-восстановительных реакций путем записи и уравновешивания отдельных полуреакций.. (Есть и другие способы уравновешивания окислительно-восстановительных реакций, но это единственный, который будет использоваться в этом тексте. Причина этого будет рассмотрена в главе 14 «Окисление и восстановление», разделе 14.3 «Применение окислительно-восстановительных реакций: гальванические элементы». )
)
В полуреакции окисления участвует алюминий, который окисляется:
Al → Al 3+
Эта полуреакция не полностью уравновешена, поскольку общие заряды на каждой стороне не равны. Когда атом Al окисляется до Al 3+ , он теряет три электрона. Мы можем явно записать эти электроны как произведения:
Al → Al 3+ + 3e −
Теперь эта полуреакция уравновешена — с точки зрения как атомов, так и зарядов.
В полуреакции восстановления участвует серебро:
Ag + → Ag
Общий заряд не сбалансирован с обеих сторон. Но мы можем исправить это, добавив один электрон со стороны реагента, потому что ион Ag + должен принять один электрон, чтобы стать нейтральным атомом Ag:
Ag + + e − → Ag
Эта полуреакция теперь также уравновешена.
При объединении двух полуреакций в сбалансированное химическое уравнение ключевым моментом является то, что общее количество электронов должно компенсировать , поэтому количество электронов, потерянных атомами, равно количеству электронов, полученных другими атомами. Для этого может потребоваться умножить одну или обе полуреакции на целое число, чтобы количество электронов с каждой стороны было равным. С тремя электронами в качестве продуктов и одним в качестве реагента наименьшее общее кратное этих двух чисел равно трем: мы можем использовать одну реакцию с алюминием, но должны взять в три раза больше реакции с серебром:
Аль → Аль 3+ + 3e − 3 × [Ag + + e — → Ag]
3 во второй реакции распространяется на все виды в реакции:
Al → Al 3+ + 3e − 3Ag + + 3e − → 3Ag
Теперь две полуреакции можно сложить так же, как два алгебраических уравнения, со стрелкой в качестве знака равенства. Одинаковые виды по разные стороны стрелки можно отменить:
Одинаковые виды по разные стороны стрелки можно отменить:
Al + 3Ag++ 3e-→Al3++ 3Ag + 3e-
Итоговая сбалансированная окислительно-восстановительная реакция выглядит следующим образом:
Al + 3Ag + → Al 3+ + 3Ag
В каждой части химического уравнения по-прежнему есть только один атом Al, но теперь есть три атома Ag, а общий заряд в каждой части уравнения одинаков (3+ для обеих сторон). Эта окислительно-восстановительная реакция сбалансирована. Использование метода половинной реакции потребовало больше усилий, чем проверка, но была получена правильная сбалансированная окислительно-восстановительная реакция.
Пример 4
Уравновесьте эту окислительно-восстановительную реакцию, используя метод полуреакции.
Fe 2+ + Cr → Fe + Cr 3+
Решение
Начнем с записи двух полуреакций. Хром окисляется, а железо восстанавливается:
Хром окисляется, а железо восстанавливается:
Cr → Cr 3+ окисление Fe 2+ → восстановление Fe
Затем мы включаем соответствующее количество электронов с правильной стороны, чтобы сбалансировать заряды для каждой реакции:
Cr → Cr 3+ + 3e − Fe 2+ + 2e − → Fe
В первой реакции участвуют три электрона, а во второй реакции участвуют два электрона. Наименьшее общее кратное этих двух чисел равно шести, поэтому, чтобы получить шесть электронов в каждой реакции, нам нужно удвоить первую реакцию и утроить вторую:
2 × [Cr → Cr 3+ + 3e − ] = 2Cr → 2Cr 3+ + 6e − 3 × [Fe 2+ + 2e — → Fe] = 3Fe 2+ + 6e — → 3Fe
Мы можем объединить две последние реакции, заметив, что электроны компенсируются:
2Cr + 3Fe2++ 6e−→2Cr3++ 3Fe + 6e−
Общая сбалансированная окислительно-восстановительная реакция
2Cr + 3Fe 2+ → 2Cr 3+ + 3Fe
Проверьте себя
Сбалансируйте эту окислительно-восстановительную реакцию, используя метод половинной реакции.
O 2– +F 2 → O 2 +F —
Ответ
2O 2– +2F 2 ° 2 +2F 2 ° 2 2 20 2
0 20 20 2 2 2 2 2 2 2 20 2 2 2 9. окислительно-восстановительные реакции протекают в водном растворе — в воде. Благодаря этому во многих случаях H 2 O или фрагмент молекулы H 2 O (в частности, H + или OH − ) могут участвовать в окислительно-восстановительной реакции. Таким образом, нам нужно научиться включать растворитель в сбалансированное окислительно-восстановительное уравнение.Рассмотрим следующую полуреакцию окисления в водном растворе, который имеет по одному атому Cr с каждой стороны:
Cr 3+ → CrO 4 −
Здесь атом Cr переходит из степени окисления +3 в +7. Для этого атом Cr должен потерять четыре электрона. Начнем с перечисления четырех электронов как произведений:
Для этого атом Cr должен потерять четыре электрона. Начнем с перечисления четырех электронов как произведений:
Cr 3+ → CrO 4 − + 4e −
Но откуда берутся атомы O? Они происходят из молекул воды или общего фрагмента молекулы воды, который содержит атом O: OH − ион. Когда мы уравновешиваем эту полуреакцию, мы должны свободно включать любой из этих видов в реакцию, чтобы сбалансировать элементы. Давайте использовать H 2 O для баланса атомов O; нам нужно включить четыре молекулы воды, чтобы сбалансировать четыре атома O в продуктах:
4H 2 O + Cr 3+ → CrO 4 − + 4e −
Это уравновешивает атомы O, но теперь вводит в реакцию водород. Мы можем сбалансировать атомы H, добавив H 9Ион 0320 +
, являющийся еще одним фрагментом молекулы воды. Нам нужно добавить восемь ионов H + в сторону продукта:4H 2 O + Cr 3+ → CrO 4 − + 4e − + 8H +
Атомы Cr сбалансированы, атомы H сбалансированы; если мы проверим общий заряд с обеих сторон химического уравнения, они будут одинаковыми (в данном случае 3+). Эта полуреакция теперь уравновешена, используя молекулы воды и части молекул воды в качестве реагентов и продуктов.
Эта полуреакция теперь уравновешена, используя молекулы воды и части молекул воды в качестве реагентов и продуктов.
Реакции восстановления можно уравновесить аналогичным образом. Когда полуреакции окисления и восстановления уравновешены по отдельности, их можно комбинировать так же, как и раньше: взяв кратное количество каждой полуреакции, необходимое для компенсации всех электронов. Другие виды, такие как H + , OH — и H 2 O , также могут быть исключены в окончательной сбалансированной реакции.
Если не указано иное, не имеет значения, добавляете ли вы H 2 O или OH — в качестве источника атомов O, хотя реакция может указывать кислый раствор или основной раствор как намек на то, какие виды следует использовать или какие виды следует избегать. Ионы OH — не очень распространены в кислых растворах, поэтому их следует избегать в таких обстоятельствах.
Пример 5
Сбалансируйте эту окислительно-восстановительную реакцию. Предположим базовое решение.
Предположим базовое решение.
MnO 2 + CrO 3 − → Mn + CrO 4 −
Решение
Мы начинаем с разделения процессов окисления и восстановления, чтобы мы могли сбалансировать каждую полуреакцию отдельно. Реакция окисления следующая:
CrO 3 − → CrO 4 −
Атом Cr переходит из степени окисления +5 в +7 и теряет в процессе два электрона. Мы добавляем эти два электрона к стороне продукта:
CrO 3 − → CrO 4 − + 2e −
Теперь мы должны сбалансировать атомы O. Поскольку раствор является основным, мы должны использовать OH − , а не H 2 O:
. OH − + CrO 3 − → CrO 4 − + 2e −
Мы ввели атомы H в составе реагентов; мы можем сбалансировать их, добавив H + в качестве продуктов:
OH − + CrO 3 − → CrO 4 − + 2e − + H +
Если мы проверим атомы и общий заряд с обеих сторон, мы увидим, что эта реакция сбалансирована. Однако, если реакция протекает в щелочном растворе, маловероятно, что ионы Н + будут присутствовать в количестве. Чтобы решить эту проблему, добавьте дополнительный ион OH − к каждой стороне уравнения:
Однако, если реакция протекает в щелочном растворе, маловероятно, что ионы Н + будут присутствовать в количестве. Чтобы решить эту проблему, добавьте дополнительный ион OH − к каждой стороне уравнения:
OH − + CrO 3 − +OH — → CRO 4 — +2E — +H + +OH —
.
. С правой стороны ионы H + и OH − можно сгруппировать в молекулу H 2 O:2OH − + CrO 3 − → CrO 4 − + 2e − + H 2 O
Это более подходящая форма для базового раствора.
Теперь уравновешиваем реакцию восстановления:
MnO 2 → Mn
Степень окисления атома Mn меняется с +4 до 0, что требует прироста четырех электронов:
4e − + MnO 2 → Mn
Затем уравновешиваем атомы O, а затем атомы H:
4e − + MnO 2 → Mn + 2OH − 2H + + 4e − + MnO 2 → Mn + 2OH −
Мы добавляем по два иона OH − с каждой стороны, чтобы устранить ион H + в реагентах; реагенты объединяются, образуя две молекулы воды, а количество ионов OH − в продукте увеличивается до четырех:
2H 2 O + 4e − + MnO 2 → Mn + 4OH −
Эта реакция сбалансирована для основного раствора.
Теперь объединим две уравновешенные полуреакции. В реакции окисления два электрона, в реакции восстановления четыре. Наименьшее общее кратное этих двух чисел равно четырем, поэтому умножаем реакцию окисления на 2, чтобы электроны уравновесились:
2 × [2OH − + CrO 3 − → CrO 4 − + 2e − + H 2 O] 2H 2 O + 4e − + MnO 2 → Mn + 4OH −
Объединение этих двух уравнений приводит к следующему уравнению:
4OH — +2CRO 3 — +2H 2 O +4E — +MNO 2 → 2CRO 4 → 322222222222292 +222 + 2 . 4OH − Четыре электрона компенсируются. 2CrO 3 − + MnO 2 → 2CrO 4 − + Mn , который является нашей последней сбалансированной окислительно-восстановительной реакцией. Проверь себя Сбалансируй эту окислительно-восстановительную реакцию. Предположим базовое решение. CL — +MNO 4 — → MNO 2 +CLO 3 — Ответ — .0320 −  То же самое делают две молекулы H 2 O и четыре иона OH − . Остается
То же самое делают две молекулы H 2 O и четыре иона OH − . Остается
Ключевые выводы
- Окислительно-восстановительные реакции можно уравновесить методом полуреакции.
- Растворитель может участвовать в окислительно-восстановительных реакциях; в водных растворах H 2 O, H + и OH — могут быть реагентами или продуктами.

Упражнения
Сбалансируйте эти окислительно-восстановительные реакции путем проверки.
- Na + F 2 → NaF
- Al 2 O 3 + H 2 → Al + H 2 O
Сбалансируйте эти окислительно-восстановительные реакции путем проверки.
- Fe 2 S 3 + O 2 → Fe 2 O 3 + S
- Cu 2 O + H 2 → Cu + H 2 О
Сбалансируйте эти окислительно-восстановительные реакции путем проверки.
- CH 4 + O 2 → CO 2 + H 2 O
- P 2 O 5 + Cl 2 → PCl 3 + O 2
Сбалансируйте эти окислительно-восстановительные реакции путем проверки.

- PbCl 2 + FeCl 3 → PbCl 4 + FeCl 2
- SO 2 + F 2 → SF 4 + OF 2
Сбалансируйте эти окислительно-восстановительные реакции методом половинной реакции.
- Ca + H + → Ca 2+ + H 2
- Сн 2+ → Sn + Sn 4+ (Подсказка: обе полуреакции начнутся с одним и тем же реагентом.)
Сбалансируйте эти окислительно-восстановительные реакции методом половинной реакции.
- Fe 3+ + Sn 2+ → Fe + Sn 4+
- Pb 2+ → Pb + Pb 4+ (Подсказка: обе полуреакции начнутся с одним и тем же реагентом.
 )
)
Сбалансируйте эти окислительно-восстановительные реакции методом половинной реакции.
- Na + Hg 2 Cl 2 → NaCl + Hg
- Al 2 O 3 + C → Al + CO 2
Сбалансируйте эти окислительно-восстановительные реакции методом половинной реакции.
- Бр − + I 2 → I − + Br 2
- CrCl 3 + F 2 → CrF 3 + Cl 2
Сбалансируйте эти окислительно-восстановительные реакции, происходящие в водном растворе. Используйте любые виды, полученные из воды, которые необходимы; может быть более одного правильного сбалансированного уравнения.

- Cu + NO 3 − → Cu 2+ + № 2
- Fe + MnO 4 − → Fe 3+ + Mn
Сбалансируйте эти окислительно-восстановительные реакции, происходящие в водном растворе. Используйте любые виды, полученные из воды, которые необходимы; может быть более одного правильного сбалансированного уравнения.
- CrO 3 + Ni 2+ → Cr 3+ + Ni 3+
- OsO 4 + C 2 H 4 → Os + CO 2
Сбалансируйте эти окислительно-восстановительные реакции, происходящие в водном растворе. Используйте любые виды, полученные из воды, которые необходимы; может быть более одного правильного сбалансированного уравнения.

- ClO − + Ti 2+ → Ti 4+ + Cl −
- БрО 3 − + Ag → Ag + + BrO 2
Сбалансируйте эти окислительно-восстановительные реакции, происходящие в водном растворе. Используйте любые виды, полученные из воды, которые необходимы; может быть более одного правильного сбалансированного уравнения.
- H 2 O 2 + NO → N 2 O 3 + H 2 O
- ВО 2 + + НО → V 3+ + НО 2
Объясните, почему это химическое уравнение не сбалансировано, и сбалансируйте его, если его можно сбалансировать.
Cr 2+ + Cl 2 → Cr 3+ + 2Cl −
Объясните, почему это уравнение не сбалансировано, и сбалансируйте его, если его можно сбалансировать.

O 2 + 2H 2 O + Br 2 → 4OH — + 2Br —
Ответы
- 2Na + F 2 → 2NaF
- Al 2 O 3 + 3H 2 → 2Al + 3H 2 O
- CH 4 + 2O 2 → CO 2 + 2H 2 O
- 2P 2 O 5 + 6Cl 2 → 4PCl 3 + 5O 2
- Ca + 2H + → Ca 2+ + H 2
- 2Sn 2+ → Sn + Sn 4+
- 2Na + Hg 2 Cl 2 → 2NaCl + 2Hg
- 2Al 2 O 3 + 3C → 4Al + 3CO 2
- 4H + + Cu + 2NO 3 − → Cu 2+ + 2NO 2 + 2H 2 O в кислом растворе; 2H 2 O + Cu + 2NO 3 − → Cu 2+ + 2NO 2 + 4OH − в основном растворе
- 24H + + 3MnO 4 − + 7Fe → 7Fe 3+ + 3Mn + 12H 2 O в кислом растворе; 12H 2 O + 3MnO 4 − + 7Fe → 7Fe 3+ + 3Mn + 24OH − в основном растворе
- 2H + + ClO − + Ti 2+ → Cl − + H 2 O + Ti 4+ в кислом растворе; H 2 O + ClO − + Ti 2+ → Cl − + Ti 4+ + 2OH − в основном растворе
- 2ч + + BrO 3 − + Ag → BrO 2 + H 2 O + Ag + в кислом растворе; H 2 O + BrO 3 − + Ag → BrO 2 + Ag + + 2OH − в основном растворе
Заряды не сбалансированы должным образом.
 Правильное сбалансированное уравнение: 2Cr 2+ + Cl 2 → 2Cr 3+ + 2Cl − .
Правильное сбалансированное уравнение: 2Cr 2+ + Cl 2 → 2Cr 3+ + 2Cl − .
химическая реакция | Определение, уравнения, примеры и типы
сжигание
Посмотреть все СМИ
- Ключевые люди:
- Антуан Лавуазье Клод-Луи Бертолле Вильгельм Оствальд Анри-Луи Ле Шателье Сэр Дерек Х. Р. Бартон
- Похожие темы:
- кислотно-основная реакция механизм реакции окислительно-восстановительная реакция ионообменная реакция фотохимическая реакция
Просмотреть весь связанный контент →
Популярные вопросы
Каковы основы химических реакций?
- Химическая реакция – это процесс, в котором одно или несколько веществ, также называемых реагентами, превращаются в одно или несколько различных веществ, известных как продукты.
 Вещества – это либо химические элементы, либо соединения.
Вещества – это либо химические элементы, либо соединения. - Химическая реакция перестраивает составляющие атомы реагентов для создания различных веществ в качестве продуктов. Свойства продуктов отличаются от свойств реагентов.
- Химические реакции отличаются от физических изменений, которые включают изменения состояния, такие как таяние льда в воду и испарение воды в пар. Если произойдет физическое изменение, физические свойства вещества изменятся, но его химическая идентичность останется прежней.
Подробнее ниже: Основные понятия о химических реакциях
химический элемент
Узнайте об этом типе вещества, которое не может быть разложено на более простые вещества с помощью обычных химических процессов.химическое соединение
Узнайте об этом типе вещества, которое можно разложить на более простые вещества с помощью обычных химических процессов.Что происходит с химическими связями, когда происходит химическая реакция?
Согласно современному взгляду на химические реакции, связи между атомами в реагентах должны быть разрушены, а атомы или фрагменты молекул снова собираются в продукты путем образования новых связей. Энергия поглощается для разрыва связей, а энергия выделяется по мере образования связей. В некоторых реакциях энергия, необходимая для разрыва связей, больше энергии, выделяемой при образовании новых связей, и конечным результатом является поглощение энергии. Следовательно, в реакции могут образовываться различные типы связей. Кислотно-основная реакция Льюиса, например, включает образование ковалентной связи между основанием Льюиса, веществом, которое поставляет электронную пару, и кислотой Льюиса, веществом, которое может принимать электронную пару. Аммиак является примером основания Льюиса. Пара электронов, расположенных на атоме азота, может быть использована для образования химической связи с кислотой Льюиса.
Энергия поглощается для разрыва связей, а энергия выделяется по мере образования связей. В некоторых реакциях энергия, необходимая для разрыва связей, больше энергии, выделяемой при образовании новых связей, и конечным результатом является поглощение энергии. Следовательно, в реакции могут образовываться различные типы связей. Кислотно-основная реакция Льюиса, например, включает образование ковалентной связи между основанием Льюиса, веществом, которое поставляет электронную пару, и кислотой Льюиса, веществом, которое может принимать электронную пару. Аммиак является примером основания Льюиса. Пара электронов, расположенных на атоме азота, может быть использована для образования химической связи с кислотой Льюиса.
химическая связь
Узнайте о различных типах химической связи.кислотно-основная реакция: реакции кислот Льюиса
Узнайте о кислотно-основных реакциях Льюиса.Как классифицируются химические реакции?
Химики классифицируют химические реакции несколькими способами: по типу продукта, по типу реагентов, по результату реакции и по механизму реакции. Часто данную реакцию можно отнести к двум или даже трем категориям, включая реакции газообразования и реакции осаждения. Многие реакции производят газ, такой как двуокись углерода, сероводород, аммиак или двуокись серы. Подъем теста для торта вызван газообразующей реакцией между кислотой и пищевой содой (гидрокарбонатом натрия). Классификация по типам реагентов включает кислотно-основные реакции и окислительно-восстановительные реакции, которые включают перенос одного или нескольких электронов от восстановителя к окислителю. Примеры классификации по результату реакции включают реакции разложения, полимеризации, замещения, отщепления и присоединения. Цепные реакции и реакции фотолиза являются примерами классификации по механизму реакции, которая дает подробную информацию о том, как атомы перетасовываются и повторно собираются при образовании продуктов.
Часто данную реакцию можно отнести к двум или даже трем категориям, включая реакции газообразования и реакции осаждения. Многие реакции производят газ, такой как двуокись углерода, сероводород, аммиак или двуокись серы. Подъем теста для торта вызван газообразующей реакцией между кислотой и пищевой содой (гидрокарбонатом натрия). Классификация по типам реагентов включает кислотно-основные реакции и окислительно-восстановительные реакции, которые включают перенос одного или нескольких электронов от восстановителя к окислителю. Примеры классификации по результату реакции включают реакции разложения, полимеризации, замещения, отщепления и присоединения. Цепные реакции и реакции фотолиза являются примерами классификации по механизму реакции, которая дает подробную информацию о том, как атомы перетасовываются и повторно собираются при образовании продуктов.
Подробнее читайте ниже: Классификация химических реакций
кислотно-щелочные реакции
Узнать о кислотно-щелочных реакциях.
окислительно-восстановительная реакция
Узнайте об окислительно-восстановительных или окислительно-восстановительных реакциях.цепная реакция
Узнайте о цепных или самоподдерживающихся реакциях.Сводка
Прочтите краткий обзор этой темы
химическая реакция , процесс, в котором одно или несколько веществ, реагентов, превращаются в одно или несколько различных веществ, продуктов. Вещества – это либо химические элементы, либо соединения. Химическая реакция перестраивает составляющие атомы реагентов для создания различных веществ в качестве продуктов.
Химические реакции являются неотъемлемой частью технологии, культуры и самой жизни. Сжигание топлива, плавка железа, изготовление стекла и гончарных изделий, пивоварение, производство вина и сыра — вот лишь некоторые примеры деятельности, включающей химические реакции, которые были известны и использовались на протяжении тысячелетий. Химические реакции изобилуют в геологии Земли, в атмосфере и океанах, а также в огромном количестве сложных процессов, происходящих во всех живых системах.
Химические реакции следует отличать от физических изменений. Физические изменения включают изменения состояния, такие как таяние льда в воду и испарение воды в пар. Если произойдет физическое изменение, физические свойства вещества изменятся, но его химическая идентичность останется прежней. В любом физическом состоянии вода (H 2 O) — одно и то же соединение, каждая молекула которого состоит из двух атомов водорода и одного атома кислорода. Однако если вода в виде льда, жидкости или пара встречается с металлическим натрием (Na), атомы перераспределяются с образованием новых веществ: молекулярного водорода (H 2 ) и гидроксида натрия (NaOH). Таким образом, мы знаем, что произошло химическое изменение или реакция.
Исторический обзор
Концепция химической реакции возникла примерно 250 лет назад. Он берет свое начало в ранних экспериментах, которые классифицировали вещества как элементы и соединения, а также в теориях, объясняющих эти процессы. Развитие концепции химической реакции сыграло главную роль в определении науки химии, какой она известна сегодня.
Развитие концепции химической реакции сыграло главную роль в определении науки химии, какой она известна сегодня.
Викторина «Британника»
Химия: плюсы и минусы
Возможно, вы знаете, что элементы составляют воздух, которым мы дышим, и воду, которую мы пьем, но знаете ли вы о них больше? Какой элемент почти так же легок, как водород? Что вы называете смесью двух химических элементов? Узнайте ответы в этом тесте.
Первые серьезные исследования в этой области были посвящены газам. Особое значение имело определение кислорода в 18 веке шведским химиком Карлом Вильгельмом Шееле и английским священником Джозефом Пристли. Влияние французского химика Антуана-Лорана Лавуазье было особенно заметным, поскольку его идеи подтвердили важность количественных измерений химических процессов. В своей книге Traité élémentaire de chimie (1789; Elementary Treatise on Chemistry ), Лавуазье выделил 33 «элемента» — субстанции, не разделенные на более простые сущности. Среди своих многочисленных открытий Лавуазье точно измерил вес, прибавляемый при окислении элементов, и приписал результат соединению элемента с кислородом. Концепция химических реакций с участием комбинации элементов ясно возникла из его работ, и его подход побудил других заняться экспериментальной химией как количественной наукой.
Среди своих многочисленных открытий Лавуазье точно измерил вес, прибавляемый при окислении элементов, и приписал результат соединению элемента с кислородом. Концепция химических реакций с участием комбинации элементов ясно возникла из его работ, и его подход побудил других заняться экспериментальной химией как количественной наукой.
Другим событием исторического значения, касающимся химических реакций, было развитие атомной теории. Большая заслуга в этом принадлежит английскому химику Джону Дальтону, постулировавшему свою атомную теорию в начале XIX века. Дальтон утверждал, что материя состоит из маленьких неделимых частиц, что частицы или атомы каждого элемента уникальны и что химические реакции связаны с перестройкой атомов с образованием новых веществ. Этот взгляд на химические реакции точно определяет текущий предмет. Теория Дальтона послужила основой для понимания результатов более ранних экспериментаторов, в том числе закона сохранения материи (материя не создается и не разрушается) и закона постоянного состава (все образцы вещества имеют одинаковый элементный состав).
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подписаться сейчас
Таким образом, эксперимент и теория, два краеугольных камня химической науки в современном мире, вместе определили концепцию химических реакций. Сегодня экспериментальная химия дает бесчисленное множество примеров, а теоретическая химия позволяет понять их значение.
Основные понятия о химических реакциях
Создавая новое вещество из других веществ, химики говорят, что либо проводят синтез, либо синтезируют новый материал. Реагенты превращаются в продукты, и процесс символизируется химическим уравнением. Например, железо (Fe) и сера (S) объединяются, образуя сульфид железа (FeS). Fe(s) + S(s) → FeS(s) Знак плюс указывает на то, что железо реагирует с серой. Стрелка означает, что реакция «образует» или «дает» сульфид железа, продукт. Вещественное состояние реагентов и продуктов обозначается символами (s) для твердых тел, (l) для жидкостей и (g) для газов.
Стехиометрия и уравновешивающие реакции — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 240
Стехиометрия — это раздел химии, который включает использование соотношений между реагентами и/или продуктами в химической реакции для определения желаемых количественных данных. По-гречески стойхеин означает элемент, а метрон означает меру, поэтому стехиометрия в буквальном переводе означает меру элементов. Чтобы использовать стехиометрию для выполнения расчетов химических реакций, важно сначала понять отношения, которые существуют между продуктами и реагентами, и почему они существуют, что требует понимания того, как сбалансировать реакции.
Балансировка
В химии химические реакции часто записывают в виде уравнений с использованием химических символов. Реагенты отображаются в левой части уравнения, а продукты — в правой, с разделением одинарной или двойной стрелкой, обозначающей направление реакции. Значение одинарной и двойной стрелки важно при обсуждении констант растворимости, но мы не будем вдаваться в подробности в этом модуле. Чтобы сбалансировать уравнение, необходимо, чтобы в левой части уравнения было такое же количество атомов, как и в правой. Это можно сделать, подняв коэффициенты.
Реагенты для продуктов
Химическое уравнение похоже на рецепт реакции, поэтому оно отображает все ингредиенты или условия химической реакции. Он включает элементы, молекулы или ионы в реагентах и продуктах, а также их состояния и пропорцию того, сколько каждой частицы реагирует или образуется по отношению друг к другу через стехиометрический коэффициент. Следующее уравнение демонстрирует типичный формат химического уравнения:
\[\ce{2 Na(s) + 2HCl(aq) \rightarrow 2NaCl(aq) + h3(g)} \nonumber\]
В приведенном выше уравнении элементы, участвующие в реакции, представлены их химическими символами. Основываясь на Законе сохранения массы, который гласит, что материя не создается и не разрушается в результате химической реакции, каждая химическая реакция содержит одни и те же элементы в своих реагентах и продуктах, хотя элементы, с которыми они соединяются, часто меняются в ходе реакции. В этой реакции натрий (\(Na\)), водород (\(H\)) и хлорид (\(Cl\)) являются элементами, присутствующими в обоих реагентах, поэтому на основании закона сохранения массы они также присутствуют на стороне произведения уравнений. Отображение каждого элемента важно при использовании химического уравнения для преобразования между элементами.
Основываясь на Законе сохранения массы, который гласит, что материя не создается и не разрушается в результате химической реакции, каждая химическая реакция содержит одни и те же элементы в своих реагентах и продуктах, хотя элементы, с которыми они соединяются, часто меняются в ходе реакции. В этой реакции натрий (\(Na\)), водород (\(H\)) и хлорид (\(Cl\)) являются элементами, присутствующими в обоих реагентах, поэтому на основании закона сохранения массы они также присутствуют на стороне произведения уравнений. Отображение каждого элемента важно при использовании химического уравнения для преобразования между элементами.
Стехиометрические коэффициенты
В сбалансированной реакции обе части уравнения содержат одинаковое количество элементов. Стехиометрический коэффициент — это число, написанное перед атомами, ионами и молекулами в химической реакции, чтобы сбалансировать количество каждого элемента как в реагенте, так и в продукте уравнения. Хотя стехиометрические коэффициенты могут быть дробными, часто используются целые числа, и они часто предпочтительнее. Эти стехиометрические коэффициенты полезны, поскольку они устанавливают молярное соотношение между реагентами и продуктами. В сбалансированном уравнении:
Эти стехиометрические коэффициенты полезны, поскольку они устанавливают молярное соотношение между реагентами и продуктами. В сбалансированном уравнении:
\[\ce{2 Na(s) + 2HCl(aq) \rightarrow 2NaCl(aq) + h3(g)} \nonumber\]
мы можем определить, что 2 моля \(HCl\) будут реагировать с 2 моля \(Na_{(s)}\) с образованием 2 молей \(NaCl_{(aq)}\) и 1 моля \(H_{2(g)}\). Если мы знаем, сколько молей \(Na\) вступило в реакцию, мы можем использовать отношение 2 молей \(NaCl\) к 2 молям Na, чтобы определить, сколько молей \(NaCl\) было произведено, либо мы можем использовать отношение 1 моля \(H_2\) к 2 молям \(Na\) для преобразования в \(NaCl\). Это известно как фактор коэффициента. Сбалансированное уравнение позволяет преобразовать информацию об изменении одного реагента или продукта в количественные данные о другом реагенте или продукте. Понимание этого важно для решения стехиометрических задач.
Пример 1
Гидроксид свинца (IV) и серная кислота реагируют, как показано ниже. Уравновесить реакцию.
Уравновесить реакцию.
\[\ce{Pb(OH)4 + h3SO4 \rightarrow Pb(SO4)2 +h3O} \номер\]
Раствор
Начните с подсчета количества атомов каждого элемента.
НЕСБАЛАНСИРОВАННЫЙ
Элемент | Реагент (число атомов) | Продукт (число атомов) |
|---|---|---|
Пб | 1 | 1 |
О | 8 | г.9 |
Х | 6 | 2 |
С | 1 | 2 |
Реакция не сбалансирована; реакция имеет 16 атомов реагентов и только 14 атомов продукта и не подчиняется принципу сохранения массы. Чтобы сделать уравнение сбалансированным, необходимо добавить стехиометрические коэффициенты. В этом примере на стороне реагента присутствует только один атом серы, поэтому перед \(H_2SO_4\) следует добавить коэффициент 2, чтобы получить одинаковое количество серы в обеих частях уравнения. Так как на стороне реагента 12 кислорода и только 9со стороны продукта следует добавить коэффициент 4 перед \(H_2O\), если имеется дефицит кислорода. Подсчитайте количество элементов, присутствующих в настоящее время по обе стороны уравнения. Поскольку числа одинаковы, уравнение теперь сбалансировано.
Так как на стороне реагента 12 кислорода и только 9со стороны продукта следует добавить коэффициент 4 перед \(H_2O\), если имеется дефицит кислорода. Подсчитайте количество элементов, присутствующих в настоящее время по обе стороны уравнения. Поскольку числа одинаковы, уравнение теперь сбалансировано.
\[\ce{ Pb(OH)4 + 2 h3SO4 \rightarrow Pb(SO4)2 + 4h3O} \номер\]
СБАЛАНСИРОВАННЫЙ
Элемент | Реагент (число атомов) | Продукт (число атомов) |
|---|---|---|
Пб | 1 | 1 |
О | 12 | 12 |
Х | 8 | 8 |
С | 2 | 2 |
Уравновешивающие реакции включают в себя нахождение наименьших общих кратных между числом элементов, присутствующих в обеих частях уравнения. Как правило, при применении коэффициентов добавляйте коэффициенты к молекулам или непарным элементам в последнюю очередь.
Как правило, при применении коэффициентов добавляйте коэффициенты к молекулам или непарным элементам в последнюю очередь.
Сбалансированное уравнение в конечном счете должно удовлетворять двум условиям.
- Номера каждого элемента в левой и правой части уравнения должны быть равны.
- Заряд в обеих частях уравнения должен быть одинаковым. Особенно важно обращать внимание на заряд при балансировке окислительно-восстановительных реакций.
Стехиометрия и сбалансированные уравнения
В стехиометрии сбалансированные уравнения позволяют сравнивать различные элементы с помощью стехиометрического фактора , который обсуждался ранее. Это молярное соотношение между двумя факторами в химической реакции, определяемое через соотношение стехиометрических коэффициентов. Вот реальный пример, показывающий, как полезны стехиометрические факторы.
Пример 2
Имеется 12 приглашений на вечеринку и 20 марок. Каждое приглашение на вечеринку требует отправки 2 марок. Сколько приглашений на вечеринку можно отправить?
Сколько приглашений на вечеринку можно отправить?
Решение
Уравнение для этого можно записать как
\[\ce{I + 2S \rightarrow IS2}\nonumber\]
где
- \(I\) представляет приглашения,
- \(S\) представляет марки, а
- \(IS_2\) представляет собой отправленные партийные приглашения, состоящие из одного приглашения и двух штампов.
Исходя из этого, имеем соотношение 2 штампа к 1 отправленному приглашению, основанное на сбалансированном уравнении.
Приглашения Штампы Приглашения на вечеринку отправлены
В этом примере все реагенты (марки и приглашения) израсходованы? Нет, и это обычно происходит с химическими реакциями. Часто наблюдается избыток одного из реагентов. Лимитирующий реагент, тот, который заканчивается первым, препятствует продолжению реакции и определяет максимальное количество продукта, которое может образоваться.
Пример 3
Какой реагент является лимитирующим в этом примере?
Решение
Марки, потому что их хватило только на рассылку приглашений, тогда как приглашений хватило на 12 полных приглашений на вечеринку. Помимо простого взгляда на проблему, ее можно решить, используя стехиометрические коэффициенты.
Помимо простого взгляда на проблему, ее можно решить, используя стехиометрические коэффициенты.
12 I x (1IS 2 /1I) = 12 IS 2 возможно
20 S x (1IS 2 /2S) = 10 IS 2 при отсутствии ограничения возможно
3 90 соотношение всех реагентов, вызывающее их одновременное исчерпание, известно как стехиометрические пропорции .
Типы реакций
Существует 6 основных типов реакций.
- Горение : Горение – это образование CO 2 и H 2 O в результате реакции химического вещества и O 2
- Комбинация (синтез) : Комбинация представляет собой добавление 2 или более простых реагентов с образованием сложного продукта.
- Разложение: Разложение — это расщепление сложных реагентов на более простые продукты.
- Одиночное смещение : Однократное смещение — это когда элемент одного реагента переключается с элементом другого с образованием двух новых реагентов.

- Двойное смещение: Двойное смещение — это когда два элемента одного реагента меняются местами с двумя элементами другого, образуя два новых реагента.
- Кислотно-основные: Кислотно-основные реакции – это когда два реагента образуют соли и воду.
Молярная масса
Прежде чем применять стехиометрические коэффициенты к химическим уравнениям, вам необходимо понять молекулярную массу. Молярная масса — это полезное химическое соотношение между массой и молями. Атомная масса каждого отдельного элемента, указанная в периодической таблице, установила это соотношение для атомов или ионов. Для соединений или молекул вы должны взять сумму атомной массы, умноженной на число каждого атома, чтобы определить молярную массу
Пример 4
Какова молярная масса H 2 О?
Раствор
\[\text{Молярная масса} = 2 \times (1,00794\; г/моль) + 1 \times (15,9994\; г/моль) = 18,01528\; г/моль]
Используя молярную массу и коэффициенты, можно преобразовать массу реагентов в массу продуктов или наоборот.
Пример 5: Горение пропана
Пропан (\(\ce{C_3H_8}\)) горит в этой реакции: Сгорело 200 г пропана, сколько г \(H_2O\) образовалось?
Решение
Шаги для получения этого ответа: Поскольку вы не можете вычислить из граммов реагента в граммы продуктов, вы должны преобразовать граммы \(C_3H_8\) в моли \(C_3H_8\), а затем из молей \( C_3H_8\) в моли \(H_2O\). Затем переведите моли \(H_2O\) в граммы \(H_2O\).
- Этап 1: 200 г \(C_3H_8\) равно 4,54 моль \(C_3H_8\) .
- Шаг 2: Так как отношение \(H_2O\) к \(C_3H_8\) составляет 4:1, на каждые 4,54 моль \(C_3H_8\) приходится 18,18 моль \(H_2O\).
- Шаг 3: Переведите 18,18 моль \(H_2O\) в г \(H_2O\). 18,18 моль \(H_2O\) равно 327,27 г \(H_2O\).
Варианты стехиометрических уравнений
Почти каждое количественное отношение можно преобразовать в отношение, которое может быть полезно при анализе данных.
Плотность
Плотность (\(\rho\)) рассчитывается как масса/объем. Это соотношение может быть полезно при определении объема раствора по заданной массе или при нахождении массы по заданному объему. В последнем случае будет использоваться обратная зависимость.
Это соотношение может быть полезно при определении объема раствора по заданной массе или при нахождении массы по заданному объему. В последнем случае будет использоваться обратная зависимость.
Объем x (масса/объем) = масса
Масса x (объем/масса) = объем
Масса в процентах
Проценты также устанавливают взаимосвязь. Процент массы показывает, сколько граммов смеси приходится на определенный элемент или молекулу. Процент X% означает, что из каждых 100 граммов смеси X граммов приходится на указанный элемент или соединение. Это полезно при определении массы желаемого вещества в молекуле.
Пример 6
Вещество содержит 5% углерода по массе. Если общая масса вещества 10 граммов, какова масса углерода в пробе? Сколько молей углерода?
Раствор
10 г образца x (5 г углерода/100 г образца) = 0,5 г углерода
0,5 г углерода x (1 моль углерода/12,011 г углерода) = 0,0416 моль углерода моль/л) устанавливает связь между молями и литрами. Зная объем и молярность, можно рассчитать моль или использовать моли и молярность для расчета объема. Это полезно в химических уравнениях и разбавлениях.
Зная объем и молярность, можно рассчитать моль или использовать моли и молярность для расчета объема. Это полезно в химических уравнениях и разбавлениях.
Пример 7
Сколько 5 М исходного раствора необходимо для приготовления 100 мл 2 М раствора?
Раствор
100 мл разбавленного раствора (1 л/1000 мл)(2 моль/1 л раствора)(1 л исходного раствора/5 моль раствора)(1000 мл исходного раствора/1 л исходного раствора) = 40 мл исходного раствора решение.
Эти отношения молярности, плотности и массовых процентов полезны в сложных примерах, которые будут приведены ниже.
Определение эмпирических формул
Эмпирическую формулу можно определить с помощью химической стехиометрии, определяя, какие элементы присутствуют в молекуле и в каком соотношении. Соотношение элементов определяется путем сравнения количества молей каждого присутствующего элемента.
Пример 8: Горение органических молекул
1,000 г органической молекулы полностью сгорает в присутствии избытка кислорода. Получается 0,0333 моль СО 2 и 0,599 г Н 2 О. Какова эмпирическая формула органической молекулы?
Получается 0,0333 моль СО 2 и 0,599 г Н 2 О. Какова эмпирическая формула органической молекулы?
Раствор
Это реакция горения. Задача требует, чтобы вы знали, что органические молекулы состоят из некоторой комбинации элементов углерода, водорода и кислорода. Имея это в виду, напишите химическое уравнение, заменив неизвестные числа переменными. Не беспокойтесь о коэффициентах здесь.
\[ \ce{C_xH_yO_z(g) + O_2(g) \rightarrow CO_2(g) + H_2O(g)} \nonumber\]
Так как все моли C и H в CO 2 и H 2 O соответственно должны быть получены из 1-граммового образца неизвестного вещества, начните с подсчета количества молей каждого элемента, присутствующего в неизвестном образце.
0,0333 моль CO 2 (1 моль C/ 1 моль CO 2 ) = 0,0333 моль C в неизвестном0294 2 O)(2 моль H/1 моль H 2 O) = 0,0665 моль H в неизвестном
Рассчитайте количество молей кислорода, взяв сумму молей кислорода в CO 2 и H 2 O Это даст вам количество молей как от неизвестной органической молекулы, так и от O 2 , поэтому вы должны вычесть моли кислорода, перенесенного из O 2 .
Моль кислорода в CO 2 :
0,0333 моль CO 2 (2 моль O/1 моль CO 2 ) = 0,0666 моль O
моль кислорода в H 2 O:
0,599 г H 2 O (1MOL H 2 O/18.01528 G. 2944 2944 2944 2944 294 4.10294 2944 2944 2944 294 4.10294 294 4. 2 295. 2 o). /1моль H 2 O) = 0,0332 моль O
Используя закон сохранения, мы знаем, что масса до реакции должна равняться массе после реакции. При этом мы можем использовать разницу конечной массы продуктов и начальной массы неизвестной органической молекулы для определения массы O 2 реагент.
0,3333MOL CO 2 (44,0098G CO 2 / 1MOL CO 2 ) = 1,466G CO 2
1,466G CO 2 + 0,599G HIC HIIC 269G 269G 2694 2694 2694 2694 2694 2694 2694. = 1,065G O 2
моль кислорода в O 2
1,065G O 2 (1MOL O 2 / 31. 9988G O 2 2 / 31,9988G O 2 ) 2 ) 2 ) 2 ) 2 ) 2 ) 2 ) 2 ) 2 2 ) 2 2 ) 2 ) 2 ) 2 ) 2 2 ) 2 2 ). ) = 0,0666 моль O
9988G O 2 2 / 31,9988G O 2 ) 2 ) 2 ) 2 ) 2 ) 2 ) 2 ) 2 ) 2 2 ) 2 2 ) 2 ) 2 ) 2 ) 2 2 ) 2 2 ). ) = 0,0666 моль O
Моль кислорода в неизвестном
(0,0666 моль O + 0,0332 моль O) — 0,0666 моль O = 0,0332 моль O
Рассчитайте молярное отношение C, H и O в неизвестном веществе и разделите на наименьшее число.
(1/0,0332)(0,0333 моль C : 0,0665 моль H : 0,0332 моль O) => 1 моль C: 2 моль H: 1 моль O
Определение молекулярных формул
Чтобы определить молекулярную формулу, сначала определите эмпирическую формулу соединения, как показано в разделе выше, а затем экспериментально определите молекулярную массу. Далее разделите молекулярную массу на молярную массу эмпирической формулы (рассчитывается путем нахождения суммы полных атомных масс всех элементов в эмпирической формуле). Умножьте индексы молекулярной формулы на этот ответ, чтобы получить молекулярную формулу.
Пример 9
В приведенном выше примере было определено, что неизвестная молекула имеет эмпирическую формулу CH 2 O.
1. Найдите молярную массу эмпирической формулы CH 2 O.
12,011 г C + (1,008 г H) * (2 H) + 15,999 г O = 30,026 г/моль CH 2 O
2. Экспериментально определить молекулярную массу. Для нашего соединения она составляет 120,056 г/моль.
3. Разделите экспериментально определенную молекулярную массу на массу эмпирической формулы.
(120,056 г/моль) / (30,026 г/моль) = 3,9984
4. Поскольку 3,9984 очень близко к четырем, можно безопасно округлить и предположить, что в экспериментально определенной молекулярной массе была небольшая ошибка . Если ответ не близок к целому числу, то имела место либо ошибка в расчете эмпирической формулы, либо большая ошибка в определении молекулярной массы.
5. Умножьте отношение из шага 4 на нижние индексы эмпирической формулы, чтобы получить молекулярную формулу.
СН 2 О * 4 = ?
C: 1 * 4 = 4
H: 2 * 4 = 8
O 1 * 4 = 4
CH 2 O * 4 = C 4 H 8 O 4
8 O 4 8 O 4 6. Проверьте свой результат, рассчитав молярную массу молекулярной формулы и сравнив ее с экспериментально определенной массой.молярная масса C 4 H 8 O 4 = 120,104 г/моль
экспериментально определенная масса = 120,056 г/моль
% ошибка = | теоретический — экспериментальный | / теоретическое * 100%
% ошибка = | 120,104 г/моль — 120,056 г/моль | / 120,104 г/моль * 100 %
% ошибка = 0,040 %
Пример 10: Комплексная задача стехиометрии
Сварщик-любитель плавит два металла, чтобы получить сплав, состоящий из 45 % меди и 55 % железа (II). по массе. Плотность сплава 3,15 г/л. Один литр сплава полностью заполняет форму объемом 1000 см 3 . Он случайно ломает 1,203 см 3 часть однородной смеси и выметает ее наружу, где она годами вступает в реакцию с кислотными дождями. Если предположить, что кислота реагирует со всем железом(II), а не с медью, сколько граммов H 2 (g) выбрасывается в атмосферу из-за невнимательности любителя? (Обратите внимание, что ситуация вымышленная.)
Он случайно ломает 1,203 см 3 часть однородной смеси и выметает ее наружу, где она годами вступает в реакцию с кислотными дождями. Если предположить, что кислота реагирует со всем железом(II), а не с медью, сколько граммов H 2 (g) выбрасывается в атмосферу из-за невнимательности любителя? (Обратите внимание, что ситуация вымышленная.)
Решение
Шаг 1 : Напишите сбалансированное уравнение после определения продуктов и реагентов. В этой ситуации, поскольку мы предполагаем, что медь не вступает в реакцию, реагентами являются только H 9{2+}(aq)} \nonumber\]
Шаг 2: Запишите всю предоставленную информацию
Плотность сплава = (3,15 г сплава/1 л сплава)
x грамм сплава = 45% меди = ( 45 г Cu(s)/100 г сплава)
x грамм сплава = 55% железа(II) = (55 г Fe(s)/100 г сплава)
1 литр сплава = 1000 см см 3 сплав
Шаг 3: Ответьте на заданный вопрос. Вопрос спрашивает, сколько h3(g) было произведено. Ожидается, что вы определите количество образовавшегося продукта.
Вопрос спрашивает, сколько h3(g) было произведено. Ожидается, что вы определите количество образовавшегося продукта.
Шаг 4: Начните с соединения, о котором вы знаете больше всего, и используйте заданные соотношения, чтобы преобразовать его в желаемое соединение.
Преобразуйте данное количество реагента сплава в число молей прореагировавшего Fe(s).
1,203 см 3 сплав (1 л сплава/1000 см 3 сплав) (3,15 г сплава/1 л сплава) (55 г Fe(s)/100 г сплава) (1 моль Fe(s)/55,8 г Fe(s)) =3,74 x 10 -5 моль Fe(s)
Убедитесь, что все единицы сокращаются, чтобы получить моли \(\ce{Fe(s)}\). Приведенное выше преобразование включает использование нескольких стехиометрических соотношений плотности, процентной массы и молярной массы.
Теперь необходимо использовать сбалансированное уравнение для преобразования молей Fe(s) в моли H 2 (g). Помните, что коэффициенты сбалансированного уравнения определяют стехиометрический коэффициент или молярное соотношение реагентов и продуктов.
3,74 x 10 -5 моль Fe (т) (1 моль H 2 (г)/1 моль Fe(s)) = 3,74 x 10 -5 моль H 2 (г)
2 9 Шаг 5:
Проверить единицыВопрос спрашивает сколько грамм H 2 (г), поэтому моли H 2 (г) все еще должны быть преобразованы в граммы с использованием молярной массы H 2 (г). Поскольку в каждом H 2 содержится два H, его молярная масса в два раза больше, чем у одного атома H.
молярная масса = 2(1,00794 г/моль) = 2,01588 г/моль (г)) = 7,53 x 10 -5 г H 2 (г) освобожден
Задачи 9{2+}_{(водн.)} + Ag_{(s)}\)
2) Соляная кислота реагирует с твердым куском алюминия с образованием газообразного водорода и ионов алюминия. Напишите сбалансированное химическое уравнение этой реакции.
3) Учитывая исходный раствор 10,1 М, сколько мл необходимо добавить к воде, чтобы получить 200 мл раствора 5 М?
4) Если 0,502 г газообразного метана реагируют с 0,27 г кислорода с образованием углекислого газа и воды, какой реагент является лимитирующим и сколько молей воды образуется? Ниже приведено несбалансированное уравнение.
\[\ce{Ch5(г) + O2(г) \rightarrow CO2(г) + h3O(ж)} \номер\]
5) Образец органического соединения массой 0,777 г полностью сгорает. Он производит 1,42 г CO 2 и 0,388 г H 2 O. Зная, что все атомы углерода и водорода в CO 2 и H 2 O происходят из образца 0,777 г, какова эмпирическая формула органическое соединение?
Веб-ссылки для получения дополнительной информации
- 1. См. http://chemistry.about.com/cs/stoich…/aa042903a.htm как внешний ресурс о том, как сбалансировать химические реакции.
- 2. Обратитесь к http://www.learnchem.net/tutorials/stoich.shtml как к внешнему ресурсу по стехиометрии.
Ссылки
- Т. Э. Браун, Х. Э. ЛеМэй, Б. Берстен, К. Мерфи. Химия: Центральная наука. Прентис Холл, 8 января 2008 г.
- Дж. К. Коц П.М. Трейчел, Дж. Таунсенд. Химия и химическая реактивность. Брукс Коул, 7 февраля 2008 г.
- Петруччи, Харвуд, Сельдь, Мадура.
 Общие принципы химии и современные приложения. Прентис Холл. Нью-Джерси, 2007.
Общие принципы химии и современные приложения. Прентис Холл. Нью-Джерси, 2007.
Авторы и ссылки
- Джозеф Неймех (UCD), Марк Тай (DVC)
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Показать страницу TOC г.
- № на стр.
- Теги
- Кислотно-щелочной
- Балансировка
- Балансирующие реакции
- химическая реакция
- химические символы
- Комбинация
- сжигание
- разложение
- плотность
- Двойной рабочий объем
- элементов
- Эмпирические формулы
- закон сохранения массы
- масса
- метрон
- молекулярная формула
- Процент массы
- Продукция
- Реагенты
- Одинарный рабочий объем
- стехиометрический коэффициент
- стехиометрия
- стоихейн
- синтез
- том
Моль в химических реакциях – Введение в химию – 1-е канадское издание
Глава 5. Стехиометрия и моль
Стехиометрия и моль
- Составьте химическое уравнение в молях.
- Используйте сбалансированное уравнение для построения коэффициентов преобразования в молях.
- Вычислите моли одного вещества из молей другого вещества, используя сбалансированное химическое уравнение.
Рассмотрим это сбалансированное химическое уравнение:
2H 2 + O 2 → 2H 2 O
Мы интерпретируем это как «две молекулы водорода реагируют с одной молекулой кислорода, образуя две молекулы воды». Химическое уравнение сбалансировано, пока коэффициенты находятся в соотношении 2:1:2. Например, это химическое уравнение также сбалансировано:
100H 2 + 50O 2 → 100H 2 O
Это уравнение не является обычным, потому что соглашение говорит, что мы используем наименьшее отношение коэффициентов, но оно сбалансировано. Так же и это химическое уравнение:
5000H 2 + 2500O 2 → 5000H 2 O
Опять же, это не обычно, но все же сбалансировано. Предположим, мы используем гораздо большее число:
Предположим, мы используем гораздо большее число:
12,044 × 10 23 H 2 + 6,022 × 10 23 O 2 → 12,044 × 10 23 H 2 O
Эти коэффициенты также находятся в соотношении 2:1:2. Но эти числа связаны с количеством вещей в кроте: первое и последнее числа — это удвоенное число Авогадро, а второе число — это число Авогадро. Это означает, что первое и последнее число представляют 2 моля, а среднее число — всего 1 моль. Почему бы просто не использовать количество молей для балансировки химического уравнения?
2H 2 + O 2 → 2H 2 O
Это то самое сбалансированное химическое уравнение, с которого мы начали! Это означает, что химические уравнения не просто сбалансированы с точки зрения молекул; они также сбалансированы по количеству молей . Мы можем так же легко прочитать это химическое уравнение, как «два моля водорода реагируют с одним молем кислорода, чтобы получить два моля воды». Все сбалансированные химические реакции сбалансированы с точки зрения молей.
Все сбалансированные химические реакции сбалансированы с точки зрения молей.
Интерпретируйте это сбалансированное химическое уравнение в молях.
P 4 + 5O 2 → P 4 O 10
Раствор
Коэффициенты представляют количество реагирующих молей, а не только молекул. Мы бы сказали об этом уравнении, как «один моль молекулярного фосфора реагирует с пятью молями элементарного кислорода, чтобы получить один моль деоксида тетрафосфора».
Объясните это сбалансированное химическое уравнение в молях.
N 2 + 3H 2 → 2NH 3
Ответ
Один моль элементарного азота реагирует с тремя молями элементарного водорода с образованием двух молей аммиака.
В главе 4 «Химические реакции и уравнения», в разделе «Химическое уравнение», мы заявили, что химическое уравнение — это просто рецепт химической реакции. Как таковые, химические уравнения также дают нам эквивалентности — эквивалентности между реагентами и продуктами. Однако теперь мы понимаем, что эти эквивалентности выражаются в молях . Рассмотрим следующее химическое уравнение:
Однако теперь мы понимаем, что эти эквивалентности выражаются в молях . Рассмотрим следующее химическое уравнение:
2H 2 + O 2 → 2H 2 O
Эта химическая реакция дает нам следующие эквиваленты:
2 моль H 2 ⇔ 1 моль O 2 ⇔ 2 моль H 2 O
Любые две из этих величин могут быть использованы для построения коэффициента преобразования, который позволяет нам связать количество молей одного вещества с эквивалентным количеством молей другого вещества. Если, например, мы хотим знать, сколько молей кислорода прореагирует с 17,6 моль водорода, мы строим коэффициент преобразования между 2 моль H 2 и 1 моль O 2 и использовать его для преобразования молей одного вещества в моли другого:
Обратите внимание, что единица моль H 2 сокращается, а моль O 2 является новой введенной единицей. Это пример , когда вы начинаете с молей одного вещества и конвертируете в моли другого вещества, используя сбалансированное химическое уравнение. Пример может показаться простым, потому что числа маленькие, но числа не всегда будут такими простыми!
Пример может показаться простым, потому что числа маленькие, но числа не всегда будут такими простыми!
Рассмотрим следующее сбалансированное химическое уравнение:
2C 4 H 10 (г) + 13O 2 → 8CO 2 (г) + 10H 2 O(ℓ) 90 моль
2 вступают в реакцию, сколько молей CO 2 образуется?Решение
Мы связываем количество кислорода с количеством углекислого газа, поэтому нам нужна эквивалентность между этими двумя веществами. Согласно сбалансированному химическому уравнению, эквивалентность равна:
13 моль O 2 ⇔ 8 моль CO 2
Мы можем использовать эту эквивалентность для построения надлежащего коэффициента преобразования. Начнем с того, что нам дано, и применим коэффициент преобразования:
Единица моль O 2 находится в знаменателе коэффициента преобразования, поэтому он сокращается. И 8, и 13 являются точными числами, поэтому они не влияют на количество значащих цифр в окончательном ответе.
Используя приведенное выше уравнение, сколько молей H 2 O образуется при реакции 154 моль O 2 ?
Ответ
118 моль
Важно повторить, что сбалансированные химические уравнения сбалансированы с точки зрения молей . Не граммы, килограммы или литры — а моли. Любая проблема со стехиометрией, вероятно, в какой-то момент должна будет решаться через единицу моля, особенно если вы работаете со сбалансированной химической реакцией.
- Сбалансированные химические реакции уравновешены с точки зрения молей.
- Сбалансированная химическая реакция дает эквивалентность в молях, что позволяет выполнять стехиометрические расчеты.
- Выразите в молях значение этого химического уравнения.
CH 4 + 2O 2 → CO 2 + 2H 2 O
- Выразите в молях значение этого химического уравнения.
Na 2 CO 3 + 2HCl → 2NaCl + H 2 O + CO 2
- Сколько молекул каждого вещества входит в уравнение в упражнении 1, если его интерпретировать в терминах молей?
- Сколько молекул каждого вещества входит в уравнение в упражнении 2, если его интерпретировать в терминах молей?
- Для химического уравнения 2C 2 H 6 + 7O 2 → 4CO 2 + 6H 2 O, какие эквивалентности можно записать в молях? Используйте знак ⇔.

- Для химического уравнения 2Al + 3Cl 2 → 2AlCl 3 какие эквивалентности можно записать в молях? Используйте знак ⇔.
- Напишите сбалансированную химическую реакцию сгорания C 5 H 12 (продуктами являются CO 2 и H 2 O) и определите, сколько молей H 2 O образуется при 5,8 моль O 2 вступают в реакцию.
- Напишите сбалансированную химическую реакцию образования Fe 2 (SO 4 ) 3 из Fe 2 O 3 и SO 3 и определите, сколько молей Fe 2 0294 4
 ) → Al 3+ (водн.) + 3Ag(s), сколько молей Ag образуется при реакции 0,661 моль Al?
) → Al 3+ (водн.) + 3Ag(s), сколько молей Ag образуется при реакции 0,661 моль Al?

 10.2020 XLIII Турнир Ломоносова задания и ответы
10.2020 XLIII Турнир Ломоносова задания и ответы 12.17 Ответы и задания по русскому языку 11 класс СтатГрад варианты РЯ10701-РЯ10702
12.17 Ответы и задания по русскому языку 11 класс СтатГрад варианты РЯ10701-РЯ10702 10.17 Физика 11 класс СтатГрад задания и ответы варианты ФИ10101-ФИ10104
10.17 Физика 11 класс СтатГрад задания и ответы варианты ФИ10101-ФИ10104 10.2017 Обществознание 11 класс работа СтатГрад задания и ответы ОБ10101-ОБ10104
10.2017 Обществознание 11 класс работа СтатГрад задания и ответы ОБ10101-ОБ10104 09.2017 Биология 9 класс тренировочная работа «СтатГрад» БИ90101-БИ90104 ответы и задания
09.2017 Биология 9 класс тренировочная работа «СтатГрад» БИ90101-БИ90104 ответы и задания 09. Математика 10 класс задания и ответы
09. Математика 10 класс задания и ответы 09 Входная контрольная работа русский язык 7 класс для 56 региона задания и ответы
09 Входная контрольная работа русский язык 7 класс для 56 региона задания и ответы 10 Задания и ответы олимпиады по литературе 7-11 класс муниципальный этап 2017
10 Задания и ответы олимпиады по литературе 7-11 класс муниципальный этап 2017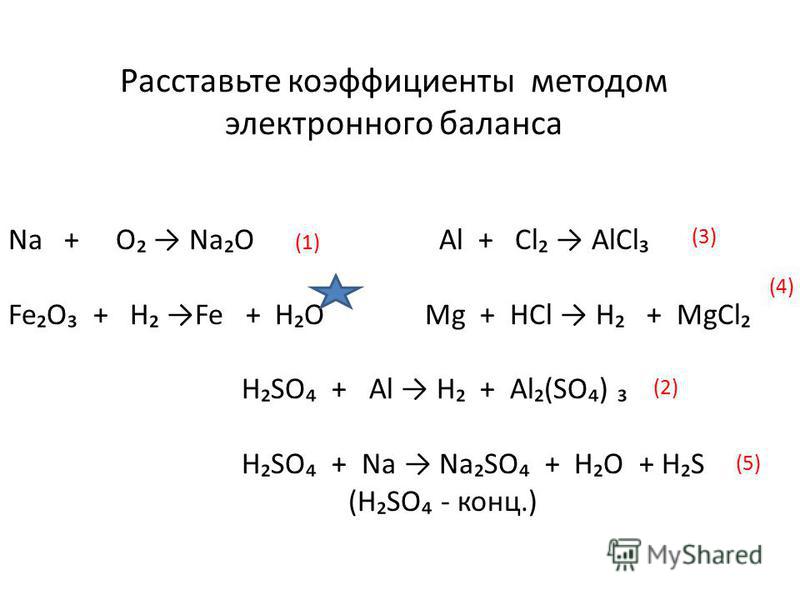 09.17 Математика 11 класс мониторинговая работа ЕГЭ 3 варианта задания и ответы
09.17 Математика 11 класс мониторинговая работа ЕГЭ 3 варианта задания и ответы 04.2019
04.2019 11.17 Математика 9 класс работа «СтатГрад» задания и ответы варианты МА90201-МА90204
11.17 Математика 9 класс работа «СтатГрад» задания и ответы варианты МА90201-МА90204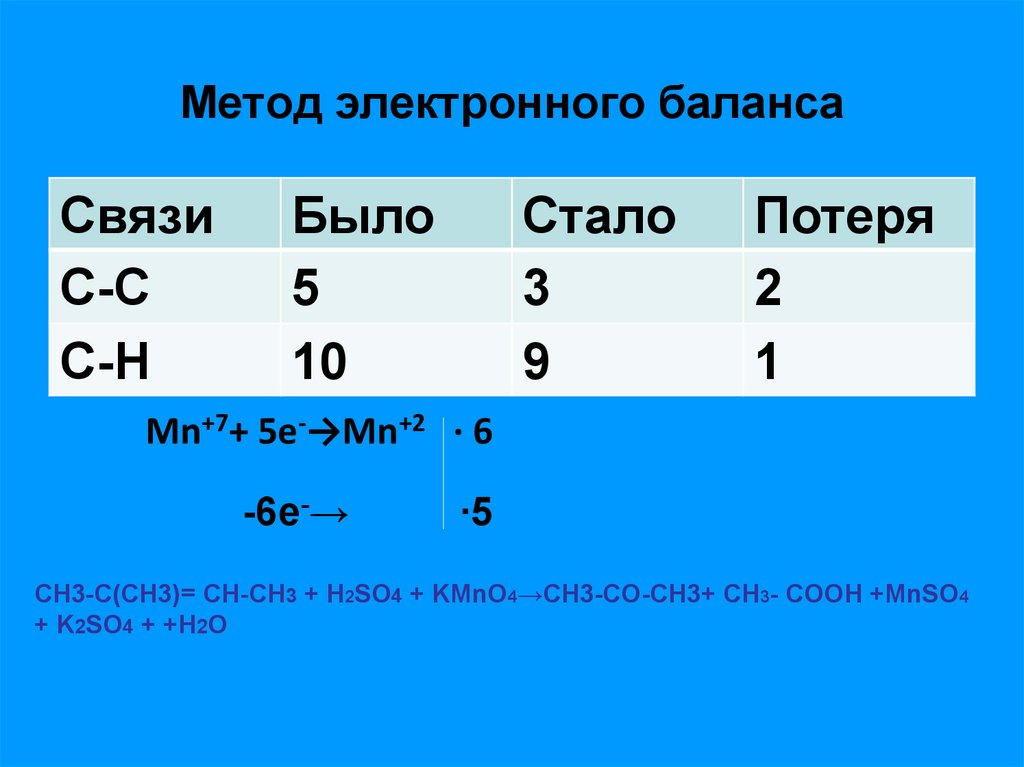 11
11 09.2017 Варианты и ответы контрольной работы математика 8 класс для 56 региона
09.2017 Варианты и ответы контрольной работы математика 8 класс для 56 региона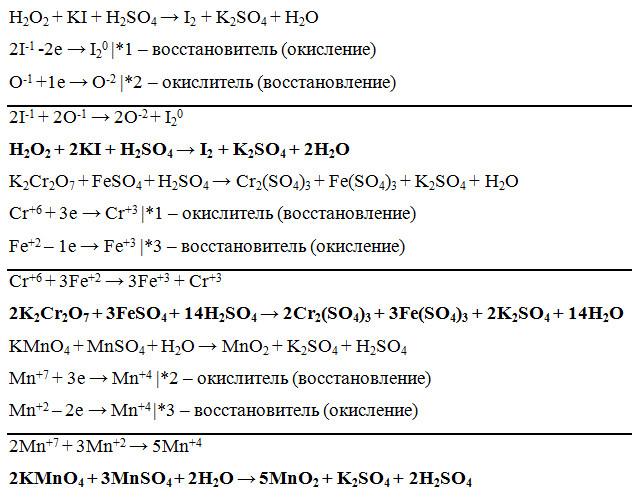 10.2018
10.2018