| 1 | Найти число нейтронов | H | |
| 2 | Найти массу одного моля | H_2O | |
| 3 | Баланс | H_2(SO_4)+K(OH)→K_2(SO_4)+H(OH) | |
| 4 | Найти массу одного моля | H | |
| 5 | Найти число нейтронов | Fe | |
| 6 | Найти число нейтронов | Tc | |
| 7 | Найти конфигурацию электронов | H | |
| 8 | Найти число нейтронов | Ca | |
| 9 | Баланс | CH_4+O_2→H_2O+CO_2 | |
| 10 | Найти число нейтронов | C | |
| 11 | Найти число протонов | H | |
| 12 | Найти число нейтронов | O | |
| 13 | Найти массу одного моля | CO_2 | |
| 14 | Баланс | C_8H_18+O_2→CO_2+H_2O | |
| 15 | Найти атомную массу | H | |
| 16 | Определить, растворима ли смесь в воде | H_2O | |
| 17 | Найти конфигурацию электронов | Na | |
| 18 | Найти массу одного атома | H | |
| 19 | Найти число нейтронов | Nb | |
| 20 | Найти число нейтронов | Au | |
| 21 | Найти число нейтронов | Mn | |
| 22 | Найти число нейтронов | Ru | |
| 23 | Найти конфигурацию электронов | ||
| 24 | Найти массовую долю | H_2O | |
| 25 | Определить, растворима ли смесь в воде | NaCl | |
| 26 | Найти эмпирическую/простейшую формулу | H_2O | |
| 27 | Найти степень окисления | H_2O | |
| 28 | Найти конфигурацию электронов | K | |
| 29 | Найти конфигурацию электронов | Mg | |
| 30 | Найти конфигурацию электронов | Ca | |
| 31 | Найти число нейтронов | Rh | |
| 32 | Найти число нейтронов | Na | |
| 33 | Найти число нейтронов | Pt | |
| 34 | Найти число нейтронов | Be | Be |
| 35 | Найти число нейтронов | Cr | |
| 36 | Найти массу одного моля | H_2SO_4 | |
| 37 | Найти массу одного моля | HCl | |
| 38 | Найти массу одного моля | Fe | |
| 39 | Найти массу одного моля | C | |
| 40 | Найти число нейтронов | Cu | |
| 41 | Найти число нейтронов | S | |
| 42 | Найти степень окисления | H | |
| 43 | Баланс | CH_4+O_2→CO_2+H_2O | |
| 44 | Найти атомную массу | O | |
| 45 | Найти атомное число | H | |
| 46 | Найти число нейтронов | Mo | |
| 47 | Найти число нейтронов | Os | |
| 48 | Найти массу одного моля | NaOH | |
| 49 | Найти массу одного моля | O | |
| 50 | Найти конфигурацию электронов | Fe | |
| 51 | Найти конфигурацию электронов | C | |
| 52 | Найти массовую долю | NaCl | |
| 53 | Найти массу одного моля | ||
| 54 | Найти массу одного атома | Na | |
| 55 | Найти число нейтронов | N | |
| 56 | Найти число нейтронов | Li | |
| 57 | Найти число нейтронов | V | |
| 58 | Найти число протонов | N | |
| 59 | Упростить | H^2O | |
| 60 | Упростить | h*2o | |
| 61 | Определить, растворима ли смесь в воде | H | |
| 62 | Найти плотность при стандартной температуре и давлении | H_2O | |
| 63 | Найти степень окисления | NaCl | |
| 64 | Найти атомную массу | He | He |
| 65 | Найти атомную массу | Mg | |
| 66 | Найти число электронов | H | |
| 67 | Найти число электронов | O | |
| 68 | Найти число электронов | S | |
| 69 | Найти число нейтронов | Pd | |
| 70 | Найти число нейтронов | Hg | |
| 71 | Найти число нейтронов | B | |
| 72 | Найти массу одного атома | Li | |
| 73 | Найти эмпирическую формулу | H=12% , C=54% , N=20 | , , |
| 74 | Найти число протонов | Be | Be |
| 75 | Найти массу одного моля | Na | |
| 76 | Найти конфигурацию электронов | Co | |
| 77 | Найти конфигурацию электронов | S | |
| 78 | Баланс | C_2H_6+O_2→CO_2+H_2O | |
| 79 | Баланс | H_2+O_2→H_2O | |
| 80 | Найти конфигурацию электронов | P | |
| 81 | Найти конфигурацию электронов | Pb | |
| 82 | Найти конфигурацию электронов | Al | |
| 83 | Найти конфигурацию электронов | Ar | |
| 84 | Найти массу одного моля | O_2 | |
| 85 | Найти массу одного моля | H_2 | |
| 86 | Найти число нейтронов | K | |
| 87 | Найти число нейтронов | P | |
| 88 | Найти число нейтронов | Mg | |
| 89 | Найти число нейтронов | W | |
| 90 | Найти массу одного атома | C | |
| 91 | Упростить | na+cl | |
| 92 | Определить, растворима ли смесь в воде | H_2SO_4 | |
| 93 | Найти плотность при стандартной температуре и давлении | NaCl | |
| 94 | Найти степень окисления | C_6H_12O_6 | |
| 95 | Найти степень окисления | Na | |
| 96 | Определить, растворима ли смесь в воде | C_6H_12O_6 | |
| 97 | Найти атомную массу | Cl | |
| 98 | Найти атомную массу | Fe | |
| 99 | Найти эмпирическую/простейшую формулу | CO_2 | |
| 100 | Найти число нейтронов | Mt |
список примеров / Справочник :: Бингоскул
Число протонов, нейтронов и определение заряда ядра: список примеровдобавить в закладки удалить из закладок
Содержание:
Атом – частица, которая включает протоны, нейтроны и электроны. Совокупность протонов и нейтронов атома формирует ядро, вокруг которого движутся электроны. Все элементы, содержащиеся в атоме, имеют свои особенности.
Совокупность протонов и нейтронов атома формирует ядро, вокруг которого движутся электроны. Все элементы, содержащиеся в атоме, имеют свои особенности.
Строение атомного ядра
В 1911 году английский ученый Эрнест Резерфорд доказал, что ядро имеет положительный заряд и располагается в центре атома. Ядерный заряд численно совпадает с порядковым номером атома в периодической таблице Менделеева. Около 99 % массы сконцентрировано именно в ядре, при этом диаметр ядра примерно в 100 тысяч раз меньше диаметра самого атома.
У протонов и нейтронов масса примерно одинакова и равна 1. Они схожи по строению, но различны по заряду. Протоны обладают положительным зарядом, а нейтроны – нулевым. Сумма протонов и нейтронов в одном атоме называется массовым числом.
Порядковый номер атома кремния равен 14. Таким образом, заряд ядра атома кремния равен 14. Ядро составляют 14 протонов и 14 нейтронов. Массовое число кремния равно 28.
Электроны
Электроны – отрицательно заряженные частицы.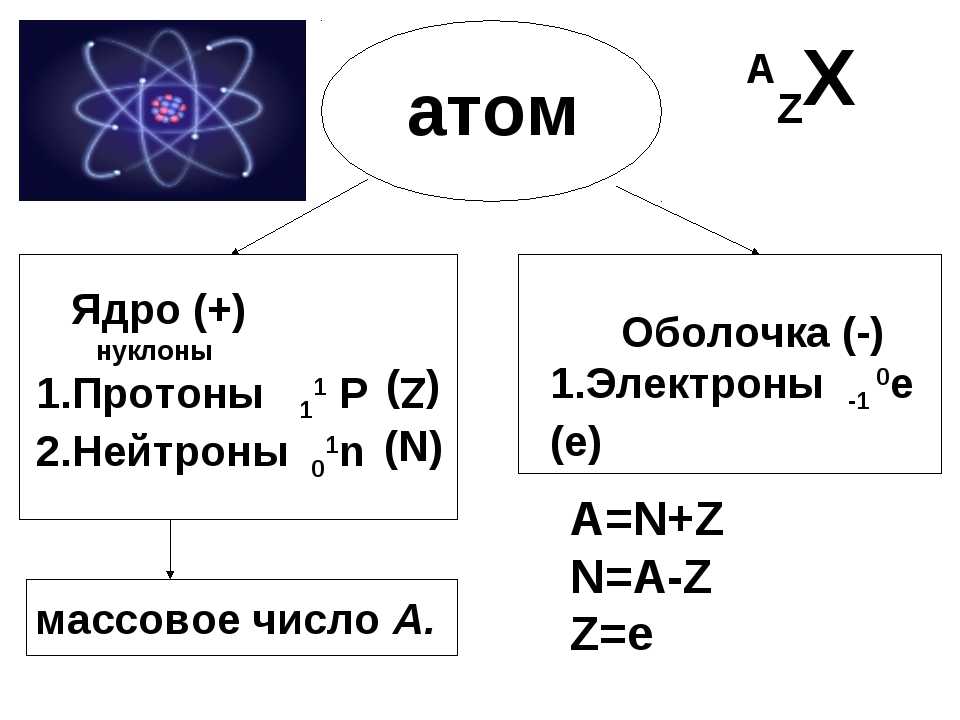 У электронов запас энергии неодинаков. Эту энергию электроны излучают или поглощают определенными порциями – квантами. Значение энергии электрона задается главным квантовым числом, которое выражается в виде целых чисел. Электроны в атоме находятся на различных энергетических уровнях.
У электронов запас энергии неодинаков. Эту энергию электроны излучают или поглощают определенными порциями – квантами. Значение энергии электрона задается главным квантовым числом, которое выражается в виде целых чисел. Электроны в атоме находятся на различных энергетических уровнях.
Электроны, главное число которых равно одному (n=1), размещаются на первом энергетическом уровне. Изменение главного квантового числа связано со скачкообразным изменением энергии. При этом электроны могут переходить на следующий уровень. Максимальное число электронов на энергетическом уровне определяется по формуле:
N=2n2, где n – главное квантовое число.
Например, на первом энергетическом уровне согласно формуле может располагаться только два электрона, а на втором – восемь электронов.
Электроны, находящиеся на внешнем уровне, слабо связаны с атомным ядром, поэтому при химических взаимодействиях эти электроны легко отсоединяются. В электронейтральных атомах число электронов соответствует его порядковому номеру.
Сколько электронов в электронейтральном атоме кремния, можно узнать по порядковому номеру элемента. Таким образом, у кремния 14 электронов.
Изотопы
В экспериментальных условиях было установлено, что некоторые атомы имеют разные массовые числа. Например, для кремния характерны атомы с массовыми числами 28, 29, 40, при этом заряд атома кремния всегда равен 14. Таким образом, меняется только число нейтронов, а количество протонов постоянно. Разновидности атомов одного и того же элемента, имеющие одинаковое число протонов, но разное число нейтронов в ядре, называются изотопами.
Поделитесь в социальных сетях:
5 ноября 2021, 15:15
Could not load xLike class!
Как можно определить количество нейтронов в атоме? — High School/Honors/AP® Chemistry Resources
Как определить количество нейтронов в данном атоме?
Во-первых, давайте определим некоторые термины, с которыми вам необходимо ознакомиться.
• Атомный номер атома представляет собой число протонов в ядре этого атома.
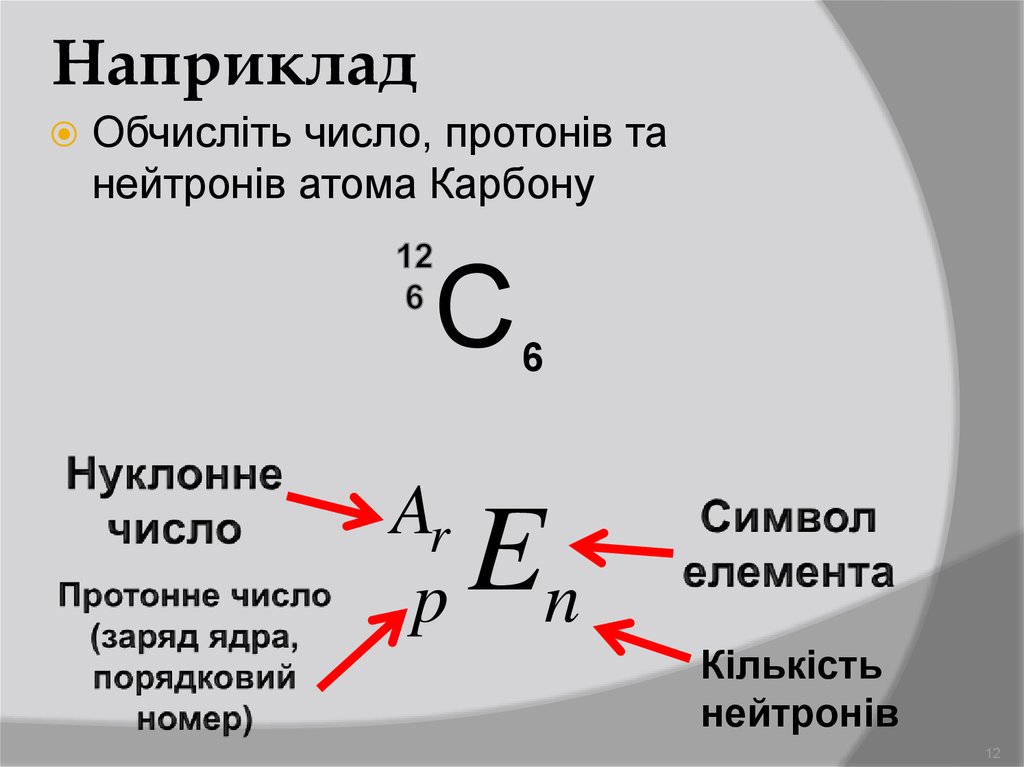
• Массовое число (также называемое нуклонным числом) атома равно общее количество протонов и нейтронов в ядре этого атома.
• Наконец, относительная атомная масса (символ Aᵣ) элемента представляет собой средневзвешенное значение масс атомов каждого изотопа этого элемента .
Единицей этой величины является атомная единица массы (а.е.м.), которая определяется как 1/12 массы атома углерода-12, то есть изотопа углерода с 6 протонами и 6 нейтронами.
Для относительной атомной массы мы должны взять средневзвешенное значение , потому что одних изотопов больше, чем других – это означает, что в природе существует больше некоторых изотопов, поэтому средняя масса атомов этот элемент будет ближе к массе более распространенных изотопов.
Это много информации — давайте рассмотрим в качестве примера хлор.
Хлор имеет два изотопа, которые существуют в значительном количестве, Cl-35 (75%) и Cl-37 (25%).
Помните, что числа над символом являются массовыми числами, поэтому в Cl-35 всего 35 протонов и нейтронов, а в Cl-37 всего 37 протонов и нейтронов.
Поскольку мы знаем, что атомный номер Cl равен 17, мы можем вычислить, что Cl-35 имеет 18 нейтронов, а Cl-37 — 20 нейтронов.
Помните: атомный номер элемента постоянен для всех изотопов, поскольку именно число протонов фактически определяет, к какому элементу относится атом.
Для расчета относительной атомной массы хлора необходимо взять средневзвешенное значение, поэтому расчет выглядит следующим образом:
:
Реальный ответ 35,45, наблюдаемый в периодической таблице, исходит от всех других второстепенных изотопов, которые мы не рассматривали, но 35,5 — достаточно хороший ответ, потому что все эти другие изотопы на самом деле не имеют значения.
 Вы заметите, что 35,45 в любом случае округляется до 35,5 до трех значащих цифр.
Вы заметите, что 35,45 в любом случае округляется до 35,5 до трех значащих цифр.Определение количества нейтронов
А как же нейтроны?
В примере с хлором мы видели, что для определенного изотопа элемента, если мы знаем массовое число этого изотопа, мы можем вычислить число нейтронов в атоме этого изотопа, взяв массовое число (общее число протоны и нейтроны) и вычитание атомного номера (количество протонов). Это оставляет нас с количеством нейтронов в этом изотопе.
Но как ученые выясняют, какие изотопы элемента существуют в значительных пропорциях? Ключом является масс-спектрометрия.
Масс-спектрометрия — это способ измерения изотопов, присутствующих в данном образце элемента. Если вы возьмете масс-спектр хлора, например, вы получите график, который выглядит следующим образом:
x ось отношение массы к заряду , m/z.
Для этого спектра все заряды равны +1, поэтому эта ось соответствует массе изотопа, дающего каждый сигнал.
Мы знаем, что хлор существует в виде двухатомного газа, Cl 2 — вот почему мы видим сигналы около 70. Самая интересная часть — это два сигнала на 35 и 37. Они соответствуют атомам хлора, в частности изотопам. Кл-35 и Кл-37.
Соотношение примерно 3:1, и именно так ученый определил бы, какие изотопы существуют и в каких относительных количествах они присутствуют. Приведенный выше спектр немного упрощен, так как в нем также могут быть очень небольшие количества других изотопов, но нам не нужно беспокоиться об этом.
Как рассчитать количество протонов, нейтронов и электронов
Как рассчитать количество протонов, нейтронов и электроновПрежде чем мы начнем с некоторых примеров расчета количества протонов, нейтронов и электронов , давайте вспомним, какую информацию мы получаем о том или ином элементе из таблицы Менделеева. Например, если мы посмотрим на калий, K в периодической таблице, мы увидим следующие числа:
Первое, что вы хотите идентифицировать, это атомный номер элемента, поскольку он уникален для каждого элемента . Это число обычно указывается над символом, и в данном случае это 19.
Это число обычно указывается над символом, и в данном случае это 19.
Итак, калий имеет 19 протонов, и это верно для всех его изотопов. Другого элемента с атомным номером 19 быть не может.
Далее на кнопке указана средняя атомная масса калия, равная 390,098. Это средняя атомная масса всех изотопов калия, и поэтому это не целое число.
Если вам даются данные о том, что атомная масса калия равна, например, 39, то это относится к этому конкретному изотопа.
Теперь запомните, изотопов это атомы с одинаковым количеством протонов , но разным количеством нейтронов и, следовательно, разница в массовых числах возникает из-за разного количества протонов.
В простом примере вас могут попросить просто определить количество протонов для данного элемента.
Например, , сколько протонов имеет Са?
Для этого вам просто нужно найти атомный номер Ca, который мы находим из периодической таблицы, что он равен 20. Следовательно, Ca имеет 20 протонов.
Следовательно, Ca имеет 20 протонов.
Не запутайтесь, если элемент указан с некоторыми другими данными, такими как атомная масса или средняя атомная масса. 9{107}{\rm{Pd}}\]
Опять же, нам все равно, какой это изотоп, какая у него масса и сколько у него нейтронов. Pd всегда будет иметь 46 протонов, поскольку атомный номер является идентификатором элемента .
Количество протонов из нейтронов
Предположим, вам не дана периодическая таблица, а в вопросах предлагается определить количество протонов из числа нейтронов. В этом случае должно быть указано массовое число.
Например , сколько протонов содержит элемент с массовым числом 35, если в нем 18 нейтронов?
Мы знаем, что массовое число (А) = количество протонов + количество нейтронов, следовательно, количество протонов равно:
p = 35 – 18 = 17, а значит, элемент Cl
Количество протонов из электронов
Для нейтрального атома количество протонов равно количеству электронов. Именно это делает атом свободным от заряда. Следовательно, вы можете определить количество протонов, если дано количество электронов.
Именно это делает атом свободным от заряда. Следовательно, вы можете определить количество протонов, если дано количество электронов.
Например, идентифицируйте элемент атома с 54 электронами.
Все, что нам нужно сделать, это найти элемент с атомным номером 54, и это Xe.
Первое, что вам нужно здесь запомнить, это то, что заряд иона является результатом дисбаланса между числом протонов и электронов. Если это катион , то положительный показатель указывает, на сколько больше протонов он имеет по сравнению с числом электронов. Для анионов , заряд говорит о том, сколько дополнительных электронов по сравнению с количеством протонов.
Вспомните эту схему образования анионов и катионов:
Металлы имеют тенденцию терять электроны и превращаться в катионы (положительно заряженные ионы).
Неметаллы имеют тенденцию приобретать электрон(ы) и становиться анионами (отрицательно заряженными ионами).
Обратите внимание, что количество протонов не изменилось, а ионов заряжены, потому что, в отличие от атомов, их число протонов и электронов не равно .
Например, , какой элемент имеет заряд 3+ с 10 электронами?
Заряд 3+ означает, что элемент потерял 3 электрона. Итак, если у катиона 10 электронов, у нейтрального атома должно быть 13 электронов, потому что потеря 3 из них приводит к заряду 3+. Отсюда мы знаем, что у элемента 13 протонов, потому что количество протонов равно количеству электронов в нейтральном атоме. Элемент с атомным номером 13 — Al.
Самая важная часть, которая вам понадобится для расчета числа нейтронов, это то, что вместе с протонами они составляют атомную массу данного изотопа. Итак, если у нас есть массовое число данного изотопа, мы можем легко определить количество его нейтронов.
Например, , сколько нейтронов у изотопа 65 Cu?
Первым делом, опять же, нужно найти число протонов для Cu, и это атомный номер . Из периодической таблицы мы находим, что у него 29 протонов. Массовое число (65) представляет собой сумму количества протонов и нейтронов. Следовательно, мы можем вычесть количество протонов из атомного номера, чтобы получить количество нейтронов:
Из периодической таблицы мы находим, что у него 29 протонов. Массовое число (65) представляет собой сумму количества протонов и нейтронов. Следовательно, мы можем вычесть количество протонов из атомного номера, чтобы получить количество нейтронов:
# n = A – Z = 65 – 29 = 36
Число нейтронов из числа электронов
Поскольку количество протонов и электронов в нейтральных атомах одинаково, мы можем определить количество нейтронов по количеству электронов и массовому числу.
Например , сколько нейтронов у атома с массой 79 и 35 электронов?
Наличие 35 электронов означает, что у него также есть 35 протонов, и если мы вычтем это из атомной массы, мы узнаем, сколько у него нейтронов.
# e- = # p = 35
# n = массовое число – # p = 79 – 35 = 44
Число нейтронов в ионах
Число нейтронов всегда будет связано к числу протонов и атомной массе. Итак, точно так же, как мы делали это для количества протонов в ионе, мы собираемся использовать заряд для определения количества нейтронов.