Примеры тестовых заданий к приложению1
1. Число нейтронов в ядре атома 39Ca равно
1.19 2.20 3.39 4.40
2.Ядро изотопа фосфора 31 Р содержит
1.15 2.46 3.16 4.31
3. Электронная конфигурация 1s22s22p63s23p6соответствует частице
1) Li+ 2) K+ 3) Cs+ 4) Na+
4.Иону О2- соответствует электронная конфигурация…
1. 1s22s22p3 2. 1s22s22p4 3. 1s22s22p5 4. 1s22s22p6
5. Изотопы одного и того же элемента отличаются друг от друга
1) числом нейтронов и атомной массой 3) числом протонов и числом электронов
2) числом электронов и числом нейтронов 4) зарядом ядра и числом протонов
6. Орбитальное квантовое
число может принимать значения…
Орбитальное квантовое
число может принимать значения…
1.1,2,3,…,∞ 2. 0,…,(n-1) 3. -l,0,+l 4. ±1/2
7. Химический элемент, формула высшего оксида которого R2O7, имеет электронную конфигурацию атома
1) 1s2 2s22р63s1 2) 1s22s22р63s23р5 3) 1s2 2s22р63s23р64s1 4) 1s2 2s1
8.Формула водородного соединения элемента, образующего высший оксид Э2О5, имеет вид…
1.ЭН 2.ЭН2 3. ЭН3 4. ЭН4
9.На внешнем энергетическом уровне атома элемента, образующего высший гидроксид состава НЭО4 содержится ____ электронов
1. 4 2. 5 3. 6 4. 7
10.В основном состоянии неспаренные электроны отсутствуют у атома
1. кремния 2.алюминия 3.магния 4.фосфора
11.Атом углерода в основном состоянии содержит__ неспаренных электронов
1. 2 2. 3. 3. 4 4. 0
2 2. 3. 3. 4 4. 0
12. наибольшее число неспаренных электронов в основном состоянии содержит атом…
1.хлора 2.фосфора 3.кремния 4.кислорода
13.Магнитное квантовое число может принимать значения…
1.1,2,3,…,∞ 2. 0,…,(n-1) 3. —ℓ,…0,…,ℓ 4. ±1/2
14. Неспаренные электроны в основном состоянии содержит частица…
1.Zn2+ 2.Ni2+ 3.Ca2+ 4.Ba2+
15. Число неспаренных электронов в атоме алюминия в основном состоянии равно
1)1 2)2 3)3 4)0
16. Сульфид-иону соответствует электронная формула
1)
1s2 2s22р63s23р6 3)
1s
2)1s22s22р63s23р4 4)1s2 2s2 2р63s23р2
17. Электронная конфигурация 1s22s22р63s23р6 соответствует иону ‘
Электронная конфигурация 1s22s22р63s23р6 соответствует иону ‘
1)Sc2+ 2) Al3+ 3)Cr3+ 4) Ca2+
18. На 4s-энергетическом подуровне расположены все валентные электроны атома
1) железа 2) кальция 3) углерода 4) серы
19. Атом элемента, максимальная степень окисления которого +4, в основном состоянии имеет электронную конфигурацию внешнего энергетического уровня
1) 3s23р4 2)2s2
2р2 3)2s22р4 4) 2s22р620. Электронную формулу 1s22s22р63s23р64s2 имеет атом элемента
1) Ba 2) Mg 3) Са 4) Sr
Ответы
к тестовым заданиям к приложению1: 1.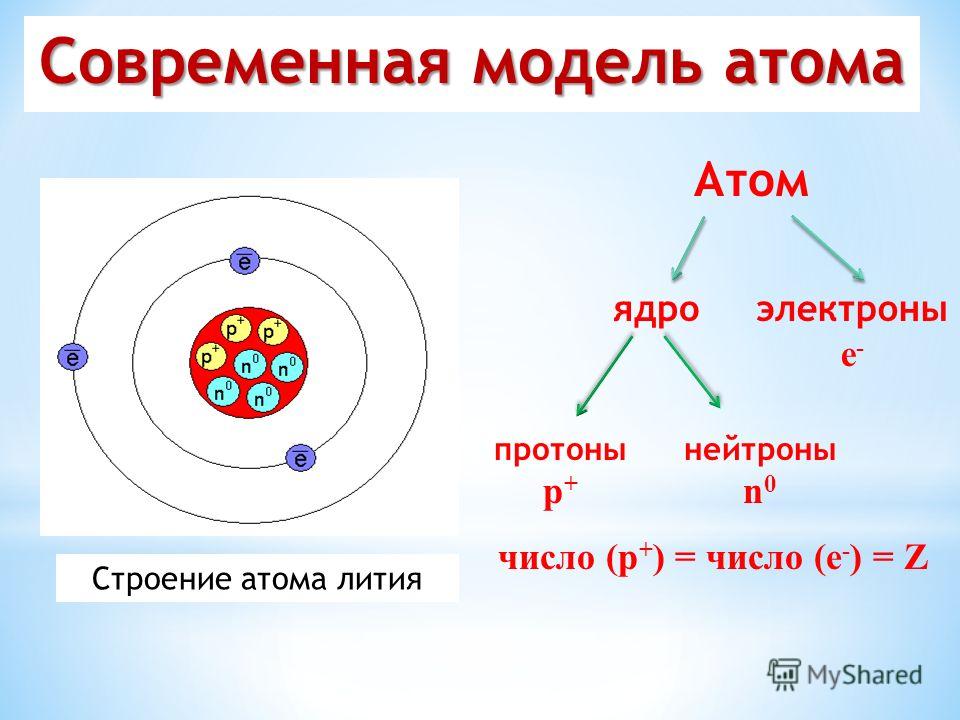 1;
2.3;3.2;4.4;5.1;6.2;7.2; 8.3; 9.4; 10.3; 11.1; 12.2; 13.3; 14.2;
15.1; 16.1; 17.4; 18.2; 19.2;20.3
1;
2.3;3.2;4.4;5.1;6.2;7.2; 8.3; 9.4; 10.3; 11.1; 12.2; 13.3; 14.2;
15.1; 16.1; 17.4; 18.2; 19.2;20.3
Ковалентная связь – связь, образованная за счет общей электронной пары.
Важнейшие характеристики химической связи: длина, энергия, полярность и поляризуемость. Энергия связи – это энергия, выделяющаяся при образовании связи или необходимая для разъединения двух связанных атомов. Длина связи – это расстояние между центрами связанных атомов Полярность связи
 Причиной полярности связи служит
различие в электроотрицательностях
связанных атомов. Электроотрицательность
– мера способности атома смещать к себе
электронную плотность химической связи. С увеличением электроотрицательности
атома возрастает степень смещения в
его сторону электронов связи.
Шкала
электроотрицательности по Полингу
Причиной полярности связи служит
различие в электроотрицательностях
связанных атомов. Электроотрицательность
– мера способности атома смещать к себе
электронную плотность химической связи. С увеличением электроотрицательности
атома возрастает степень смещения в
его сторону электронов связи.
Шкала
электроотрицательности по Полингу Элемент | K | Na | H | P | C | S | I | Br | Cl | N | O | F |
О. | 0,8 | 0,9 | 2,1 | 2,1 | 2,5 | 2,5 | 2,8 | 3,0 | 3,0 | 3,5 | 4,0 |
∆э.о.=0 – ковалентная неполярная связь
∆э.о.≤ 0,4 – малополярная ковалентная связь
∆э.о.>0,5 – сильно полярная ковалентная связь
∆э.о.> 2,0 – ионная связь
Поляризуемость связи выражается в смещении электронов связи под влиянием внешнего электрического поля, в том числе и другой реагирующей частицы. Поляризуемость π-связи выше, т.к. π-электроны находятся дальше от ядра и более подвижны.
Классификация ковалентной связи по типу перекрывания электронных облаков
Поскольку
электронные облака имеют различную
форму, их взаимное перекрывание может
осуществляться разными способами.
-связь осуществляется при лобовом перекрывании орбиталей вдоль линии, соединяющей центры атомов. Все одинарные связи являются -связями.
-связь возникает при боковом перекрывании р-орбиталей по обе стороны от линии соединения ядер атомов.
Например, возникновение π-связи в молекуле этилена СН2=СН2:
Или, например, в молекуле азота одна -связь и две -связи.
Электроны s-орбиталей могут участвовать лишь в -связывании, а р-электроны – как в -, так и в -связывании.
-связи
являются энергетически самыми выгодными
связями, т.к. имеет место глубокое
перекрывание облаков. Если между двумя
атомами возникает единственная связь,
то непременно -связь.
-связи возникают в том случае, если между двумя атомами образуются кратные связи (двойные или тройные). Например, в молекуле СО2 атом углерода образует с каждым атомом кислорода одну -связь и одну -связь:
| Меченые атомыRadioactive tracers Меченые атомы (изотопные индикаторы) – изотопы, при добавлении в исследуемые объекты способные
выполнять роль индикаторов, выявляющих особенности поведения атомов химических
элементов, молекул и других химических соединений в этих объектах. См. также
|
Сколько нейтронов содержится в ядре атома фосфора?
Последняя обновленная дата: 19 февраля 2023 г.
•
Всего просмотров: 236,7K
•
Просмотр сегодня: 7.24K
Ответ
Проверено
236,7K+ просмотры
HINT:
202 236,7K+ Views
HINT: 20202 236,7K+ Views
HINT: 2020202 236,7K+
: 20202 236,7K+. числа нейтронов, присутствующих в ядре атома фосфора, мы должны знать об атомном номере и массовом числе атома фосфора. Зная, что будет легко вычислить количество нейтронов, присутствующих в атомах фосфора.
числа нейтронов, присутствующих в ядре атома фосфора, мы должны знать об атомном номере и массовом числе атома фосфора. Зная, что будет легко вычислить количество нейтронов, присутствующих в атомах фосфора.
Полный ответ:
Сначала давайте посмотрим, что такое атом. Вся материя состоит из мельчайших частиц, которые называются атомами. В атомах присутствуют субатомные частицы, такие как протоны, нейтроны, электроны. Атом состоит из ядра, вокруг которого вращаются электроны. Ядро атома состоит из протонов и нейтронов. Протоны и нейтроны вместе называются нуклонами.
Давайте сначала разберемся с атомным номером. Атомный номер — это общее количество электронов или протонов, присутствующих в атомах, и он представлен символом Z.
Теперь давайте перейдем к массовому числу. Массовое число — это общее количество протонов и нейтронов, вместе присутствующих в ядре атома, и оно обозначается символом A.
Теперь давайте рассмотрим атом фосфора. Фосфор имеет атомный номер 15 и массовое число 31.

 э.о.
э.о. Боттомоний
Боттомоний Чармоний
Чармоний
 Этот изотоп (32Р)
бета-радиоактивен и распадается, испуская электроны с периодом полураспада
14.3 дня. Таким образом, роль фосфора в исследуемом биологическом объекте
(его миграция, локализация, накопление и выход) можно установить, регистрируя
детекторами электроны распада 32Р.
Этот изотоп (32Р)
бета-радиоактивен и распадается, испуская электроны с периодом полураспада
14.3 дня. Таким образом, роль фосфора в исследуемом биологическом объекте
(его миграция, локализация, накопление и выход) можно установить, регистрируя
детекторами электроны распада 32Р.