Видео с вопросами: Определение химического уравнения с символами состояний, которое соответствует химическому утверждению
Стенограмма видео
Твердый карбонат кальция разлагается при нагревании с образованием углекислого газа и твердого оксида кальция. Какой из перечисленных символических уравнения с символами состояния описывает эту химическую реакцию? (A) Газ CaCO3 вступает в реакцию с образованием CaO газ плюс CO2 твердый. (B) Твердое вещество CaCO3 реагирует с образованием CaO твердое вещество плюс газ CO2. (C) Твердое вещество Ca2CO3 реагирует с образованием CaO газ плюс угарный газ. (D) Реакция твердого вещества CaCO3 и газообразного O2 с образованием твердого CaO и газообразного CO2. (E) Реакция твердого CaCO3 и газообразного CO2 с образованием твердого CaO.
Первое предложение в этом вопросе
является химическим утверждением. Химическое утверждение описывает
химическая реакция словами. С другой стороны, ответ
выборы являются символическими уравнениями. Символьные уравнения, также известные как
химические уравнения, используйте химические символы для обозначения реакции. Например, мы видим CaCO3 в
несколько вариантов ответа. Ca — это химический символ,
представляет собой элемент кальция. C — химический символ, который
представляет собой углерод. А О — это химический символ, который
представляет собой кислород. Три — это индекс, который говорит
нам, сколько определенного типа атома присутствует. В целом, CaCO3 является химическим
формула.
Химическое утверждение описывает
химическая реакция словами. С другой стороны, ответ
выборы являются символическими уравнениями. Символьные уравнения, также известные как
химические уравнения, используйте химические символы для обозначения реакции. Например, мы видим CaCO3 в
несколько вариантов ответа. Ca — это химический символ,
представляет собой элемент кальция. C — химический символ, который
представляет собой углерод. А О — это химический символ, который
представляет собой кислород. Три — это индекс, который говорит
нам, сколько определенного типа атома присутствует. В целом, CaCO3 является химическим
формула.
Химические формулы в символах
за уравнениями также могут следовать символы состояния. Буква s, l или g пишется
в круглых скобках, чтобы сказать, является ли вещество в реакции твердой жидкостью или
газ.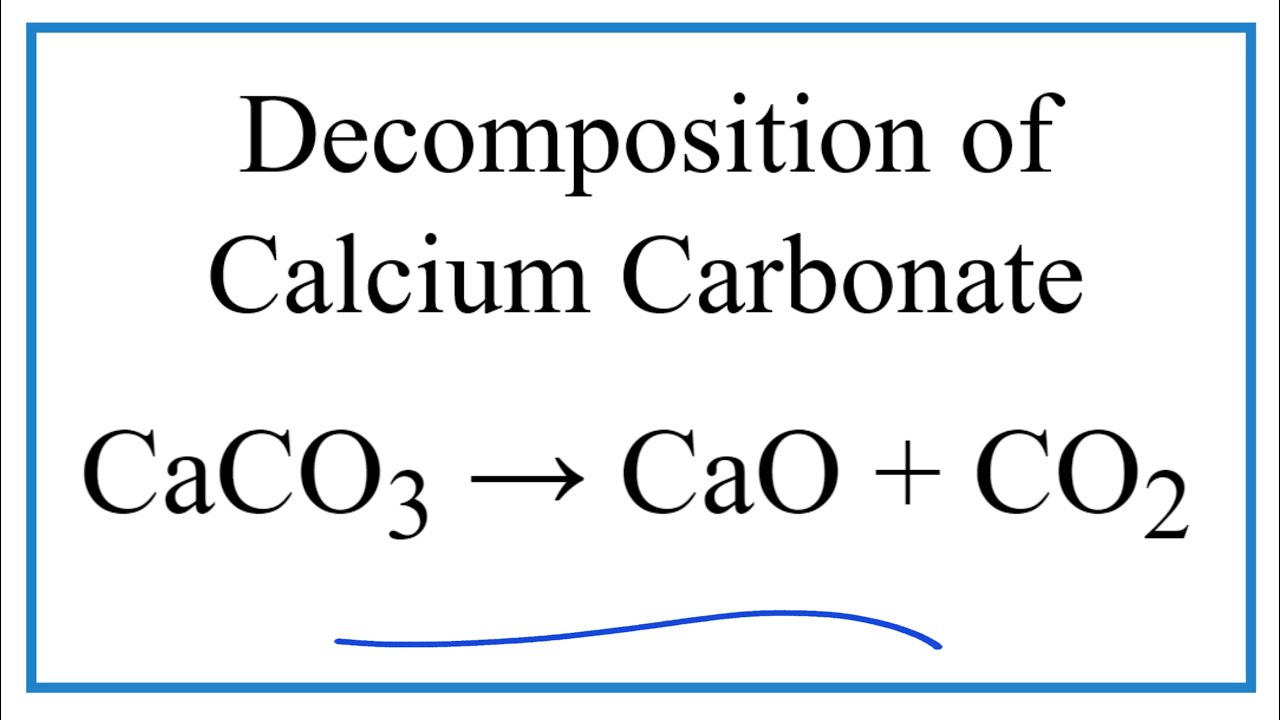 Наша задача ответить на этот вопрос
состоит в том, чтобы взять представленную химическую формулировку и перевести ее в правильную символическую форму.
уравнение. В предоставленном химическом заявлении,
мы можем определить слово «разлагает» как ключевое слово. Химические виды, появляющиеся на
слева от ключевого слова находятся реагенты химической реакции. Только один вид, кальций
карбонат, появляется слева от ключевого слова. Это означает, что химический
реакция имеет только один реагент.
Наша задача ответить на этот вопрос
состоит в том, чтобы взять представленную химическую формулировку и перевести ее в правильную символическую форму.
уравнение. В предоставленном химическом заявлении,
мы можем определить слово «разлагает» как ключевое слово. Химические виды, появляющиеся на
слева от ключевого слова находятся реагенты химической реакции. Только один вид, кальций
карбонат, появляется слева от ключевого слова. Это означает, что химический
реакция имеет только один реагент.
При изучении вариантов ответа (D) и (E), мы видим, что в левой части каждого уравнения используется знак плюс. Это говорит нам о том, что есть два реагенты. Правильное символьное уравнение может содержат только один реагент. Таким образом, мы можем устранить эти два варианты ответов, потому что они содержат слишком много реагентов.
Продолжим читать
химическое заявление. «Производство» — еще одно ключевое слово.
что свидетельствует о том, что реагент образует продукты. Справа от этого ключевого слова мы
может найти слова, которые представляют продукты. Углекислый газ и твердый кальций
оксида разделены словом «и», что означает наличие двух разных
продукты, образующиеся в результате реакции.
«Производство» — еще одно ключевое слово.
что свидетельствует о том, что реагент образует продукты. Справа от этого ключевого слова мы
может найти слова, которые представляют продукты. Углекислый газ и твердый кальций
оксида разделены словом «и», что означает наличие двух разных
продукты, образующиеся в результате реакции.
Давайте создадим базовое уравнение слова используя названия реагентов и продуктов. Слева от стрелки реакции, напишем карбонат кальция. И справа от реакции стрелка, напишем углекислый газ плюс оксид кальция. Химическое утверждение говорит нам о состояния двух видов, участвующих в реакции. И карбонат кальция, и кальций оксид – это твердое вещество. И хотя он не включен в химическом утверждении мы ожидаем, что углекислый газ будет газом.
Перепишем наше основное слово
уравнение, используя правильные символы состояния. После карбоната кальция и кальция
оксид, мы напишем «s» внутри скобок. И после углекислого газа мы
напишите букву «г» внутри скобок.
После карбоната кальция и кальция
оксид, мы напишем «s» внутри скобок. И после углекислого газа мы
напишите букву «г» внутри скобок.
Наконец-то мы сможем узнайте, что химическая формула углекислого газа – CO2. Давайте продолжим и заменим слова «углекислый газ» с CO2 в нашем уравнении. Мы можем исключить выбор (A) потому что символ штата рядом с карбонатом кальция и оксидом кальция должен быть «s» для твердого тела. Кроме того, государственный символ рядом с CO2 должно быть «g» для газа. Вариант (А) не является правильным ответом выбор, потому что символьное уравнение содержит неправильные символы состояния.
Мы также можем исключить выбор ответа
(C) потому что символ состояния рядом с оксидом кальция должен быть «s» для твердого вещества, а не «g»
для газа. В дополнение к этому неправильному состоянию
означает, что химическая формула углекислого газа неверна. В этом уравнении записывается как
CO — химическая формула угарного газа.
В этом уравнении записывается как
CO — химическая формула угарного газа.
Остается только выбор ответа (B), что является нашим правильным выбором ответа. Вариант ответа (В) правильный символьное уравнение с символами состояния, которое соответствует химическому утверждению, представленному в вопрос.
атомная масса Ca = 40, C = 12, O = 16)
Вопрос
Обновлено: 26.04.2023 видео
РЕКЛАМА
লিখিত জবাব
Подтверждено экспертами CaCO3(s)тепло−−→ CaO(s)+ CO2(g)Карбонат кальция Оксид кальцияДвуокись углерода 1 молекула 1 молекула 1 молекула 1 моль 1 моль 1 моль40+12+ 48=100г 40+ 16=56g 12+32=44g
Информация, собранная из приведенных данных, может быть резюмирована следующим образом:
(i) Карбонат кальция, также называемый известняком, при нагревании разлагается с образованием оксида кальция и диоксида углерода.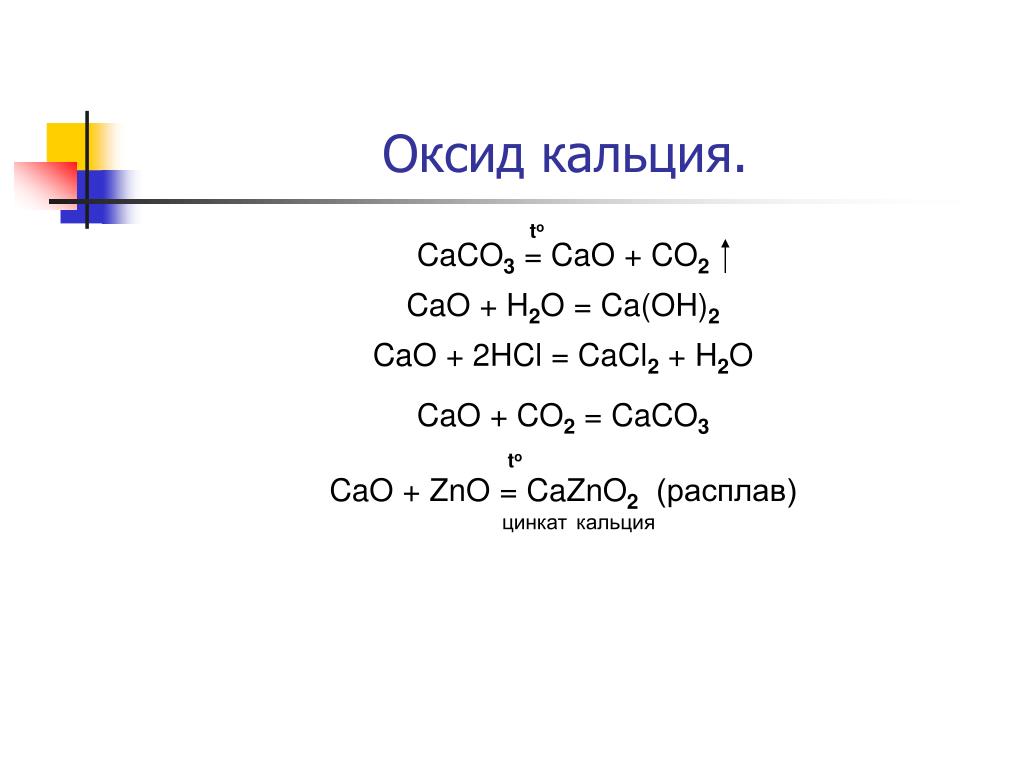
(ii) С точки зрения символьного уравнения, CaCO3(s) разлагается с образованием CaO(s) и CO2g.
(iii) 1 молекула CaCO3 распадается на 1 молекулу CaO и 1 молекулу CO2.
(iv) 1 моль CaCO3 разлагается на 1 моль CaO и 1 моль CO2.
(v) 100 г CaCO3 разлагаются на 56 г CaO и 44 г CO2.
Был ли этот ответ полезен?
698
Аб Падхаи каро бина адс ке
Khareedo DN Про и дехо сари видео бина киси объявление ки рукаават ке!
সংশ্লিষ্ট ভিডিও
Для реакции : CaCO_(3) (s) hArr CaO (s) + CO_(2) (g)
3070 7541
Карбонат кальция разлагается при нагревании по следующим уравнениям: CaCO_(3 )(s) Leftrightarrow CaO(s)+CO_(2)(g) Сколько молей CO_(2) получится при разложении 50 г CaCO_(3) ?
34507031
75 ग्राम CaCO3 को ग्राम करने पर उत्पन्न CO2 का Н.Т.П. पर आयतन व मात्रा ज्ञात करो ।
(दिया है : Ca=40,C=12,O=16)
142060462
Какая масса CaO получится при нагревании 3 молей CaCO3? [Атомная масса Ca=40]
203078763
CaCO3 реагирует с HCl с образованием CaCl2, CO2 и h3O. Приблизительная масса (в г) CaCO3, необходимая для полной реакции с 25 мл 0,75 М HCl, составляет (атомная масса Ca=40, C=12O=16, Cl=35,5 и H=1)
Приблизительная масса (в г) CaCO3, необходимая для полной реакции с 25 мл 0,75 М HCl, составляет (атомная масса Ca=40, C=12O=16, Cl=35,5 и H=1)
233092353
Что такое количество тепла, необходимое для получения 128 г CaCO3 с использованием CaCO3 и последующим восстановлением углеродом. Реакции
CaCO3(т)=CaO(т)+CO2(г),ΔH∘=42,8 ккал
CaO(т)+3C(т)=CaC2+CO(г),ΔH∘=111 ккал
328699379
Предсказать знак ΔS для реакции :
CaCO3(s)Δ−−→CaO(s)+CO2(g)
435647894
Напишите значение Kp и уравнение KC для CaCO3(s)⇔CaO(s)+CO2 (g)
508091020
Text Solution
Назовите тип химической реакции, представленный следующими уравнениями: CaCO_(3)(s)overset(«Heat»)(to)CaO(s)+CO_(2)( ж)
571116073
Text Solution
Назовите тип химической реакции, представленной следующими уравнениями:
CaCO3(s)Heat—→CaO(s)+CO2(g)
571116167
Text Solution
At 1000 K in 0,654 Сосуд L CaCO3(s) берется.
