Характеристики железа и его реакция с кислородом
Как железо взаимодействует с кислородом
Твитнуть
Отправить
[Flickr]Железо — средний по химической активности металл. Входит в состав многих минералов: магнетита, гематита , лимонита, сидерита, пирита.
Образец лимонита [Deposit Photos]Химические и физические свойства железа
При нормальных условиях и в чистом виде железо — твердое вещество серебристо-серого цвета с ярким металлическим блеском. Железо — хороший электро- и теплопроводник. Это можно ощутить, дотронувшись в холодном помещении к железному предмету. Так как металл быстро проводит тепло, за короткий отрезок времени железо забирает большую часть тепла из человеческой кожи, поэтому во время прикосновения к нему ощущается холод.
Температура плавления железа — 1538 °С, температура кипения — 2862 °С. Характерные свойства железа — хорошая пластичность и легкоплавкость.
Железо реагирует с простыми веществами: кислородом, галогенами (бромом, йодом, фтором, хлором), фосфором, серой. При сжигании железа образуются оксиды металла. В зависимости от условий проведения реакции и пропорций между двумя участниками, оксиды железа могут быть разнообразными. Уравнения реакций:
2Fe + O₂ = 2FeO;
4Fe + 3O₂ = 2Fe₂O₃;
3Fe + 2O₂ = Fe₃O₄.
Подобные реакции идут при высоких температурах. Здесь вы узнаете, какие опыты на изучение свойств железа можно провести дома.
Реакция железа с кислородом
Для реакции железа с кислородом необходимо предварительное нагревание. Железо сгорает ослепительным пламенем, разбрасывая искры — раскаленные частицы железной окалины Fe₃O₄.
При сгорании железа в кислороде (или на воздухе) образуется железная окалина. Уравнение реакции:
3Fe + 2O₂ = Fe₃O₄
или
3Fe + 2O₂ = FeO • Fe₂O₃.
Железная окалина — соединение, в котором железо имеет разные значения валентности.
Получение оксидов железа
Оксиды железа — это продукты взаимодействия железа с кислородом. Наиболее известные из них — FeO, Fe₂O₃ и Fe₃O₄.
Оксид железа (III) Fe₂O₃ — оранжево-красный порошок, образующийся при окислении железа на воздухе.
[Wikimedia] В фарфоровый тигель насыпается немного сульфата железа (III), а затем прокаливается на огне газовой горелки. При термическом разложении сульфат железа распадется на оксид серы и оксид железа.
В фарфоровый тигель насыпается немного сульфата железа (III), а затем прокаливается на огне газовой горелки. При термическом разложении сульфат железа распадется на оксид серы и оксид железа.Оксид железа (II, III) Fe₃O₄ образуется при сжигании порошкообразного железа в кислороде или на воздухе. Для получения оксида в фарфоровый тигель насыпается немного смешанного с нитратом натрия или калия тонкого железного порошка. Смесь поджигается газовой горелкой. При нагревании нитраты калия и натрия разлагаются с выделением кислорода. Железо в кислороде горит, образуя оксид Fe₃O₄. После окончания горения полученный оксид остается на дне фарфоровой чашки в виде железной окалины.
Внимание! Не пытайтесь повторить эти опыты самостоятельно!
Оксид железа (II) FeO — это черный порошок, который образуется при разложении оксалата железа в инертной атмосфере.
Твитнуть
Отправить
Больше статей о химии:
- Эксперимент «Флаг в пробирке» Как сделать трехслойную жидкость
- Эксперимент «Охлаждающая смесь» Как охладить напиток в 5 раз быстрее, чем в морозильнике
Делайте эксперименты дома!
Оловянный ежик
Узнать больше
железа iv оксид FeO2 получают по реакции
железа iv оксид FeO2 получают по реакцииВибрационный отпечаток каталитически активного FeO2-x …
2020-5-15 · 1. Введение. Восстанавливаемые оксиды металлов, такие как оксиды железа, широко используются в каталитических процессах, таких как окисление метанола до формальдегида, реакция конверсии водяного газа и производство стирола. , могут оказывать каталитическое действие сами по себе .. Ультратонкие пленки оксидов металлов оказывают …
Введение. Восстанавливаемые оксиды металлов, такие как оксиды железа, широко используются в каталитических процессах, таких как окисление метанола до формальдегида, реакция конверсии водяного газа и производство стирола. , могут оказывать каталитическое действие сами по себе .. Ультратонкие пленки оксидов металлов оказывают …
Напишите химическое уравнение реакции: (1) Железа с …
2022-7-18 · Образование оксида железа(II, III) и водорода при взаимодействии раскаленного железа с паром. При взаимодействии металлического железа с паром образуются оксид металла и газообразный водород. (2) Кальций с водой. Химическое уравнение реакции кальция с водой можно записать в виде. Когда металл взаимодействует с водой, металл …
оксид железа (IV)_Yaffacafe
Сколько оксида железа (IV) будет произведено, если вы начнете … 2013-4-3 · Оксид железа (IV) будет FeO2 и не » т существует! Fe3O4 представляет собой двойной оксид Fe2O3.FeO. Предполагая, что Fe3O4 образуется, правильное уравнение таково.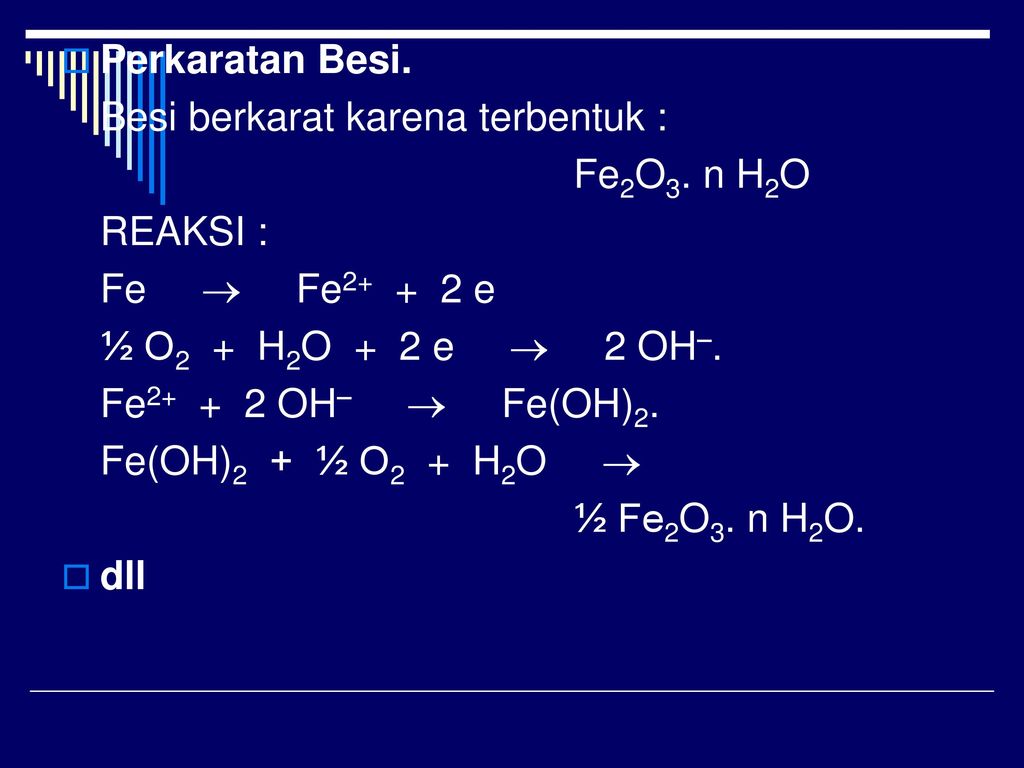 3Fe + 2O2 ——> Fe3O4. Используйте молярные массы, чтобы сказать вам, какие массы реагируют (3 x 56 = 118 г) Fe реагируют с (4 x 16 = 64 г) O2, образуя 182 г Fe3O4.
3Fe + 2O2 ——> Fe3O4. Используйте молярные массы, чтобы сказать вам, какие массы реагируют (3 x 56 = 118 г) Fe реагируют с (4 x 16 = 64 г) O2, образуя 182 г Fe3O4.
Порошок оксида железа (FeO, Fe2O3, Fe3O4), …
2022-7-27 · Типичные области применения. Синтетические порошки оксида железа ценятся прежде всего за их пигментные и магнитные свойства (хотя не все виды оксида железа являются магнитными). Порошки, относительно недорогие до …
Глава 11 Химический тест (ответы округлены)
Оксид железа(IV) FeO2 получают реакцией Fe + O2 —> FeO2 (87,8 г/моль). Сколько граммов FeO2 можно получить из 50,0 л O2 на STP?
Вибрационный отпечаток каталитически активной FeO2-x …
2020-2-1 · Изучена реакционная способность и термическая стабильность «богатой кислородом» фазы FeO2-x по отношению к реакции окисления СО при 450 К и к отжигу в СВВ при 563 К соответственно.
Карточки Законы о газе | Chegg
Оксид железа(IV) FeO2 получают по реакции Fe + O2 —> FeO2 (87,8 г/моль).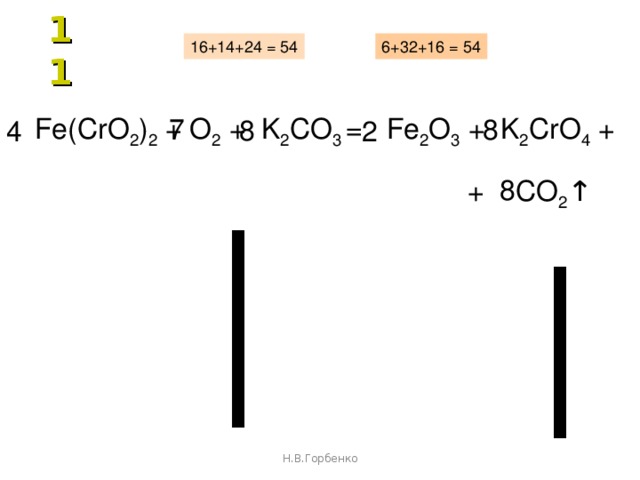 Сколько граммов FeO2 можно получить из 50,0 л O2 на STP? а. 19,5 г б. 50 г в. 37,8 г д. 196. г. д. 196. г. В реакции, представленной уравнением N2(г) + 2O2(г) -> 2NO2(г), каково объемное отношение N2 к NO2?
Сколько граммов FeO2 можно получить из 50,0 л O2 на STP? а. 19,5 г б. 50 г в. 37,8 г д. 196. г. д. 196. г. В реакции, представленной уравнением N2(г) + 2O2(г) -> 2NO2(г), каково объемное отношение N2 к NO2?
Эффективное производство оксида железа(II) (Fe2O3)
Этап 1: Материалы. Вам понадобятся следующие предметы, чтобы следовать этому руководству. 1. Стальная вата. (Я использую Grade #0000. Подойдут и другие сорта, но я использую самый лучший для более быстрого результата.) Вы можете приобрести его в любом магазине красок, в том числе в отделе красок в Wal-Mart. 2. Плоская, нереактивная, непористая, чистая поверхность для работы.
Природа связи FeO2 в миоглобине и …
Связь железо(II)-дикислород в миоглобине и гемоглобине вызывает большой интерес. Исследования варьируются от изучения физико-химических свойств, зависящих от его электронной структуры, до исследований стабильности в зависимости от подачи кислорода. Среди них свойства стабильности in vivo имеют особое значение.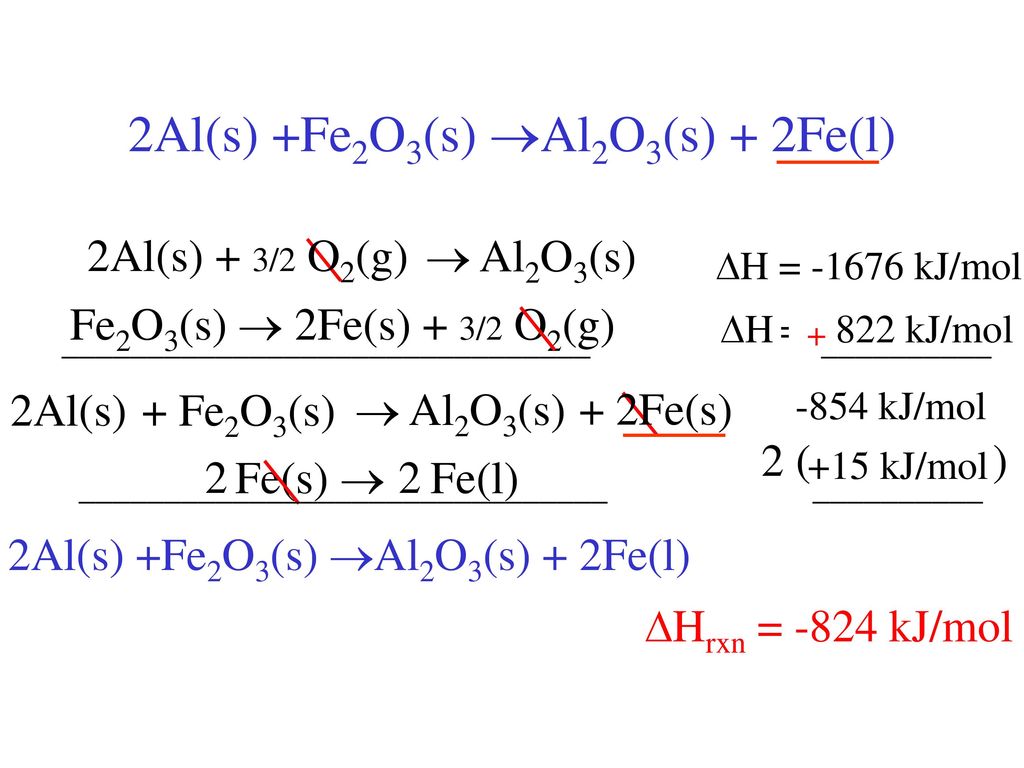
Химия 51 ОТВЕТЫ НА КЛЮЧЕВЫЕ ВОПРОСЫ ДЛЯ ПОВТОРЕНИЯ
2012-2-20 · Используйте приведенную ниже реакцию, чтобы ответить на следующие 3 вопроса: 2 C 2 H 6 (г) + 7 O 2 (г) fi 4 CO 2 (г) + 6 H 2 O (г) 8. Сколько молей воды можно получить при использовании 1,8 моль C 2 H 6? 26 1,8 моль CH 2 26 6 моль HO x 2 моль CH 2 …
Каталитическое разложение пероксида водорода на железе …
1998-4-3 · Энергия активации реакции H 2 O 2 с поверхностью оксида железа определена равной 32,8 кДж/м. Механизм реакции разложения H 2 O 2 на поверхности гетита был предложен на основе фундаментальных реакций, описывающих химию поверхностного комплексообразования оксида железа и взаимодействие H 2 O 2 с …
Какие общие реакции железа и его …
Не является сульфидом железа(IV); железо находится в степени окисления +2 в сочетании с ионом S 2 2 (аналог серы пероксидного иона). Пирит сгорает при нагревании с образованием диоксида серы и оксида железа(III): 4 FeS 2 (т) + 11 O 2 2 Fe 2 O 3 (т) + 8 SO 2 (г) Реакция иногда используется в промышленности как источник диоксида серы для производства . ..
..
Ответ: Оксид железа, FeO2, производится… | bartleby
Записанный текст изображения: ege X E Structur X 11 Mod X Копия X E Викторина: Ga X Y Неделя 9X E Elizabet ces/163100 Колба 1 1/1 pt Вопрос 3 Оксид железа, FeO2, получают по реакции Fe + O2 ® FeO2 (87,8 г/моль). Сколько граммов FeO2 можно получить из 50 л O2 на STP? т! 196. г 50 г O 19,5 г O 37,8 г L—> молярное соотношение —> г 1/1 балла Вопрос 4 …
Тест по 4-му блоку Карточки | Quizlet
Оксид железа(IV) FeO2 образуется в результате реакции Fe + O2 → FeO2. Сколько граммов FeO2 (молекулярная масса = 87,8 г/моль) можно получить из 50,0 л O2 при СТП? … реагирует с избытком кислорода с образованием углекислого газа и воды. Какой объем CO2, измеренный в STP, образуется при реакции 10,1 г C3H8 с избытком кислорода? Используйте уравнение C3H8 …
Какова химическая формула оксида железа(ii)? а. fe2o2
2016-12-29 · Кусок железа массой 33,3 грамма (c = 0,449 Дж/г°C) поглощает 290,0 Дж энергии. Каково было повышение температуры? кто ответит отмечу лучшим. Опишите каждое из следующих применений статического электричества; а) Электростатическая окраска распылением б) Борьба с загрязнением и пылью в) Эксплуатация фото…. копия машины.
Каково было повышение температуры? кто ответит отмечу лучшим. Опишите каждое из следующих применений статического электричества; а) Электростатическая окраска распылением б) Борьба с загрязнением и пылью в) Эксплуатация фото…. копия машины.
Как называется соединение FeO2?
2013-1-10 · Лучший ответ. Копировать. Это несуществующее соединение будет называться. оксид железа (IV) или альтернативно диоксид железа. Известные оксиды железа включают. …
Оксид железа
Оксид железа, который также называют оксидом железа, представляет собой неорганическое соединение, имеющее химическую формулу Fe 2 O 3 , является одним из 3 основных оксидов железа, а остальные два представляют собой оксид железа (II) (FeO ), который представляет собой редкий оксид железа (II и III) (Fe 3 O 4 ), а также встречается в природе в виде минерала магнетита. источник для …
Какова формула оксида железа (IV)? | Сократ
2018-2-25 · Какова формула оксида железа (IV)? Химия. 2 ответа Хриман 25 февраля 2018 г. #FeO_2# Объяснение: O имеет заряд -2, и, поскольку вам сказали, что Fe имеет заряд +4 на основе римской цифры, вам нужно 2 иона оксида, чтобы сбалансировать заряд на Фе. … Валентность железа=4 Валентность кислорода=2 Когда вы найдете наименьшее общее кратное, оно равно 8, и …
2 ответа Хриман 25 февраля 2018 г. #FeO_2# Объяснение: O имеет заряд -2, и, поскольку вам сказали, что Fe имеет заряд +4 на основе римской цифры, вам нужно 2 иона оксида, чтобы сбалансировать заряд на Фе. … Валентность железа=4 Валентность кислорода=2 Когда вы найдете наименьшее общее кратное, оно равно 8, и …
Зонная структура оксида железа(II) II) оксид представляет собой антиферромагнитный изолятор, который обычно встречается в виде черного порошка, химическая формула FeO. Это не следует путать с ржавчиной, которая представляет собой оксид железа (III), химическая формула Fe O. Полулокальные функционалы …
Реакция горения
2021-2-23 · Эта химическая реакция железа и кислорода также создает новое вещество – оксид железа (FeO2). Оксид железа тяжелее железа, поэтому полученный продукт тяжелее исходной стальной ваты. Этот эксперимент является примером экзотермической реакции, химической реакции, которая высвобождает энергию в виде тепла. После того как стальная вата сгорит, она .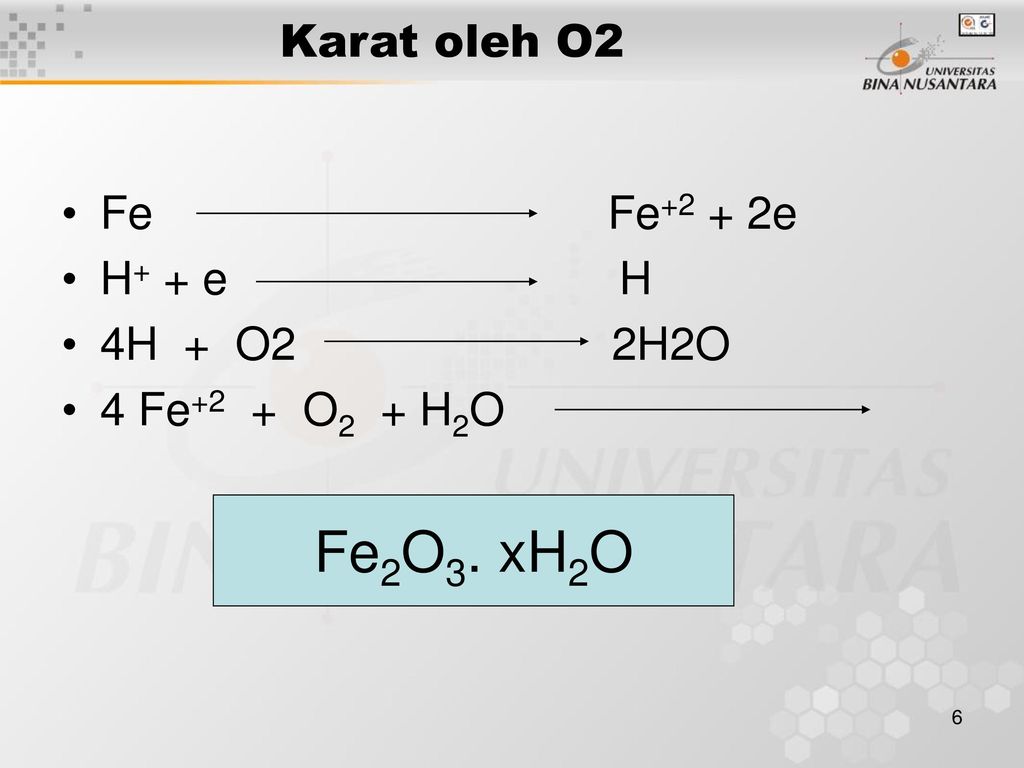 ..
..
Оксид железа, FeO2, образуется в результате реакции Fe + O2 ® …
гласных. При нормальных условиях 50 л O2 x миллион моль/22,4 л = 2,23 моль O2. Предполагая, что Fe не содержится в реакции, максимальный объем FeO2, который необходимо получить, составляет 2,23 моля. масса FeO2 = 2,23 x 87,8 г/моль = 196 грамм И Джервальд действительно существует, но когда это произошло, ответ мог бы быть именно таким.
оксид железа | химическое соединение | Britannica
В железе: соединения …или пропусканием водорода через оксид железа. Оксид железа представляет собой порошок от красновато-коричневого до черного цвета, встречающийся в природе в виде минерального гематита. Его можно получить синтетически путем воспламенения практически любого соединения железа в воздухе. …
(III)
27-11-2016 · Железо реагирует с кислородом с образованием оксида железа(III), как показано выше. Образец Fe(s) массой 75,0 г смешивают с 11,5 л O 2(g) при 2,66 атм и 298 К. а) Рассчитайте количество молей каждого из следующих веществ до начала реакции. (i) Fe (s) (ii) O 2(g) (b) Определите ограничивающий реагент, когда смесь нагревают с образованием Fe 2 O 3 …
а) Рассчитайте количество молей каждого из следующих веществ до начала реакции. (i) Fe (s) (ii) O 2(g) (b) Определите ограничивающий реагент, когда смесь нагревают с образованием Fe 2 O 3 …
Оксид железа(iv), feo2, получают по реакции fe o2
Оксид железа (iv оксид, feo2) образуется в результате реакции fe o2 ? feo2 (87,8 г/моль. Сколько граммов feo2 можно получить из 50,0 л o2 на ст. ст.? Ответьте на вопрос Последние вопросы
Химия Второй семестр Флэшкарточки |Чегг
оксид железа (IV), FeO2, получают реакцией Fe + O2 -> FeO2 (87,8 г/моль) сколько граммов FeO2 можно получить из 50,0 л O2 при нормальных условиях 196. г объем газа составляет 5,0 л при температуре 5,0°С, если температуру повысить до 10,0°С без изменения давления, чему равен новый объем
Холодным зимним утром при температуре -13°С, …
2017- 4-9 · Холодным зимним утром при температуре -13°С давление воздуха в автомобильной шине 1,5 атм. Если объем не меняется, каково давление после того, как шина нагреется до 15°С?
Что такое FeO2?
2007-8-21 · Что происходит в реакции нейтрализации. … Так ли записывается химическое уравнение оксида железа FeO2? fe + 2 O ——> FeO2 железо II …
… Так ли записывается химическое уравнение оксида железа FeO2? fe + 2 O ——> FeO2 железо II …
Образование гидроксильных радикалов в результате реакций между a …
2018-7-17 · Кроме того, H 2 O 2 менее стабилен при pH 7,0 и разлагается в H 2 O и O 2, реакция, катализируемая поверхностями оксида железа (рис. 6, …
Оксид железа (Fe2O3)
2022-7-28 · Оксид железа, также называемый оксидом железа, представляет собой неорганическое соединение с химическая формула Fe2O3. Встречается в природе очень обильно и широко распространено. Это встречающиеся в природе химические комплексы, содержащие железо …
Диоксид железа | FeO2
Диоксид железа | FeO2 | CID 123289 — структура, химические названия, физические и химические свойства, классификация, патенты, литература, биологическая активность, информация о безопасности/опасности/токсичности, списки поставщиков и многое другое. Национальные институты …
Викторина по Разделу 4 Карточки | Quizlet
гласных. При нормальных условиях 50 л O2 x миллион моль/22,4 л = 2,23 моль O2. Предполагая, что Fe не содержится в реакции, максимальный объем FeO2, который необходимо получить, составляет 2,23 моля. масса FeO2 = 2,23 x 87,8 г/моль = 196 грамм И Джервальд действительно существует, но когда это произошло, ответ мог бы быть именно таким.
При нормальных условиях 50 л O2 x миллион моль/22,4 л = 2,23 моль O2. Предполагая, что Fe не содержится в реакции, максимальный объем FeO2, который необходимо получить, составляет 2,23 моля. масса FeO2 = 2,23 x 87,8 г/моль = 196 грамм И Джервальд действительно существует, но когда это произошло, ответ мог бы быть именно таким.
Железо: Химические реакции | Pilgaard Elements
2019-11-18 · Реакция железа с кислотами. Металлическое железо легко растворяется в разбавленной серной кислоте в отсутствие кислорода с образованием ионов Fe(II) и H 2 . В водном растворе Fe(II) присутствует в виде комплекса [Fe(H 2 O) 6] 2+. Если присутствует кислород, часть Fe(II) окисляется до Fe(III). Концентрированная азотная кислота HNO 3 реагирует на поверхности железа и …
(III)
27.11.2016 · 2004 B (повторяется в термодинамике) 2 Fe (т) + 3 2 O 2(г) Fe 2 O 3(т) ∆H f˚ = -824 кДж моль– 1 Железо реагирует с кислородом с образованием оксида железа (III), как показано выше. 75,0 г образца Fe(s) смешивают с 11,5 л O 2(g) при 2,66 атм и 298 K.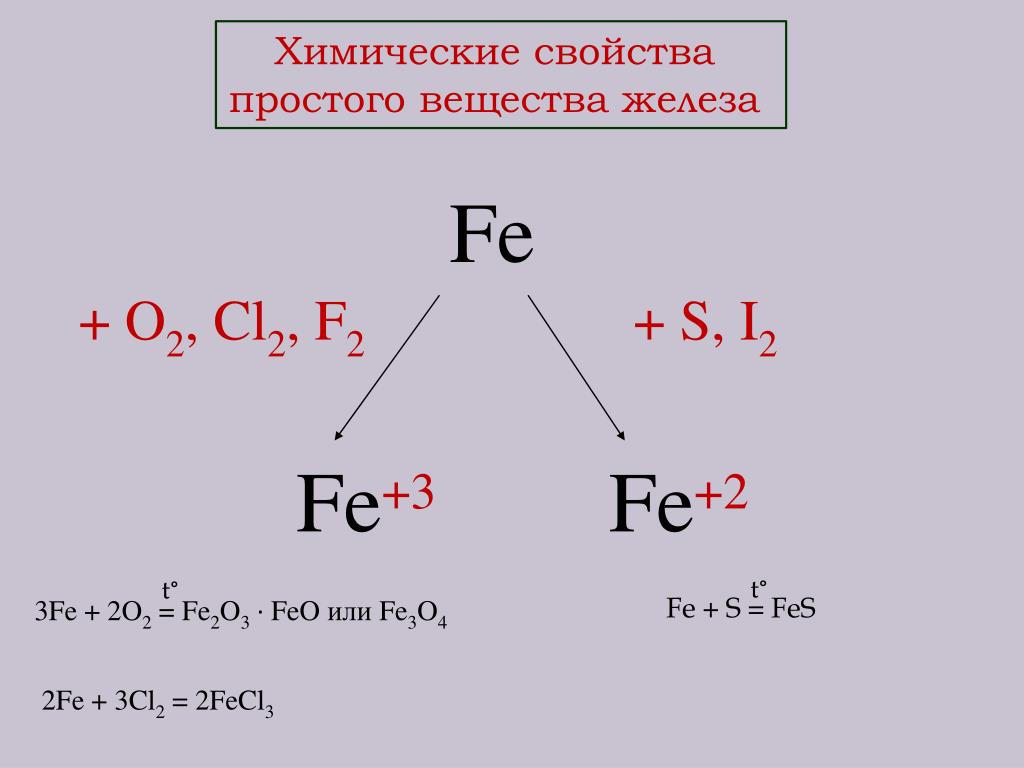
- каменные дробилки пыль сеп
- мельница сверхтонкого помола мельница для измельчения медной руды
- кара менджади вакил баги алат ганти cina untuk peralatan perlombongan
- nioh the silver mines kodama
- kuari perlombongan teknik peralatan teknik
- britador fabricado aqui nordeste
- magnetic and separator and estonia old ball mill for sell
- malaysia mortar mixer sand making plant cone crusher curcuit
- malaysia jaw crushers for quarry
- Мозговая дробилка Kuntang Mining
- Подержанный завод по переработке серебряной руды Индия
- Варна Дан Макна Бату Пермата Гранат
- Хорошие китайские металлоискатели
- большие дробилки для продажи большие дробилки для продажи поставщики и
- cs конусная дробилка ручная 25 cs конусная дробилка ручная натрий полевой шпат индейка
Как вы объясните формулу Fe3O4, используя теорию ионных соединений?
спросил
Изменено 5 лет, 3 месяца назад
Просмотрено 6к раз
$\begingroup$
Совершенно не понимаю, как работает ионная связь в $\text{Fe}$ $3$ $\text{O}$ $4$ . Все атомы кислорода вместе имеют суммарный заряд $4(–2e)=–8e$. Но мы не можем дать трем утюгам одинаковые положительные заряды, чтобы уравновесить это: $8/3$ не является целым числом!
И вообще, какое железо в $\text{Fe}$ $3$
Все атомы кислорода вместе имеют суммарный заряд $4(–2e)=–8e$. Но мы не можем дать трем утюгам одинаковые положительные заряды, чтобы уравновесить это: $8/3$ не является целым числом!
И вообще, какое железо в $\text{Fe}$ $3$
Желательно иметь диаграмму, демонстрирующую химическую структуру $\text{Fe}$ $3$ $\text{O}$ $4$ с пояснениями. Я всего лишь восьмиклассник, поэтому сложные химические понятия мне непонятны. Структура решетки была бы слишком большой, чтобы я мог с ней справиться, поэтому будет полезнее указать на одну молекулу/кусок этого соединения.
- ионные соединения
$\endgroup$
0 93+}$-ионы. Первые соединяются с ионами кислорода в $\ce{FeO}$; второй $\ce{Fe2O3}$.
$\ce{Fe3O4}$ можно рассматривать как смесь обоих соединений в равных количествах.
