Fe (железо) = Na2SO4 (сульфат натрия)
| Поиск |
железо = сульфат натрия
Новости Только 5% НАСЕЛЕНИЯ знают
Реклама
2 результатов найдено
Отображение уравнения от 1 до 2 Страница 1 — Пожалуйста, прокрутите до конца, чтобы увидеть больше результатов
Уравнение Результат #1
Нажмите, чтобы увидеть более подробную информацию и рассчитать вес/моль >>
Oxidation-reduction reaction
| → | sodium nitrate | water | сульфат натрия | азота монооксид | |||||||||
| 2 | 4 | 2 | 1 | 4 | 1 | 2 | Hệ số | ||||||
| Nguyên — Phân tử khối (g/mol) | |||||||||||||
| Сомол | |||||||||||||
| Хой лунг (г) |
Реклама
Further information about equation 2Fe + 4H
2 SO 4 + 2NaNO 3 → Fe 2 (SO 4 ) 3 + 4H 2 O + Na 2 SO 4 + 2NOКаковы условия реакции Fe (железо) вступает в реакцию с h3SO4 (серная кислота) вступает в реакцию с NaNO3 (нитрат натрия) ?
Для этого химического уравнения не найдено информации
Объяснение: идеальные условия окружающей среды для реакции, такие как температура, давление, катализаторы и растворитель.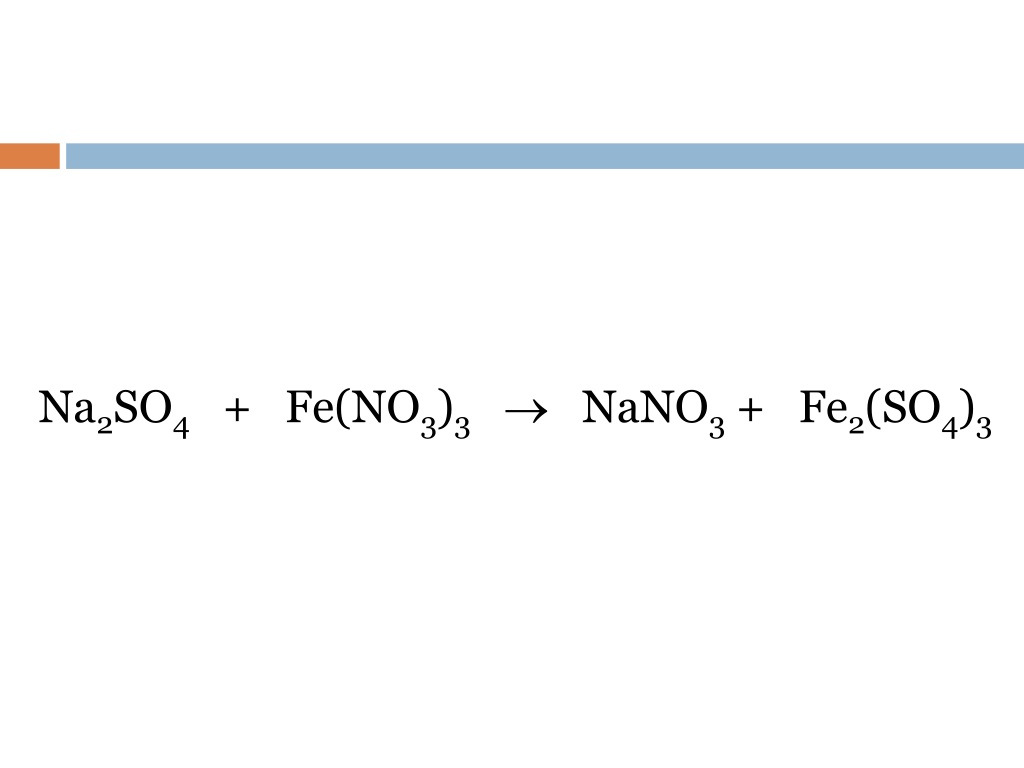 Катализаторы — это вещества, которые ускоряют темп (скорость) химической реакции, не потребляясь и не становясь частью конечного продукта.
Катализаторы не влияют на равновесные ситуации.
Катализаторы — это вещества, которые ускоряют темп (скорость) химической реакции, не потребляясь и не становясь частью конечного продукта.
Катализаторы не влияют на равновесные ситуации.
Как могут происходить реакции с образованием Fe2(SO4)3 () и h3O (вода) и Na2SO4 (сульфат натрия) и NO (моноксид азота)?
Явление после взаимодействия Fe (железа) с h3SO4 (серная кислота) с NaNO3 (нитрат натрия)
Это уравнение не несет никакой конкретной информации о явлении.
В этом случае вам просто нужно наблюдать, чтобы убедиться, что вещество продукта NO
(моноксид азота), появляющийся в конце реакции.Или если какое-либо из следующих реагентов NaNO3 (нитрат натрия), исчезающий
Какую другую важную информацию вы должны знать о реакции
У нас нет дополнительной информации об этой химической реакции.
Категории уравнений
Нажмите, чтобы увидеть более подробную информацию и рассчитать вес/моль >>
2 SO 4 + 2NaNO 3 → Fe 2 (SO 4 ) 3 + 4H 2 O + Na 2 SO 4 + 2NO
Вопросы, связанные с реагентом Fe (железо)
Каковы химические и физические характеристики Fe (железа)? В каких химических реакциях используется Fe (железо) в качестве реагента?
Вопросы, связанные с реагентом h3SO4 (серная кислота)
Каковы химические и физические характеристики h3SO4 (серная кислота)? В каких химических реакциях используется h3SO4 (серная кислота) в качестве реагента?
Вопросы, связанные с реагентом NaNO3 (нитрат натрия)
Каковы химические и физические характеристики NaNO3 (нитрат натрия)? В каких химических реакциях используется NaNO3 (нитрат натрия) в качестве реагента?
Вопросы, связанные с продуктом Fe2(SO4)3 ()
Каковы химические и физические характеристики Fe2(SO4)3 (нитрат натрия)? Какие химические реакции имеют Fe2(SO4)3 () в качестве продукта?
Вопросы, связанные с продуктом h3O (вода)
Каковы химические и физические характеристики h3O (нитрата натрия)? Каковы химические реакции, в результате которых образуется h3O (вода)?
Вопросы, связанные с продуктом Na2SO4 (сульфат натрия)
Каковы химические и физические характеристики Na2SO4 (нитрата натрия)? Каковы химические реакции, в результате которых образуется Na2SO4 (сульфат натрия)?
Вопросы, связанные с продуктом NO (моноксид азота)
Каковы химические и физические характеристики NO (нитрата натрия)? Каковы химические реакции, в результате которых NO (моноксид азота) является продуктом?
Уравнение Результат #2
Нажмите, чтобы увидеть более подробную информацию и рассчитать вес/моль >>
| png» substance-weight=»55.8450″> Fe | + | ||||||||
| 1 | 2 | 1 | 1 | 1 | Hệ số | ||||
| Нгуен-Фантухой (г/моль) | |||||||||
| Số MOL | |||||||||
кхин
РекламаДополнительная информация об уравнении Fe + 2NaHSO4 → H 2 + Na 2 SO 4 + FeSO 4В каких условиях Fe (железо) реагирует с NaSOH4?Для этого химического уравнения не найдено информации Объяснение: идеальные условия окружающей среды для реакции, такие как температура, давление, катализаторы и растворитель. Как могут происходить реакции с образованием h3 (водорода) и Na2SO4 (сульфата натрия) и FeSO4 () ?Явление после реакции Fe (железа) с NaHSO4 ()Это уравнение не несет никакой конкретной информации о явлении. В этом случае вам просто нужно наблюдать, чтобы убедиться, что вещество продукта FeSO4 , появляющийся в конце реакции. Или если какое-либо из следующих реагентов NaHSO4 , исчезает Какую другую важную информацию вы должны знать о реакцииУ нас нет дополнительной информации об этой химической реакции. Категории уравненийНажмите, чтобы увидеть более подробную информацию и рассчитать вес/моль >> Дополнительные вопросы, связанные с химическими реакциями Fe + 2NaHSO4 → H 2 + Na 2 SO 4 + FeSO 4Вопросы, связанные с химическим веществом9 FeO (железо) 90 физическая характеристика Fe (железа)? В каких химических реакциях используется Fe (железо) в качестве реагента?Вопросы, связанные с реагентом NaHSO4 ()Каковы химические и физические характеристики NaHSO4 ()? В каких химических реакциях используется NaHSO4 () в качестве реагента? Вопросы, связанные с продуктом h3 (водород)Каковы химические и физические характеристики h3 ()?Каковы химические реакции, в которых продуктом является h3 (водород)? Вопросы, связанные с продуктом Na2SO4 (сульфат натрия)Каковы химические и физические характеристики Na2SO4 ()? Каковы химические реакции, в которых Na2SO4 (сульфат натрия) является продуктом? Вопросы, связанные с продуктом FeSO4 ()Каковы химические и физические характеристики FeSO4 ()? Каковы химические реакции, в которых FeSO4 () является продуктом? 2 результатов найдено Коррозионное поведение нержавеющей стали Fe-12Cr-2Mo в среде Na2SO4-50%NaCl с проточной средой Ar-20%O2 при высокой температуреЗаголовки статей Влияние гибких подложек на структурно-оптические свойства пленок ZnO, осажденных методом напыления Влияние гамма-излучения на тонкие пленки нанокомпозита ПВА, легированного ZnO, для сенсора Escherichia coli Высокочувствительный оптический датчик POF для обнаружения низкой концентрации этанола в воде Модульный биосенсор поверхностного плазмонного резонанса (SPR) на основе модуляции длины волны Синтез и характеристика нанокомпозитных тонких пленок металлов (Co, Al), легированных PVA-Ag, биосенсоров для обнаружения E. coli в воде Оценка объемной скорости травления твердотельного ядерного трекового детектора CR-39 ZT-измерения термоэлементов при большой разнице температур Моделирование малоуглового рассеяния нейтронов в Малайзии с использованием Монте-Карло Коррозионное поведение нержавеющей стали Fe-12Cr-2Mo в Na 2 SO 4 -50%NaCl с потоком Ar-20%O 2 Среды при высокой температуре Главная Advanced Materials Research Advanced Materials Research Vol. 1107 Коррозионное поведение нержавеющей стали Fe-12Cr-2Mo… Предварительный просмотр статьи Аннотация: Изучено поведение нержавеющей стали Fe-12Cr-2Mo при изотермической выдержке в трубчатой печи при 700°C в течение 10 ч в различных средах; смешанной среды (Ar-20%O 2 с покрытием Na 2 SO 4 -50% соли NaCl), расплав солей (Na 2 SO 4 -50% NaCl) и сухой кислород (Ar-20%O 2 ) . Доступ через ваше учреждение Вас также могут заинтересовать эти электронные книги Предварительный просмотр * — Автор, ответственный за переписку использованная литература [1]
Т. [2] Н. Ариважаган, С. Нараянан, С. Сингх, С. Пракаш и Г.М. Редди, Исследования высокотемпературной коррозии сваренных трением низколегированных и нержавеющих сталей на воздухе и в среде расплавленных солей при 650 oC, Матер. Дизайн. 34 (2012) 459-468. DOI: 10.1016/j.matdes.2011.08.034 [3]
Г. Лю, М. Ли, Ю. Чжоу и Ю. Чжан, Влияние предварительного окисления на горячую коррозию Ti3SiC2 в смеси расплавов Na2SO4-NaCl, Corr. DOI: 10.1016/j.corsci.2005.02.002 [4] CC Цаур, Дж. К. Рок, К. Дж. Ван и Ю. Х. Su, Горячая коррозия нержавеющей стали 310 с предварительно нанесенными смесями NaCl/Na2SO4 при 750oC, Mater. хим. и физ. 89 (2005) 445-453. DOI: 10.1016/j.matchemphys.2004.10.002 [5] С.П. Акбар Хуссейн, В. Пандурангаду и С.С.К. Редди, Исследование влияния хлорида натрия на низкотемпературную горячую коррозию Mar-M 509 при 750°C, Int. Дж. Инж. и наук. 2 (2013) 31-34. [6]
Х. [7] С.М. Цзян, H.Q. Ли, Дж. Ма, К.З. Сюй, Дж. Гонг и К. Сан, Коррозионное поведение градиентного покрытия NiCoCrAlYSi II при высоких температурах: Окисление и горячая коррозия, Corr. науч. 52 (2010) 2316-2322. DOI: 10.1016/j.corsci.2010.03.032 [8]
Д. Дас, Р. Баласубраманиам и М.Н. Мунголе, Горячая коррозия легированных углеродом алюминидов железа на основе Fe3Al, Матер. науч. DOI: 10.1016/s0921-5093(02)00072-2 [9] Н.К. Отман, Н. Отман и А. Джалар, Коррозионное поведение сплавов Fe-Cr в атмосфере Ar-10% O2, Key. инж., мэтр. 462-463 (2011) 1250-1254. DOI: 10.4028/www.scientific.net/kem.462-463.1250 [10] Й. Зурек, Э. Вессель, Л. Неволак, Ф. Шмитц, Т.У. Керн, Л. Зингхайзер и В. Дж. Квадаккерс, Аномальная температурная зависимость кинетики окисления при паровом окислении ферритных сталей в диапазоне температур 550 — 650 oC, Corr. науч. 46 (2004). DOI: 10. |

 Катализаторы — это вещества, которые ускоряют темп (скорость) химической реакции, не потребляясь и не становясь частью конечного продукта.
Катализаторы не влияют на равновесные ситуации.
Катализаторы — это вещества, которые ускоряют темп (скорость) химической реакции, не потребляясь и не становясь частью конечного продукта.
Катализаторы не влияют на равновесные ситуации. 678
678 712
712 Экспонированные образцы были охарактеризованы с помощью оптической микроскопии (ОМ), сканирующего электронного микроскопа (СЭМ), энергодисперсионного рентгеновского излучения (EDX) и рентгеновской дифракции (XRD). Результаты показали, что образец, выставленный в смешанной среде, подвергается самой высокой скорости коррозии по сравнению с другими образцами. Основная фаза, присутствующая во всех образцах, как правило, представляла собой богатые железом оксиды, которые не обладали защитными свойствами и были густыми. И наоборот, анализ EDX на образцах поперечного сечения показал обогащение хромом, развивающееся под чешуйками оксида, богатого железом, по мере увеличения концентрации хрома ближе к подложке. В присутствии смеси солей происходит скалывание оксидных чешуек, однако трещин не наблюдается. Катастрофическая коррозия образца произошла в комбинированной среде также из-за окисления, вызванного явлениями хлорирования и сульфидирования.
Экспонированные образцы были охарактеризованы с помощью оптической микроскопии (ОМ), сканирующего электронного микроскопа (СЭМ), энергодисперсионного рентгеновского излучения (EDX) и рентгеновской дифракции (XRD). Результаты показали, что образец, выставленный в смешанной среде, подвергается самой высокой скорости коррозии по сравнению с другими образцами. Основная фаза, присутствующая во всех образцах, как правило, представляла собой богатые железом оксиды, которые не обладали защитными свойствами и были густыми. И наоборот, анализ EDX на образцах поперечного сечения показал обогащение хромом, развивающееся под чешуйками оксида, богатого железом, по мере увеличения концентрации хрома ближе к подложке. В присутствии смеси солей происходит скалывание оксидных чешуек, однако трещин не наблюдается. Катастрофическая коррозия образца произошла в комбинированной среде также из-за окисления, вызванного явлениями хлорирования и сульфидирования. С. Сидху, С. Пракаш и Р. Д. Агравал, Горячая коррозия и характеристики покрытий на основе никеля, Curr. науч. 90 (2006) 41-47.
С. Сидху, С. Пракаш и Р. Д. Агравал, Горячая коррозия и характеристики покрытий на основе никеля, Curr. науч. 90 (2006) 41-47. науч. 48 (2006) 650-661.
науч. 48 (2006) 650-661. Сингх, Д. Пури и С. Пракаш, Обзор вызванной Na2SO4 и/или V2O5 горячей коррозии жаропрочных сплавов на основе Fe и Ni, Rev. Adv. Матер. науч. 16 (2007) 27-50.
Сингх, Д. Пури и С. Пракаш, Обзор вызванной Na2SO4 и/или V2O5 горячей коррозии жаропрочных сплавов на основе Fe и Ni, Rev. Adv. Матер. науч. 16 (2007) 27-50. англ. А. 338 (2002) 24.
англ. А. 338 (2002) 24.