Презентация к уроку химии «Окислительно-восстановительные реакции» — К уроку — Химия
Егорова Елена 5.0
Отзыв о товаре ША PRO Анализ техники чтения по классам
и четвертям
Хочу выразить большую благодарность от лица педагогов начальных классов гимназии «Пущино» программистам, создавшим эту замечательную программу! То, что раньше мы делали «врукопашную», теперь можно оформить в таблицу и получить анализ по каждому ученику и отчёт по классу. Великолепно, восторг! Преимущества мы оценили сразу. С начала нового учебного года будем активно пользоваться. Поэтому никаких пожеланий у нас пока нет, одни благодарности. Очень простая и понятная инструкция, что немаловажно! Благодарю Вас и Ваших коллег за этот важный труд. Очень приятно, когда коллеги понимают, как можно «упростить» работу учителя.
Наговицина Ольга Витальевна 5.0
учитель химии и биологии, СОШ с. Чапаевка, Новоорский район, Оренбургская область
Чапаевка, Новоорский район, Оренбургская область
по ХИМИИ
Спасибо, аналитическая справка замечательная получается, ОГЭ химия и биология. Очень облегчило аналитическую работу, выявляются узкие места в подготовке к экзамену. Нагрузка у меня, как и у всех учителей большая. Ваш шаблон экономит время, своим коллегам я Ваш шаблон показала, они так же его приобрели. Спасибо.
Чазова Александра 5.0
Отзыв о товаре ША Шаблон Excel Анализатор результатов ОГЭ по
МАТЕМАТИКЕ
Очень хороший шаблон, удобен в использовании, анализ пробного тестирования занял считанные минуты. Возникли проблемы с распечаткой отчёта, но надо ещё раз разобраться. Большое спасибо за качественный анализатор.
Лосеева Татьяна Борисовна 5.0
учитель начальных классов, МБОУ СОШ №1, г.
Отзыв о товаре Изготовление сертификата или свидетельства конкурса
Большое спасибо за оперативное изготовление сертификатов! Все очень красиво. Мой ученик доволен, свой сертификат он вложил в портфолио. Обязательно продолжим с Вами сотрудничество!
Язенина Ольга Анатольевна 4.0
учитель начальных классов, ОГБОУ «Центр образования для детей с особыми образовательными потребностями г. Смоленска»
Отзыв о товаре Вебинар Как создать интересный урок:
инструменты и приемы
Я посмотрела вебинар! Осталась очень довольна полученной
информацией. Всё очень чётко, без «воды». Всё, что сказано, показано, очень
пригодится в практике любого педагога. И я тоже обязательно воспользуюсь полезными материалами вебинара.
Арапханова Ашат 5. 0
0
ША Табель посещаемости + Сводная для ДОУ ОКУД
Хотела бы поблагодарить Вас за такую помощь. Разобралась сразу же, всё очень аккуратно и оперативно. Нет ни одного недостатка. Я не пожалела, что доверилась и приобрела у вас этот табель. Благодаря Вам сэкономила время, сейчас же составляю табель для работников. Удачи и успехов Вам в дальнейшем!
Дамбаа Айсуу 5.0
Отзыв о товаре ША Шаблон Excel Анализатор результатов ЕГЭ по
РУССКОМУ ЯЗЫКУ
Спасибо огромное, очень много экономит времени, т.к. анализ уже готовый, и особенно радует, что есть варианты с сочинением, без сочинения, только анализ сочинения! Превосходно!
функциональных групп
функциональных группФункциональные группы
| Функциональные группы | Окислительно-восстановительные реакции |
Функциональные группы
Бром реагирует с 2-бутеном с образованием 2,3-дибромбутана.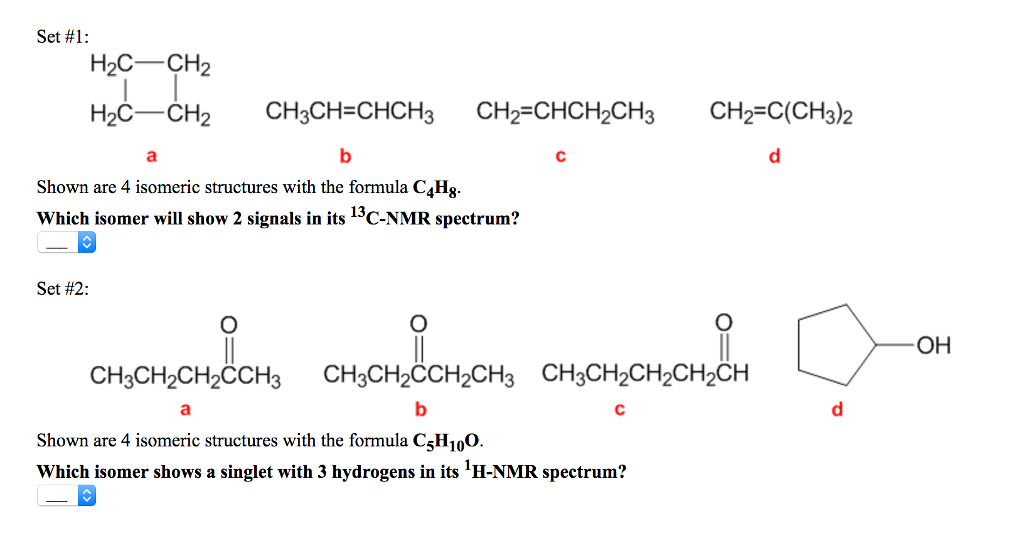
Он также реагирует с 3-метил-2-пентеном с образованием 2,3-дибромпентана.
Вместо того, чтобы пытаться запомнить оба уравнения, мы можем построить общее правило, согласно которому бром
реагирует с соединениями, содержащими двойную связь С=С, с образованием продукта, ожидаемого от
присоединение по двойной связи. Такой подход к пониманию химии органических
соединений предполагает, что определенные атомы или группы атомов, известные как
Функциональные группы обращают внимание на важные аспекты структуры
молекула. Нам не нужно беспокоиться о различиях между структурами 1-бутена.
и 2-метил-2-гексен, например, когда эти соединения реагируют с бромистым водородом. Мы
можно сфокусироваться на том факте, что оба соединения представляют собой алкены, которые присоединяют HBr к двойной цепи C=C.
связь в направлении, предсказанном Марковниковым
правило.
Некоторые общие функциональные группы приведены в таблице ниже.
Общие функциональные группы
| Функциональная группа | Имя | Пример | ||
| Алкан | CH 3 CH 2 CH 3 (пропан) | |||
| Алкен | CH 3 CH=CH 2 (пропилен) | |||
| Алкин | CH 3 CCH (пропин) | |||
| F, Cl, Br или I | Алкилгалогенид | CH 3 Br (бромистый метил) | ||
| Алкоголь | CH 3 CH 2 OH (этанол) | |||
| Эфир | CH | |||
| Амин | CH 3 NH 2 (метиламин) |
Группа C=O играет особенно важную роль в органической химии.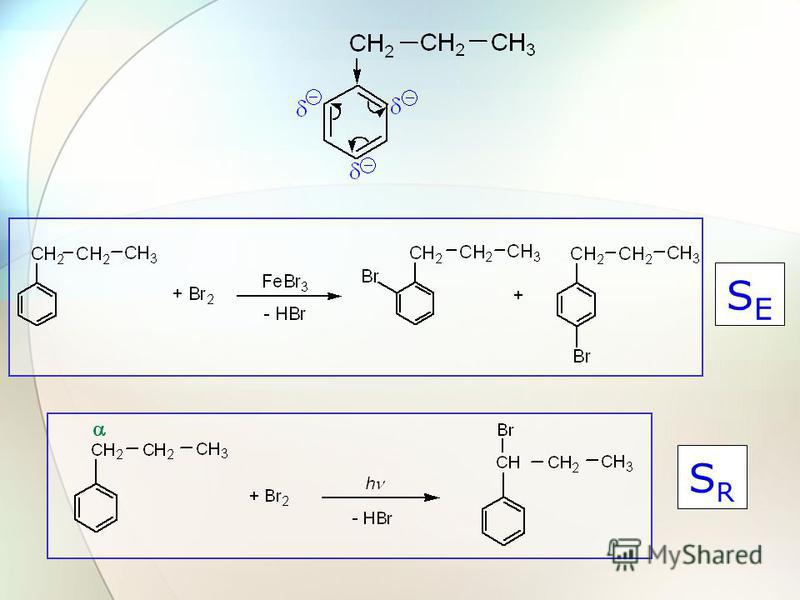 Эта группа
называется карбонилом , а некоторые функциональные группы основаны на карбониле
показаны в таблице ниже.
Эта группа
называется карбонилом , а некоторые функциональные группы основаны на карбониле
показаны в таблице ниже.
Функциональные группы, содержащие карбонил
| Функциональная группа | Имя | Пример | ||
| Альдегид | CH 3 CHO (ацетальдегид) | |||
| Кетон | CH 3 COCH 3 (ацетон) | |||
| Ацилхлорид | CH 3 COCl (ацетилхлорид) | |||
| Карбоновая кислота | CH 3 CO2H (уксусная кислота) | |||
| Эстер | CH 3 CO 2 CH 3 (метилацетат) | |||
| Амид | CH 3 NH 2 (ацетамид) |
| Практическая задача 1: Корневое пиво не имеет прежнего вкуса с тех пор
использование масла сассафраса в качестве пищевой добавки было запрещено, потому что масло сассафраса на 80% состоит из
сафрол, вызывающий рак у крыс и мышей. Нажмите здесь, чтобы проверить свой ответ на практика задача 1 |
| Практическая задача 2: Следующие соединения являются активными ингредиенты безрецептурных препаратов, используемых в качестве анальгетиков (для облегчения боли без снижение чувствительности или сознания), жаропонижающие (для снижения температуры тела когда она повышена) и/или противовоспалительные средства (для противодействия отеку или воспаление суставов, кожи и глаз). Определите функциональные группы в каждом молекула. Нажмите здесь, чтобы проверить свой ответ на практическая задача 2 |
| Практическая задача 3: Открытие пенициллина в 1928 г. Нажмите здесь, чтобы проверить свой ответ на практическая задача 3 |
Сосредоточение внимания на функциональных группах в молекуле позволяет нам распознавать закономерности в поведение родственных соединений. Рассмотрим, что мы знаем о реакции между натрием металл и вода, например.
2 Na( с ) + 2 H 2 O( л ) H 2 ( г ) + 2 Na + ( водный раствор ) + 2 OH — ( водный раствор )
Эту реакцию можно разделить на две полуреакции. Один связан с окислением
металлический натрий с образованием ионов натрия.
Один связан с окислением
металлический натрий с образованием ионов натрия.
| Окисление: | На | Na + + e — |
Другой включает восстановление иона H + в воде с образованием нейтрального атом водорода, который соединяется с другим атомом водорода с образованием молекулы H 2 .
| Сокращение: |
Как только мы узнаем, что вода содержит функциональную группу OH, мы можем предсказать, что может произойти, когда металлический натрий вступит в реакцию
со спиртом, содержащим ту же функциональную группу. Металлический натрий должен реагировать с
метанол (СН 3 OH), например, для получения газа H 2 и раствора
Ионы Na + и CH 3 O — растворены в этом спирте.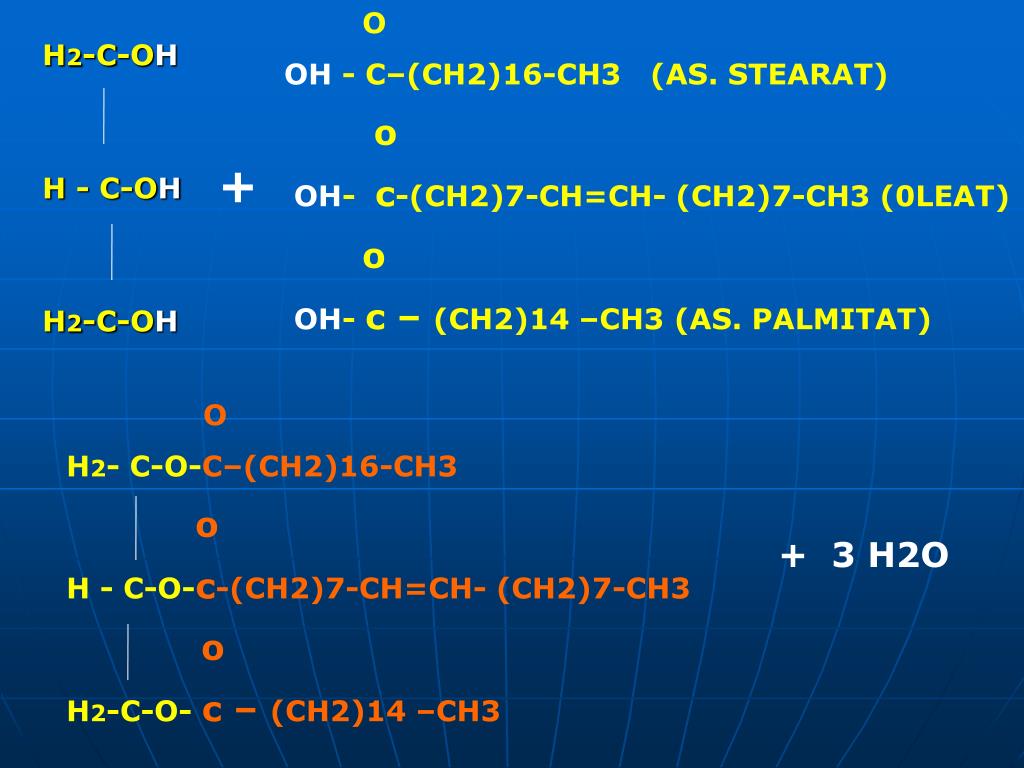
2 Na( с ) + 2 CH 3 OH( л ) H 2 ( г ) + 2 Na + ( алк ) + 2 CH 3 O — ( алк )
Поскольку они связаны с переносом электронов, реакция между металлическим натрием и либо вода, либо спирт являются примерами окислительно-восстановительных реакций. Но что насчет следующая реакция, в которой газообразный водород реагирует с алкеном в присутствии катализатор на основе переходного металла для образования алкана?
Число валентных электронов ни на одном из атомов в этом
реакция. Как до, так и после реакции каждый атом углерода имеет в общей сложности восемь
валентных электронов, и каждый атом водорода разделяет два электрона. Вместо электронов это
реакция включает перенос атомов, в данном случае атомов водорода. Существует так много реакций переноса атома, что
химики разработали концепцию степени окисления , чтобы расширить идею
окисление и восстановление до реакций, в которых электроны не обязательно приобретаются или теряются.
| Окисление включает увеличение степени окисления атома. |
| Восстановление происходит, когда степень окисления атома уменьшается . |
При превращении этена в этан происходит уменьшить в степень окисления атома углерода. Таким образом, эта реакция включает восстановление этилена в этан.
Реакции, в которых ни один из атомов не изменяет степени окисления, называются -метатезисом. реакции . Рассмотрим реакцию между карбоновой кислотой и амином, для пример.
Или реакция между спиртом и бромистым водородом.
Это реакции метатезиса, потому что нет изменений в окислении число любого атома в любой реакции.
Степени окисления атомов углерода в различных соединениях приведены в
таблица ниже .
Типичные степени окисления углерода
| Функциональная группа | Пример | Степень окисления Углерод в примере | ||
| Алкан | СН 4 | -4 | ||
| Алкиллитий | CH 3 Li | -4 | ||
| Алкен | Н 2 С=СН 2 | -2 | ||
| Алкоголь | CH 3 OH | -2 | ||
| Эфир | СН 3 ОСН 3 | -2 | ||
| Алкилгалогенид | Ч 3 Класс | -2 | ||
| Амин | CH 3 NH 2 | -2 | ||
| Алкин | ХКЧ | -1 | ||
| Альдегид | H 2 CO | 0 | ||
| Карбоновая кислота | HCO 2 H | 2 | ||
| СО 2 | 4 |
Эти степени окисления можно использовать для классификации органических реакций. либо окислительно-восстановительные реакции, либо реакции метатезиса.
либо окислительно-восстановительные реакции, либо реакции метатезиса.
| Практическая задача 4: Классифицируйте следующее как окислительно-восстановительные реакции или реакции метатезиса. Нажмите здесь, чтобы проверить свой ответ на практическое задание 4 |
Поскольку электроны не создаются и не уничтожаются, окисление не может происходить в отсутствие редукции или наоборот. Однако часто бывает полезно сосредоточьте внимание на одном компоненте реакции и спросите: это вещество окисляется или уменьшенный?
| Практическая задача 5: Определите, выполняются ли следующие
превращения включают окисление или восстановление атома углерода. Нажмите здесь, чтобы проверить свой ответ на практическое задание 5 |
Присвоение степеней окисления отдельным атомам углерода в сложной молекуле может быть трудный. К счастью, есть еще один способ распознать окислительно-восстановительные реакции в органическая химия:
Окисление происходит при удалении атомов водорода от атома углерода или при атом кислорода присоединен к атому углерода .
Восстановление происходит при присоединении атомов водорода к атому углерода или при атом кислорода удален от атома углерода.
Первая реакция в практической задаче 5 включает окисление атома углерода, потому что пара атомов водорода удаляется от этого атома, когда спирт окисляется до альдегид.
Вторая реакция в практической задаче 5 является примером
окисление, поскольку атом кислорода присоединяется к атому углерода при окислении альдегида
до карбоновой кислоты.
Восстановление, с другой стороны, происходит, когда атомы водорода присоединяются к атому углерода или при удалении атома кислорода от атома углерода. Алкен восстанавливается, например, когда он реагирует с H 2 с образованием соответствующего алкана.
Рисунок ниже представляет собой полезное руководство по окислительно-восстановительным реакциям органические соединения. Каждая из стрелок на этом рисунке связана с двухэлектронным окислением атом углерода на пути к углекислому газу. Линия проводится через первую стрелка, потому что невозможно выполнить это преобразование за один шаг.
Органическая химия: функциональные группы
Функциональные группы | Алкилгалогениды | Спирты и эфиры | Альдегиды и Кетоны | Карбонильная группа | Амины, алкалоиды и амиды | Реактивы Гриньяра
Исследования 1990-х годов: Химия чеснока
Периодический Таблица | Глоссарий | прохладно Апплеты
Тематический обзор Gen Chem
| Главная страница справки по общей химии | Поиск: Сайт общей химии.
[Решено] Как мне их назвать?. 1. Назовите соединения: a h3C-Ch4…
Получите больше от подписки*
- Доступ к более чем 100 миллионам учебных ресурсов по конкретным курсам
- Круглосуточная помощь опытных наставников по более чем 140 предметам
- Полный доступ к более чем 1 миллиону решений для учебников
*Вы можете изменить, приостановить или отменить в любое время
Вопрос задан HighnessInternet3858
Как мне их назвать?
Текст транскрипции изображения
1. Назовите соединения: а h3C-Ch4 h4C-CH-Ch3Ch3 Ch4 б. ЧС h4C-Ch3-Ch4 Ч4 С. Ч4 Ч,ЧЧЧ4 Ч4 (по 2 балла = 10 баллов) г) Ч4 — Ч3 Ч4-Ч3-Ч3-Ч-Ч-Ч3-Ч3-Ч4 Ч4 д) CH СН,-СН-Ч3-Ч3-Ч4 H&C-CH-CH-CH-CH-Ch4
… Показать больше
Химия Наука Органическая химия БМЕ 151
Ответ и объяснение
Решено проверенным экспертом
Рейтинг Полезно
Ответил PureMind
ipsum dolor sit amet, consectetur adipiscing elit. Nam lacinia pulvinar tortor nec facilisis. Pellentesque dapibus efficitur laoreet. Nam risus ante, dapibus a molestie consequat, ultrices ac magna. Fusce dui lectus, congue vel laoreet ac, dictum vitae odi
Nam lacinia pulvinar tortor nec facilisis. Pellentesque dapibus efficitur laoreet. Nam risus ante, dapibus a molestie consequat, ultrices ac magna. Fusce dui lectus, congue vel laoreet ac, dictum vitae odi
Получите полный доступ к Course Hero
Изучите более 16 миллионов пошаговых ответов из нашей библиотеки
Подпишитесь, чтобы посмотреть ответ
t. Nam risus ante, dapibus a molestie consequat, ult
gue
molestie consequat
et, consectetur
usce dui lectu
ec facilisis. Pell
icitur laoree
inia pulvinar tort
at, ultrices ac m
consectetur adipis
usce dui lectus,
icitur laoreet. N
sus ante, dapibus a mo
ce dui lectus, congue vel laoreet ac, dictum ec f dictum v
entesque dapibus efficitur laoreet. Nam ipiscing elit llentesq
ac, dictum vitae odio.

 положило начало так называемому «золотому веку химиотерапии».
при котором ранее опасные для жизни бактериальные инфекции трансформировались в мало
больше, чем источник дискомфорта. Для тех, у кого аллергия на пенициллин, различные
антибиотики, в том числе тетрациклин, доступны. Определите многочисленные функциональные
группы в молекуле тетрациклина.
положило начало так называемому «золотому веку химиотерапии».
при котором ранее опасные для жизни бактериальные инфекции трансформировались в мало
больше, чем источник дискомфорта. Для тех, у кого аллергия на пенициллин, различные
антибиотики, в том числе тетрациклин, доступны. Определите многочисленные функциональные
группы в молекуле тетрациклина.