With Several Elements Reaction – Lambda Geeks
Hydrochloric acid and Aluminum hydroxide are chemical elements present in liquid form HCl are acid and Al(OH)3 is the base. Let us discuss HCl + Al(OH)3 both Element’s Reactions.
Hydrochloric is an acid that contains an ionic bond between hydrogen and chlorine and aluminum hydroxide has a Ковалентная связь both are in a liquid state and should be kept in a glass bottle with a closed cap as HCl is highly reactive with air as compared to Aluminum hydroxide.
This article will discuss the product, balance reaction, titration, ionic equation, conjugate pair, and intermolecular forces of attraction with a detailed explanation.
What is the product of HCl and Al(OH)3The HCl is a strong acid and completely dissociates in an aqueous medium
HCl = Н+ + Кл–
Aluminum chloride is a weak base that partially dissociates in an aqueous medium
Al (OH)3 = Al+ + OH3–
Hence, the product formed in the reaction is 3HCl + Al(OH)3 = AlCl3 + 3H2O
What type of reaction is HCl + Аl(ОЙ)3The reaction of hydrochloric acid and aluminum hydroxide is a neutralization reaction because HCl is acid and Al(OH)3 is a base and they neutralize each other.
The reactant is HCL + Al (OH)3 and the product is AlCl3 + H2O. The number of moles of reactant is equal to the number of moles of product, 3 moles of HCl are needed to balance the AlCl3 and now there are a total of 6 hydrogens, and 3 oxygen in the reactant, 3 moles of H2O is needed.
3HCl + Al (OH)3 ——> AlCl3 + 3H2O
HCl+ Al(OH)3титрованиеApparatus used –Burette, beaker, dropper, funnel, conical flask
ИндикаторныеThe ‘phenolphthalein indicator’ used during the титрование of strong acid v/s strong base endpoint is colorless to pink.
Процедура-Fill the burette with Al (OH)3 with the help of a beaker and place it on the stand. Place the conical flask below the burette and add a few drops of HCl to it with this release the Al (OH)3 in the same flask. Add the indicator with the help of a drop till it hits the endpoint and the color changes to pink.
Place the conical flask below the burette and add a few drops of HCl to it with this release the Al (OH)3 in the same flask. Add the indicator with the help of a drop till it hits the endpoint and the color changes to pink.
- The following steps can determine the ionic reaction
- Should write the balance equation first 3HCl + Al (OH)3 ——> AlCl3 + 3H2O
- Split the components into constituent ions which are net Ionic equation for HCL + AL(OH)3
H+ + Кл– + Аль+ + OH3– = Al + + Кл3– + 3H2O
HCl+ Al(OH)3 сопряженные парыWhenever an acid donates a proton it converts to a conjugate base and a strong acid is a weak conjugate base and vice-versa. so, the сопряженное основание это Cl– for HCl, and OH– is a base so, the acid is Al(OH)3
so, the сопряженное основание это Cl– for HCl, and OH– is a base so, the acid is Al(OH)3
- HCl is an ionic compound that contains the dipole-dipole force of attraction with the London force in the molecules.
- AL(OH)3 contains hydrogen forces with the Лондонская дисперсионная сила of attraction.
Enthalpy is the amount of energy required to complete the reaction for the reactant and product. The reaction enthalpy of 3HCl + Al (OH)3 ——> AlCl3 + 3H2O будет,
AlCl3(s) = -705.6 kJ/mol HCl(g) = -92 kJ/mol. H2O(l) = -285.8 kJ/mol. Al(OH)3(s) = −285.8 кДж / моль
Enthalpy for final reaction will be = (-285. 8kJ/mol.Al + 3 x −285.8) – (−1277.0) – (3 x −92.0) знак равно 10.0 кДж / моль
8kJ/mol.Al + 3 x −285.8) – (−1277.0) – (3 x −92.0) знак равно 10.0 кДж / моль
HCl is a strong acid that can never make a buffer solution and Al(OH)3 is not an acid but have a pH value of 8 it also does not make a буферный раствор because the pH value of buffer must be always 14.
Is HCl + Al(OH)3 a complete reactionHCl + Al(OH)3 is a complete reaction because HCl is a strong acid and Al (OH)3 is a strong base both neutralize the ions of each other and completely dissociate in water to form new compounds.
Is HCl + Al(OH)3 an exothermic reaction or endothermic reactionHydrochloric acid with aluminum hydroxide is an экзотермическая реакция which means it releases a good amount of heat and the entropy is also less than zero and Энергия Гиббса становится отрицательным.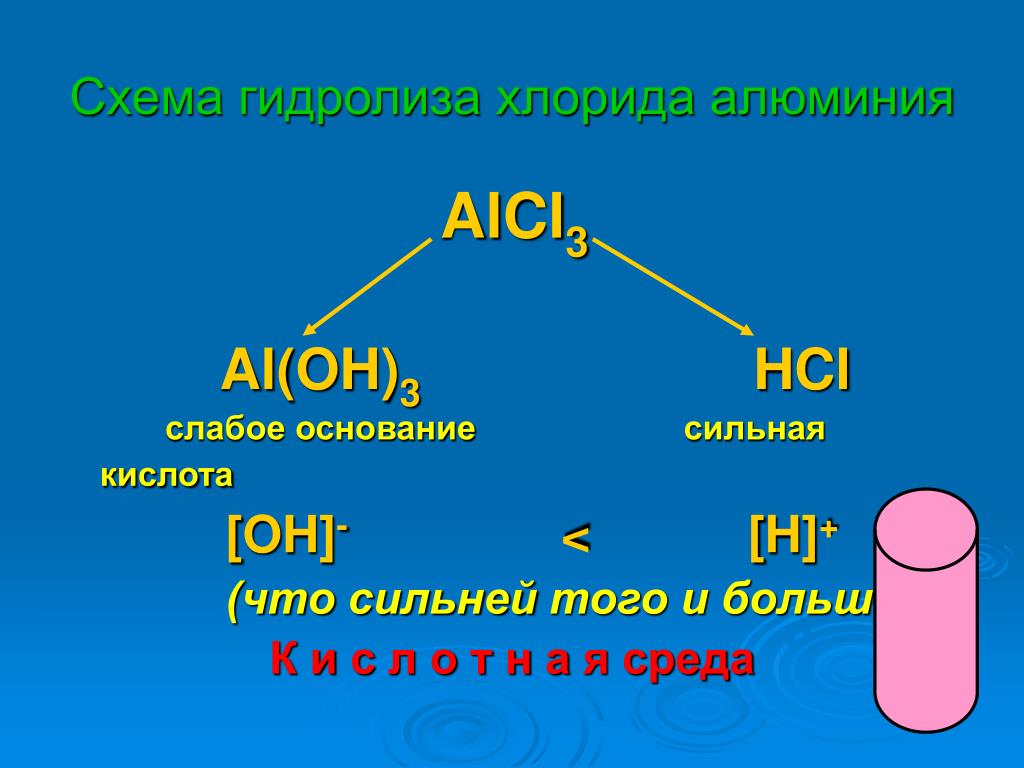
The reaction HCl+ Al(OH)3 is not a redox reaction because in a окислительно-восстановительная реакция oxidation and reduction take place simultaneously and the oxidation state will change because of the transfer of electrons.
Is HCl + Al(OH)3 a precipitation reactionThe reaction of Is HCl + Al(OH)3 is not a precipitation reaction because there is no precipitate formation after the completion of the reaction.
Is HCl+ Al(OH)3 reversible or irreversible reactionThe reaction HCl + Al(OH)3 is reversible by adding a good amount of HCl to the Al(OH)3 precipitate by complex formation.
Is HCl + Al(OH)3 реакция смещенияThe reaction HCl + AL(OH)3 is not a displacement reaction as it forms a new product instead of displacing any reactant or product.
Hydrochloric acid (HCl) is a very strong acid and aluminum hydroxide (Al(OH)3)is a strong base they both together neutralize each other and are the best example of neutralization reaction and titration for calculating endpoints.
Помощь студентам в учёбе от Людмилы Фирмаль
Здравствуйте!
Я, Людмила Анатольевна Фирмаль, бывший преподаватель математического факультета Дальневосточного государственного физико-технического института со стажем работы более 17 лет. На данный момент занимаюсь онлайн обучением и помощью по любыми предметам. У меня своя команда грамотных, сильных бывших преподавателей ВУЗов. Мы справимся с любой поставленной перед нами работой технического и гуманитарного плана. И не важно: она по объёму на две формулы или огромная сложно структурированная на 125 страниц! Нам по силам всё, поэтому не стесняйтесь, присылайте.
Срок выполнения разный: возможно онлайн (сразу пишите и сразу помогаю), а если у Вас что-то сложное – то от двух до пяти дней.
Для качественного оформления работы обязательно нужны методические указания и, желательно, лекции. Также я провожу онлайн-занятия и занятия в аудитории для студентов, чтобы дать им более качественные знания.
Моё видео:
Вам нужно написать сообщение в Telegram . После этого я оценю Ваш заказ и укажу срок выполнения. Если условия Вас устроят, Вы оплатите, и преподаватель, который ответственен за заказ, начнёт выполнение и в согласованный срок или, возможно, раньше срока Вы получите файл заказа в личные сообщения.
Сколько может стоить заказ?Стоимость заказа зависит от задания и требований Вашего учебного заведения. На цену влияют: сложность, количество заданий и срок выполнения. Поэтому для оценки стоимости заказа максимально качественно сфотографируйте или пришлите файл задания, при необходимости загружайте поясняющие фотографии лекций, файлы методичек, указывайте свой вариант.
Минимальный срок выполнения заказа составляет 2-4 дня, но помните, срочные задания оцениваются дороже.
Как оплатить заказ?Сначала пришлите задание, я оценю, после вышлю Вам форму оплаты, в которой можно оплатить с баланса мобильного телефона, картой Visa и MasterCard, apple pay, google pay.
Какие гарантии и вы исправляете ошибки?В течение 1 года с момента получения Вами заказа действует гарантия. В течении 1 года я и моя команда исправим любые ошибки в заказе.
Качественно сфотографируйте задание, или если у вас файлы, то прикрепите методички, лекции, примеры решения, и в сообщении напишите дополнительные пояснения, для того, чтобы я сразу поняла, что требуется и не уточняла у вас. Присланное качественное задание моментально изучается и оценивается.
Теперь напишите мне в Telegram или почту и прикрепите задания, методички и лекции с примерами решения, и укажите сроки выполнения. Я и моя команда изучим внимательно задание и сообщим цену.
Я и моя команда изучим внимательно задание и сообщим цену.
Если цена Вас устроит, то я вышлю Вам форму оплаты, в которой можно оплатить с баланса мобильного телефона, картой Visa и MasterCard, apple pay, google pay.
Мы приступим к выполнению, соблюдая указанные сроки и требования. 80% заказов сдаются раньше срока.
После выполнения отправлю Вам заказ в чат, если у Вас будут вопросы по заказу – подробно объясню. Гарантия 1 год. В течении 1 года я и моя команда исправим любые ошибки в заказе.
youtube.com/embed/FTtp-vAv3lI» frameborder=»0″ allow=»accelerometer; autoplay; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»/>
youtube.com/embed/ZfNUaigadEY» frameborder=»0″ allow=»accelerometer; autoplay; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»/>
Можете смело обращаться к нам, мы вас не подведем. Ошибки бывают у всех, мы готовы дорабатывать бесплатно и в сжатые сроки, а если у вас появятся вопросы, готовы на них ответить.
В заключение хочу сказать: если Вы выберете меня для помощи на учебно-образовательном пути, у вас останутся только приятные впечатления от работы и от полученного результата!
Жду ваших заказов!
С уважением
Пользовательское соглашение
Политика конфиденциальности
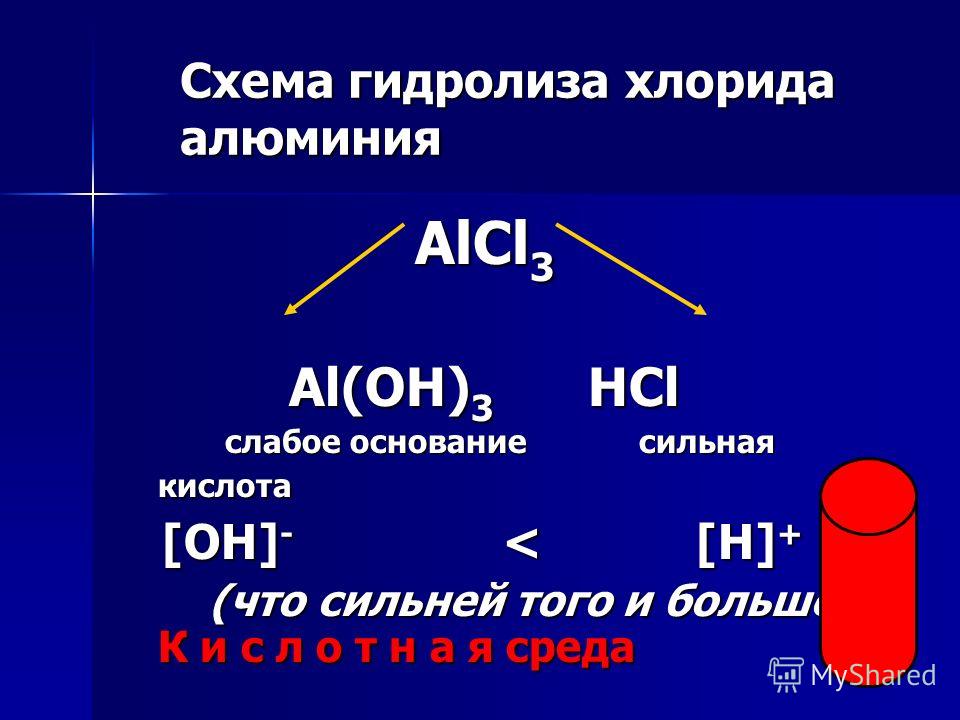
{3+}$) в гидроксиде алюминия составляет 3:1. Это условие предполагает, что дозирование воды солями алюминия сильно влияет на pH системы в свете того факта, что гидролиз создает соляную коррозию.
Полный пошаговый ответ:
\[Al{\left({OH} \right)_3} + {\text{}}3HCl \Rightarrow AlC{l_3} + 3{H_2}O\;\]
Из уравнения 1 моль $AlCl_3$ образует 3 моля HCl и 1 моль $Al(OH)_3$ . молярные нагрузки:
молярные нагрузки:
\[AlC{l_3} = {\text{}}27{\text{}} + {\text{}}\left({3{\text{}}x{\text{} }35,5} \right){\text{}} = {\text{}}133,5{\text{}}g{\text{}}HCl{\text{}} = {\text{}}\left( {35,5 {\ text { }} + {\ text { }} 1} \ right) {\ text { }} = {\ text { }} 36,5 {\ text { }} g \; Al {\ left ( {OH } \right)_3} = {\text{}}27{\text{}} + {\text{}}3{\text{}}x{\text{}}\left({16{\text{ }} + {\text{}}1}\right){\text{}} = {\text{}}78{\text{}}g\]
Мы можем использовать коэффициенты условия для определения количества молей Al(OH)3, которые реагируют, понимая, что 1 моль AlCl3 имеет структуру:
Что является хорошим предзнаменованием, учитывая их молярную пропорцию \[1:1.\]
В настоящее время, мы можем использовать молярную массу гидроксида алюминия \[\left( {78,00{\text{}} г/моль} \right)\]для расчета количества граммов, которые отвечают:
\[1mol{\text{}}Al{\left({OH} \right)_3}*\left( {78.
 00lg{\text{}}Al{{\left({OH} \right)}_3 }*1mol{\text{}}Al{{\left({OH} \right)}_3}} \right){\text{}} = {\text{}}80{\text{}}g{ \text{ }}Al{\left( {OH} \right)_3}\]
00lg{\text{}}Al{{\left({OH} \right)}_3 }*1mol{\text{}}Al{{\left({OH} \right)}_3}} \right){\text{}} = {\text{}}80{\text{}}g{ \text{ }}Al{\left( {OH} \right)_3}\] , что, я думаю, будет соответствовать 1 огромной цифре, сумме, указанной в выпуске..
Таким образом, для ответа \[3 {\ text { }} моли {\ text { }} HCl {\ text { }} в {\ text { }} один {\ text { }} моль {\ text { }} AlC {l_3} и {\ text { }}Al{\left( {OH} \right)_3}.\]
Примечание: 9- }_4\]
Гидроксид алюминия дополнительно называют Алюминий коррозионно-активным или Гидроксид алюминия или Гидроксид алюминия (III).
Недавно обновленные страницы
Большинство эубактериальных антибиотиков получены из биологии ризобия класса 12 NEET_UG
Биоинсектициды саламин были извлечены из класса 12 Biology NEET_UG
Какое из следующих утверждений, касающихся Baculovirussess, Neet_ug
. Какое из следующих утверждений, касающихся Baculoviruses, Neet_ug
. муниципальные канализационные трубы не должны быть непосредственно 12 класса биологии NEET_UG
Очистка сточных вод осуществляется A Микробами B Удобрения 12-го класса биологии NEET_UG
Иммобилизация ферментов – это A Преобразование активного фермента 12-го класса биологии NEET_UG
Большинство эубактериальных антибиотиков получают из A Rhizobium class 12 биологии NEET_UG
3 90 Экстракт инсектицидов из 12-го класса биологии NEET_UGКакое из следующих утверждений относительно бакуловирусов 12-го класса биологии NEET_UG
Канализационные или муниципальные канализационные трубы не должны относиться непосредственно к 12-му классу биологии NEET_UG
Очистка сточных вод выполняется с помощью микробов B Clartilizers Class 12 Biology NEET_UG
Иммобилизация фермента. Биология активного фермента. Реакция
Биология активного фермента. Реакция
Реакция между тиосульфатом натрия и йодидом калия
Реакция Мицунобу
Реакция Фентона
Реакция Финкельштейна
Окислительно-восстановительная реакция
Реакция Вудворда
Реакция присоединения
Реакция HVZ (реакция Хелла-Фольгарда-Зелинского)
Реакция Шмидта
Реакция с несколькими элементами – лямбда-окись содержит химические элементы в хлористоводородной кислоте и
1 форма HCl является кислотой, а Al(OH) 3 является основанием. Давайте обсудим HCl + Al(OH) 3 реакции обоих элементов .
Соляная кислота представляет собой кислоту, которая содержит ионную связь между водородом и хлором, а гидроксид алюминия имеет ковалентную связь. Обе они находятся в жидком состоянии и должны храниться в стеклянной бутылке с закрытой крышкой, поскольку HCl сильно реагирует с воздухом, поскольку по сравнению с гидроксидом алюминия .
В этой статье будет обсуждаться продукт, балансовая реакция, титрование, ионное уравнение, сопряженная пара и силы межмолекулярного притяжения с подробным объяснением.
Что является продуктом HCl и Al(OH) 3HCl является сильной кислотой и полностью диссоциирует в водной среде
HCl = H + + Cl
Хлорид алюминия – слабое основание, частично диссоциирующее в водной среде
AL (OH) 3 = AL + + OH 3 —
HENCE, продукт, формированный в продукте в «Реактивном». 3 = ALCL 3 + 3H 2 O
Какой тип реакции — HC L + A L ( OH) 3 . Реакция Hydrohlor -intrhlor intrhlor intrhlor intrhlor intrhlor. реакция нейтрализации, потому что HCl является кислотой, а Al(OH) 3 является базой и они нейтрализуют друг друга.
реакция нейтрализации, потому что HCl является кислотой, а Al(OH) 3 является базой и они нейтрализуют друг друга.
The reactant is HCL + Al(OH) 3 and the product is AlCl 3 + H 2 O. Количество молей реагента равно количеству молей продукта, 3 моля HCl необходимо, чтобы уравновесить AlCl 3 , и теперь в реагенте всего 6 атомов водорода и 3 кислорода, 3 моля H 2 O необходим.
3HCl + Al(OH) 3 ——> AlCl 3 + 3H 2 O
HCl+ Al(OH) 3 titration Apparatus used –Бюретка, химический стакан, пипетка, воронка, коническая колба
Индикатор «Фенолфталеиновый индикатор», используемый при титровании сильной кислоты по сравнению с сильным основанием, имеет цвет от бесцветного до розового.
Заполните бюретку Al(OH) 3 с помощью стакана и поместите ее на подставку. Поместите коническую колбу под бюретку и добавьте в нее несколько капель HCl с этим выпуском Al(OH) 3 в той же колбе . Добавляйте индикатор с помощью капли, пока он не достигнет конечной точки, а цвет не изменится на розовый.
HCl + Al (OH) 3 Чистое ионное уравнение- Следующие шаги могут определить ионную реакцию
- Должны написать уравнение равновесия. ——> AlCl 3 + 3H 2 O
- Разделить компоненты на составляющие ионы, которые являются общими Ионное уравнение для HCl + AL(OH) 3 50097 H + + Cl – + Al + + OH 3 – = Al + + Cl 3 – + 3H 2 O HCl+ Al(OH) 3 сопряженные пары
Всякий раз, когда кислота отдает протон, она превращается в сопряженное основание и сильную кислоту.
Сопряженная кислота-основа HCl и Al(OH) 3 1 межмолекулярные силы 9019 наоборот таким образом, сопряженным основанием является Cl – для HCl и OH – является основанием, поэтому кислота представляет собой Al(OH) 3
наоборот таким образом, сопряженным основанием является Cl – для HCl и OH – является основанием, поэтому кислота представляет собой Al(OH) 3 - HCl представляет собой ионное соединение, которое содержит диполь-дипольную силу притяжения с силой Лондона в молекулах .
- AL(OH) 3 содержит водородные силы с лондонской дисперсионной силой притяжения .
Энтальпия – это количество энергии, необходимое для завершения реакции реагента и продукта. Энтальпия реакции 3HCl + AL (OH) 3 -> ALCL 3 + 3H 2 O будет ,
ALCL 3 (S) –705. /моль HCl(г) = -92 кДж/моль. H 2 O(ж) = -285,8 кДж/моль. Al(OH) 3 (с) = −285,8 кДж/моль
H 2 O(ж) = -285,8 кДж/моль. Al(OH) 3 (с) = −285,8 кДж/моль
Энтальпия конечной реакции будет = (-285,8 кДж/моль Al + 3 x -285,8) – (-1277,0) – (3 x –92,0) = – 10,0 кДж/моль
Is HCl + Al(ОН) 3 буферный растворне делайте буферный раствор, потому что значение pH буфера всегда должно быть 14.
Is HCl + Al(OH) 3 полная реакцияHCl + Al(OH) 3 является полной реакцией, потому что HCl является сильной кислотой, а Al(OH) 3 70098 является сильным основанием,
8 нейтрализуют оба8 ионы друг друга и полностью диссоциируют в воде с образованием новых соединений. Is HCl + Al(OH) 3 экзотермическая или эндотермическая реакцияСоляная кислота с гидроксидом алюминия является экзотермической реакцией, что означает выделение большого количества тепла, а энтропия также меньше


 наоборот таким образом, сопряженным основанием является Cl – для HCl и OH – является основанием, поэтому кислота представляет собой Al(OH) 3
наоборот таким образом, сопряженным основанием является Cl – для HCl и OH – является основанием, поэтому кислота представляет собой Al(OH) 3