Фосфор, его соединения и химические свойства
Похожие презентации:
Сложные эфиры. Жиры
Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Газовая хроматография
Хроматографические методы анализа
Искусственные алмазы
Титриметрические методы анализа
Биохимия гормонов
Антисептики и дезинфицирующие средства. (Лекция 6)
Клиническая фармакология антибактериальных препаратов
Биохимия соединительной ткани
Фосфор, его
соединения
и химические
свойства
Электронное строение атома фосфора и
сравнение его с азотом
P
3s
Валентность III
3d
3p
P*
3s
Валентность V
3d
3p
Энергия химических
связей (кДж/моль)
Свойство
N
P
Степени окисления
-3, -2, -1, 0, +1, +2, +3, +4, +5
-3, 0, +3, +5
Энергия ионизации,
кДж/моль
Электроотрицательн
ость по Полингу
I1
∑ I1-3
1402
8835
3,0
I1
1012
5825
2,1
2
Природные соединения
Из-за большой химической активности
встречается в природе только в виде соединений.

Важнейшими минералами фосфора являются:
Фосфорит
Апатит
Са3(РО4)2
Са3(РО4)2•СаF2
Са3(РО4)2•СаCl2
3
Получение
Фридрих Вёлер 1829 год!
Фосфор производят в электрических печах,
восстанавливая апатит углем в присутствии
кремнезема:
2Ca3(PO4)2 + 6SiO2 + 10C = 6CaSiO3 + 10CO + P4
апатит,
кости
Пары фосфора при этой температуре почти
полностью состоят из молекул Р2, которые при
охлаждении конденсируются в молекулы Р4.
4
Аллотропные модификации
P
Белый
Черный
Красный
tпл.= 44,1°С ; tкип = 287,3°С
Белое кристаллическое
вещество.
Чесночный запах. Ядовит,
самовозгорается на
воздухе. Не растворим в
воде. Очень хорошо
растворим в сероуглероде.
tпл.= 590°С; tкип = 416°С
Красный кристаллический или
аморфный порошок.
Без запаха. Не ядовит. Загорается на
воздухе только при поджигании.
tпл.= 1000°С; Наиболее устойчивая
форма. Имеет сходство с
графитом.

Без запаха. Не ядовит и не
огнеопасен.
Проводит электрический ток.
5
Аллотропные модификации
P
Белый
Черный
Красный
tпл.= 44,1°С ; tкип = 287,3°С
Белое кристаллическое
вещество.
Чесночный запах. Ядовит,
самовозгорается на
воздухе. Не растворим в
воде. Очень хорошо
растворим в сероуглероде.
tпл.= 590°С; tкип = 416°С
Красный кристаллический или
аморфный порошок.
Без запаха. Не ядовит. Загорается на
воздухе только при поджигании.
tпл.= 1000°С; Наиболее устойчивая
форма. Имеет сходство с
графитом.
Без запаха. Не ядовит и не
огнеопасен.
6
Химические свойства
Восстановитель с более электроотрицательными неметаллами:
5О2 (изб.) + 4Р = 2Р2О5
3О2 (недост.) + 4Р = 2Р2О3
3Сl2 + 2P = 2PCl3
PСl3 + Cl2 = PCl5
3P + 5HNO3 + 2h3O = 3h4PO4 + 5NO
Окислитель взаимодействует со многими металлами, образуя фосфиды :
2Р + 3Mg = Mg3P2
7
Химические свойства
Реакция с водой (в нейтральной среде):
P + h3 O =
Реакция с водой в щелочной среде:
4P + 3NaOH + 3h3O = 3Nah3PO2 + Ph4
8
Химические свойства
Реакция с водой (в нейтральной среде):
P + h3 O =
Реакция с водой в щелочной среде:
4P + 3NaOH + 3h3O = 3Nah3PO2 + Ph4
Гипофосфит натрия
9
Химические свойства
Реакция с водой (в нейтральной среде):
P + h3 O =
Реакция с водой в щелочной среде:
4P + 3NaOH + 3h3O = 3Nah3PO2 + Ph4
Гипофосфит натрия
Реакция при наличии ионов Ag(I)/Cu(II):
2Р + 5CuSO4 + 8Н2O = 2Н3РO4 + 5Cu + 5h3SO4
Каталитическая реакция красного фосфора с водой:
t, Pt/Cu
2P + 8h3O = 2h4PO4 + 5h3
10
Фосфин
Фосфор в степени окисления -3 образует водородное
соединение фосфин Ph4, аналогичное аммиаку.
 Эта степень
Эта степеньокисления менее характерна для фосфора, чем для азота.
Фосфин – ядовитый газ с неприятным запахом тухлой рыбы и
чеснока. Он может быть получен из фосфидов обычным
гидролизом или действием кислоты.
Zn3P2 + 6h3O = 3Zn(OH)2 + 2Ph4
Zn3P2 + 6HCl = 2Ph4 + 3ZnCl2
11
Кислотно-основные свойства фосфина
Основные свойства фосфина слабее, чем у аммиака:
Ph4 + HCl = Ph5Cl
Соли фосфония в водных растворах крайне неустойчивы:
Ph5+ + h3O Ph4 + h4O+
В то же время фосфин является кислотой: активные металлы
замещают в нем один водород, образуя фосфиниды МРН2.
Ph4 + M = Ph3M + h3 (M = Li,…,Na)
Кислотность фосфина во много раз превосходит кислотность
гидридов:
Nh4 + РН3 = Nh5+РН212
Окислительно-восстановительные свойства
Фосфин имеет сильные восстановительные свойства
(низшая несвойственная степень окисления фосфора),
самовоспламеняется на воздухе:
РН3 + 2O2 = НРO3 + Н2O
13
14
15
Окислительно-восстановительные свойства
Фосфин имеет сильные восстановительные свойства
(низшая несвойственная степень окисления фосфора),
самовоспламеняется на воздухе:
РН3 + 2O2 = НРO3 + Н2O
в избытке кислорода:
2Ph4 + 4O2 P2O5 + 3h3O или Ph4 + 2O2 h4PO4
Окисляется очень многими окислителями:
Ph4 + 8HNO3(к) → 8NO2↑ + h4PO4 + 4h3O
Ph4 + 4Cl2 + 4h3O = h4PO4 + 8HCl
16
Оксид фосфора (III) – P2O3 /P4O6
Белый рыхлый кристаллический порошок (tпл = 24 °С, tкип =
174 °С), легко возгоняющийся.
 Имеет неприятный запах,
Имеет неприятный запах,ядовит.
P4O6 окисляется кислородом воздуха
P4O6 + 2O2 = P4O10
Реакция сопровождается хемилюминесценцией и является
причиной свечения белого фосфора.
17
Оксид фосфора (III) – P2O3 /P4O6
Называют фосфористым ангидридом, так как он
взаимодействует с холодной водой с образованием
фосфористой кислоты:
P4O6 + 6Н2O = 4Н3РO3
При повышенной температуре фосфористая кислота
диспропорционирует на ортофосфорную кислоту и
фосфин:
4Н3РO3 = Ph4 + 3h4PO4
18
Оксид фосфора (V) – P2O5 /P4O10
Белый порошок, очень гигроскопичен (эффективный
осушитель). Способен отнимать воду от других
соединений.
2HNO3 + P2O5 = 2HPO3 + N2O5
19
Химические свойства P2O5
Типичный кислотный оксид — взаимодействует с основаниями и основными
оксидами. Ему соответствует мета- и ортофосфорная кислота.
Реакция с водой:
P2O5 + h3O = 2HPO3 метафосфорная кислота
P2O5 + 3h3O = 2h4PO4 ортофосфорная кислота
Реакция с основными оксидами:
С основаниями:
P2O5 + 6NaOH = 2Na3РО4 + 3h3O
Не проявляет окислительных свойств.

20
Ортофосфорная кислота
Кристаллическое (tпл = 42 ºС), нелетучее, твердое, бесцветное
вещество.
В промышленности фосфорную кислоту получают действием серной
кислоты на фосфорит:
Ca3(PO4)2 + 3h3SO4 3CaSO4 + 2h4PO4
Альтернативные способы:
3P + 5HNO3 + 2h3O = 3h4PO4 + 5NO
P2O5 + 3h3O = 2h4PO4
Смешивается с водой в любых отношениях.
Типичная кислота неокислитель.
Кислота средней силы.
Не проявляет окислительных свойств.
21
Химические свойства
С металлами, стоящими в ряду напряжения до водорода:
3Mg + 2h4PO4 = Mg3(PO4)2 + 3h3↑
С основными оксидами:
3CaO + 2h4PO4 Сa3(PO4)2 + 3h3O
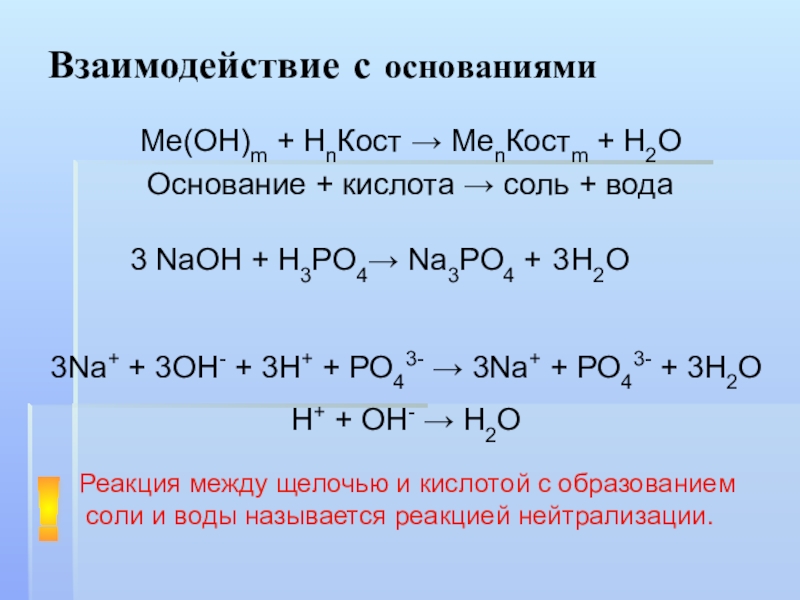
С основаниями:
h4PO4 + NaOH → Nah3PO4 + h3O
h4PO4 + 2NaOH → Na2HPO4 + 2h3O
h4PO4 + 3NaOH → Na3PO4 + 3h3O
h4PO4 + Nh4 → (Nh5)2HPO4
22
Химические свойства
С солями более слабых кислот:
2h4PO4 + 3Na2CO3 = 2Na3PO4 + 3h3O + 3CO2↑
При нагревании превращается в пирофосфорную кислоту:
2h4PO4 = h5P2O7 + h3O пирофосфорная кислота
При действии раствора нитрата серебра появляется
желтый осадок:
h4PO4 + 3AgNO3 → Ag3PO4 ↓ + 3HNO3
желтый осадок
Это качественная реакция на фосфорную кислоты и
фосфаты.

23
Соли фосфорной кислоты
Средние соли — фосфаты (Na3PO4)
Кислые соли — гидрофосфаты (Na2HPO4)
и дигидрофосфаты (Nah3PO4).
Фосфорная кислота вытесняется более сильными кислотами
из её солей:
Сa3(PO4)2 + 3h3SO4(конц.) = 3CaSO4 + 2h4PO4
24
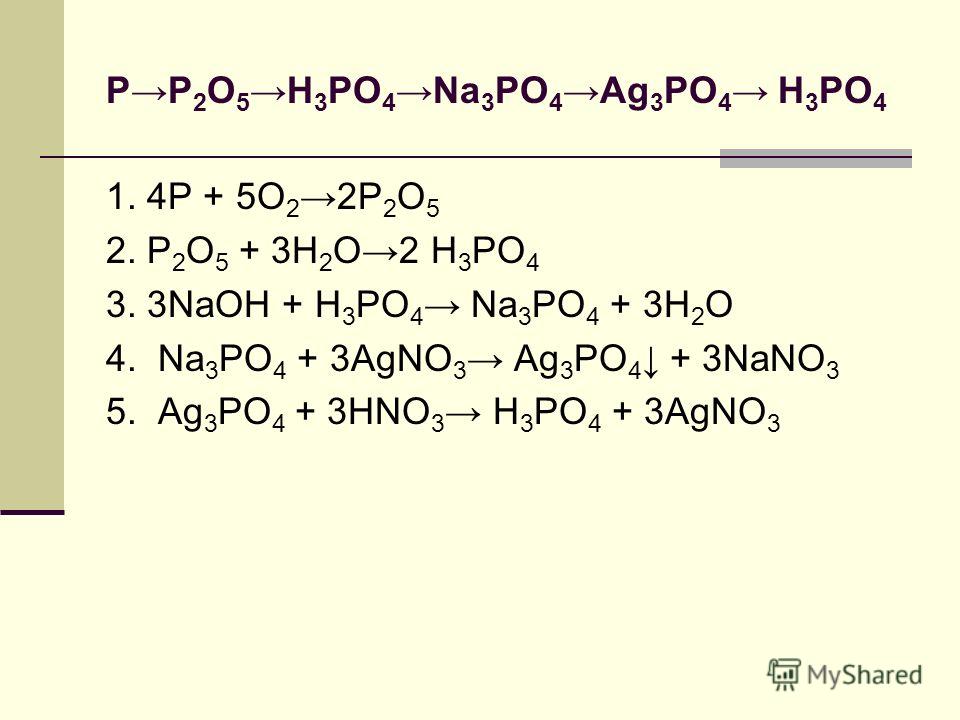
Применение фосфора
• Около 80% от всего производства белого фосфора идет на
синтез чистой ортофосфорной кислоты. Она используется
снижения жесткости питьевой воды) и пищевых фосфатов.
• Зажигательная поверхность спичечного коробка покрыта
смесью красного фосфора и порошка стекла. В состав
спичечной головки входят окислители (PbO2, KСlO3,
BaCrO4) и восстановители (S, Sb2S3). При трении от
зажигательной поверхности смесь, нанесенная на спичку,
воспламеняется.
Триполифосфат натрия (Е451)
26
28
English Русский Правила
Осуществите схему превращений, назовите продукты реакцииP-P2O5-h4PO4-Na3PO4-Ba3(PO4)2 — Знания.
 site
siteКто не видел белого медведя? В зоопарках он – обычный гость. Нет нужды описывать, каков он на вид. Напомним лишь, что у него только нос черный, сам медведь белый и зимой, и летом (а не как, скажем, песец или заяц-беляк – те лишь зимой белые). Подошвы лап у белого медведя густой шерстью поросли, а пальцы примерно на половину своей длины соединены плавательными перепонками.
Плавают и ныряют белые медведи отлично. Две минуты могут пробыть под водой, но погружаются в нее редко глубже двух метров. Далеко в открытом море не раз видели белых медведей, даже медведиц с медвежатами. Плывут со скоростью 5 километров в час, не беспокоясь, что ни земли, ни льдов нигде вблизи не видно.
Белый медведь и тюленей ловит не только на льду, украдкой к ним подползая. Обычный его прием, так сказать, атаки с моря такой: поблизости от лежбищ тюленей медведь осторожно, без плеска и шума, сползает в воду, плывет туда, где заметил тюленей. Затем он бесшумно ныряет и выныривает уже у самого лежбища, быстро карабкается на лед, отрезая тем самым тюленям путь к спасительной воде. По отвесным ледяным стенам медведь может прямо из воды выпрыгнуть на льдину, даже если высота ее над водой два метра.
По отвесным ледяным стенам медведь может прямо из воды выпрыгнуть на льдину, даже если высота ее над водой два метра.
Тюлени – главная охотничья добыча белого медведя весной. За год ловит и съедает он примерно 50 тюленей. Летом меню его более разнообразно. Ловит он рыбу на мелкой воде, на берегу – леммингов, песцов, лакомится яйцами птиц. Когда голоден, ест ягоды, водоросли, мхи, лишайник, грибы.
Белый медведь – самый могучий из сухопутных хищных зверей. Лев и тигр в сравнении с ним легковесы: средний вес медведиц 310 килограммов, медведей-самцов – 420 килограммов. Если медведь матерый и хорошо упитанный, то он может весить целую тонну!
Акимушкин И.И. Мир животных: Млекопитающие, или звери. – М., 1988 г
IV. Тест по русскому языку
1. В тексте про белых медведей больше всего предложений:
а) повествовательных; б) вопросительных
2. Восклицательное предложение находится:
а) в начале текста; б) в конце текста
3. Вопросительное предложение находится
а) в начале текста; б) в конце текста
4. Выпиши из второй части текста (из второго абзаца) первое предложение. Разбери его по членам предложения. Что ты можешь сказать о сказуемых? Они являются
Выпиши из второй части текста (из второго абзаца) первое предложение. Разбери его по членам предложения. Что ты можешь сказать о сказуемых? Они являются
а) родственными словами; б) однородными членами предложения
5. Что можно сказать о глаголах, которыми выражены сказуемые? Эти глаголы:
а) I спряжения; б) II спряжения
6. Эти глаголы стоят в форме:
а) настоящего времени; б) будущего времени; в) прошедшего времени
7. Эти глаголы стоят в форме:
а) единственного числа; б) множественного числа
8. Эти глаголы стоят в форме:
а) 1-го лица; б) 2-го лица; в) 3-го лица; г)нельзя определить лицо
9. Эти глаголы стоят в форме:
а) ж.р.; б) м.р.; в) ср.р.; г) нельзя определить род
10. Найди во второй части текста (во втором абзаце) все слова, которые являются родственными существительному, являющемуся подлежащим в первом предложении. Запиши их столбиком, поставив в начальную форму. У тебя получилось:
а) два слова; б) три слова
11. Найди во второй части текста (во втором абзаце) другую форму слова, которое является подлежащим в первом предложении. Выпиши такое словосочетание с формой этого слова, из которого можно определить его падеж. Этот падеж:
Найди во второй части текста (во втором абзаце) другую форму слова, которое является подлежащим в первом предложении. Выпиши такое словосочетание с формой этого слова, из которого можно определить его падеж. Этот падеж:
а) Р.п.; б) В.п.
Ответ: NaOH реагирует с h4PO4 с образованием натрия…
Задача 1RQ: Определите и объясните различия между следующими терминами. а. право и теория б. теория и… Проблема 2RQ: Подходит ли научный метод для решения проблем только в естественных науках? Объясните. Задача 3RQ: Какое из следующих утверждений может быть проверено количественным измерением? а. Тай Кобб был… Задача 4RQ: Для каждого из следующих предметов стеклянной посуды укажите размеры образца и обсудите количество… Задача 5RQ: Студент провел анализ образца на содержание в нем кальция и получил следующие результаты. :…Задача 6RQ: Сравните и сопоставьте правило значащей цифры умножения/деления со значащей цифрой… Задача 7RQ: Объясните, как плотность можно использовать в качестве коэффициента преобразования для преобразования объема объекта в. .. Задача 8RQ: На какой температурной шкале (F, C. или K) 1 градус соответствует наименьшему изменению температуры? Задача 9RQ: Различайте физические изменения и химические изменения. Задача 10RQ: Почему разделение смесей на чистые или относительно чистые вещества так важно, когда… Задача 1ALQ: a. В году 365 дней, 24 часа в сутках, 12 месяцев в году и 60 минут в часе. Используйте… Задача 2ALQЗадача 3ALQ: Когда шарик брошен в стакан с водой, он опускается на дно. Что из следующего является… Задача 4ALQЗадача 5ALQ: Вы могли заметить, что когда вода кипит, вы можете видеть пузырьки, которые поднимаются на поверхность… Задача 6ALQ: Если вы поместите стеклянную палочку над горящей свечой, кажется, что стекло становится черным. Что происходит… Задача 7ALQ: Какие характеристики твердого тела, жидкости и газа проявляются в каждом из следующих… Задача 8ALQ: Нарисуйте увеличенное изображение (показывающее атомы/молекулы) каждого из следующих и объяснить: а. а… Задача 9ALQ: Парацельс, алхимик и целитель шестнадцатого века, принял в качестве своего лозунга: «Пациенты — это ваши.
.. Задача 8RQ: На какой температурной шкале (F, C. или K) 1 градус соответствует наименьшему изменению температуры? Задача 9RQ: Различайте физические изменения и химические изменения. Задача 10RQ: Почему разделение смесей на чистые или относительно чистые вещества так важно, когда… Задача 1ALQ: a. В году 365 дней, 24 часа в сутках, 12 месяцев в году и 60 минут в часе. Используйте… Задача 2ALQЗадача 3ALQ: Когда шарик брошен в стакан с водой, он опускается на дно. Что из следующего является… Задача 4ALQЗадача 5ALQ: Вы могли заметить, что когда вода кипит, вы можете видеть пузырьки, которые поднимаются на поверхность… Задача 6ALQ: Если вы поместите стеклянную палочку над горящей свечой, кажется, что стекло становится черным. Что происходит… Задача 7ALQ: Какие характеристики твердого тела, жидкости и газа проявляются в каждом из следующих… Задача 8ALQ: Нарисуйте увеличенное изображение (показывающее атомы/молекулы) каждого из следующих и объяснить: а. а… Задача 9ALQ: Парацельс, алхимик и целитель шестнадцатого века, принял в качестве своего лозунга: «Пациенты — это ваши. .. Проблема 10ALQ: Что не так со следующим утверждением?» Результаты эксперимента не согласуются с… Задача 11ALQ: Почему неправильно говорить, что результаты измерения были точными, но неточными? Задача 14ALQ: У вас есть образец свинца объемом 1,0 см3 и образец стекла объемом 1,0 см3. Вы опускаете каждую в отдельный стакан… Задача 15ALQ: Рассмотрите прибавление 15,4 к 28. Какой ответ сказал бы математик? Что бы… Задача 16ALQ: Попробуйте умножить 26,2 на 16,43. Какой ответ сказал бы математик? Что бы… Задача 17ALQ: Правда или ложь? Для математической операции, выполненной на двух измерениях, число значимых… Задача 18ALQ: Есть ли разница между гомогенной смесью водорода и кислорода в соотношении 2:1 и… Задача 19В: Разница между законом и теорией — это разница между «что» и «почему». Объясните. Проблема 20Q: Научный метод — это динамический процесс. Что это значит? Задача 21Q. Объясните основные этапы научного метода. Задача 22Q. Проблема 23Q. Измерение — это количественное наблюдение, включающее как число, так и единицу измерения.
.. Проблема 10ALQ: Что не так со следующим утверждением?» Результаты эксперимента не согласуются с… Задача 11ALQ: Почему неправильно говорить, что результаты измерения были точными, но неточными? Задача 14ALQ: У вас есть образец свинца объемом 1,0 см3 и образец стекла объемом 1,0 см3. Вы опускаете каждую в отдельный стакан… Задача 15ALQ: Рассмотрите прибавление 15,4 к 28. Какой ответ сказал бы математик? Что бы… Задача 16ALQ: Попробуйте умножить 26,2 на 16,43. Какой ответ сказал бы математик? Что бы… Задача 17ALQ: Правда или ложь? Для математической операции, выполненной на двух измерениях, число значимых… Задача 18ALQ: Есть ли разница между гомогенной смесью водорода и кислорода в соотношении 2:1 и… Задача 19В: Разница между законом и теорией — это разница между «что» и «почему». Объясните. Проблема 20Q: Научный метод — это динамический процесс. Что это значит? Задача 21Q. Объясните основные этапы научного метода. Задача 22Q. Проблема 23Q. Измерение — это количественное наблюдение, включающее как число, так и единицу измерения. Что такое… Задача 24В: Чтобы определить объем куба, учащийся измерил одно из измерений куба несколькими… Задача 25В: Что такое значащие цифры? Покажите, как указать число одна тысяча до 1 значащей цифры,… Задача 26В: Проходит холодный фронт, и температура падает на 20 градусов. В какой температурной шкале будет… Задача 28В: В многоступенчатом расчете лучше ли округлить числа до правильного числа… Задача 29В: Плотность газообразного вещества больше или меньше плотности жидкости или твердого тела при… Задача 30В: Приведите четыре примера, иллюстрирующие каждый из следующих терминов. а. однородная смесь б. гетерогенные… Задача 31E: Какие из следующих чисел являются точными? а. В 1 м 100 см. б. Один метр равен 1,094… Задача 32E: Укажите количество значащих цифр в каждом из следующих чисел: a. Эта книга содержит более… Задача 33E: Сколько значащих цифр в каждом из следующих значений? а. 6.07 1015 б. 0,003840 c…. Задача 34E: Сколько значащих цифр в каждом из следующих чисел? а.
Что такое… Задача 24В: Чтобы определить объем куба, учащийся измерил одно из измерений куба несколькими… Задача 25В: Что такое значащие цифры? Покажите, как указать число одна тысяча до 1 значащей цифры,… Задача 26В: Проходит холодный фронт, и температура падает на 20 градусов. В какой температурной шкале будет… Задача 28В: В многоступенчатом расчете лучше ли округлить числа до правильного числа… Задача 29В: Плотность газообразного вещества больше или меньше плотности жидкости или твердого тела при… Задача 30В: Приведите четыре примера, иллюстрирующие каждый из следующих терминов. а. однородная смесь б. гетерогенные… Задача 31E: Какие из следующих чисел являются точными? а. В 1 м 100 см. б. Один метр равен 1,094… Задача 32E: Укажите количество значащих цифр в каждом из следующих чисел: a. Эта книга содержит более… Задача 33E: Сколько значащих цифр в каждом из следующих значений? а. 6.07 1015 б. 0,003840 c…. Задача 34E: Сколько значащих цифр в каждом из следующих чисел? а. 100 б. 102 в. 103 д. 100. э. 0,0048… Задача 35E: Округлите каждое из следующих чисел до указанного количества значащих цифр и запишите… Задача 36E: Используйте экспоненциальную запись, чтобы представить число 385 500 в a. одна значащая цифра. б. два… Задача 37E: У вас есть жидкость в каждом показанном градуированном цилиндре: Затем вы добавляете оба образца в химический стакан. Как бы… Задача 38E: Пробирки, показанные ниже, имеют разную точность. а. Обозначьте количество воды в каждом из трех… Задача 39E: Оцените каждое из следующих действий и запишите ответ с соответствующим числом значащих… Задача 40E: Выполните следующие математические операции и приведите каждый результат к правильному числу… Задача 41E: Выполните следующие математические операции , и приведите результат к правильному количеству… Задача 42E: Выполните следующие математические операции и приведите результат к правильному количеству… Задача 43E: Выполните каждое из следующих преобразований. а. 8,43 см в миллиметры b.
100 б. 102 в. 103 д. 100. э. 0,0048… Задача 35E: Округлите каждое из следующих чисел до указанного количества значащих цифр и запишите… Задача 36E: Используйте экспоненциальную запись, чтобы представить число 385 500 в a. одна значащая цифра. б. два… Задача 37E: У вас есть жидкость в каждом показанном градуированном цилиндре: Затем вы добавляете оба образца в химический стакан. Как бы… Задача 38E: Пробирки, показанные ниже, имеют разную точность. а. Обозначьте количество воды в каждом из трех… Задача 39E: Оцените каждое из следующих действий и запишите ответ с соответствующим числом значащих… Задача 40E: Выполните следующие математические операции и приведите каждый результат к правильному числу… Задача 41E: Выполните следующие математические операции , и приведите результат к правильному количеству… Задача 42E: Выполните следующие математические операции и приведите результат к правильному количеству… Задача 43E: Выполните каждое из следующих преобразований. а. 8,43 см в миллиметры b. 2.41 102 см в метры c….Задача 44E: a. Сколько килограммов в 1 тераграмме? б. Сколько нанометров в 6,50 х 102 тераметров? в. Как… Задача 45E: Выполните следующие преобразования единиц измерения. а. Поздравляем! Вы и ваш супруг гордитесь… Задача 46E: Выполните следующие преобразования единиц измерения. а. 908 унций в килограммы b. 12,8 л в галлоны c. 125 мл в… Задача 47E: Используйте следующие точные коэффициенты преобразования для выполнения заявленных расчетов: 512 ярдов -= 1 стержень 40… Задача 48E: Хотя предпочтительной единицей площади в системе СИ является квадратный метр, часто измеряется земля в метрической… Задача 49E: Драгоценные металлы и драгоценные камни измеряются в тройских весах в английской системе: 24 грана 1 пеннивейт… Задача 50E: Аптеки (фармацевты) используют следующий набор мер в английской системе: 20 гран ap = 1… Задача 51E: Фармацевту, выдающему пилюли или капсулы, часто бывает легче взвесить лекарство, чтобы быть… Задача 52E: Детский обезболивающий эликсир содержит 80 мг ацетаминофена на 0,50 чайной ложки.
2.41 102 см в метры c….Задача 44E: a. Сколько килограммов в 1 тераграмме? б. Сколько нанометров в 6,50 х 102 тераметров? в. Как… Задача 45E: Выполните следующие преобразования единиц измерения. а. Поздравляем! Вы и ваш супруг гордитесь… Задача 46E: Выполните следующие преобразования единиц измерения. а. 908 унций в килограммы b. 12,8 л в галлоны c. 125 мл в… Задача 47E: Используйте следующие точные коэффициенты преобразования для выполнения заявленных расчетов: 512 ярдов -= 1 стержень 40… Задача 48E: Хотя предпочтительной единицей площади в системе СИ является квадратный метр, часто измеряется земля в метрической… Задача 49E: Драгоценные металлы и драгоценные камни измеряются в тройских весах в английской системе: 24 грана 1 пеннивейт… Задача 50E: Аптеки (фармацевты) используют следующий набор мер в английской системе: 20 гран ap = 1… Задача 51E: Фармацевту, выдающему пилюли или капсулы, часто бывает легче взвесить лекарство, чтобы быть… Задача 52E: Детский обезболивающий эликсир содержит 80 мг ацетаминофена на 0,50 чайной ложки. Дозировка… Проблема 53E: Научная фантастика часто использует морские аналогии для описания космических путешествий. Если бы звездолет U.S.S…. Задача 54E: Мировой рекорд в беге на сто метров — 90,58 с. Какова соответствующая средняя скорость в… Задача 55E: Вы едете со скоростью 65 миль/ч и отводите взгляд от дороги всего на секунду. Какое расстояние (в футах)… Задача 56E: Вы проезжаете мимо дорожного знака, говорящего о Нью-Йорке 112 км. Если вы едете с постоянной скоростью 65 миль/ч, как долго… Задача 57E: Дозировка антибиотика составляет 8,0 мг на килограмм массы тела два раза в день… Задача 58E: В последнее время лет был большой толчок к увеличению использования возобновляемых ресурсов для… Проблема 59EПроблема 60E: Детекторы угарного газа (CO) подают сигнал тревоги, когда пиковые уровни угарного газа достигают 100 частей… Задача 61E: Преобразуйте следующие температуры по шкале Фаренгейта в шкалы Цельсия и Кельвина. а. 459F, an… Задача 62E: Термометр показывает 96,1F 0,2F.
Дозировка… Проблема 53E: Научная фантастика часто использует морские аналогии для описания космических путешествий. Если бы звездолет U.S.S…. Задача 54E: Мировой рекорд в беге на сто метров — 90,58 с. Какова соответствующая средняя скорость в… Задача 55E: Вы едете со скоростью 65 миль/ч и отводите взгляд от дороги всего на секунду. Какое расстояние (в футах)… Задача 56E: Вы проезжаете мимо дорожного знака, говорящего о Нью-Йорке 112 км. Если вы едете с постоянной скоростью 65 миль/ч, как долго… Задача 57E: Дозировка антибиотика составляет 8,0 мг на килограмм массы тела два раза в день… Задача 58E: В последнее время лет был большой толчок к увеличению использования возобновляемых ресурсов для… Проблема 59EПроблема 60E: Детекторы угарного газа (CO) подают сигнал тревоги, когда пиковые уровни угарного газа достигают 100 частей… Задача 61E: Преобразуйте следующие температуры по шкале Фаренгейта в шкалы Цельсия и Кельвина. а. 459F, an… Задача 62E: Термометр показывает 96,1F 0,2F. Какая температура в С? Что такое неопределенность? Задача 63E: Преобразуйте следующие значения температуры по Цельсию в градусы Кельвина и Фаренгейта. а. температура… Задача 64E: Преобразуйте следующие температуры Кельвина в градусы Цельсия и Фаренгейта. а. температура, которая… Задача 65E: При какой температуре температура в градусах Фаренгейта равна удвоенной температуре в… Задача 66E: Средняя дневная температура на Земле и Юпитере составляет 72F и 313 K соответственно. Вычислите… Задача 67E: Используйте рисунок ниже, чтобы ответить на следующие вопросы. а. Выведите соотношение между C и X…. Задача 68E: Этиленгликоль является основным компонентом автомобильного антифриза. Чтобы следить за температурой… Задача 69E: Материал будет плавать на поверхности жидкости, если этот материал имеет плотность меньше плотности… Задача 70E: Один металлический предмет представляет собой куб с ребрами 3,00 см и массой 140,4 г. Второй металлический объект — это… Задача 71E. По оценкам, звезда имеет массу 2 1036 кг.
Какая температура в С? Что такое неопределенность? Задача 63E: Преобразуйте следующие значения температуры по Цельсию в градусы Кельвина и Фаренгейта. а. температура… Задача 64E: Преобразуйте следующие температуры Кельвина в градусы Цельсия и Фаренгейта. а. температура, которая… Задача 65E: При какой температуре температура в градусах Фаренгейта равна удвоенной температуре в… Задача 66E: Средняя дневная температура на Земле и Юпитере составляет 72F и 313 K соответственно. Вычислите… Задача 67E: Используйте рисунок ниже, чтобы ответить на следующие вопросы. а. Выведите соотношение между C и X…. Задача 68E: Этиленгликоль является основным компонентом автомобильного антифриза. Чтобы следить за температурой… Задача 69E: Материал будет плавать на поверхности жидкости, если этот материал имеет плотность меньше плотности… Задача 70E: Один металлический предмет представляет собой куб с ребрами 3,00 см и массой 140,4 г. Второй металлический объект — это… Задача 71E. По оценкам, звезда имеет массу 2 1036 кг. Предполагая, что это сфера среднего радиуса 7,0 … Задача 72E: Прямоугольный блок имеет размеры 2,9 см 3,5 см 10,0 см. Масса блока 615,0 г. Что… Задача 73E: Бриллианты измеряются в каратах, а 1 карат = 0,200 г. Плотность алмаза 3,51 г/см3. a….Задача 74E: При комнатной температуре элемент бром, Br2, представляет собой жидкость с плотностью 3,12 г/см3. Вычислите… Задача 75E: Образец, содержащий 33,42 г металлических гранул, сначала высыпается в градуированный цилиндр… Задача 76E: Плотность чистого серебра составляет 10,5 г/см3 при 20°C. Если 5,25 г гранул чистого серебра добавить к… Задача 77E: Какая из следующих пар имеет большую массу в каждой из следующих пар? (См. Таблицу 1.5.) а. 1,0 кг перьев… Задача 78E: a. Рассчитайте массу этанола в 1,50 л этанола. (См. Таблицу 1.5.) б. Вычислите массу… Задача 79Э: Какая из следующих пар имеет больший объем? а. 1,0 кг пера или 1,0 кг… Задача 80E: Используя таблицу 1.5, рассчитайте объем 25,0 г каждого из следующих веществ при 1 атм.
Предполагая, что это сфера среднего радиуса 7,0 … Задача 72E: Прямоугольный блок имеет размеры 2,9 см 3,5 см 10,0 см. Масса блока 615,0 г. Что… Задача 73E: Бриллианты измеряются в каратах, а 1 карат = 0,200 г. Плотность алмаза 3,51 г/см3. a….Задача 74E: При комнатной температуре элемент бром, Br2, представляет собой жидкость с плотностью 3,12 г/см3. Вычислите… Задача 75E: Образец, содержащий 33,42 г металлических гранул, сначала высыпается в градуированный цилиндр… Задача 76E: Плотность чистого серебра составляет 10,5 г/см3 при 20°C. Если 5,25 г гранул чистого серебра добавить к… Задача 77E: Какая из следующих пар имеет большую массу в каждой из следующих пар? (См. Таблицу 1.5.) а. 1,0 кг перьев… Задача 78E: a. Рассчитайте массу этанола в 1,50 л этанола. (См. Таблицу 1.5.) б. Вычислите массу… Задача 79Э: Какая из следующих пар имеет больший объем? а. 1,0 кг пера или 1,0 кг… Задача 80E: Используя таблицу 1.5, рассчитайте объем 25,0 г каждого из следующих веществ при 1 атм. a….Задача 81E: Плотность осмия (самого плотного металла) равна 22,57 г/см3. Если прямоугольный блок осмия весом 1,00 кг… Задача 82E: Медная проволока (плотность = 8,96 г/см3) имеет диаметр 0,25 мм. Если образец этой медной проволоки имеет… Задача 83E: Сопоставьте каждое приведенное ниже описание со следующими микроскопическими изображениями. Может подойти более одной картинки… Задача 84E: Дайте определение следующим терминам: твердое тело, жидкость, газ, чистое вещество, элемент, соединение, однородное… Задача 85E: В чем разница между гомогенным и гетерогенным веществом? Классифицируйте каждое из следующего… Задача 86E: Классифицируйте следующие смеси как гомогенные или гетерогенные. а. горшечная почва б. белое вино c…. Задача 87E: Классифицируйте каждое из следующих веществ как смесь или чистое вещество. а. вода б. кровь в. океаны d…. Задача 88E: Предположим, что чайная ложка магниевых опилок и чайная ложка порошкообразной серы помещены вместе в… Задача 89.E: Если кусок твердого белого школьного мела сильно нагреть в пламени, масса куска.
a….Задача 81E: Плотность осмия (самого плотного металла) равна 22,57 г/см3. Если прямоугольный блок осмия весом 1,00 кг… Задача 82E: Медная проволока (плотность = 8,96 г/см3) имеет диаметр 0,25 мм. Если образец этой медной проволоки имеет… Задача 83E: Сопоставьте каждое приведенное ниже описание со следующими микроскопическими изображениями. Может подойти более одной картинки… Задача 84E: Дайте определение следующим терминам: твердое тело, жидкость, газ, чистое вещество, элемент, соединение, однородное… Задача 85E: В чем разница между гомогенным и гетерогенным веществом? Классифицируйте каждое из следующего… Задача 86E: Классифицируйте следующие смеси как гомогенные или гетерогенные. а. горшечная почва б. белое вино c…. Задача 87E: Классифицируйте каждое из следующих веществ как смесь или чистое вещество. а. вода б. кровь в. океаны d…. Задача 88E: Предположим, что чайная ложка магниевых опилок и чайная ложка порошкообразной серы помещены вместе в… Задача 89.E: Если кусок твердого белого школьного мела сильно нагреть в пламени, масса куска. .. Задача 90E: В очень холодную зиму температура может оставаться ниже нуля в течение длительного времени. Однако… Задача 91E: Классифицируйте следующие физические или химические изменения. а. Шарики от моли постепенно испаряются в… Задача 92E: Свойства смеси обычно являются средними значениями свойств ее компонентов. Задача 93AE: Два сферических объекта имеют одинаковую массу. Один плавает по воде; другой тонет. Какой объект имеет… Задача 94AE: 194-граммовый образец кофеина (C8h20N4O2) содержит 6,02·1023 молекул кофеина. Если типичная… Проблема 95AE: Липитор, фармацевтический препарат, который, как было показано, снижает уровень плохого холестерина при одновременном повышении… Проблема 96AE: В пьесе Шекспира «Ричард III, Первый Убийца» говорит: Возьми то и это! [Пронзает Кларенса] Если это… Задача 97AEПроблема 98AE: В первых сценах фильма «В поисках утраченного ковчега» Индиана Джонс пытается извлечь золото… Задача 99AEПроблема 100AE: Активным ингредиентом таблеток аспирина является ацетилсалициловая кислота, который имеет плотность 1,4 г/см3.
.. Задача 90E: В очень холодную зиму температура может оставаться ниже нуля в течение длительного времени. Однако… Задача 91E: Классифицируйте следующие физические или химические изменения. а. Шарики от моли постепенно испаряются в… Задача 92E: Свойства смеси обычно являются средними значениями свойств ее компонентов. Задача 93AE: Два сферических объекта имеют одинаковую массу. Один плавает по воде; другой тонет. Какой объект имеет… Задача 94AE: 194-граммовый образец кофеина (C8h20N4O2) содержит 6,02·1023 молекул кофеина. Если типичная… Проблема 95AE: Липитор, фармацевтический препарат, который, как было показано, снижает уровень плохого холестерина при одновременном повышении… Проблема 96AE: В пьесе Шекспира «Ричард III, Первый Убийца» говорит: Возьми то и это! [Пронзает Кларенса] Если это… Задача 97AEПроблема 98AE: В первых сценах фильма «В поисках утраченного ковчега» Индиана Джонс пытается извлечь золото… Задача 99AEПроблема 100AE: Активным ингредиентом таблеток аспирина является ацетилсалициловая кислота, который имеет плотность 1,4 г/см3. … Задача 101AE: В этом году, как и во многие прошлые годы, вы начинаете чувствовать сильную сонливость после того, как съели большую порцию… Задача 102AE: Какие из следующих химических изменений относятся к ? Какие физические изменения? а. нарезка пищи б…. Задача 103AE: У человека с высоким уровнем холестерина 250 мг холестерина на 100,0 мл крови. Если общая кровь… Задача 104AEЗадача 105AE: Обнаружено, что столб жидкости линейно расширяется при нагревании. Предположим, что столбик поднимается на 5,25 см для… Задача 106AE. Образец твердого вещества массой 25,00 г помещают в градуированный цилиндр, а затем цилиндр наполняют до… блок более плотный; оранжевый блок, синий блок или он… Задача 108AE: Согласно Официальным правилам бейсбола, бейсбольный мяч должен иметь длину окружности не более 9.25…Задача 109AE: Плотность объекта неправильной формы определялась следующим образом. Масса объекта была… Задача 110AE: Химик из примера 1.14 провел еще несколько экспериментов. Она обнаружила, что пипетка используется для измерения.
… Задача 101AE: В этом году, как и во многие прошлые годы, вы начинаете чувствовать сильную сонливость после того, как съели большую порцию… Задача 102AE: Какие из следующих химических изменений относятся к ? Какие физические изменения? а. нарезка пищи б…. Задача 103AE: У человека с высоким уровнем холестерина 250 мг холестерина на 100,0 мл крови. Если общая кровь… Задача 104AEЗадача 105AE: Обнаружено, что столб жидкости линейно расширяется при нагревании. Предположим, что столбик поднимается на 5,25 см для… Задача 106AE. Образец твердого вещества массой 25,00 г помещают в градуированный цилиндр, а затем цилиндр наполняют до… блок более плотный; оранжевый блок, синий блок или он… Задача 108AE: Согласно Официальным правилам бейсбола, бейсбольный мяч должен иметь длину окружности не более 9.25…Задача 109AE: Плотность объекта неправильной формы определялась следующим образом. Масса объекта была… Задача 110AE: Химик из примера 1.14 провел еще несколько экспериментов. Она обнаружила, что пипетка используется для измерения. .. Задача 111CWP: Самая длинная река в мире — Нил, длина которой составляет 4145 миль. Какова длина Нила в… Задача 112CWP: Секретариат известен как лошадь с самым быстрым бегом в Кентукки Дерби. Если Секретариат запишет… Проблема 113CWP: Самая высокая температура, зарегистрированная в Соединенных Штатах, составляет 134F на ранчо Гренландии, Калифорния. Плавление… Задача 114CWPПроблема 115CWP: Какие из следующих утверждений верны? а. Ложка сахара – это смесь. б. Только… Задача 116CWP: Что из следующего описывает химическое свойство? а. Плотность железа 7,87 г/см3. б. A… Задача 117CP: Эмпирическое правило при планировании экспериментов состоит в том, чтобы избегать использования результата, который является небольшой разницей… Задача 118CP: Нарисуйте рисунок, показывающий отметки (градации) на стеклянной посуде, что позволит вам сделать каждый из …Задача 119КП: Часто ошибки выражаются в процентах. Процентная ошибка равна абсолютной величине… Задача 120CP: Человек взвесил на весах 15 пенни и записал следующие массы: 3,112 г 3,109 г 3,059 г.
.. Задача 111CWP: Самая длинная река в мире — Нил, длина которой составляет 4145 миль. Какова длина Нила в… Задача 112CWP: Секретариат известен как лошадь с самым быстрым бегом в Кентукки Дерби. Если Секретариат запишет… Проблема 113CWP: Самая высокая температура, зарегистрированная в Соединенных Штатах, составляет 134F на ранчо Гренландии, Калифорния. Плавление… Задача 114CWPПроблема 115CWP: Какие из следующих утверждений верны? а. Ложка сахара – это смесь. б. Только… Задача 116CWP: Что из следующего описывает химическое свойство? а. Плотность железа 7,87 г/см3. б. A… Задача 117CP: Эмпирическое правило при планировании экспериментов состоит в том, чтобы избегать использования результата, который является небольшой разницей… Задача 118CP: Нарисуйте рисунок, показывающий отметки (градации) на стеклянной посуде, что позволит вам сделать каждый из …Задача 119КП: Часто ошибки выражаются в процентах. Процентная ошибка равна абсолютной величине… Задача 120CP: Человек взвесил на весах 15 пенни и записал следующие массы: 3,112 г 3,109 г 3,059 г. .. Задача 121CP: 21 октября 1982 г. Монетный двор изменил состав пенни (см. упражнение 120)…. Задача 122CP: В рамках научного проекта вы изучаете схемы движения в своем городе на перекрестке в… Задача 123CP: Чистое серебро является твердым решением серебро и медь. Если кусок ожерелья из стерлингового серебра… Задача 124CP: Сделайте рисунки на молекулярном уровне (микроскопические) для каждого из следующего. а. Покажите отличия… Задача 125CP: столкнувшись с коробкой, показанной на диаграмме, вы хотите узнать что-нибудь о ее внутренней… format_list_bulleted
.. Задача 121CP: 21 октября 1982 г. Монетный двор изменил состав пенни (см. упражнение 120)…. Задача 122CP: В рамках научного проекта вы изучаете схемы движения в своем городе на перекрестке в… Задача 123CP: Чистое серебро является твердым решением серебро и медь. Если кусок ожерелья из стерлингового серебра… Задача 124CP: Сделайте рисунки на молекулярном уровне (микроскопические) для каждого из следующего. а. Покажите отличия… Задача 125CP: столкнувшись с коробкой, показанной на диаграмме, вы хотите узнать что-нибудь о ее внутренней… format_list_bulleted
Химия Вопрос о молярности
Последние синие сообщения
Час назад
Час назад
7 часов назад
7 часов назад
23 часа назад
23 часа назад
Вчера
9002 4 Перейдите в Blue Tracker »Последние сообщения на форуме
01:06
01:01
00:35
00:17
23:22
22:53 9 0005
22:26
Перейти к форумам »Фильтры форумов27 сентября 2011 г., 03:34 #1
Фосфат натрия, Na3PO4, реагирует с HCl с образованием h4PO4 и NaCl. Сколько литров 0,1 М HCl (водн.) требуется для реакции с 0,1 моль фосфата натрия?
Ответить с цитатойЭто моя попытка:
Сначала бели уравнение и уравновешивай его: — Затем найди родинки HCL!NA3PO4+3HCL —> h4PO4 + 3NACL
0,1 моль NA3PO4*(3 моль HCl/1 моль NA3PO4) = 0,3 моль HCL … затем 0,3 моль HCl*(1/0,1 моль) = 3 л
Мой ответ верно ?27 сентября 2011 г.