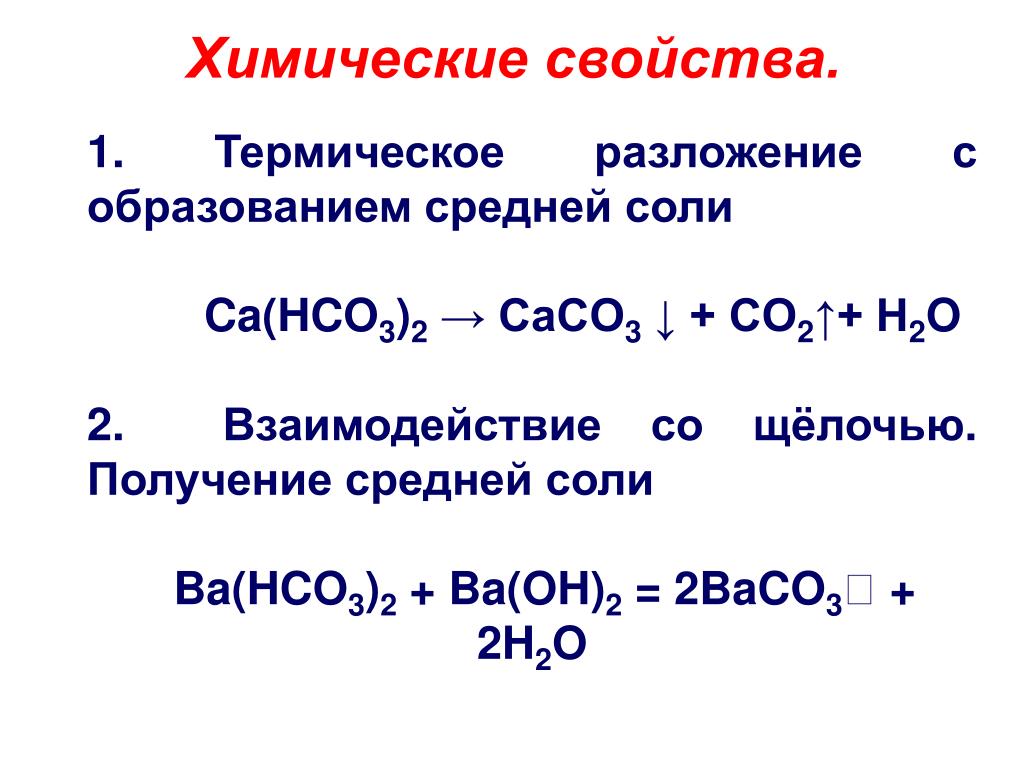
На 50 литров воды, содержащей Ca(HCO3)2, при преобразовании в мягкую воду требуется 22,2 г Ca(OH)2. Рассчитайте количество Ca(HCO3)2 на литр жесткой воды.
ICSE-НЕКОТОРЫЕ ОСНОВНЫЕ ПОНЯТИЯ ХИМИИ -ЧИСЛЕННЫЕ ПРОБЛЕМЫ
20 видеоРЕКЛАМА
Ab Padhai karo bina ads ke
Khareedo DN Pro and dekho sari videos bina kisi ad ki rukaavat ke!
Обновлено: 27-06-2022
Текст Решение
Ответ
Правильный ответ 0,972 г/л
Раствор
Соответствующее химическое уравнение: =162,116 г
∴22,2 г Ca(OH)2 будет реагировать с Ca(HCO3)2
=162,11674,096×22,2=48,6 г
Такое количество Ca(HCO3)2 содержится в 50 л жесткой воды.
∴ Количество Ca(HCO3)2 в одном литре жесткой воды.
= 48,0650 = 0,972 г
Ответ
Пошаговое решение от экспертов, которое поможет вам в сомнениях и получении отличных оценок на экзаменах.
Transcript
love you ni aarti Kaushal 15 литров воды, содержащей cahco32, были преобразованы в мягкую воду. Потребность в 2,2 граммах Co2 называется удвоенным количеством csu 3 целых два раза для буквы жесткой воды Австралия напишите химическое уравнение для лучшего понимания когда caco3 + вступает в реакцию с cuso4 +, это дает csmt сделать это здесь, мы видели, что один моль caco3 реагирует с одним молем caco3 и формулой для 16 лет 3 молярных
Потребность в 2,2 граммах Co2 называется удвоенным количеством csu 3 целых два раза для буквы жесткой воды Австралия напишите химическое уравнение для лучшего понимания когда caco3 + вступает в реакцию с cuso4 +, это дает csmt сделать это здесь, мы видели, что один моль caco3 реагирует с одним молем caco3 и формулой для 16 лет 3 молярных
масса caco3 в целом дважды равна 162, а молярная масса молярной массы СА и цены это количество молей в 40 2,2 г ch5 + количество шариков 22,2 грамма серебра все игрушки равны заданной массе 22,2 открытая молекула 8074 находим количество молекул
точка 3 0,3 балла Промышленность 7.0.3 Молл chcl3, потому что количество молей когда, потому что здесь один моль хлористого натрия 3 реагирует с HCl с образованием молла Sohail 0,3 моль требуется 0,3 моль caco3 всего в два раза больше, поэтому вес от веса 0,3 Mol aur h v автобус равен 0,3 на 162 48,6 так грамм на литр так грамм на литр
aap cahco32 48,6 50-50 учитывая 50 литров воды, так что это 0,972 грамм на литр безопасности спасибо
Связанные видео
Ca HCO3) 2 युक्त जल के 50 लीट को मृदु जल में प परिवा कठोर जल के प्रति लीटर में Ca(HCO3)2 की मात्रा की गणना की मात्रा की गणना की
110393048
Какая масса CaO потребуется для устранения жесткости 1000 литров воды, содержащей 1,62 г Ca(HCO_3)_2 на литр?
344167744
Текст Раствор
Степень жесткости пробы воды 100ppm. Если эта проба содержит соли Mg(HCO_3)_2, вызывающие жесткость, рассчитайте массу Ca(OH)_2, необходимую для обработки 10 кг пробы воды.
Если эта проба содержит соли Mg(HCO_3)_2, вызывающие жесткость, рассчитайте массу Ca(OH)_2, необходимую для обработки 10 кг пробы воды.
630389564
105 г пробы воды содержали 16,2 г Ca(HCO3)2, жесткость
630389869
5 кг воды содержат 24 мг MgSO4 и 32,4 мг Ca(HCO3)2 . Общая жесткость воды составляет
642629262
CaCO3 ও Ca(HCO3)2 -এর মধ্যে কোনটি জলে দ্রাব্য?
642631404
Classify the following into those causing temporary hardness : [Mg(HCO3)2,Ca(HCO3)2,CaSO_4]
642939288
कठोर जल के नमूने में MgSO4=0.012ग्राम/लीटर तथा Ca(HCO3) 2=0,081ग्राम/लीटर है। जल की कठोरता है
643167592
Текстовое раствор
CA (HCO3) 2 के विघटन होने के कारण जल की सхов कठो कठो विघटन उब के दू हो जल की स स कठो कठो कठो कठो उब से दू हो की है है है।।। है है है है है है है है है स स स है है है है है है o यह इसलिए है कि Ca (HCO3) 2
643167600
Текстовое решение
कठो जल के नमूने में MgSO4 = 0,012 ग् Как/लीट तथा CA (HCO3) 2 = 0,081 ग्रedम/लीट लीट तथा CA (hco3) 2 = 0,081 ग्रedम/लीट लीट लीट तथा CA (HCO3) 2 = 0,081 जल की कठोरता है
643167614
Текстовое раствор
कठो выполненные जल की कठोरता है
643170353
Текстовое решение
CA (HCO3) 2 के विघटन होने के क क जल की स स्थायी कठोरता जल उब उब से दू हो ज है है।।।।।। यह इसलिए है कि Ca (HCO3) 2
643170361
Текстовый раствор
कठो जल के नमूने में MgSO4 = 0,012 ग Вивра/लीट तथा CA (HCO3) 2 = 0,081 गшить/लीट है है तथा CA (HCO3) 2 = 0,081 ग Как/लीट है तथा CA (HCO3) 2 = 0,081 जल की कठोरता है
643170375
Текстовое решение
CA (HCO3) 2 का विघटन होने क क जल की स सхов स कठो कठो उब उब से दू दू की स स स स स स स स स स स स स स स स स स स स स स स स स स स स स स स स स स स स है स है है है है है है दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू दू यह इसलिए है कि Ca(HCO3)2 :
644580516
Растворимость карбоната кальция в воде
по Moses Donell | 22 января 2023 г. | Часто задаваемые вопросы о воде
| Часто задаваемые вопросы о воде
При растворении в воде карбонат кальция (CaCO3) разлагается на гидроксид кальция (Ca(OH)2) и угольную кислоту (h3CO3), которая быстро распадается на воду (h3O) и диоксид углерода (CO2). Общая химическая реакция может быть представлена следующим уравнением: CaCO3(s) + h3O(l) → Ca(OH)2(aq) + CO2(g) Как правило, карбонат кальция плохо растворим в воде, с растворимостью всего около 1 грамма на литр воды при комнатной температуре. Однако растворимость карбоната кальция увеличивается с повышением температуры и увеличением концентрации углекислого газа (CO2) в воде. Это связано с тем, что угольная кислота, образующаяся при растворении карбоната кальция в воде, является слабой кислотой, а присутствие дополнительного количества СО2 повышает кислотность воды, что способствует растворению карбоната кальция.
Нерастворимый карбонат кальция осаждается, и в результате кипяченая вода фильтруется для его удаления, в результате чего остается мягкая вода без солей кальция, присутствующих в других типах воды. В результате для удаления Ca(HCO3)2 требуется кипячение (тепло).
В результате для удаления Ca(HCO3)2 требуется кипячение (тепло).
Поскольку присутствуют гидрокарбонат кальция Ca(HCO3)2(водн.) и гидрокарбонат магния Mg(HCO3)2(водн. ), требуется временное повышение твердости.
Ca(HCO3)2 CaCO3 (нерастворимый) + CO2 + h3O (кипящий).
Металлы в твердом состоянии не представлены бикарбонатами металлов (i) LiHCO3 (ii) Ca(HCO3)2 (iii) Zn(HCO3)2 (iv) AgHCO3. Что касается бикарбоната карбоната натрия (3,4), то твердое состояние отсутствует.
Почему Ca Hco3 2 растворим в воде?
Изображение: https://slidesharecdn.comПричина, по которой HCO3-2 растворяется в воде, заключается в том, что это слабый электролит. Это означает, что он не полностью диссоциирует на свои ионы при растворении в воде.
Ионный радиус ионов определяет их способность связываться с водой. Из-за большего радиуса нитрат-иона по сравнению с хлорат-ионом нитрат (NO3–) обладает большей растворимостью, чем хлорат (ClO3–). Водорастворимые анионные соединения с меньшими анионами, чем катионы, с большей вероятностью будут ионными соединениями. Растворимость хлорида (ClO3–) больше, чем растворимость бикарбоната (HCO3–), потому что ион хлорида имеет меньший радиус, чем ион бикарбоната . Содержание растворимой воды в воде будет ниже в присутствии аниона, имеющего больший радиус, чем катион. Бикарбонат (HCO3–), например, менее растворим, чем ацетат (C2h4O2–), потому что ион бикарбоната имеет больший радиус, чем ион ацетата. Например, снижается растворимость бикарбоната (HCO3–).
Водорастворимые анионные соединения с меньшими анионами, чем катионы, с большей вероятностью будут ионными соединениями. Растворимость хлорида (ClO3–) больше, чем растворимость бикарбоната (HCO3–), потому что ион хлорида имеет меньший радиус, чем ион бикарбоната . Содержание растворимой воды в воде будет ниже в присутствии аниона, имеющего больший радиус, чем катион. Бикарбонат (HCO3–), например, менее растворим, чем ацетат (C2h4O2–), потому что ион бикарбоната имеет больший радиус, чем ион ацетата. Например, снижается растворимость бикарбоната (HCO3–).
Раствор бикарбоната кальция в воде?
Изображение: https://quoracdn.netКогда карбонат кальция добавляется в воду, он реагирует с образованием бикарбоната кальция . Это прозрачный бесцветный раствор, который можно пить.
Это процесс композиции. Процесс растворения карбоната кальция протекает медленно и ускоряется при наличии воды. Процесс разложения тормозится углекислым газом. В природе карбонат кальция чаще всего встречается в камни из карбоната кальция . Эти камни обычно состоят из небольших фрагментов карбоната кальция, которые смешиваются с водой и углекислым газом, образуя твердое вещество. Это минерал, который можно найти в изобилии в самых разных местах по всему миру. Из этого материала обычно делают статую. Поскольку он чрезвычайно стабилен, часто используется карбонат кальция. Карбонат кальция не может разлагаться в присутствии воды. Если карбонат кальция удалить из воды, он разложится. Разложение тела занимает много времени. Вода ускоряет процесс в процессе. Этому процессу способствует присутствие углекислого газа.
В природе карбонат кальция чаще всего встречается в камни из карбоната кальция . Эти камни обычно состоят из небольших фрагментов карбоната кальция, которые смешиваются с водой и углекислым газом, образуя твердое вещество. Это минерал, который можно найти в изобилии в самых разных местах по всему миру. Из этого материала обычно делают статую. Поскольку он чрезвычайно стабилен, часто используется карбонат кальция. Карбонат кальция не может разлагаться в присутствии воды. Если карбонат кальция удалить из воды, он разложится. Разложение тела занимает много времени. Вода ускоряет процесс в процессе. Этому процессу способствует присутствие углекислого газа.
Растворим ли карбонат кальция в воде
Карбонат кальция слабо растворим в воде, его растворимость составляет около 2,8 г в 100 мл воды при 25 °C. Эта низкая растворимость обусловлена сильным притяжением между катионами кальция и карбонатными анионами .