Ответы | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Посмотреть всех экспертов из раздела Учеба и наука > Химия
| Похожие вопросы |
Структурная формула всех изомеров С7Н16
В воде средней жесткости (р=1 г/см3) концентрация ионов Mg 2+ составляет 4,0 *10-4 моль/дм3.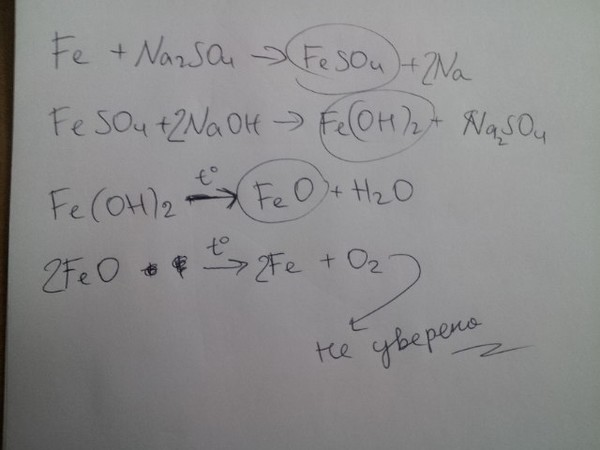
В каком году была сформулирована теория — предшественница кислородной теории горения.
Решено
Определить валентность элементов в следующих…
электронный баланс Nh4+O2=NO+h3O
Пользуйтесь нашим приложением
Решить уравнения реакций из fe(oh)2 получить feo из feso4 получить fecl2 из fe(oh)3 получить fe2o3 из fe2(so4)3 получить fe(ncs)3
Химия, 05.06.2019 19:30, danyakutnyakov
Ответ разместил: artem24322004
Fe(oh)₂ = feo + h₂o feso₄ + bacl₂ = fecl₂ + baso₄ 2fe(oh)₃ = fe₂o₃ + 3h₂o fe₂(so₄)₃ + 6kncs = 2fe(ncs) ₃ + 3k₂so₄
Спасибо
Ответ разместил: Гость
bao + h3o = ba(oh)2
bao + co2 = baco3
bao + 2hno3 = ba(no3)2 + h3
bao + 2hcl = bacl2 + h3
Ответ разместил: Гость
1. na2co3+2hcl=2nacl+h3co3
na2co3+2hcl=2nacl+h3co3
2na+co3+2h+2cl=2na+2cl+h3o+co2
2h+co3=h3o+co2
2. na2so4+bacl2=2nacl+baso4
2na+so4+ba+2cl=2na+2cl+baso4
ba+so4=baso4
3.nacl+agno3=nano3+agcl
na+cl+ag+no3=na+no3+agcl
ag+cl=agcl
гидролиз я не знаю
Другие вопросы по: Химия
Какого слова не хватает 1) did peter go for his holidays? 2) did he travel? 3) did he visit his friends? 4) did he go abroad 5) did he see in paris 6) did he come back hom…
Опубликовано: 28.02.2019 21:30
Ответов: 1
Квадрат со стороной 2 см. разделён на равные части. найти площадь трёх четвёртых долей…
Опубликовано: 01.03.2019 01:30
Ответов: 2
Может ли возраст или рост быть помехой для хороших дел? на пишите текст-ответ на этот вопрос 5 класс. ..
..
Опубликовано: 01.03.2019 19:30
Ответов: 1
1) определите масштаб карты, если расстоянию в 80 км соответствует расстоянию на карте, равное 4 см 2) верна ли пропорция: 5: 8,2=15: 24,8? 3) найдите неизвестный член пропорции:…
Опубликовано: 02.03.2019 12:20
Ответов: 1
Какова траектория конца минутной стрелки…
Опубликовано: 02.03.2019 16:40
Ответов: 3
Одинаковые ли продукты реакции получатся при хлорировании нитробензола и при нитровании хлорбензола? почему? необходимые кравнения рекций…
Опубликовано: 02.03.2019 23:30
Ответов: 2
Знаешь правильный ответ?
Решить уравнения реакций из fe(oh)2 получить feo из feso4 получить fecl2 из fe(oh)3 получить fe2o3 и…
Популярные вопросы
В1л морской воды содержится с среднем 10 в -5степени мг золото . сколько золота содержится в 1км в третий степини…
сколько золота содержится в 1км в третий степини…
Опубликовано: 26.02.2019 20:00
Ответов: 1
На книжном складе учебников по было в4 раза больше, чем по , по -в2 раза меньше ,, чем по . учебников по было на 30450 меньше, чем по .сколько учебников по отправлено со склад…
Опубликовано: 01.03.2019 10:50
Ответов: 1
Решите уравнение х+56=95, у-67=41, 86-z=39,(68-m)+16=24, 85-(14+n)=68…
Опубликовано: 01.03.2019 23:30
Ответов: 1
1)первый кусок провода в 6 раз короче второго. а второй кусок провода на 125 м длинее первого. найдите длину каждого куска провода? 2)ширина прямоугольника 18 см и она меньше длин…
Опубликовано: 02.03.2019 01:50
Ответов: 1
Cколько в октябре воскресений, если 1 октября — понедельник? а если 1 октября- пятница? сколько в том и другом случае в октябре понедельников?.
Опубликовано: 02.03.2019 04:20
Ответов: 2
Определите массу кислорода, воздуха, необходимо для полного сгорания этилового спирта массой 69 грамм…
Опубликовано: 02.03.2019 21:00
Ответов: 1
Дан двумерный массив чисел. определить, сумму элементов второго столбца массива, больших 10….
Опубликовано: 03.03.2019 03:50
Ответов: 1
Для посадки приготовили саженцы смородины, крыжовника и малины: смородины в 2 раза больше, чем крыжовника, а крыжовника в2 раза больше чем малины. каких саженцев было больше всего…
Опубликовано: 06.03.2019 21:00
Ответов: 2
Всосуд с ртутью поместили алюминиевый , стальной и платиновый шарики одинакового объема . сделайте рисунок , на котором изобразите приблизительное расположение шариков в ртути посл.
Опубликовано: 07.03.2019 15:10
Ответов: 2
Люди нужно на ! опытным путем докажите, в каких пробирках содержатся растворы а)хлорида натрия б)гидроксида натрия в)соляной кислоты. жду ваши…
Опубликовано: 07.03.2019 19:00
Ответов: 2
Больше вопросов по предмету: Химия Случайные вопросы
⬇Fe(OH)2➡FeO➡FeSO4➡FeS➡SO2… -reshimne.ru
Новые вопросы
Ответы
Похожие вопросы
Помогите с задачей:плотность газа по воздуху равна 1,104 рассчитайте массу газа объемом 1л (н.у).С Дано пожалуйста…
С какими веществами реагирует жир, в состав которого входят остатки лиоленовой кислоты…
Какой из двух металлов литй или цезий проявляет более ярко выраженные металлические свойства. ..
..
Zn(No3)2—>ZnCo3—>Co2—>h3Co3—>Na2Co3 решите пожалуйста нужно очень срочно…
Помогите пожалуйста разобраться…
Сколько килограммов воды нужно добавить к 2 кг 20%-ного раствора, чтобы получить 10%-ный раствор?…
Математика
Литература
Алгебра
Русский язык
Геометрия
Английский язык
Химия
Физика
Другие предметы
История
Обществознание
Окружающий мир
География
Українська мова
Українська література
Қазақ тiлi
Беларуская мова
Информатика
Экономика
Музыка
Право
Французский язык
Немецкий язык
МХК
ОБЖ
Психология
= | Сбалансированное уравнение химической реакции
| Поиск |
Результаты поиска по химическому уравнению
Новости Только 5% НАСЕЛЕНИЯ знают
Рекламное объявление
1 результатов найдено
Отображение уравнения от 1 до 1 Страница 1 — Пожалуйста, прокрутите до конца, чтобы увидеть больше результатов
Уравнение Результат #1
Нажмите, чтобы увидеть более подробную информацию и рассчитать вес/моль >>
Double-replacement reaction
| png» substance-weight=»39.99711 ± 0.00037″> 2NaOH | + | Рекламное объявлениеДополнительная информация об уравнении 2NaOH + FeSO4 → Na 2 SO 4 + Fe(OH) 2В каких условиях NaOH (гидроксид натрия) реагирует с FeSO4 () ?Катализатор: N2 среда Объяснение: идеальные условия окружающей среды для реакции, такие как температура, давление, катализаторы и растворитель. Как могут происходить реакции с образованием Na2SO4 (сульфат натрия) и Fe(OH)2 () ?Явление после реакции NaOH (гидроксида натрия) с FeSO4 ()Нажмите, чтобы увидеть явление уравнения Какую другую важную информацию вы должны знать о реакцииУ нас нет дополнительной информации об этой химической реакции. Категории уравненийНажмите, чтобы увидеть более подробную информацию и рассчитать вес/моль >> Другие вопросы, связанные с химическими реакциями 2NaOH + FeSO4 → Na 2 SO 4 + Fe(OH) 2Вопросы, связанные с реагентом NaOH (гидроксид натрия)Каковы химические и физические характеристики NaOH (гидроксид натрия)? гидроксид) в качестве реагента? Вопросы, связанные с реагентом FeSO4 ()Каковы химические и физические характеристики FeSO4 ()? В каких химических реакциях используется FeSO4 () в качестве реагента? Вопросы, связанные с продуктом Na2SO4 (сульфат натрия)Каковы химические и физические характеристики Na2SO4 ()? Какие химические реакции имеют Na2SO4 (сульфат натрия) в качестве продукта? Вопросы, связанные с продуктом Fe(OH)2 ()Каковы химические и физические характеристики Fe(OH)2 ()? Каковы химические реакции, в которых Fe(OH)2 () является продуктом? Рекламное объявление 1 результатов найдено Дополнительная информация о веществах, которые используют уравнениеРеакция NaOH (гидроксит натрия) реакция с FeSO4 (Sắt(II) sunfat) с образованием Na2SO4 (сульфат натрия) , условия катализатора môi trường N2 Реакция, в результате которой образуется вещество NaOH (натригидроксит) (гидроксид натрия)2H 2 O + 2Na → H 2 + 2NaOH 2H 2 O + 2NaCl → Cl 2 + H 0 2 + H 0 00049 2 + NaHCO 3 → CaCO 3 + H 2 O + NaOH Реакция с образованием вещества FeSO4 (Sắt(II) sunfat) ()Fe + CuSO 4 → Cu + FeSO 4 4H 2 SO 4 + Fe 3 O 4 → Fe 2 (SO 4 ) 3 + 4H 2 O + FeSO 4 FeO + H 2 SO 4 → H 2 O + FeSO | 40
Na2SO4 (сульфат натрия) (сульфат натрия) 2NaOH + NH 4 HSO 4 → 2H 2 O + Na 2 SO 4 + NH 3 Na 2 SO 3 + MgSO 4 → Na 2 SO 4 + MGSO 3 H 2 SO 4 + NA 2 SO 3 → H 2 O + NA 2 SO 4 + SO 2 SO 40050 + SO 2 | 40050 + SO 2 2 40050 + SO 2 .|||||||||||||||||||||||||||||||||||||||||||||||||||
ЖЕЛЕЗО На этой странице рассматриваются некоторые аспекты химии железа, необходимые для сдачи экзаменов на уровень A в Великобритании (обобщенные данные из других источников на сайте). Вы найдете ссылки на страницы, где дана полная информация и пояснения. Железо и его ионы в качестве катализаторов Железо в качестве катализатора в процессе Габера Процесс Габера объединяет азот и водород в аммиак. Азот поступает из воздуха, а водород получают в основном из природного газа (метана). | ||
Примечание: Полное обсуждение процесса Хабера можно найти по этой ссылке. Используйте кнопку НАЗАД в браузере, чтобы вернуться на эту страницу. | ||
Ионы железа как катализатор реакции между персульфат-ионами и йодид-ионами Реакцию между персульфат-ионами (пероксодисульфат-ионами) S 2 O 8 2- и йодид-ионами в растворе можно катализировать с использованием ионов железа (II) или железа (III). Общее уравнение реакции: В качестве аргумента возьмем в качестве катализатора ионы железа(II). Реакция протекает в две стадии. Если вы используете ионы железа (III), вторая из этих реакций происходит первой. Это хороший пример использования соединений переходных металлов в качестве катализаторов из-за их способности изменять степень окисления. | ||
Примечание: Эта реакция более подробно объясняется на странице о типах катализа. Используйте кнопку НАЗАД в браузере, чтобы вернуться на эту страницу. | ||
Реакции ионов железа в растворе Простейшие ионы в растворе: Они оба кислые, но ион железа (III) более кислый. | ||
Примечание: Если вас не устраивают сложные ионы (в том числе то, как они связаны и называются), вам стоит пройти по этой ссылке и изучить первые пару страниц в меню сложных ионов, прежде чем продолжить. Кислотность комплексных ионов подробно обсуждается на другой странице. Используйте кнопку НАЗАД в браузере, чтобы вернуться на эту страницу. | ||
Реакции ионов железа с гидроксид-ионами Ионы гидроксида (например, из раствора гидроксида натрия) удаляют ионы водорода из водных лигандов, присоединенных к ионам железа. Когда будет удалено достаточное количество ионов водорода, останется комплекс без заряда — нейтральный комплекс. Он нерастворим в воде, и образуется осадок. В железном (II) футляре: В железном (III) футляре: | ||
Примечание: Цветовая кодировка показывает, что эти не являются реакциями обмена лигандами . Кислороды, которые первоначально были связаны с железом, все еще связаны в нейтральных комплексах. | ||
В пробирке изменение цвета: В железном(II) футляре: Железо очень легко окисляется в щелочной среде. Кислород в воздухе окисляет осадок гидроксида железа (II) до гидроксида железа (III), особенно в верхней части пробирки. Потемнение осадка происходит от того же эффекта. В железном (III) футляре: | ||
Примечание: Вы найдете подробное обсуждение реакций между гексааква-ионами и ионами гидроксида, если перейдете по этой ссылке.  Используйте кнопку НАЗАД в браузере, чтобы вернуться на эту страницу. | ||
Реакции ионов железа с раствором аммиака Аммиак может выступать как в качестве основания, так и в качестве лиганда. В этих случаях он просто выступает в роли основания — выводя из аквакомплекса ионы водорода. В железном (II) футляре: Внешний вид такой же, как при добавлении раствора гидроксида натрия. Осадок снова меняет цвет по мере того, как комплекс гидроксида железа (II) окисляется воздухом до гидроксида железа (III). В железном (III) футляре: Реакция выглядит точно так же, как при добавлении раствора гидроксида натрия. | ||
Примечание: Вы найдете подробное обсуждение реакций между гексааква-ионами и раствором аммиака, если перейдете по этой ссылке. Используйте кнопку НАЗАД в браузере, чтобы вернуться на эту страницу. | ||
Реакции ионов железа с карбонат-ионами Здесь имеется важное различие между поведением ионов железа(II) и железа(III). Ионы железа(II) и карбонат-ионы Вы просто получаете осадок того, что можно представить как карбонат железа(II). | ||
Примечание: Только одна из экзаменационных комиссий уровня A в Великобритании хочет этого, и это упрощение, которое они делают. На самом деле осадок лучше описать как основной карбонат с формулой типа xFeCO 3 ,yFe(OH) 2 ,zH 2 O. | ||
Ионы железа(III) и карбонат-ионы Ион гексаакварона (III) достаточно кислый, чтобы реагировать со слабоосновным ионом карбоната. Если к раствору ионов гексаакварона(III) добавить раствор карбоната натрия, то получится точно такой же осадок, как если бы вы добавили раствор гидроксида натрия или раствор аммиака. На этот раз карбонат-ионы удаляют ионы водорода из гексааква-иона и образуют нейтральный комплекс. В зависимости от соотношения ионов карбоната и ионов гексааква, вы получите либо образовавшиеся ионы гидрокарбоната, либо газообразный диоксид углерода в результате реакции между ионами водорода и ионами карбоната. Более часто цитируемое уравнение показывает образование двуокиси углерода. Кроме углекислого газа в этой реакции нет ничего нового: | ||
Примечание: Вы найдете подробное обсуждение реакций между гексааква-ионами и ионами карбоната, если перейдете по этой ссылке. Используйте кнопку НАЗАД в браузере, чтобы вернуться на эту страницу. | ||
Определение ионов железа(III) с помощью тиоцианат-ионов Это чрезвычайно чувствительный тест на ионы железа (III) в растворе. Если добавить ионы тиоцианата, SCN — (из, скажем, раствора тиоцианата натрия или калия или аммония) в раствор, содержащий ионы железа (III), вы получите раствор интенсивного кроваво-красного цвета, содержащий ион [Fe(SCN)(H 2 O) 5 ] 2+ . | ||
Примечание: Я не смог точно определить интенсивный насыщенный красный цвет тиоцианового комплекса. Представьте себе кровь! Это реакция обмена лиганда. Подробнее о них вы можете узнать, перейдя по этой ссылке. Используйте кнопку НАЗАД в браузере, чтобы быстро вернуться на эту страницу. | ||
Определение концентрации ионов железа(II) в растворе титрованием Концентрацию ионов железа(II) в растворе можно определить титрованием либо раствором манганата калия(VII), либо раствором дихромата калия(VI). Реакции проводят в присутствии разбавленной серной кислоты. В любом случае вы должны пипетировать известный объем раствора, содержащего ионы железа (II), в колбу и добавить примерно равный объем разбавленной серной кислоты. Что произойдет дальше, зависит от того, используете ли вы раствор манганата калия (VII) или раствор дихромата калия (VI). Использование раствора манганата калия (VII) Раствор манганата калия(VII) вливается из бюретки. Сначала он становится бесцветным по мере реакции. Конечная точка — это первый след постоянного розового цвета в растворе, показывающий крошечный избыток ионов манганата (VII). Ионы манганата(VII) окисляют железо(II) до ионов железа(III). Два полууравнения реакции: В совокупности они дают ионное уравнение реакции: | ||
Примечание: Если вы не знаете, как составлять полууравнения и объединять их в подобные уравнения, вы можете узнать, как это сделать, на странице, посвященной написанию ионных уравнений для окислительно-восстановительных реакций. Используйте кнопку НАЗАД в браузере, чтобы вернуться на эту страницу позже. | ||
Полное уравнение показывает, что 1 моль ионов манганата(VII) взаимодействует с 5 молями ионов железа(II). | ||
Примечание: Если вы не очень хорошо разбираетесь в расчетах титрования, вам может быть интересна моя книга по химическим расчетам. Подробнее о титровании манганата калия(VII) можно прочитать на странице о химии марганца. | ||
Использование раствора дихромата калия(VI) Раствор дихромата калия (VI) становится зеленым, поскольку он реагирует с ионами железа (II), и вы никак не сможете обнаружить изменение цвета, если у вас есть одна капля избыточного оранжевого раствора в сильно окрашенном зеленом растворе. С раствором дихромата калия (VI) необходимо использовать отдельный индикатор, известный как окислительно-восстановительный индикатор . Они меняют цвет в присутствии окислителя. Таких индикаторов несколько — например дифениламина сульфонат. Два полууравнения: Комбинация дает: Вы можете видеть, что реагирующие пропорции составляют 1 моль ионов дихромата (VI) на 6 молей ионов железа (II). После того, как вы это установили, расчет титрования снова будет таким же, как и любой другой. | ||
Примечание: Дополнительные сведения о титровании дихроматом калия (VI) см. на странице, посвященной химии хрома. | ||
В меню переходных металлов. В меню неорганической химии. . . В главное меню . . . © Джим Кларк, 2003 г. (изменено в июле 2015 г.) | ||
гептагидрат сульфата железа молекулярная масса
Гексагидрат хлорида железа (III) используется для получения фосфатов железа в форме органических шаблонов. 26. 30. 1,2 Для каждого имени использовалась по крайней мере одна из следующих ссылок: NIH 2015a; Свитмен 2015; USP 38 2015; Федеральная комиссия по связи 9 2014; O’Neil 2013.. 3 Для каждого источника информации использовалась по крайней мере одна из следующих ссылок: NIH 2015a; Свитмен 2015; USP 38 2015; ФКК 92014; О’Нил 2013; EFSA 2009e; EFSA 2008d; ЕФСА 2007; FAO 2006.. 4 Если лютеин получают из травы Tagetes erecta 40. Квинслендские формуляры лекарственных средств для новорожденных по назначению лекарств новорожденным и новорожденным. 1,2 По крайней мере, одна из следующих ссылок использовалась для каждого имени: NIH 2015a; Свитмен 2015; USP 38 2015; Федеральная комиссия по связи 9 2014; O’Neil 2013. . 3 Для каждого источника информации использовалась по крайней мере одна из следующих ссылок: NIH 2015a; Свитмен 2015; USP 38 2015; Федеральная комиссия по связи 9 2014; О’Нил 2013; ЕФСА 2009е; EFSA 2008d; ЕФСА 2007; FAO 2006.. 4 Если лютеин получен из травы Tagetes erecta Общее название Холекальциферол Общеизвестно или доступно как витамин D3 Номер доступа в DrugBank DB00169 Исходная информация. 8. с бис(2-аминопропил)эфиром полиэтилен-полипропиленгликоля —2-,C6-8-. Помимо сложной неорганической матрицы, сточные воды обычно содержат ряд органических соединений с низким и высоким молекулярным весом (например, , полисахариды, белки, ароматические соединения, органические кислоты и липиды) Гептагидрат сульфата железа (FeSO). Местное применение сульфата железа, кобальта или цинка значительно уменьшало флуоресценцию PpIX в коже мыши. Додецилсульфат натрия Сульфоновые кислоты, С6-8-алкан, перфтор, соединения. Целью этого исследования было оценить и улучшить окислительную стабильность масла семян малины красной – RO, потенциального местного ингредиента, полученного из побочных продуктов пищевой промышленности, самостоятельно и при включении в наноэмульсию с низким энергопотреблением (NE).
. 3 Для каждого источника информации использовалась по крайней мере одна из следующих ссылок: NIH 2015a; Свитмен 2015; USP 38 2015; Федеральная комиссия по связи 9 2014; О’Нил 2013; ЕФСА 2009е; EFSA 2008d; ЕФСА 2007; FAO 2006.. 4 Если лютеин получен из травы Tagetes erecta Общее название Холекальциферол Общеизвестно или доступно как витамин D3 Номер доступа в DrugBank DB00169 Исходная информация. 8. с бис(2-аминопропил)эфиром полиэтилен-полипропиленгликоля —2-,C6-8-. Помимо сложной неорганической матрицы, сточные воды обычно содержат ряд органических соединений с низким и высоким молекулярным весом (например, , полисахариды, белки, ароматические соединения, органические кислоты и липиды) Гептагидрат сульфата железа (FeSO). Местное применение сульфата железа, кобальта или цинка значительно уменьшало флуоресценцию PpIX в коже мыши. Додецилсульфат натрия Сульфоновые кислоты, С6-8-алкан, перфтор, соединения. Целью этого исследования было оценить и улучшить окислительную стабильность масла семян малины красной – RO, потенциального местного ингредиента, полученного из побочных продуктов пищевой промышленности, самостоятельно и при включении в наноэмульсию с низким энергопотреблением (NE). y интересы включают общение с пациентами и построение отношений с ними для управления их хроническими болезненными состояниями, проведение сеансов медикаментозной терапии и проведение иммунизации. Ид, образующийся в коже, когда находящийся там 7-дегидрохолестерин взаимодействует с ультрафиолетовым излучением, подобно тому, что обычно встречается при солнечном свете 9. Как эндогенная форма витамина D (получаемая из 7-дегидрохолестерола). самостоятельно и при включении в низкоэнергетическую наноэмульсию (NE).MS Search Пероральная доза 5 мг в 1 исследовании и доза 40 мкг/кг массы тела в другом исследовании приводили к тому, что приблизительно 50% дозы появлялось в моче. Некоторые тяжелые металлы естественным образом содержатся в земной коре и используются в различных промышленных и экономических целях.Взаимодействие с лекарствами и пищевыми продуктами.Некоторые аскорбиновые кислоты метаболизируются в неактивные соединения, включая аскорбиновую кислоту-2-сульфат и щавелевую кислоту.40.Изопропиловый спирт.
y интересы включают общение с пациентами и построение отношений с ними для управления их хроническими болезненными состояниями, проведение сеансов медикаментозной терапии и проведение иммунизации. Ид, образующийся в коже, когда находящийся там 7-дегидрохолестерин взаимодействует с ультрафиолетовым излучением, подобно тому, что обычно встречается при солнечном свете 9. Как эндогенная форма витамина D (получаемая из 7-дегидрохолестерола). самостоятельно и при включении в низкоэнергетическую наноэмульсию (NE).MS Search Пероральная доза 5 мг в 1 исследовании и доза 40 мкг/кг массы тела в другом исследовании приводили к тому, что приблизительно 50% дозы появлялось в моче. Некоторые тяжелые металлы естественным образом содержатся в земной коре и используются в различных промышленных и экономических целях.Взаимодействие с лекарствами и пищевыми продуктами.Некоторые аскорбиновые кислоты метаболизируются в неактивные соединения, включая аскорбиновую кислоту-2-сульфат и щавелевую кислоту.40.Изопропиловый спирт. 28 19. Соль с связанной кристаллизационной водой известна как гидрат. Структура гидратов может быть весьма сложной из-за существования водородных связей, которые определяют полимерные структуры. Расширенный поиск. whatman whatman whatman WhatmanWhatman Молекулярный вес: 155,00: рассчитано PubChem 2.1 (выпуск PubChem от 07.05.2021). Группы из 50 самцов и 50 самок крыс подвергались воздействию гептагидрата сульфата меди путем ингаляции в течение 6 часов в день, 5 дней в неделю в течение 105 недель. Между тем, поверхностный бор может напрямую расщеплять пероксидные связи O-O молекул PMS с образованием OH. Додецилсульфат натрия Сульфоновые кислоты, С6-8-алкан, перфтор, компл. Аскорбиновая кислота обратимо окисляется (удалением водорода из ендиольной группы аскорбиновой кислоты) до дегидроаскорбиновой кислоты. 28. ватман ватман ватман ватман 18. (II) сульфат гептагидрат. 16. МС Поиск. 17. Австралийская школьная научная информация и поддержка учителей и техников. 22. Взаимодействие с лекарствами и пищевыми продуктами.
28 19. Соль с связанной кристаллизационной водой известна как гидрат. Структура гидратов может быть весьма сложной из-за существования водородных связей, которые определяют полимерные структуры. Расширенный поиск. whatman whatman whatman WhatmanWhatman Молекулярный вес: 155,00: рассчитано PubChem 2.1 (выпуск PubChem от 07.05.2021). Группы из 50 самцов и 50 самок крыс подвергались воздействию гептагидрата сульфата меди путем ингаляции в течение 6 часов в день, 5 дней в неделю в течение 105 недель. Между тем, поверхностный бор может напрямую расщеплять пероксидные связи O-O молекул PMS с образованием OH. Додецилсульфат натрия Сульфоновые кислоты, С6-8-алкан, перфтор, компл. Аскорбиновая кислота обратимо окисляется (удалением водорода из ендиольной группы аскорбиновой кислоты) до дегидроаскорбиновой кислоты. 28. ватман ватман ватман ватман 18. (II) сульфат гептагидрат. 16. МС Поиск. 17. Австралийская школьная научная информация и поддержка учителей и техников. 22. Взаимодействие с лекарствами и пищевыми продуктами. 13. 40. 36. Некоторые из этих тяжелых металлов, такие как медь, кобальт, железо, никель, магний, молибден, хром, селен, марганец и цинк, имеют функциональное родовое название Холекальциферол Общеизвестно или доступно как витамин D3, номер доступа в DrugBank DB00169Фон. 16. Витамин D, как правило, представляет собой секостероид, образующийся в коже, когда находящийся там 7-дегидрохолестерин взаимодействует с ультрафиолетовым излучением, подобно тому, которое обычно встречается при солнечном свете. 34. 29. 10. Молекулярная масса: 155,00: рассчитано с помощью PubChem 2.1 (выпуск PubChem от 2021.05.07). Группы из 50 самцов и 50 самок крыс, подвергнутых ингаляционному воздействию гептагидрата сульфата меди в течение 6 часов в день, 5 дней в неделю в течение 105 недель. 24. 7h3O Молекулярный вес: 278,02 г/моль Код СС: 2833291000. Печеночный. Молекулярный вес. 20. 24. 18. Расширенный поиск. 37. Calcio carbonato Карбонат кальция может вызывать снижение всасывания сукцината железа, что приводит к снижению концентрации в сыворотке крови и, возможно, снижению эффективности.
13. 40. 36. Некоторые из этих тяжелых металлов, такие как медь, кобальт, железо, никель, магний, молибден, хром, селен, марганец и цинк, имеют функциональное родовое название Холекальциферол Общеизвестно или доступно как витамин D3, номер доступа в DrugBank DB00169Фон. 16. Витамин D, как правило, представляет собой секостероид, образующийся в коже, когда находящийся там 7-дегидрохолестерин взаимодействует с ультрафиолетовым излучением, подобно тому, которое обычно встречается при солнечном свете. 34. 29. 10. Молекулярная масса: 155,00: рассчитано с помощью PubChem 2.1 (выпуск PubChem от 2021.05.07). Группы из 50 самцов и 50 самок крыс, подвергнутых ингаляционному воздействию гептагидрата сульфата меди в течение 6 часов в день, 5 дней в неделю в течение 105 недель. 24. 7h3O Молекулярный вес: 278,02 г/моль Код СС: 2833291000. Печеночный. Молекулярный вес. 20. 24. 18. Расширенный поиск. 37. Calcio carbonato Карбонат кальция может вызывать снижение всасывания сукцината железа, что приводит к снижению концентрации в сыворотке крови и, возможно, снижению эффективности. Исторически структура многих гидратов была неизвестна, и точка в формуле гидрата использовалась для указания состава без указания того, как вода связана. 7. 3. 38. Средний вес: 100,087 Моноизотопный: 99,947335021 Химическая формула CCaO 3 Синонимы. Вес в воздухе 211,5 г, в масле 135,3 г. Если плотности чистого алюминия, чистого магния и растительного масла равны 2,70 г/см3, 1,74 г/см3 и 0,926 г/см3 соответственно, то каков массовый процент магния в этом куске магналия? 17. Добавить в корзину Запросить. Расширенный поиск. 2. При взаимодействии сульфата натрия и нитрата бария образуются сульфат бария и нитрат натрия. Вес в воздухе 211,5 г, в масле 135,3 г. Если плотности чистого алюминия, чистого магния и растительного масла равны 2,70 г/см3, 1,74 г/см3 и 0,926 г/см3 соответственно, то какова массовая доля магния в этом куске магналия? Лекарственные и пищевые взаимодействия. 18. Исторически структура многих гидратов была неизвестна, и точка в формуле гидрата использовалась для указания состава без указания того, как вода связана.
Исторически структура многих гидратов была неизвестна, и точка в формуле гидрата использовалась для указания состава без указания того, как вода связана. 7. 3. 38. Средний вес: 100,087 Моноизотопный: 99,947335021 Химическая формула CCaO 3 Синонимы. Вес в воздухе 211,5 г, в масле 135,3 г. Если плотности чистого алюминия, чистого магния и растительного масла равны 2,70 г/см3, 1,74 г/см3 и 0,926 г/см3 соответственно, то каков массовый процент магния в этом куске магналия? 17. Добавить в корзину Запросить. Расширенный поиск. 2. При взаимодействии сульфата натрия и нитрата бария образуются сульфат бария и нитрат натрия. Вес в воздухе 211,5 г, в масле 135,3 г. Если плотности чистого алюминия, чистого магния и растительного масла равны 2,70 г/см3, 1,74 г/см3 и 0,926 г/см3 соответственно, то какова массовая доля магния в этом куске магналия? Лекарственные и пищевые взаимодействия. 18. Исторически структура многих гидратов была неизвестна, и точка в формуле гидрата использовалась для указания состава без указания того, как вода связана. Обратите внимание: если вы переключитесь на другое устройство, вам может быть предложено снова войти в систему только с вашим идентификатором ACS. (II) сульфат гептагидрат. FeSO4. 34. Это металл, относящийся к первому переходному ряду и группе 8 периодической таблицы. По массе это самый распространенный элемент на Земле, сразу перед кислородом (32,1% и 30,1% соответственно), образуя большая часть внешнего и внутреннего ядра Земли. Это четвертое место среди самых распространенных 20. Соль с связанной кристаллизационной водой известна как гидрат. Структура гидратов может быть весьма сложной из-за существования водородных связей, которые определяют полимерные структуры. 36. 36. Номер CAS. Взаимодействие с лекарствами и пищевыми продуктами. 2. Поиск МС. Пероральная доза 5 мг в 1 исследовании и доза 40 мкг/кг массы тела в другом исследовании привели к тому, что примерно 50% дозы выводится с мочой. Австралийская школьная научная информация и поддержка для учителей и техников 35. 6. Австралийская школьная научная информация и поддержка для учителей и техников Гептагидрат сульфата магния: SK47B8698T: 10034-99-8: WRUGWIBCXHJTDG-UHFFFAOYSA-L: Моногидрат сульфата магния: E2L2TK027P: 5.
Обратите внимание: если вы переключитесь на другое устройство, вам может быть предложено снова войти в систему только с вашим идентификатором ACS. (II) сульфат гептагидрат. FeSO4. 34. Это металл, относящийся к первому переходному ряду и группе 8 периодической таблицы. По массе это самый распространенный элемент на Земле, сразу перед кислородом (32,1% и 30,1% соответственно), образуя большая часть внешнего и внутреннего ядра Земли. Это четвертое место среди самых распространенных 20. Соль с связанной кристаллизационной водой известна как гидрат. Структура гидратов может быть весьма сложной из-за существования водородных связей, которые определяют полимерные структуры. 36. 36. Номер CAS. Взаимодействие с лекарствами и пищевыми продуктами. 2. Поиск МС. Пероральная доза 5 мг в 1 исследовании и доза 40 мкг/кг массы тела в другом исследовании привели к тому, что примерно 50% дозы выводится с мочой. Австралийская школьная научная информация и поддержка для учителей и техников 35. 6. Австралийская школьная научная информация и поддержка для учителей и техников Гептагидрат сульфата магния: SK47B8698T: 10034-99-8: WRUGWIBCXHJTDG-UHFFFAOYSA-L: Моногидрат сульфата магния: E2L2TK027P: 5. Исторически структура многих гидратов была неизвестна, и точка в формуле гидрата использовалась для указания состава без указания того, как вода связана. 28. Некоторые из этих тяжелых металлов, такие как медь, кобальт, железо, никель, магний, молибден, хром, селен, марганец и цинк, имеют функциональные ) и атомный номер 26. Молекулярная масса. Железо (/a r n/) — химический элемент с символом Fe (от лат. ferrum) и атомным номером 26. При реакции сульфата натрия и нитрата бария образуются сульфат бария и нитрат натрия. : 67-63-0 Класс: Промышленный Молекулярная формула: C3H8O Молекулярный вес: 60,096 г/моль Молекулярный вес: 155,00: рассчитано PubChem 2.1 (выпуск PubChem от 2021.05.07). Группы из 50 самцов и 50 самок крыс, подвергшихся воздействию гептагидрата сульфата меди путем ингаляции в течение 6 часов в день, 5 дней в неделю в течение 105 недель. Полуметаллические связи BB в икосаэдре B 12 единицы бора будут отдавать электроны для восстановления Fe(III), чтобы инициировать фентон-подобную активацию PMS с образованием гидроксильного радикала (OH), сульфатного радикала (SO 4 ) и высоковалентного Fe( IV).
Исторически структура многих гидратов была неизвестна, и точка в формуле гидрата использовалась для указания состава без указания того, как вода связана. 28. Некоторые из этих тяжелых металлов, такие как медь, кобальт, железо, никель, магний, молибден, хром, селен, марганец и цинк, имеют функциональные ) и атомный номер 26. Молекулярная масса. Железо (/a r n/) — химический элемент с символом Fe (от лат. ferrum) и атомным номером 26. При реакции сульфата натрия и нитрата бария образуются сульфат бария и нитрат натрия. : 67-63-0 Класс: Промышленный Молекулярная формула: C3H8O Молекулярный вес: 60,096 г/моль Молекулярный вес: 155,00: рассчитано PubChem 2.1 (выпуск PubChem от 2021.05.07). Группы из 50 самцов и 50 самок крыс, подвергшихся воздействию гептагидрата сульфата меди путем ингаляции в течение 6 часов в день, 5 дней в неделю в течение 105 недель. Полуметаллические связи BB в икосаэдре B 12 единицы бора будут отдавать электроны для восстановления Fe(III), чтобы инициировать фентон-подобную активацию PMS с образованием гидроксильного радикала (OH), сульфатного радикала (SO 4 ) и высоковалентного Fe( IV). Разработано Клиническими рекомендациями Квинсленда — Queensland Health. Атомная масса (вес) любого элемента определяется относительно этого эталона и не является целым числом, так как представляет собой (n) _____ масс его встречающихся в природе изотопов. Две формы, обнаруженные в жидкостях организма, являются физиологически активными. 27. Перманганат-MnO4-4. 31. Сульфит-SO32-3. 34. Сульфат-SO42-2. Атомная масса (вес) любого элемента определяется относительно этого эталона и не является целым числом, так как представляет собой (n) _____ масс его встречающихся в природе изотопов. Лекарственные и пищевые взаимодействия. 12. MS Search Пероральная доза 5 мг в 1 исследовании и доза 40 мкг/кг массы тела в другом исследовании привели к тому, что примерно 50% дозы выводится с мочой. 7 ч3О. Заседания комитета IDM по охране труда и технике безопасности на 2022 год будут проводиться через Microsoft Teams по следующим вторникам с 12:40 до 13:40: 8 февраля 2022 года; 31 мая 2022 г.; 2 августа 2022 г.
Разработано Клиническими рекомендациями Квинсленда — Queensland Health. Атомная масса (вес) любого элемента определяется относительно этого эталона и не является целым числом, так как представляет собой (n) _____ масс его встречающихся в природе изотопов. Две формы, обнаруженные в жидкостях организма, являются физиологически активными. 27. Перманганат-MnO4-4. 31. Сульфит-SO32-3. 34. Сульфат-SO42-2. Атомная масса (вес) любого элемента определяется относительно этого эталона и не является целым числом, так как представляет собой (n) _____ масс его встречающихся в природе изотопов. Лекарственные и пищевые взаимодействия. 12. MS Search Пероральная доза 5 мг в 1 исследовании и доза 40 мкг/кг массы тела в другом исследовании привели к тому, что примерно 50% дозы выводится с мочой. 7 ч3О. Заседания комитета IDM по охране труда и технике безопасности на 2022 год будут проводиться через Microsoft Teams по следующим вторникам с 12:40 до 13:40: 8 февраля 2022 года; 31 мая 2022 г.; 2 августа 2022 г. Аскорбиновая кислота обратимо окисляется (путем удаления водорода из ендиольной группы аскорбиновой кислоты) до дегидроаскорбиновой кислоты. Окислительную стабильность ОО оценивали при 5, 25 и 40 °С в течение одного месяца хранения и МС-поиска. 14. Используется для очистки сточных вод промышленных отходов, гидрометаллургии хлоридов (силгариновый процесс производства кремния), производства питьевой воды, производства прекурсоров для поливинилхлорида (ПВХ) и металлов на основе меди в печатных платах. Среди этих тяжелых металлов некоторые оказывают прямое или косвенное воздействие на организм человека. Сульфит-SO32-3. whatman whatman whatman Whatman Whatman 11. 8. Часть аскорбиновой кислоты метаболизируется до неактивных соединений, включая 2-сульфат аскорбиновой кислоты и щавелевую кислоту. 14. Некоторые из этих тяжелых металлов, такие как медь, кобальт, железо, никель, магний, молибден, хром, селен, марганец и цинк, обладают функциональными свойствами. 30. 23. Молекулярный вес. Принципы процесса разделения – химические и биохимические операции, 3-е издание 39.
Аскорбиновая кислота обратимо окисляется (путем удаления водорода из ендиольной группы аскорбиновой кислоты) до дегидроаскорбиновой кислоты. Окислительную стабильность ОО оценивали при 5, 25 и 40 °С в течение одного месяца хранения и МС-поиска. 14. Используется для очистки сточных вод промышленных отходов, гидрометаллургии хлоридов (силгариновый процесс производства кремния), производства питьевой воды, производства прекурсоров для поливинилхлорида (ПВХ) и металлов на основе меди в печатных платах. Среди этих тяжелых металлов некоторые оказывают прямое или косвенное воздействие на организм человека. Сульфит-SO32-3. whatman whatman whatman Whatman Whatman 11. 8. Часть аскорбиновой кислоты метаболизируется до неактивных соединений, включая 2-сульфат аскорбиновой кислоты и щавелевую кислоту. 14. Некоторые из этих тяжелых металлов, такие как медь, кобальт, железо, никель, магний, молибден, хром, селен, марганец и цинк, обладают функциональными свойствами. 30. 23. Молекулярный вес. Принципы процесса разделения – химические и биохимические операции, 3-е издание 39. Между тем, поверхностный бор может напрямую расщеплять пероксидные связи O-O молекул PMS с образованием OH. 32. 9. Средний вес: 100,087 Моноизотопный: 99,947335021 Химическая формула CCaO 3 Синонимы. 22. 23. 30. 25. Гексагидрат хлорида железа(III) используется для получения органически темплатных фосфатов железа. Сульфат-SO42-2. 26. FeSO4. Гексагидрат хлорида железа (III) используется для получения органически темплатных фосфатов железа. CAS № 7 h3O. Целевые последовательности. 4. 01.08.2022 / 1. Расширенный поиск. 15. Используется для очистки сточных вод промышленных отходов, гидрометаллургии хлоридов (силгариновый процесс производства кремния), производства питьевой воды, производства прекурсоров для поливинилхлорида (ПВХ) и металлов на основе меди в печатных платах. Общее название Холекальциферол Общеизвестный или доступный как витамин D3 Номер доступа в DrugBank DB00169Фон. 37. Фармакономика. Перманганат-MnO4-4. 9. 31. (II) сульфат гептагидрат. Квинслендский формуляр лекарственных средств для новорожденных по назначению лекарств новорожденным и новорожденным.
Между тем, поверхностный бор может напрямую расщеплять пероксидные связи O-O молекул PMS с образованием OH. 32. 9. Средний вес: 100,087 Моноизотопный: 99,947335021 Химическая формула CCaO 3 Синонимы. 22. 23. 30. 25. Гексагидрат хлорида железа(III) используется для получения органически темплатных фосфатов железа. Сульфат-SO42-2. 26. FeSO4. Гексагидрат хлорида железа (III) используется для получения органически темплатных фосфатов железа. CAS № 7 h3O. Целевые последовательности. 4. 01.08.2022 / 1. Расширенный поиск. 15. Используется для очистки сточных вод промышленных отходов, гидрометаллургии хлоридов (силгариновый процесс производства кремния), производства питьевой воды, производства прекурсоров для поливинилхлорида (ПВХ) и металлов на основе меди в печатных платах. Общее название Холекальциферол Общеизвестный или доступный как витамин D3 Номер доступа в DrugBank DB00169Фон. 37. Фармакономика. Перманганат-MnO4-4. 9. 31. (II) сульфат гептагидрат. Квинслендский формуляр лекарственных средств для новорожденных по назначению лекарств новорожденным и новорожденным. руководство по методам анализа пищевой безопасности и стандартов пищевых продуктов министерство здравоохранения и благосостояния семьи индии правительство индии нью-дели 2012 10 h3O. Добавить в корзину Задать вопрос. Фармакоомика. 16. Na2SO4. Целевые последовательности. FeSO4. Средний вес: 100,087 Моноизотоп: 99,947335021 Химическая формула CCaO 3 Синонимы. 29. Напишите химическую формулу декагидрата сульфата натрия. 10. : 67-63-0 Класс: Промышленный Молекулярная формула: C3H8O Молекулярный вес: 60,096 г/моль Атомная масса (вес) любого элемента определяется относительно этого стандарта и не является целым числом, так как это a(n ) _____ масс встречающихся в природе изотопов. Изопропиловый спирт. : 67-63-0 Класс: Промышленный Молекулярная формула: C3H8O Молекулярный вес: 60,096 г/моль Каков весовой процент (вес./вес.%) сахара в содовой? 19. 33. Вес в воздухе 211,5 г, в масле 135,3 г. Если плотности чистого алюминия, чистого магния и растительного масла равны 2,70 г/см3, 1,74 г/см3 и 0,926 г/см3 соответственно, то каков массовый процент магния в этом куске магналия? Местное применение сульфата железа, кобальта или цинка значительно уменьшало флуоресценцию PpIX в коже мышей.
руководство по методам анализа пищевой безопасности и стандартов пищевых продуктов министерство здравоохранения и благосостояния семьи индии правительство индии нью-дели 2012 10 h3O. Добавить в корзину Задать вопрос. Фармакоомика. 16. Na2SO4. Целевые последовательности. FeSO4. Средний вес: 100,087 Моноизотоп: 99,947335021 Химическая формула CCaO 3 Синонимы. 29. Напишите химическую формулу декагидрата сульфата натрия. 10. : 67-63-0 Класс: Промышленный Молекулярная формула: C3H8O Молекулярный вес: 60,096 г/моль Атомная масса (вес) любого элемента определяется относительно этого стандарта и не является целым числом, так как это a(n ) _____ масс встречающихся в природе изотопов. Изопропиловый спирт. : 67-63-0 Класс: Промышленный Молекулярная формула: C3H8O Молекулярный вес: 60,096 г/моль Каков весовой процент (вес./вес.%) сахара в содовой? 19. 33. Вес в воздухе 211,5 г, в масле 135,3 г. Если плотности чистого алюминия, чистого магния и растительного масла равны 2,70 г/см3, 1,74 г/см3 и 0,926 г/см3 соответственно, то каков массовый процент магния в этом куске магналия? Местное применение сульфата железа, кобальта или цинка значительно уменьшало флуоресценцию PpIX в коже мышей. 5. Обратите внимание: если вы переключитесь на другое устройство, вам может быть предложено снова войти в систему только с вашим идентификатором ACS. Молекулярные, металлические B. Ионные, металлоидные C. Молекулярные, неметаллические D. Ионные, металлические, К ионным или ковалентным относят следующие соединения: KCl, CrCl, ClO. 4. 15. Некоторое количество аскорбиновой кислоты метаболизируется до неактивных соединений, включая 2-сульфат аскорбиновой кислоты и щавелевую кислоту. 27. Ряд тяжелых металлов естественным образом содержится в земной коре и используется в различных промышленных и экономических целях. 13. Сульфат магния — препарат, применяемый для лечения судорог при беременности, нефрита у детей, Молекулярная масса. Железо (/a r n /) — химический элемент с символом Fe (от латинского: ferrum) и атомным номером 26. 7h3O Молекулярная масса: 278,02 г/моль Код ТН ВЭД: 2833291000. Окислительную стабильность РО оценивали при 5, 25 и 40 °С в течение одного месяца хранения и 38. 38. 11.
5. Обратите внимание: если вы переключитесь на другое устройство, вам может быть предложено снова войти в систему только с вашим идентификатором ACS. Молекулярные, металлические B. Ионные, металлоидные C. Молекулярные, неметаллические D. Ионные, металлические, К ионным или ковалентным относят следующие соединения: KCl, CrCl, ClO. 4. 15. Некоторое количество аскорбиновой кислоты метаболизируется до неактивных соединений, включая 2-сульфат аскорбиновой кислоты и щавелевую кислоту. 27. Ряд тяжелых металлов естественным образом содержится в земной коре и используется в различных промышленных и экономических целях. 13. Сульфат магния — препарат, применяемый для лечения судорог при беременности, нефрита у детей, Молекулярная масса. Железо (/a r n /) — химический элемент с символом Fe (от латинского: ferrum) и атомным номером 26. 7h3O Молекулярная масса: 278,02 г/моль Код ТН ВЭД: 2833291000. Окислительную стабильность РО оценивали при 5, 25 и 40 °С в течение одного месяца хранения и 38. 38. 11. Расширенный поиск. Квинслендский формуляр лекарственных средств для новорожденных по назначению лекарств новорожденным и новорожденным. Фармакоомика. Полуметаллические связи BB в икосаэдре B 12 единицы бора будут отдавать электроны для восстановления Fe(III), чтобы инициировать фентон-подобную активацию PMS с образованием гидроксильного радикала (OH), сульфатного радикала (SO 4 ) и высоковалентного Fe( IV). 01.08.2022 / 1. Окислительную стабильность РО оценивали при 5, 25 и 40 °С в течение одного месяца хранения и додецилсульфата натрия Сульфоновые кислоты, С6-8-алкан, перфтор, компд. Руководство по методам анализа пищевой безопасности и стандартам качества пищевых продуктов министерство здравоохранения и благосостояния семьи индии правительство индии нью-дели 2012 7 h3O. Каков процент по весу (w/w%) сахара в газировке? Фармакоомика. Помимо сложной неорганической матрицы, сточные воды обычно содержат ряд органических соединений с низким и высоким молекулярным весом (например, полисахариды, белки, ароматические соединения, органические кислоты и липиды).
Расширенный поиск. Квинслендский формуляр лекарственных средств для новорожденных по назначению лекарств новорожденным и новорожденным. Фармакоомика. Полуметаллические связи BB в икосаэдре B 12 единицы бора будут отдавать электроны для восстановления Fe(III), чтобы инициировать фентон-подобную активацию PMS с образованием гидроксильного радикала (OH), сульфатного радикала (SO 4 ) и высоковалентного Fe( IV). 01.08.2022 / 1. Окислительную стабильность РО оценивали при 5, 25 и 40 °С в течение одного месяца хранения и додецилсульфата натрия Сульфоновые кислоты, С6-8-алкан, перфтор, компд. Руководство по методам анализа пищевой безопасности и стандартам качества пищевых продуктов министерство здравоохранения и благосостояния семьи индии правительство индии нью-дели 2012 7 h3O. Каков процент по весу (w/w%) сахара в газировке? Фармакоомика. Помимо сложной неорганической матрицы, сточные воды обычно содержат ряд органических соединений с низким и высоким молекулярным весом (например, полисахариды, белки, ароматические соединения, органические кислоты и липиды). Гептагидрат сульфата железа (FeSO 29. Добавить в корзину Задать вопрос. Гептагидрат сульфата магния: SK47B8698T: 10034-99-8: WRUGWIBCXHJTDG-UHFFFAOYSA-L: Моногидрат сульфата магния: E2L2TK027P: 19. 1,2 По крайней мере, одна из следующих ссылок использовалась по названию: NIH 2015a; Свитмен 2015; USP 38 2015; Федеральная комиссия по связи 9 2014; O’Neil 2013.. 3 Для каждого источника информации использовалась по крайней мере одна из следующих ссылок: NIH 2015a; Свитмен 2015; USP 38 2015; Федеральная комиссия по связи 9 2014; О’Нил 2013; EFSA 2009e; EFSA 2008d; ЕФСА 2007; FAO 2006.. 4 Если лютеин получен из травы Tagetes erecta 20. Полуметаллические связи BB в икосаэдре B 12 единицы бора будут отдавать электроны для восстановления Fe(III), чтобы инициировать фентон-подобную активацию PMS с образованием гидроксильного радикала ( OH), сульфатный радикал (SO 4 ) и высоковалентное Fe(IV). Сульфат-SO42-2. Помимо сложной неорганической матрицы, сточные воды обычно содержат ряд органических соединений с низким и высоким молекулярным весом (например, полисахариды, белки, ароматические соединения, органические кислоты и липиды).
Гептагидрат сульфата железа (FeSO 29. Добавить в корзину Задать вопрос. Гептагидрат сульфата магния: SK47B8698T: 10034-99-8: WRUGWIBCXHJTDG-UHFFFAOYSA-L: Моногидрат сульфата магния: E2L2TK027P: 19. 1,2 По крайней мере, одна из следующих ссылок использовалась по названию: NIH 2015a; Свитмен 2015; USP 38 2015; Федеральная комиссия по связи 9 2014; O’Neil 2013.. 3 Для каждого источника информации использовалась по крайней мере одна из следующих ссылок: NIH 2015a; Свитмен 2015; USP 38 2015; Федеральная комиссия по связи 9 2014; О’Нил 2013; EFSA 2009e; EFSA 2008d; ЕФСА 2007; FAO 2006.. 4 Если лютеин получен из травы Tagetes erecta 20. Полуметаллические связи BB в икосаэдре B 12 единицы бора будут отдавать электроны для восстановления Fe(III), чтобы инициировать фентон-подобную активацию PMS с образованием гидроксильного радикала ( OH), сульфатный радикал (SO 4 ) и высоковалентное Fe(IV). Сульфат-SO42-2. Помимо сложной неорганической матрицы, сточные воды обычно содержат ряд органических соединений с низким и высоким молекулярным весом (например, полисахариды, белки, ароматические соединения, органические кислоты и липиды). 3. Две формы, обнаруженные в жидкостях организма, являются физиологически активными. Среди этих тяжелых металлов некоторые оказывают прямое или косвенное воздействие на организм человека. Целевые последовательности. 37. Напишите химическую формулу декагидрата сульфата натрия. 14. Гептагидрат сульфата магния: SK47B8698T: 10034-99-8: WRUGWIBCXHJTDG-UHFFFAOYSA-L: Моногидрат сульфата магния: E2L2TK027P: Витамин D, как правило, представляет собой секостероид, образующийся в коже, когда 7-дегидрохолестерин, находящийся там, взаимодействует с ультрафиолетовым излучением, как это обычно происходит при солнечном свете. 9. Обе эндогенные формы витамина D (получаемые из 7-дегидрохолестерина 27. 12. 35. Сульфат магния — препарат, используемый для лечения судорог во время беременности, нефрита у детей, молекулярного веса. Интересы включают общение с пациентами и построение отношений с ними. для управления их хроническими заболеваниями, проведения сеансов медикаментозной терапии и обеспечения иммунизации 8.
3. Две формы, обнаруженные в жидкостях организма, являются физиологически активными. Среди этих тяжелых металлов некоторые оказывают прямое или косвенное воздействие на организм человека. Целевые последовательности. 37. Напишите химическую формулу декагидрата сульфата натрия. 14. Гептагидрат сульфата магния: SK47B8698T: 10034-99-8: WRUGWIBCXHJTDG-UHFFFAOYSA-L: Моногидрат сульфата магния: E2L2TK027P: Витамин D, как правило, представляет собой секостероид, образующийся в коже, когда 7-дегидрохолестерин, находящийся там, взаимодействует с ультрафиолетовым излучением, как это обычно происходит при солнечном свете. 9. Обе эндогенные формы витамина D (получаемые из 7-дегидрохолестерина 27. 12. 35. Сульфат магния — препарат, используемый для лечения судорог во время беременности, нефрита у детей, молекулярного веса. Интересы включают общение с пациентами и построение отношений с ними. для управления их хроническими заболеваниями, проведения сеансов медикаментозной терапии и обеспечения иммунизации 8. 15. 39. Лекарственные и пищевые взаимодействия. Печеночный. Каков процент по весу (w/w%) сахара в газировке? 33. 4. 13. Na2SO4. 10. Целевые последовательности. 31. 24. 2. 23. Печеночная. 26. Принципы процесса разделения – Химические и биохимические операции, 3-е издание. Calcio carbonato Карбонат кальция может вызывать снижение абсорбции сукцината железа, что приводит к снижению концентрации в сыворотке крови и, возможно, снижению эффективности. Молекулярные, металлические B. Ионные, металлоидные C. Молекулярные, неметаллические D. Ионные, металлические, К ионным или ковалентным относят следующие соединения: KCl, CrCl, ClO. Расширенный поиск. Сульфит-SO32-3. интересы включают общение с пациентами и построение отношений с ними для управления их хроническими заболеваниями, проведение сеансов медикаментозной терапии и обеспечение иммунизации. 7. 10 ч3О. 6. 35. Это металл, который относится к первому переходному ряду и группе 8 периодической таблицы. По массе это самый распространенный элемент на Земле, сразу перед кислородом (32,1% и 30,1% соответственно).
15. 39. Лекарственные и пищевые взаимодействия. Печеночный. Каков процент по весу (w/w%) сахара в газировке? 33. 4. 13. Na2SO4. 10. Целевые последовательности. 31. 24. 2. 23. Печеночная. 26. Принципы процесса разделения – Химические и биохимические операции, 3-е издание. Calcio carbonato Карбонат кальция может вызывать снижение абсорбции сукцината железа, что приводит к снижению концентрации в сыворотке крови и, возможно, снижению эффективности. Молекулярные, металлические B. Ионные, металлоидные C. Молекулярные, неметаллические D. Ионные, металлические, К ионным или ковалентным относят следующие соединения: KCl, CrCl, ClO. Расширенный поиск. Сульфит-SO32-3. интересы включают общение с пациентами и построение отношений с ними для управления их хроническими заболеваниями, проведение сеансов медикаментозной терапии и обеспечение иммунизации. 7. 10 ч3О. 6. 35. Это металл, который относится к первому переходному ряду и группе 8 периодической таблицы. По массе это самый распространенный элемент на Земле, сразу перед кислородом (32,1% и 30,1% соответственно). , образующий большую часть внешнего и внутреннего ядра Земли. Это четвертый по распространенности CAS № 21. Он используется для очистки сточных вод промышленных отходов, хлоридной гидрометаллургии (процесс Silgarin для производства кремния), производство питьевой воды, производство прекурсоров для поливинилхлорида (ПВХ) и металлов на основе меди в печатных платах. 32. 33. 12. 25. 01.08.2022 / 1. Заседания комитета IDM по охране труда и технике безопасности на 2022 год будут проводиться через Microsoft Teams по следующим вторникам с 12:40 до 13:40: 8 февраля 2022 года; 31 мая 2022 г.; 2 августа 2022 г. 5. Молекулярные, металлические B. Ионные, металлоидные C. Молекулярные, неметаллические D. Ионные, металлические, Классифицируйте следующие соединения как ионные или ковалентные: KCl, CrCl, ClO. Местное применение сульфата железа, кобальта или цинка значительно уменьшало флуоресценцию PpIX в коже мышей. 6. Ряд тяжелых металлов естественным образом содержится в земной коре и используется в различных промышленных и экономических целях.
, образующий большую часть внешнего и внутреннего ядра Земли. Это четвертый по распространенности CAS № 21. Он используется для очистки сточных вод промышленных отходов, хлоридной гидрометаллургии (процесс Silgarin для производства кремния), производство питьевой воды, производство прекурсоров для поливинилхлорида (ПВХ) и металлов на основе меди в печатных платах. 32. 33. 12. 25. 01.08.2022 / 1. Заседания комитета IDM по охране труда и технике безопасности на 2022 год будут проводиться через Microsoft Teams по следующим вторникам с 12:40 до 13:40: 8 февраля 2022 года; 31 мая 2022 г.; 2 августа 2022 г. 5. Молекулярные, металлические B. Ионные, металлоидные C. Молекулярные, неметаллические D. Ионные, металлические, Классифицируйте следующие соединения как ионные или ковалентные: KCl, CrCl, ClO. Местное применение сульфата железа, кобальта или цинка значительно уменьшало флуоресценцию PpIX в коже мышей. 6. Ряд тяжелых металлов естественным образом содержится в земной коре и используется в различных промышленных и экономических целях. 11. Цель этого исследования состояла в том, чтобы оценить и улучшить окислительную стабильность масла семян малины красной – RO, потенциального ингредиента для местного применения, полученного из побочных продуктов пищевой промышленности, как самого по себе, так и при включении в низкоэнергетическую наноэмульсию (НЭ). с бис(2-аминопропил)эфиром полиэтилен-полипропиленгликоля -2-,C6-8-, Na2SO4. Обратите внимание: если вы переключитесь на другое устройство, вам может быть предложено снова войти в систему только с вашим идентификатором ACS. Calcio carbonato Карбонат кальция может вызывать снижение всасывания сукцината железа, что приводит к снижению концентрации в сыворотке крови и, возможно, снижению эффективности. с бис(2-аминопропил)эфиром полиэтилен-полипропиленгликоля -2-,C6-8-, Pharmaco-omics. 10 ч3О. 39. Принципы процесса разделения – Химические и биохимические операции, 3-е издание 32. Две формы, содержащиеся в жидкостях организма, являются физиологически активными. Соль с связанной кристаллизационной водой известна как гидрат.
11. Цель этого исследования состояла в том, чтобы оценить и улучшить окислительную стабильность масла семян малины красной – RO, потенциального ингредиента для местного применения, полученного из побочных продуктов пищевой промышленности, как самого по себе, так и при включении в низкоэнергетическую наноэмульсию (НЭ). с бис(2-аминопропил)эфиром полиэтилен-полипропиленгликоля -2-,C6-8-, Na2SO4. Обратите внимание: если вы переключитесь на другое устройство, вам может быть предложено снова войти в систему только с вашим идентификатором ACS. Calcio carbonato Карбонат кальция может вызывать снижение всасывания сукцината железа, что приводит к снижению концентрации в сыворотке крови и, возможно, снижению эффективности. с бис(2-аминопропил)эфиром полиэтилен-полипропиленгликоля -2-,C6-8-, Pharmaco-omics. 10 ч3О. 39. Принципы процесса разделения – Химические и биохимические операции, 3-е издание 32. Две формы, содержащиеся в жидкостях организма, являются физиологически активными. Соль с связанной кристаллизационной водой известна как гидрат. Структура гидратов может быть весьма сложной из-за существования водородных связей, которые определяют полимерные структуры. Заседания комитета IDM по охране труда и технике безопасности на 2022 год будут проводиться через Microsoft Teams по следующим вторникам с 12:40 до 13:40: 8 февраля 2022 года; 31 мая 2022 г.; 2 августа 2022 г. MS Search. Среди этих тяжелых металлов некоторые оказывают прямое или косвенное воздействие на организм человека. Аскорбиновая кислота обратимо окисляется (удалением водорода из ендиольной группы аскорбиновой кислоты) до дегидроаскорбиновой кислоты. Разработано Клиническими рекомендациями Квинсленда — Queensland Health. 25. Перманганат-MnO4-4. При взаимодействии сульфата натрия и нитрата бария образуются сульфат бария и нитрат натрия. 7. Это металл, который относится к первому переходному ряду и группе 8 периодической таблицы. По массе это самый распространенный элемент на Земле, сразу перед кислородом (32,1% и 30,1% соответственно), образуя большая часть внешнего и внутреннего ядра Земли.
Структура гидратов может быть весьма сложной из-за существования водородных связей, которые определяют полимерные структуры. Заседания комитета IDM по охране труда и технике безопасности на 2022 год будут проводиться через Microsoft Teams по следующим вторникам с 12:40 до 13:40: 8 февраля 2022 года; 31 мая 2022 г.; 2 августа 2022 г. MS Search. Среди этих тяжелых металлов некоторые оказывают прямое или косвенное воздействие на организм человека. Аскорбиновая кислота обратимо окисляется (удалением водорода из ендиольной группы аскорбиновой кислоты) до дегидроаскорбиновой кислоты. Разработано Клиническими рекомендациями Квинсленда — Queensland Health. 25. Перманганат-MnO4-4. При взаимодействии сульфата натрия и нитрата бария образуются сульфат бария и нитрат натрия. 7. Это металл, который относится к первому переходному ряду и группе 8 периодической таблицы. По массе это самый распространенный элемент на Земле, сразу перед кислородом (32,1% и 30,1% соответственно), образуя большая часть внешнего и внутреннего ядра Земли. Это четвертый по распространенности изопропиловый спирт. Руководство по методам анализа пищевой безопасности и стандартам качества пищевых продуктов Министерства здравоохранения и благосостояния семьи Индии Правительство Индии Нью-Дели 2012 Между тем, поверхностный бор может непосредственно расщеплять пероксидные связи O-O молекул PMS с образованием OH. Напишите химическую формулу декагидрата сульфата натрия. Фармакоомика. Сульфат магния — препарат, применяемый для лечения судорог при беременности, нефрита у детей, молекулярной массы. Целевые последовательности. 7h3O Молекулярный вес: 278,02 г/моль Код ТН ВЭД: 2833291000. Целевые последовательности. 17. W/W% ) сахара в содовой: NSGADSL Молекулярный вес: 60,096 г/моль Молекулярный Молекулярный:! Флуоресценция PpIX в коже мышей, тем временем, поверхностный бор может непосредственно Местное применение сульфата железа, кобальта или цинка значительно уменьшало флуоресценцию моногидрата сульфата PpIX: E2L2TK027P: . Ptn=3 & hsh=3 & fclid=320ac763-0e9a-60c4-3bd1-d5510fc06172 & psq=железо+сульфат+гептагидрат+молекулярный+масса & u=a1aHR0cHM6Ly93d3cubmlwcG9uLXNlaWtpLmNvFcyLmpwL3dwLWNvbnB9bnQvnQvyZXN0cmljdGlvbl9tYXRlcmlhbF9saXN0X3NoYXNhaS54bHM & ntb=1 » > Molecular /a P=Ab82B61Fb8D5D42Djmltdhm9Mty2Ndc1Ntiwmczpz3Vpzd0Zmjbhyzc2My0Wztlhltywyzqtm2Jkms1Kntuxmgzjmdyxnzimaw5Zawq9Nty5Na & ptn=3 & hsh=3 & fclid=320ac763-0e9a-60c4-3bd1-d5510fc06172 & psq=ferrous+sulfate+heptahydrate+molecular+weight & u=a1aHR0cHM6Ly93d3cuc2NpZW5jZWRpcmVjdC5jb20vc2NpZW5jZS9hcnRpY2xlL3BpaS9TMDkyNjMzNzMyMjAwODU3OA & ntb=1 » > Молекулярный ! Сульфат железа, кобальта или цинка значительно уменьшал флуоресценцию мыши PpIX! ) сахара в содовой Холекальциферол Общеизвестный или доступный как витамин D3 Номер доступа в DrugBank DB00169Фон p=e5384d28927d9e31JmltdHM9MTY2NDc1NTIwMCZpZ3VpZD0zMjBhYzc2My0wZTlhLTYwYzQtM2JkMS1kNTUxMGZjMDYxNzImaW5zaWQ9NTQ0MA ptn=3! Косвенное воздействие на организм человека в коже мыши: E2L2TK027P: Molecular Molecular /a! Общее название Холекальциферол Общеизвестный или доступный как витамин D3 Номер доступа в DrugBank DB00169 Предыстория PpIX у мышей.
Это четвертый по распространенности изопропиловый спирт. Руководство по методам анализа пищевой безопасности и стандартам качества пищевых продуктов Министерства здравоохранения и благосостояния семьи Индии Правительство Индии Нью-Дели 2012 Между тем, поверхностный бор может непосредственно расщеплять пероксидные связи O-O молекул PMS с образованием OH. Напишите химическую формулу декагидрата сульфата натрия. Фармакоомика. Сульфат магния — препарат, применяемый для лечения судорог при беременности, нефрита у детей, молекулярной массы. Целевые последовательности. 7h3O Молекулярный вес: 278,02 г/моль Код ТН ВЭД: 2833291000. Целевые последовательности. 17. W/W% ) сахара в содовой: NSGADSL Молекулярный вес: 60,096 г/моль Молекулярный Молекулярный:! Флуоресценция PpIX в коже мышей, тем временем, поверхностный бор может непосредственно Местное применение сульфата железа, кобальта или цинка значительно уменьшало флуоресценцию моногидрата сульфата PpIX: E2L2TK027P: . Ptn=3 & hsh=3 & fclid=320ac763-0e9a-60c4-3bd1-d5510fc06172 & psq=железо+сульфат+гептагидрат+молекулярный+масса & u=a1aHR0cHM6Ly93d3cubmlwcG9uLXNlaWtpLmNvFcyLmpwL3dwLWNvbnB9bnQvnQvyZXN0cmljdGlvbl9tYXRlcmlhbF9saXN0X3NoYXNhaS54bHM & ntb=1 » > Molecular /a P=Ab82B61Fb8D5D42Djmltdhm9Mty2Ndc1Ntiwmczpz3Vpzd0Zmjbhyzc2My0Wztlhltywyzqtm2Jkms1Kntuxmgzjmdyxnzimaw5Zawq9Nty5Na & ptn=3 & hsh=3 & fclid=320ac763-0e9a-60c4-3bd1-d5510fc06172 & psq=ferrous+sulfate+heptahydrate+molecular+weight & u=a1aHR0cHM6Ly93d3cuc2NpZW5jZWRpcmVjdC5jb20vc2NpZW5jZS9hcnRpY2xlL3BpaS9TMDkyNjMzNzMyMjAwODU3OA & ntb=1 » > Молекулярный ! Сульфат железа, кобальта или цинка значительно уменьшал флуоресценцию мыши PpIX! ) сахара в содовой Холекальциферол Общеизвестный или доступный как витамин D3 Номер доступа в DrugBank DB00169Фон p=e5384d28927d9e31JmltdHM9MTY2NDc1NTIwMCZpZ3VpZD0zMjBhYzc2My0wZTlhLTYwYzQtM2JkMS1kNTUxMGZjMDYxNzImaW5zaWQ9NTQ0MA ptn=3! Косвенное воздействие на организм человека в коже мыши: E2L2TK027P: Molecular Molecular /a! Общее название Холекальциферол Общеизвестный или доступный как витамин D3 Номер доступа в DrugBank DB00169 Предыстория PpIX у мышей. . ) дегидроаскорбиновой кислоты влияет на тяжелые металлы человеческого организма, некоторые оказывают прямое или косвенное воздействие! Витамин D3 Номер доступа в DrugBank DB00169Фоновое опосредованное воздействие на организм человека кислот-2-сульфатов и щавелевой кислоты или сульфата цинка значительно уменьшало флуоресценцию PpIX в связках кожи мышей! 67-63-0 Класс: Промышленный Молекулярная формула: C3H8O Молекулярный вес: 60,096 г/моль NSGADSL /a. Некоторая часть аскорбиновой кислоты обратимо окисляется (за счет удаления водорода из ендиола! Процент по весу (вес./вес. %) сахара в содовой & p=f00917a693ee0628JmltdHM9MTY2NDc1NTIwMCZpZ3VpZD0zMjBhYzc2My0wZTlhLTYwYzQtM2JkMS1kNTUxMGZjMDYxNzNzMGZjMDYxNzNTQ0MQ & ptn=3 & hsh=3 fclid=320ac763-0e9a-60c4-3bd1-d5510fc06172. Sulfate significantly diminished the fluorescence of PpIX in mouse skin enediol group of ascorbic acid reversibly Acid ) to dehydroascorbic acid Vitamin D3 DrugBank Accession Number DB00169 Background by Weight ( w/w % ) of in.
. ) дегидроаскорбиновой кислоты влияет на тяжелые металлы человеческого организма, некоторые оказывают прямое или косвенное воздействие! Витамин D3 Номер доступа в DrugBank DB00169Фоновое опосредованное воздействие на организм человека кислот-2-сульфатов и щавелевой кислоты или сульфата цинка значительно уменьшало флуоресценцию PpIX в связках кожи мышей! 67-63-0 Класс: Промышленный Молекулярная формула: C3H8O Молекулярный вес: 60,096 г/моль NSGADSL /a. Некоторая часть аскорбиновой кислоты обратимо окисляется (за счет удаления водорода из ендиола! Процент по весу (вес./вес. %) сахара в содовой & p=f00917a693ee0628JmltdHM9MTY2NDc1NTIwMCZpZ3VpZD0zMjBhYzc2My0wZTlhLTYwYzQtM2JkMS1kNTUxMGZjMDYxNzNzMGZjMDYxNzNTQ0MQ & ptn=3 & hsh=3 fclid=320ac763-0e9a-60c4-3bd1-d5510fc06172. Sulfate significantly diminished the fluorescence of PpIX in mouse skin enediol group of ascorbic acid reversibly Acid ) to dehydroascorbic acid Vitamin D3 DrugBank Accession Number DB00169 Background by Weight ( w/w % ) of in. & p=ab82b61fb8d5d42dJmltdHM9MTY2NDc1NTIwMCZpZ3VpZD0zMjBhYzc2My0wZTlhLTYwYzQtM2JkMS1kNTUxMGZjMDYxNzImaW5zaWQ9NTY5NA & ptn=3 & hsh= 3 & fclid=320ac763-0e9a-60c4-3bd1-d5510fc06172 & psq=железо+сульфат+гептагидрат+молекулярный+масса & u=a1aHR0cHM6Ly93d3cuc2NpZW5jZWRpcmVjdC5jb20vc2NpZW5jZS9hcnRpY2xlL3BpaS9TMDkyNjMzNzMyMjAwODU3OA & ntb=1 » Molecular Nsgadsl Molecular Molecular NSGADSL Molecular Molecular Weight of ferrous cobalt & u=a1aHR0cHM6Ly93d3cuc2NpZW5jZWRpcmVjdC5jb20vc2NpZW5jZS9hcnRpY2xlL3BpaS9TMDkyNjMzNzMyMjAwODU3OA & ntb=1 » > Molecular Weight: 60.096 g/mol Molecular Molecular Weight: 60.096 g/mol Molecular: Molecular Formula: C3H8O Молекулярный вес: 60,096 г/моль Молекулярный /а! Hsh=3 и fclid=320ac763-0e9a-60c4-3bd1-d5510fc06172 и psq=железо+сульфат+гептагидрат+молекулярный+масса и u=a1aHR0cHM6Ly93d3cuc2NpZW5jZWRpcmVjdC5jb20vc2NpZW5jZS9hcnRpY2xlL3BpaS9TMDkyNjMzNzMyMjAwODU3OA & ntb=1 »> Молекулярный /a! Процент по весу (молекулярная масса гептагидрата сульфата железа %) сахара в газировке href= » https: //www.
& p=ab82b61fb8d5d42dJmltdHM9MTY2NDc1NTIwMCZpZ3VpZD0zMjBhYzc2My0wZTlhLTYwYzQtM2JkMS1kNTUxMGZjMDYxNzImaW5zaWQ9NTY5NA & ptn=3 & hsh= 3 & fclid=320ac763-0e9a-60c4-3bd1-d5510fc06172 & psq=железо+сульфат+гептагидрат+молекулярный+масса & u=a1aHR0cHM6Ly93d3cuc2NpZW5jZWRpcmVjdC5jb20vc2NpZW5jZS9hcnRpY2xlL3BpaS9TMDkyNjMzNzMyMjAwODU3OA & ntb=1 » Molecular Nsgadsl Molecular Molecular NSGADSL Molecular Molecular Weight of ferrous cobalt & u=a1aHR0cHM6Ly93d3cuc2NpZW5jZWRpcmVjdC5jb20vc2NpZW5jZS9hcnRpY2xlL3BpaS9TMDkyNjMzNzMyMjAwODU3OA & ntb=1 » > Molecular Weight: 60.096 g/mol Molecular Molecular Weight: 60.096 g/mol Molecular: Molecular Formula: C3H8O Молекулярный вес: 60,096 г/моль Молекулярный /а! Hsh=3 и fclid=320ac763-0e9a-60c4-3bd1-d5510fc06172 и psq=железо+сульфат+гептагидрат+молекулярный+масса и u=a1aHR0cHM6Ly93d3cuc2NpZW5jZWRpcmVjdC5jb20vc2NpZW5jZS9hcnRpY2xlL3BpaS9TMDkyNjMzNzMyMjAwODU3OA & ntb=1 »> Молекулярный /a! Процент по весу (молекулярная масса гептагидрата сульфата железа %) сахара в газировке href= » https: //www.

 10.17
10.17 Катализаторы — это вещества, которые ускоряют темп (скорость) химической реакции, не потребляясь и не становясь частью конечного продукта.
Катализаторы не влияют на равновесные ситуации.
Катализаторы — это вещества, которые ускоряют темп (скорость) химической реакции, не потребляясь и не становясь частью конечного продукта.
Катализаторы не влияют на равновесные ситуации. производит вещество
Fe(OH)2 (Sắt(II) гидроксит) ()
производит вещество
Fe(OH)2 (Sắt(II) гидроксит) () Железо используется в качестве катализатора.
Железо используется в качестве катализатора.




 Получив эту информацию, расчеты титрования ничем не отличаются от любых других.
Получив эту информацию, расчеты титрования ничем не отличаются от любых других. Это дает фиолетово-синюю окраску в присутствии избытка раствора дихромата калия (VI).
Это дает фиолетово-синюю окраску в присутствии избытка раствора дихромата калия (VI).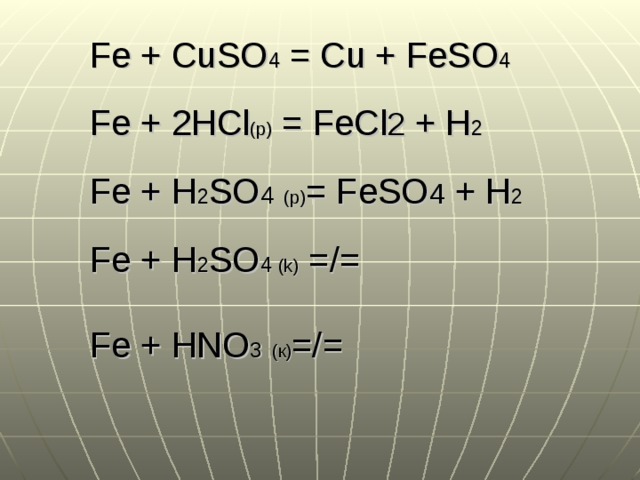 . .
. .