Закон эквивалентов | Химик.ПРО – решение задач по химии бесплатно
Закон эквивалентов — массы реагирующих веществ прямопропорциональны молярным массам эквивалента этих веществ.
Масса сульфита натрия
Какая масса сульфита натрия (Na2SO3) потребуется для восстановления 0,05 литра 0,1 нормального перманганата калия (KMnO4) в присутствии серной кислоты?
Категории: Закон эквивалентов , Основные законы химии и стехиометрические расчеты , Расчеты по химическим уравнениям
Комментировать
Молярная масса эквивалента хромата калия
Вычислите молярную массу эквивалента хромата калия (K2CrO4) как окислителя, если хромат калия (K2CrO4) восстанавливается до хромита калия (KCrO2).
Категории: Закон эквивалентов , Основные законы химии и стехиометрические расчеты
Комментировать
Эквивалентная масса металла
При растворении в кислоте металла массой 11,9 грамм выделился водород объемом 2,24 литра (нормальные условия). Чему равна эквивалентная масса металла ( Мэкв) и фактор эквивалентности металла (fэкв).
Чему равна эквивалентная масса металла ( Мэкв) и фактор эквивалентности металла (fэкв).
Категории: Закон эквивалентов , Основные законы химии и стехиометрические расчеты
Комментировать
Соляная кислота вода
К какому объёму воды следует добавить 1 миллилитр соляной кислоты (HCl) с молярной концентрацией 0,1 моль/л, чтобы получить раствор с рОН 11?
Категории: Закон эквивалентов , Основные законы химии и стехиометрические расчеты , Разбавление и приготовление более концентрированных растворов , Растворы
Комментировать
Молярная масса эквивалента вещества
Вычислить молярные массы эквивалента вещества: хлорида цинка (ZnCl2), карбоната натрия (Na2CO3), гидроксида алюминия (Al(OH)3).
Категории: Закон эквивалентов , Основные законы химии и стехиометрические расчеты
Комментировать
Вычислить молярные массы эквивалентов (тригидроксид железа)
Определите эквиваленты и вычислить молярные массы эквивалентов тригидроксида железа (Fe(OH)3) в реакциях: Fe(OH)3 + 3 HCl = FeCl3 +3h3O; Fe(OH)3 + 2 HCl = FeOHCl2 +2h3O; Fe(OH)3 + HCl = Fe(OH)2Cl + h3O.
Категории: Закон эквивалентов , Основные законы химии и стехиометрические расчеты
4 комментария
Определить эквивалентную массу
Вычислить фактор эквивалентности и определить эквивалентную массу ортофосфорной кислоты (h4PO4) в реакциях образования гидрофосфата, дигидрофосфата и ортофосфата.
Категории: Закон эквивалентов , Основные законы химии и стехиометрические расчеты
Комментировать
Эквивалентная масса серы
Какова эквивалентная масса серы (S), если 4 грамма ее окисляются 2,8 литрами кислорода (O) (нормальные условия)?
Категории: Закон эквивалентов , Основные законы химии и стехиометрические расчеты
Комментировать
Молярная масса эквивалента (серная кислота)
При взаимодействии серной кислоты (h3SO4) со щелочью образуются соли гидросульфат калия (KHSO4) и сульфат калия (K2SO4). Вычислить эквивалент и молярные массы эквивалентов кислоты для каждого случая. Написать соответствующие уравнения реакций.
Категории: Закон эквивалентов , Основные законы химии и стехиометрические расчеты
Комментировать
Масса эквивалента
Найдите массу эквивалента металла, если 3 грамма его реагируют с 2 граммами кислорода (O2).
Категории: Закон эквивалентов , Основные законы химии и стехиометрические расчеты
Комментировать
Варианты ЕГЭ 2023 по химии 11 класс ХИ2210401-ХИ2210402 статград ответы и решения
Вариант ХИ2210401 с ответами
Скачать ответы и решения для варианта
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
● 1) Mg,
● 2) C,
● 3) B,
● 4) Si, ● 5) Li.
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1. Какие из указанных элементов имеют в первом возбуждённомсостоянии конфигурацию внешнего уровня ns1 np3 ? Запишите номера выбранных элементов.
2.
Из указанного ряда выберите три элемента, принадлежащие
одномупериоду Периодической системы, и расположите их в порядке увеличения
первой энергии ионизации атома.
3. Из указанного ряда выберите два элемента, у которых разностьмежду высшей и низшей степенями окисления равна 8. Запишите в поле ответа номера выбранных элементов.
4. Из предложенного перечня выберите две частицы, в которых одиниз элементов образует четыре ковалентные связи. Запишите номера выбранных ответов.
● 1) Nh4
● 2) h3O2
● 3) BF4 –
● 4) P4O6
● 5) SO2
5. Среди предложенных формул/названий веществ, расположенных впронумерованных ячейках, выберите формулы/названия: А) сильного основания; Б) основной соли; В) одноосновной кислоты. Запишите в таблицу номера ячеек, в которых расположены вещества, под соответствующими буквами.
6.
В двух пробирках находился раствор карбоната аммония. В
первуюпробирку добавили раствор вещества Х, а во вторую – раствор вещества Y. В
первой пробирке видимых признаков реакции не наблюдалось даже при нагревании, а
во второй выпал желтоватый осадок.
● 1) NaOH
● 2) CaCl2
● 3) AgNO3
● 4) K2SO4
● 5) CuSO4
7. Установите соответствие между формулой вещества и реагентами, скаждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
8. Установите соответствие между исходными веществами,вступающими в реакцию, и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
10. Установите соответствие между названием гомологического ряда иего общей формулой: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
11. Из предложенного перечня выберите два межклассовых изомера.Запишите номера выбранных ответов.
● 1) пентанон-3 ● 2) пентанол-1
● 3) 3-метилбутанон
● 4) пентановая кислота
● 5) этилизопропиловый эфир
12. Из предложенного перечня выберите все вещества, которые приопределённых
условиях могут быть восстановлены до первичного спирта. Запишите номера
выбранных ответов.
Из предложенного перечня выберите все вещества, которые приопределённых
условиях могут быть восстановлены до первичного спирта. Запишите номера
выбранных ответов.
● 1) ацетон
● 2) масляная кислота
● 3) фенол
● 4) этилацетат
● 5) 2-метилпропаналь
13. Из предложенного перечня выберите два вещества, которыепроявляют более сильные основные свойства, чем аммиак. Запишите номера выбранных ответов.
● 1) нитробензол
● 2) 1,2-диаминоэтан
● 3) анилин
● 4) пиридин
● 5) диметиламин
14. Установите соответствие между схемой реакции и веществом Х,принимающим в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
15.
Установите соответствие между реагирующими веществами
иуглеродсодержащим продуктом, который образуется при взаимодействии этих
веществ: к каждой позиции, обозначенной буквой, подберите соответствующую
позицию, обозначенную цифрой.
17. Из предложенного перечня выберите все реакции присоединения.Запишите номера выбранных ответов.
● 1) взаимодействие хлорэтана со спиртовым раствором щёлочи
● 2) взаимодействие циклопропана с бромом
● 3) взаимодействие пентана с бромом на свету
● 4) взаимодействие бутадиена с хлороводородом
● 5) димеризация ацетилена в присутствии катализатора
18. Из предложенного перечня выберите все реакции, скоростькоторых зависит от давления. Запишите номера выбранных ответов.
● 1) взаимодействие хлора с раствором щёлочи
● 2) растворение железа в соляной кислоте
● 3) восстановление оксида меди(II) водородом
● 4) нитрование бензола
● 5) горение алюминия в кислороде
19. Установите
соответствие между схемойокислительно-восстановительной реакции и степенью
окисления элемента-восстановителя: к каждой позиции, обозначенной буквой,
подберите соответствующую позицию, обозначенную цифрой.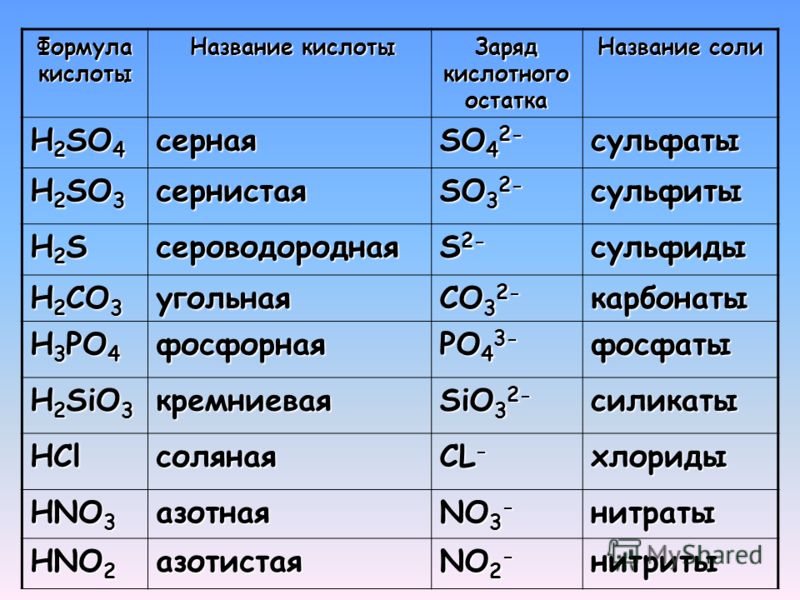
20. Установите соответствие между формулой вещества и продуктамиэлектролиза водного раствора или расплава этого вещества, выделившимися на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
21. Для веществ, приведённых в перечне, определите характер средыих водных растворов, имеющих одинаковую молярную концентрацию. Запишите номера веществ в порядке возрастания значения pH их водных растворов.
● 1) K2SO4
● 2) K2SO3
● 3) KHSO4
● 4) K2S
22. Установите соответствие между способом воздействия наравновесную систему CO3 2– (р-р) + h3O(ж.) HCO3 – (р-р) + OH– (р-р) – Q и направлением смещения равновесия при этом воздействии: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
23. В реакторе
постоянного объёма смешали азот и водород. Врезультате обратимой реакции: N2(г)
+ 3h3(г) ←→ 2Nh4(г) в реакторе установилось равновесие. Исходная концентрация
азота была равна
Исходная концентрация
азота была равна
1,0 моль/л, а равновесные концентрации водорода и аммиака составили 2,0 моль/л и 0,8 моль/л, соответственно. Найдите равновесную концентрацию азота (X) и исходную концентрацию водорода (Y). Выберите из списка номера правильных ответов.
● 1) 0,4 моль/л
● 2) 0,6 моль/л
● 3) 0,8 моль/л
● 4) 1,2 моль/л
● 5) 2,4 моль/л
● 6) 3,2 моль/л
24. Установите соответствие между названием вещества и признакомреакции, который наблюдается при взаимодействии вещества с водным раствором аммиака: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
25. Установите соответствие между смесью веществ и методом еёразделения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
26. При
охлаждении 200 г раствора гидрокарбоната аммония выпалосадок – безводная соль.
Раствор над осадком имел массу 150 г и содержал 18 % соли по массе.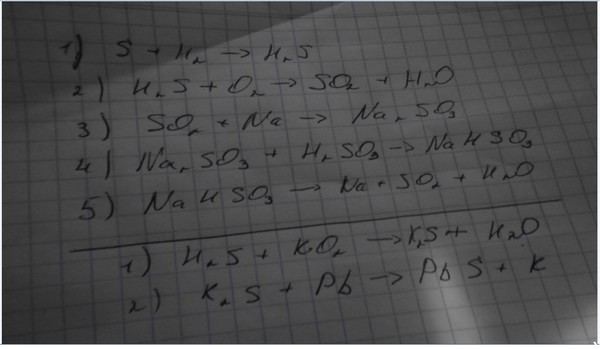 Найдите
массовую долю (в %) соли в исходном растворе. (Запишите число с точностью до
десятых.)
Найдите
массовую долю (в %) соли в исходном растворе. (Запишите число с точностью до
десятых.)
27. Горение угарного газа описывается термохимическим уравнением: CO(г) + 1/2O2(г) = CO2(г) + 284 кДж Сколько литров кислорода (н. у.) потребуется для получения 213 кДж теплоты сжиганием угарного газа? (Запишите число с точностью до десятых.)
28. Сколько килограммов бутадиена-1,3 можно получить из 20 кг 96 %-го этанола, если выход в реакции Лебедева составляет 71 %? (Ответ запишите с точностью до целых.)
29. Из предложенного перечня выберите вещества, между которымиокислительно-восстановительная реакция протекает с изменением цвета раствора. В ответе запишите уравнение только одной из возможных окислительновосстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30. Из
предложенного перечня веществ выберите вещества, которыевступают в реакцию
ионного обмена с выделением газа. Запишите молекулярное, полное и сокращённое
ионное уравнения реакции с участием выбранных веществ.
31. Серебро растворили в разбавленной азотной кислоте. Черезполученный раствор пропустили сероводород, из раствора выпал чёрный осадок. Осадок отфильтровали и прокалили на воздухе. Газ, выделившийся при прокаливании, поглотили известковой водой, в результате из раствора выпал осадок. Напишите молекулярные уравнения четырёх описанных реакций.
32. Напишите уравнения реакций, с помощью которых можноосуществить следующие превращения: С3H6 → C3H6Br2 → X1 → пропандиовая кислота → X2 → C2h4OCl При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
33. Органическое
вещество X относится к ароматическим соединениям и проявляет слабые основные
свойства. Оно реагирует с одним эквивалентом хлороводорода, образуя вещество,
содержащее 27,4 % хлора и 10,8 % азота по массе. Вещество X окисляется
перманганатом калия, не реагирует с бромной водой и азотистой кислотой. На
основании данных условия задачи: 1) проведите необходимые вычисления
(указывайте единицы измерения и обозначения искомых физических величин) и
установите молекулярную формулу вещества X; 2) составьте возможную структурную
формулу вещества X, которая однозначно отражает порядок связи атомов в его
молекуле; 3) напишите уравнение реакции вещества X с горячим водным раствором
перманганата калия (в уравнении используйте структурные формулы органических
веществ).
34. Навеску хлорида фосфора(V) растворили в 50 мл горячей воды.
Для полной нейтрализации полученного раствора потребовалось 190 г
3,6 %-го раствора гидроксида бария. Выпавший осадок отфильтровали. Рассчитайте массу осадка и массовую долю соли в фильтрате. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения и обозначения искомых физических величин).
Вариант ХИ2210402 с ответами
Для выполнения заданий 1–3 используйте следующий ряд химических элементов: 1) Na, 2) O, 3) Ar, 4) B, 5) Al Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1. Какие из указанных элементов имеют в первом возбуждённомсостоянии конфигурацию внешнего уровня ns1 np2 ? Запишите номера выбранных элементов.
2.
Из указанного ряда выберите три элемента, принадлежащие
одномупериоду Периодической системы, и расположите их в порядке уменьшения
первой энергии ионизации атома. Запишите в поле ответа номера выбранных
элементов в нужной последовательности.
Запишите в поле ответа номера выбранных
элементов в нужной последовательности.
3. Из указанного ряда выберите два элемента, способные проявлятьотрицательную степень окисления. Запишите в поле ответа номера выбранных элементов.
4. Из предложенного перечня выберите две частицы, в которых одиниз элементов образует три ковалентные связи. Запишите номера выбранных ответов.
● 1) Nh5 +
● 2) SO3
● 3) Alh5 –
● 4) h4O+
● 5) HCN
5. Среди предложенных формул/названий веществ, расположенных впронумерованных ячейках, выберите формулы/названия: А) основного оксида; Б) бескислородной кислоты; В) кислой соли. Запишите в таблицу номера ячеек, в которых расположены вещества, под соответствующими буквами.
6.
В двух пробирках находился раствор иодида алюминия. В
первуюпробирку добавили раствор вещества Х, а во вторую – раствор вещества Y. В
первой пробирке видимых признаков реакции не наблюдалось, а во второй выпал
белый осадок, при этом газ не выделялся. Из предложенного перечня выберите
вещества X и Y, которые могут вступать в описанные реакции.
Из предложенного перечня выберите
вещества X и Y, которые могут вступать в описанные реакции.
● 1) Nh5Cl
● 2) Pb(NO3)2
● 3) K2CO3
● 4) Nh4
● 5) (Nh5)2S
7. Установите соответствие между формулой вещества и реагентами, скаждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
8. Установите соответствие между исходными веществами,вступающими в реакцию, и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
10. Установите соответствие между названием гомологического ряда иего общей формулой: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
11. Из предложенного перечня выберите два структурных изомера.Запишите номера выбранных ответов.
● 1) пентандиол-2,3
● 2) пропилацетат
● 3) дипропиловый эфир
● 4) циклопентанол
● 5) 2-метилбутаналь
12.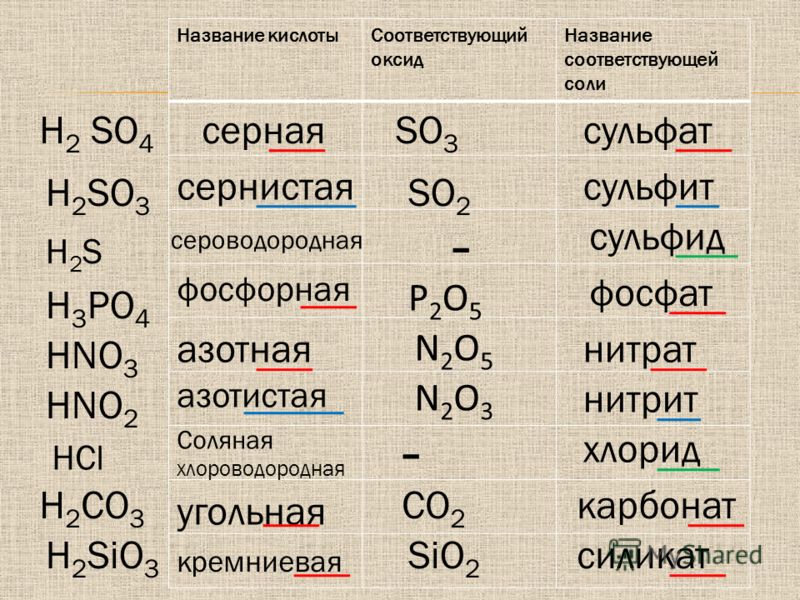 Из предложенного перечня выберите все вещества, при
гидролизекоторых в кислой среде образуется карбоновая кислота. Запишите номера
выбранных ответов.
Из предложенного перечня выберите все вещества, при
гидролизекоторых в кислой среде образуется карбоновая кислота. Запишите номера
выбранных ответов.
● 1) 2,2-дихлопропан
● 2) уксусный ангидрид
● 3) 1,1,1-трихлорэтан
● 4) цианометан
● 5) метоксибензол
13. Из предложенного перечня выберите два вещества, которыепроявляют основные свойства, но являются более слабыми основаниями, чем аммиак. Запишите номера выбранных ответов.
● 1) пиррол
● 2) пиридин
● 3) триметиламин
● 4) метилат натрия
● 5) 2-метиланилин
14. Установите соответствие между схемой реакции и веществом Х,принимающим в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
15.
Установите соответствие между реагирующими веществами
иорганическим продуктом, который преимущественно образуется при взаимодействии
этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую
позицию, обозначенную цифрой.
17. Из предложенного перечня выберите все реакции замещения.Запишите номера выбранных ответов.
● 1) взаимодействие 2-хлорпропана с водным раствором щёлочи
● 2) взаимодействие фенола с разбавленной азотной кислотой
● 3) нагревание 1,3-дибромпропана с цинком
● 4) взаимодействие ацетона с водородом
● 5) взаимодействие метиламина с хлорметаном
18. Из предложенного перечня выберите все реакции, скоростькоторых не зависит от давления. Запишите номера выбранных ответов.
● 1) горение серы в кислороде
● 2) растворение алюминия в растворе щёлочи
● 3) нейтрализация азотной кислоты гидроксидом бария
● 4) изомеризация α-глюкозы в β-глюкозу
● 5) взаимодействие аммиака и хлороводорода
19.
Установите соответствие между
схемойокислительно-восстановительной реакции и степенью окисления
элемента-окислителя: к каждой позиции, обозначенной буквой, подберите
соответствующую позицию, обозначенную цифрой.
20. Установите соответствие между формулой вещества и продуктамиэлектролиза водного раствора или расплава этого вещества, выделившимися на инертных электродах: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
21. Для веществ, приведённых в перечне, определите характер средыих водных растворов, имеющих одинаковую концентрацию (моль/л). Запишите номера веществ в порядке уменьшения значения pH их водных растворов.
● 1) NaHCO3
● 2) NaI
● 3) NaOH
● 4) HI
23.
В реакторе постоянного объёма смешали оксид серы(IV) и кислород.
В результате обратимой реакции: 2SO2(г) + O2(г) ←→ 2SO3(г) в реакторе
установилось равновесие. Исходная концентрация кислорода была равна 0,1 моль/л,
а равновесные концентрации оксида серы(VI) и оксида серы(IV) составили 0,08
моль/л и 0,12 моль/л, соответственно. Найдите равновесную концентрацию
кислорода (X) и исходную концентрацию оксида серы(IV) (Y). Выберите из списка
номера правильных ответов.
Выберите из списка
номера правильных ответов.
● 1) 0,04 моль/л
● 2) 0,06 моль/л
● 3) 0,08 моль/л
● 4) 0,12 моль/л
● 5) 0,16 моль/л
● 6) 0,2 моль/л
24. Установите соответствие между названием вещества и признакомреакции, который наблюдается при взаимодействии вещества с разбавленной соляной кислотой: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
25. Установите соответствие между смесью веществ и методом еёразделения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
26. При охлаждении 400 г 70 %-го раствора нитрата аммония выпалосадок – безводная соль. В образовавшемся растворе массовая доля нитрата аммония снизилась до 60 %. Найдите массу осадка (в г). (Запишите число с точностью до целых.)
27.
Горение бутана описывается термохимическим уравнением: C4h20(г) +
6,5O2(г) = 4CO2(г) + 5h3O(ж) + 2880 кДж Сколько миллилитров углекислого газа
(н. у.) выделится в атмосферу при получении 360 Дж теплоты сжиганием бутана?
(Ответ запишите с точностью до десятых).
у.) выделится в атмосферу при получении 360 Дж теплоты сжиганием бутана?
(Ответ запишите с точностью до десятых).
28. В результате тримеризации пропина объёмом 74 л (н. у.) получилисмесь триметилбензолов общей массой 99 г. Рассчитайте общий выход (в %) продуктов тримеризации. (Ответ запишите с точностью до целых.)
29. Из предложенного перечня выберите вещества, между которымиокислительно-восстановительная реакция протекает с выделением газа и изменением цвета раствора. В ответе запишите уравнение только одной из возможных окислительновосстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30. Из предложенного перечня веществ выберите вещества, которыевступают в реакцию ионного обмена с образованием осадка. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
31.
Чёрное вещество, образовавшееся при прокаливании нитрата
меди,растворили в соляной кислоте. Через полученный раствор пропустили
сернистый газ, в результате выпал белый осадок, который растворяется в
аммиачной воде. Напишите молекулярные уравнения четырёх описанных реакций.
Через полученный раствор пропустили
сернистый газ, в результате выпал белый осадок, который растворяется в
аммиачной воде. Напишите молекулярные уравнения четырёх описанных реакций.
32. Напишите уравнения реакций, с помощью которых можноосуществить следующие превращения: C4h20O → бутен-2 → X1 → бутин-2 → X2 → C12H6O12 При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
33. Органическое вещество X представляет собой бесцветную жидкость с запахом аммиака. Оно реагирует с двумя эквивалентами бромоводорода, образуя вещество, содержащее 72,1 % брома и 12,6 % азота по массе. Вещество X реагирует с азотистой кислотой, при этом выделяется в 2 раза больше азота, чем при сгорании X. На основании данных условия задачи:
● 1) проведите необходимые вычисления (указывайте единицы измерения и обозначения искомых физических величин) и установите молекулярную формулу вещества X;
● 2) составьте структурную формулу вещества X, которая однозначно отражает порядок связи атомов в его молекуле;
●
3) напишите уравнение реакции вещества X с избытком гидроксида
калия (в уравнении используйте структурные формулы органических веществ).
34. Для полной нейтрализации раствора, полученноговзаимодействием хлорангидрида серной кислоты SO2Cl2 со 100 мл горячей воды, потребовалось 380 г 2,7 %-го раствора гидроксида бария. Выпавший осадок отфильтровали. Рассчитайте массу осадка и массовую долю соли в фильтрате. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения и обозначения искомых физических величин).
Скачать ответы и решения для варианта
Китайский производитель тетрагидрата пербоната натрия, соединение моноперсульфата калия, поставщик силиката магния
Горячие продукты
Видео
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Видео
Свяжитесь сейчас
Свяжитесь сейчас
Популярные продукты
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Видео
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Видео
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Рекомендуется для вас
Свяжитесь сейчас
Свяжитесь сейчас
Видео
Свяжитесь сейчас
Видео
Свяжитесь сейчас
Видео
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Свяжитесь сейчас
Видео
Свяжитесь сейчас
Свяжитесь сейчас
Профиль компании
{{ util. each(imageUrls, функция(imageUrl){}}
each(imageUrls, функция(imageUrl){}}
{{ }) }}
{{ если (изображениеUrls.length > 1){ }}
{{ } }}
| Вид бизнеса: | Производитель/Фабрика | |
| Основные продукты: | тетрагидрат пербоната натрия
,
Соединение моноперсульфата калия
,
Силикат магния
,
. .. .. | |
| Зарегистрированный капитал: | 50941404 юаней | |
| Площадь завода: | 101~500 квадратных метров | |
| Сертификация системы менеджмента: | ИСО 9001, ИСО 14001, ИСО 20000 | |
| Среднее время выполнения: | Время выполнения заказа в сезон пиковой нагрузки: в течение 15 рабочих дней Время выполнения заказа в межсезонье: в течение 15 рабочих дней |
Компания Shaoxing Shangyu Jiehua Chemical Co. , Ltd. (именуемая Shangyu Jiehua) была основана в 2001 году. У нас есть сильная техническая база и производственные мощности в области пероксидов. После непрерывных технологических инноваций, расширения производственных мощностей, расширения ассортимента и развития рынка Shangyu Jiehua быстро превратилась в важную производственную базу пероксидов в Азиатско-Тихоокеанском регионе и в одного из ведущих мировых поставщиков пероксидов.
, Ltd. (именуемая Shangyu Jiehua) была основана в 2001 году. У нас есть сильная техническая база и производственные мощности в области пероксидов. После непрерывных технологических инноваций, расширения производственных мощностей, расширения ассортимента и развития рынка Shangyu Jiehua быстро превратилась в важную производственную базу пероксидов в Азиатско-Тихоокеанском регионе и в одного из ведущих мировых поставщиков пероксидов.
Наши пероксидные продукты широко используются в промышленности …
Просмотреть все
Сертификаты
3 шт.бизнес-лицензия
ИСО14001
ИСО9001
Отправить сообщение этому поставщику
* Откуда:
* Кому:
г-жа Элейн Ван
* Сообщение:
Введите от 20 до 4000 символов.
Это не то, что вы ищете? Опубликовать запрос на поставку сейчас
= | Сбалансированное уравнение химической реакции
| Поиск |
Результаты поиска по химическому уравнению
Реклама
1 результатов найдено
Отображение уравнения от 1 до 1 Страница 1 — Пожалуйста, прокрутите до конца, чтобы увидеть больше результатов
Уравнение Результат #1
Нажмите, чтобы увидеть более подробную информацию и рассчитать вес/моль >>
| png» substance-weight=»136.1688″> KHSO 4 | → | РекламаДополнительная информация об уравнении KOH + KHSO4 → H 2 O + K 2 SO 4Что такое условие реакции KOH (гидроксид калия) с KHSO4 ()?Для этого химического уравнения не найдено информации Объяснение: идеальные условия окружающей среды для реакции, такие как температура, давление, катализаторы и растворитель. |

