§ Задача на растворы. Задачи на концентрацию
Похоже, вы используете блокировщик рекламы. Наш сайт существует и развивается только за счет дохода от рекламы.
Пожалуйста, добавьте нас в исключения блокировщика.
Скрыть меню
На главную страницу
Войти при помощи
Темы уроков
Начальная школа
- Геометрия: начальная школа
- Действия в столбик
- Деление с остатком
- Законы арифметики
- Периметр
- Порядок действий
- Разряды и классы. Разрядные слагаемые
- Счет в пределах 10 и 20
Математика 5 класс
- Взаимно обратные числа и дроби
- Десятичные дроби
- Натуральные числа
- Нахождение НОД и НОК
- Обыкновенные дроби
- Округление чисел
- Перевод обыкновенной дроби в десятичную
- Площадь
- Проценты
- Свойства сложения, вычитания, умножения и деления
- Среднее арифметическое
- Упрощение выражений
- Уравнения 5 класс
- Числовые и буквенные выражения
Математика 6 класс
- Масштаб
- Модуль числа
- Окружность.
 Площадь круга
Площадь круга - Отношение чисел
- Отрицательные и положительные числа
- Периодическая дробь
- Признаки делимости
- Пропорции
- Рациональные числа
- Система координат
- Целые числа
Алгебра 7 класс
- Алгебраические дроби
- Как применять формулы сокращённого умножения
- Многочлены
- Одночлены
- Системы уравнений
- Степени
- Уравнения
- Формулы сокращённого умножения
- Функция в математике
Геометрия 7 класс
- Точка, прямая и отрезок
- Что такое аксиома и теорема
Алгебра 8 класс
- Квадратичная функция. Парабола
- Квадратные неравенства
- Квадратные уравнения
- Квадратный корень
- Неравенства
- Системы неравенств
- Стандартный вид числа
- Теорема Виета
Алгебра 9 класс
- Возрастание и убывание функции
- Нули функции
- Область определения функции
- Отрицательная степень
- Среднее
геометрическое - Чётные и нечётные функции
Алгебра 10 класс
- Иррациональные числа
Алгебра 11 класс
- Факториал
Чем больше мы размышляем, тем более убеждаемся, что ничего не знаем.
на главную
Введите тему
Поддержать сайт
Проценты Действия с процентами Основные задачи на проценты Задачи на концентрацию растворов Задачи на вклады и скидку
Для того, чтобы решать задачи на растворы и концентрацию, необходимо чётко понимать, что называется концентрацией раствора.
Запомните!
Концентрация раствора — это часть, которую составляет масса растворённого вещества от массы всего раствора.
- 9%-я концентрация раствора соли — это 9 грамм соли в 100 граммах раствора.
Разбор примера
Килограмм соли растворили в 9 л воды. Чему равна концентрация полученного раствора? (Масса 1 л воды составляет 1 кг)
Используя определение концентрации данное выше, решим задачу следующим образом.
- 1 кг — масса растворённого вещества (соли)
- 9 кг — масса воды в растворе (не путать с общей массой раствора)
- 9 + 1 = 10 кг — общая масса раствора.
Ответ: 10% — концентрация раствора.
Разбор примера
Теперь решим обратную задачу.
Сколько соли получится при выпаривании 375 граммов 12%-го раствора?
Чтобы найти массу выпаренной соли из раствора, умножим общую массу раствора на процент концентрации. Не забудем предварительно перевести процент в десятичную дробь.
Ответ: 45 г соли.
В растворе 40% соли. Если добавить 120 г соли, то процентное содержание соли станет равным 70. Сколько грамм соли было первоначально в растворе?
Для составления пропорции обозначим за «x» первоначальную массу соли в растворе, а за «y» массу воды в растворе. Так как концентрация соли в исходном растворе 40%, то соответственно вода составляет
100% − 40%= 60%
Изобразим графически условия задачи.
Составим пропорцию, связывающую эти величины до добавления соли.
Для решения задачи нам надо определить какая из неизвестных («x» или «y») остаётся неизменной после добавления соли.
Этой величиной является масса воды в растворе «y».
Выразим её, учитывая изменения в растворе после добавления соли.
- (x + 120) г — масса соли в новом растворе
- (100% − 70% = 30% — процентное содержание воды в новом растворе.
Составим пропорцию аналогично предыдущей, но с учётом изменений произошедших после добавления соли.
Так как масса воды осталось неизменной после добавления соли, приравняем её значения до и после добавления соли и решим уравнение.
Ответ: 48 г — масса соли в первоначальном растворе.
Проценты Действия с процентами Основные задачи на проценты Задачи на концентрацию растворов Задачи на вклады и скидку
Концентрация массовая: что это такое и как правильно рассчитать
Концентрация массовая: что это такое и как правильно рассчитать | Глоссарий компании «Техноформ»8 (800) 550-83-25
Пн. -Пт., 9:00 — 18:00
-Пт., 9:00 — 18:00
Вход
Регистрация
Концентрация смеси выражает содержание в ней составляющих компонентов. Показатель дает возможность определить содержание конкретного вещества в растворе. Чаще всего используются такие виды концентрации растворов: массовая, объемная, массовые доли, молярная концентрация.
Что такое раствор?
Большинство веществ, которые нас окружают, не являются чистыми. Как правило, это смеси, которые содержат в своем составе несколько компонентов, находящихся в одном или разных состояниях (жидкость, газ, твердое вещество). Смеси, которые имеют однородный состав, называются гомогенными, если состав неоднородный, – гетерогенными. Гомогенные смеси – это растворы, когда одно вещество (растворитель) полностью растворяет другое. Растворитель является компонентом раствора, который в получившейся смеси сохраняет свое состояние, как правило, его количество наибольшее.
Растворы могут быть газовыми, жидкими, твердыми.
Концентрация раствора бывает качественной и количественной. Качественная концентрация определяет растворы насыщенные, ненасыщенные, перенасыщенные. Количественная концентрация раствора выражается через доли вещества, которые входят в его состав.
Массовая концентрация
Показатель характеризует растворенное вещество. Массовая концентрация выражается в граммах, которые содержатся в 100 грамм раствора.
Каждая смесь может содержать разное количество растворителя и растворенного вещества. Если количество второго в отношении растворителя достаточно большое, раствор будет концентрированный, если меньше – слабый.
Концентрация раствора – важная характеристика при его описании. Важно установить, процентное содержание растворенного вещества в полученном растворе. Так, если масса раствора 110 г, масса вещества 10 г, то для расчета его концентрации нужно 10/110х100%. В результате получится, что концентрация раствора составляет около 9,09 процентных единиц.
Используется концентрация растворов, чтобы описать массовую долю вещества, которое в нем растворяется (w), как отношение его массы е общей массе всего раствора.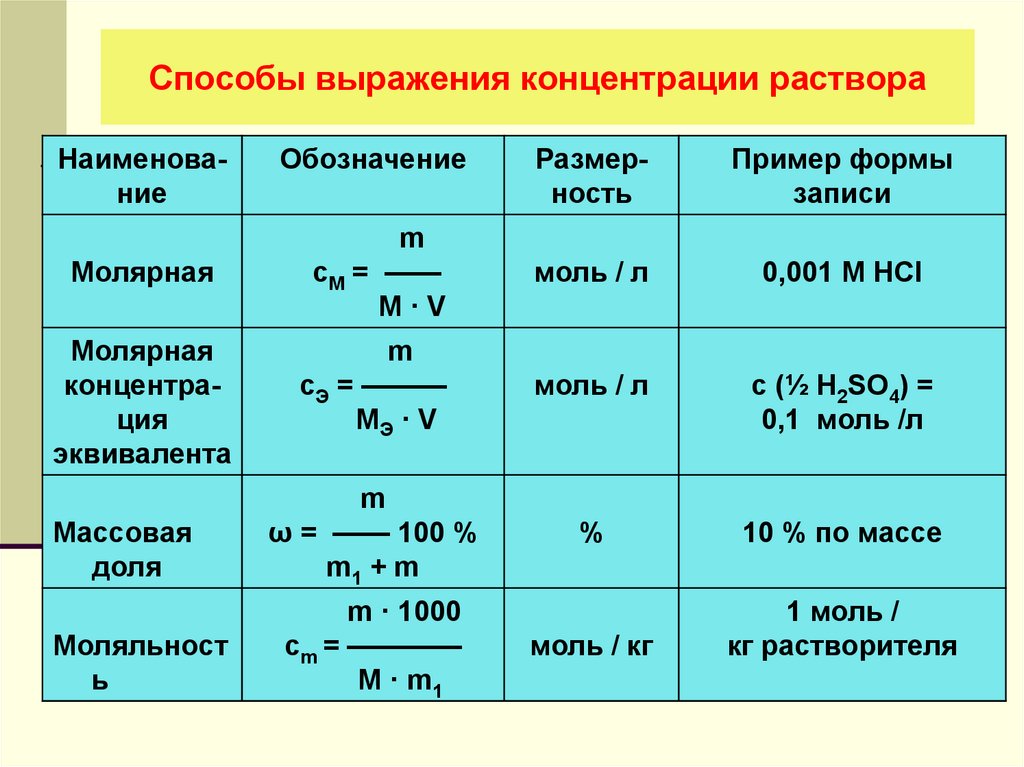 Выражается массовая доля в процентах или долях, как единица безразмерная.
Выражается массовая доля в процентах или долях, как единица безразмерная.
Если раствор имеет массу 200 г, в нем содержится 50 г растворенного вещества, то массовая доля последнего будет составлять 25% или 0,25 доли (50/200=0,25). Также можно рассчитать массовую долю растворителя. Для этого требуется выполнить такие действия: 200-50=150 г, а затем 150/200=0,75. Таким образом, массовая доля растворителя составит 75% или 0,75 долей.
Отсюда следует, что для расчета массовой доли веществ в составе раствора используется следующая формула: w(вещества) = m(вещества)/m(раствора). Зная массовую долю вещества, можно найти его массу по формуле: m(вещества) =w(вещества) х m(раствора).
Сумма массовых концентраций раствора (растворителя включительно) образует его плотность. Если химическое вещество чистое, массовая концентрация такая же, как и его плотность (масса/объем). Отсюда следует, что массовая концентрация компонента в смеси – это его плотность.
Регистрация на сайте
Регистрация на сайте — процедура, необходимая только партнерам компании.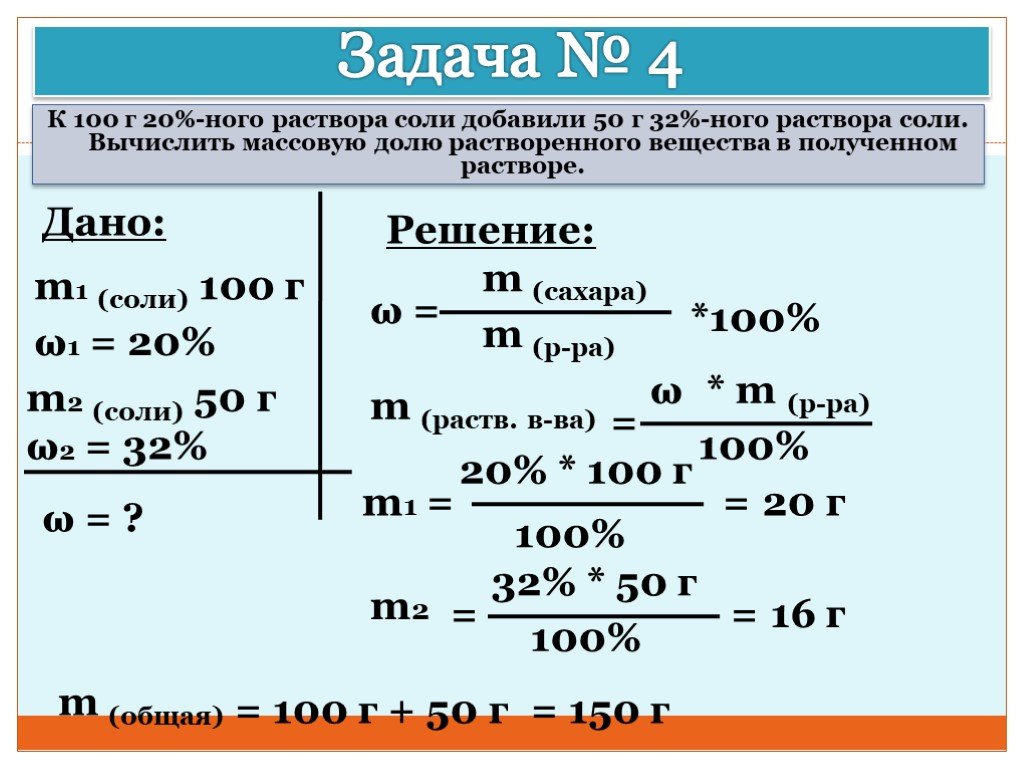
Зарегистрированным партнерам открывается доступ к закрытому разделу сайта — загрузки.
Ваша заявка
Ваша заявка
Ваша заявка
Видео-урок: Концентрация в процентах | Nagwa
Стенограмма видео
В этом видео мы узнаем, как выразить и вычислить процентную концентрацию раствора по его объему или массовое отношение. Давайте познакомимся с этой темой простая история.
Двое друзей ходят по магазинам, чтобы купить
мульча для сада и перья, чтобы набить самодельные подушки. Они кладут по одному большому мешку каждого в
корзина, почти заполняя ее. Один друг говорит: «Корзина
состоит из 50 процентов мульчи и 50 процентов пера, потому что каждый из них занимает
половину места в корзине». Другой друг, который толкает
корзина, говорит: «Я думаю, что корзина 95 процентов мульчи и пять процентов пера
потому что в тележке гораздо больше мульчи, чем килограммов перьев».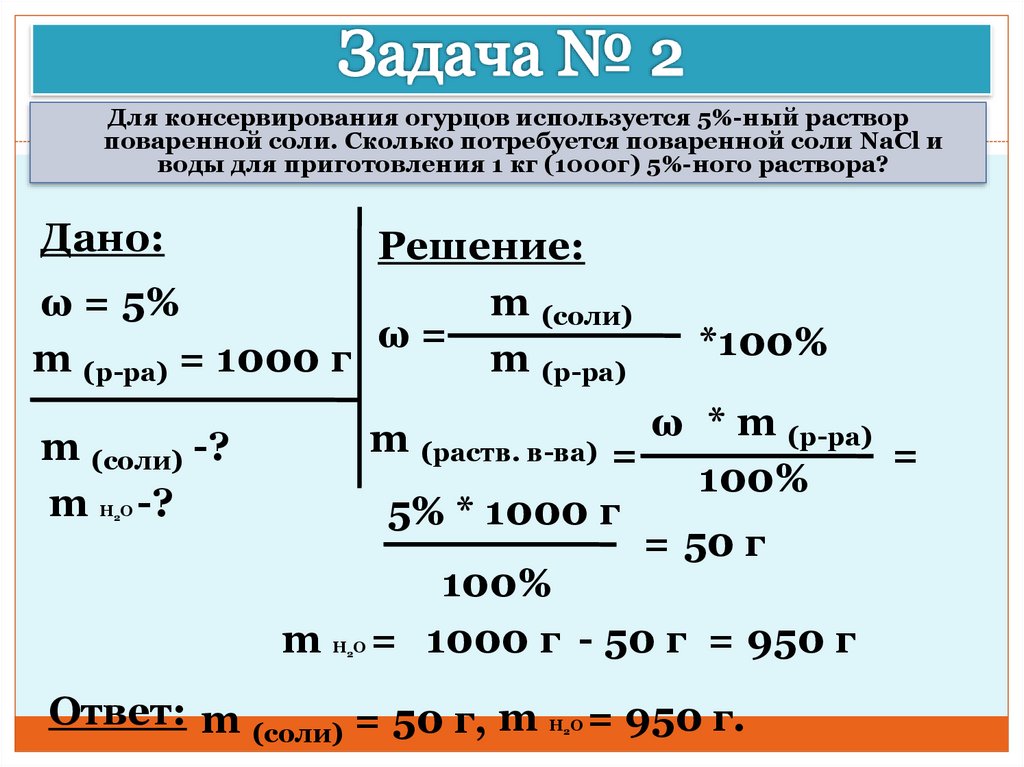
Ну, они оба. Эти друзья рассчитывают процентная концентрация корзины. Первый друг вычисляет процент по объему. Второй друг вычисляет процентная концентрация по массе. В химии мы обычно не разобраться с мульчей и перьями. Обычно мы применяем процент концентрации к количеству растворенного вещества, находящегося в растворе.
Пример процента для одного домохозяйства концентрацию можно найти на бутылке дезинфицирующего средства для рук. Если мы посмотрим на заднюю часть бутылки дезинфицирующего средства для рук, мы можем увидеть надпись: «Этиловый спирт, 70 процентов по объему». Что это значит? Ну, v/v означает, что это процентная концентрация указана по объему. Это означает, что из общего объем дезинфицирующего средства для рук в бутылке, 70 процентов объема составляет этил алкоголь.
Например, бутылочка ручной
дезинфицирующее средство, которое вы можете увидеть в ванной или на столе, будет стоить около 240
миллилитров дезинфицирующего средства для рук. Объем бутылки будет
указано на этикетке. Так как решение составляет 70 процентов
этилового спирта по объему, для приготовления этого раствора требуется количество этилового спирта
равно 70 процентам от общего объема бутылки. 70 процентов от 240 — это 168. Таким образом, компания использовала 168 миллилитров.
этилового спирта, чтобы сделать эту бутылку дезинфицирующего средства для рук.
Объем бутылки будет
указано на этикетке. Так как решение составляет 70 процентов
этилового спирта по объему, для приготовления этого раствора требуется количество этилового спирта
равно 70 процентам от общего объема бутылки. 70 процентов от 240 — это 168. Таким образом, компания использовала 168 миллилитров.
этилового спирта, чтобы сделать эту бутылку дезинфицирующего средства для рук.
Напоминаем, чтобы найти 70 процентов из 240 мы можем взять десятичную форму 70 процентов, 0,7, и умножить ее на 240, чтобы получить получаем 168. Остальные 72 миллилитра, часть дезинфицирующего средства для рук, которая не является этиловым спиртом, состоит из неактивных ингредиенты. К ним относятся наполнители, связующие и ароматы.
Еще один немного другой пример
процентную концентрацию можно найти на тюбике противозудного крема. Противозудный крем используется для клопов
укусы, сыпь и другие зуды. Его активным ингредиентом является
гидрокортизон, стероид.
Противозудный крем используется для клопов
укусы, сыпь и другие зуды. Его активным ингредиентом является
гидрокортизон, стероид.
Если мы посмотрим на заднюю часть тюбика противозудный крем, мы можем увидеть «Гидрокортизон, один процент м/м». м/м означает, что это процентная концентрация указана по массе. Другими словами, один процент масса крема в тубе — гидрокортизон. Небольшой тюбик крема от зуда, размером с маркер для сухого стирания, может иметь массу 30 грамм. Один процент от этой общей массы составляет гидрокортизон. В этом случае один процент от 30 грамм это 0,3 грамма. Итак, 0,3 грамма гидрокортизон в тюбике.
Чтобы выполнить этот расчет на
калькулятор, вы можете ввести 0,01 умножить на 30 равно 0,3. Остальные 29,7 граммов
Неактивные Ингридиенты. В большинстве своем эти неактивные
ингредиенты придают крему кремообразную текстуру, позволяя гидрокортизону проникать в кожу. наносится на кожу.
наносится на кожу.
Как мы видим, математика участие в этих двух ситуациях в основном одно и то же. Основное отличие состоит в том, можем ли мы используйте единицы для объема или единицы для массы. Мы узнаем больше о расчеты вокруг процентной концентрации в момент. Но сначала давайте определим пару ключевые термины.
В общем, мы говорим о
процентная концентрация растворенного вещества в растворе. В качестве простого примера рассмотрим
сахар, растворенный в воде, как мы определяем эти термины. Растворенное вещество – это вещество, которое
растворенный. В этом случае растворенным веществом является
сахар. Растворенное часто является твердым существом
добавляют в жидкость. Но это также может быть жидкость или
также добавляется газ. Растворитель – это вещество, которое
занимается растворением. В данном случае вода является
растворитель. И, наконец, решение
смесь растворенного вещества в растворителе. Смесь растворенного сахара
в воде образует водно-сахарный раствор.
В данном случае вода является
растворитель. И, наконец, решение
смесь растворенного вещества в растворителе. Смесь растворенного сахара
в воде образует водно-сахарный раствор.
Когда мы говорим о процентах концентрация растворенного вещества в растворе, важно знать, что это за растворенное вещество и какое решение. Но растворить и растворить может быть легко слова путать. Итак, вот удобная мнемоника устройство.
Представим на мгновение грабитель с сумкой с краденым. Когда прибудет полиция, ему может понадобиться спрятать свою сумку, чтобы сбежать. К счастью для него, он находит воздуховод рядом, поблизости. Итак, добыча грабителя идет в вентиляция Аналогично, в растворе растворенное вещество переходит в растворитель.
Когда мы знаем определения
После этих слов становится легче обсуждать расчеты, связанные с процентами. концентрация. Давайте посмотрим на некоторые из
расчеты, которые мы используем, когда говорим о процентной концентрации. Формула, которую мы будем использовать в качестве
основой для других наших формул является процентная концентрация по объему, равная
объем растворенного вещества разделить на объем раствора.
концентрация. Давайте посмотрим на некоторые из
расчеты, которые мы используем, когда говорим о процентной концентрации. Формула, которую мы будем использовать в качестве
основой для других наших формул является процентная концентрация по объему, равная
объем растворенного вещества разделить на объем раствора.
Мы также можем увидеть решение объем называется общим объемом. В качестве реального примера, если есть 300 миллилитров спирта в 500-миллилитровом растворе дезинфицирующего средства для рук, мы может рассчитать ответ 0,6, что означает, что дезинфицирующее средство для рук содержит 60% спирта. по объему.
Обратите внимание на три переменные
в этом уравнении: процентная концентрация, объем растворенного вещества и раствор
объем. В этом примере мы использовали известные
значения объема растворенного вещества и объема раствора для расчета неизвестного процента
концентрация. Но в других вопросах, если мы знаем
любые два из этих трех значений, мы можем использовать их для решения третьего неизвестного
стоимость. Например, если мы хотим решить
для неизвестного объема растворенного вещества при данной процентной концентрации и общем
объем, мы можем использовать формулу: объем растворенного вещества равен проценту концентрации, умноженному на
объем раствора.
Но в других вопросах, если мы знаем
любые два из этих трех значений, мы можем использовать их для решения третьего неизвестного
стоимость. Например, если мы хотим решить
для неизвестного объема растворенного вещества при данной процентной концентрации и общем
объем, мы можем использовать формулу: объем растворенного вещества равен проценту концентрации, умноженному на
объем раствора.
Мы могли бы использовать эту формулу, чтобы ответить вопрос типа сколько спирта будет в 700 миллилитровом растворе нашего 60 процентный спиртовой раствор. Следуя формуле, 60 процентов раз 700 миллилитров даст нам наш ответ. Этот ответ 420 миллилитров алкоголь.
Последняя формула — объем раствора
равен объему растворенного вещества, деленному на процентную концентрацию. Например, если мы хотим взять
1300 миллилитров спирта и из этих 1300 сделайте 65-процентный раствор. миллилитров, мы могли бы взять 1300 и разделить на 65 процентов или 0,65. Наш ответ: 2000 миллилитров или
двухлитровый раствор. Обратите внимание, что эти 2000 миллилитров
объем всего раствора, включая 1300 миллилитров спирта, которые мы
началось с.
миллилитров, мы могли бы взять 1300 и разделить на 65 процентов или 0,65. Наш ответ: 2000 миллилитров или
двухлитровый раствор. Обратите внимание, что эти 2000 миллилитров
объем всего раствора, включая 1300 миллилитров спирта, которые мы
началось с.
Если задать нам вопрос: «Сколько растворитель мы добавляем в спирт, чтобы получить этот раствор?», наш окончательный ответ не будет быть 2000. Вместо этого было бы 700 миллилитров растворителя нам нужно добавить к 1300 миллилитрам спирта, чтобы получить 2000 миллилитров в общем растворе.
Подводя итог, мы можем использовать это формула, составленная тремя различными способами, для определения процентной концентрации, объем растворенного вещества или объем раствора, когда нам даны два других переменные.
К счастью, расчеты
массы чрезвычайно похожи на расчеты по объему. Вместо использования объема растворенного вещества
и объем раствора, мы используем массу растворенного вещества и массу раствора. И вместо того, чтобы наши части находились в
объем, как миллилитры, они будут единицами массы, как граммы. Например, если мы используем 33 грамма
сахара для приготовления 330-граммового раствора лимонада, мы можем рассчитать ответ 0,1 или 10
процентов сахара по массе.
Вместо использования объема растворенного вещества
и объем раствора, мы используем массу растворенного вещества и массу раствора. И вместо того, чтобы наши части находились в
объем, как миллилитры, они будут единицами массы, как граммы. Например, если мы используем 33 грамма
сахара для приготовления 330-граммового раствора лимонада, мы можем рассчитать ответ 0,1 или 10
процентов сахара по массе.
Однократная замена объема массой снова получаем вторую формулу: масса растворенного вещества равна концентрации в процентах, умноженной на масса раствора. Если мы знаем массу раствора и процентной концентрации, скажем, 250-граммового раствора лимонада с пятипроцентным сахара, мы можем рассчитать массу растворенного вещества. Пять процентов от 250 — это 12,5. Итак, наш ответ означает, что есть 12,5 г сахара в этом растворе.
Последняя формула — масса раствора
равна массе растворенного вещества, деленной на процентную концентрацию. Допустим, на этот вопрос мы
хочу взять 54 грамма сахара и сделать из него шестипроцентный раствор лимонада. Какова будет масса конечного
решение?
Допустим, на этот вопрос мы
хочу взять 54 грамма сахара и сделать из него шестипроцентный раствор лимонада. Какова будет масса конечного
решение?
Мы можем взять 54 грамма сахара и разделить на шесть процентов. Наш ответ: 900 грамм. решение. Напоминаю, 900-грамм раствор включает исходные 54 грамма сахара. Таким образом, чтобы сделать это решение, мы бы нужно добавить 846 граммов растворителя, чтобы получить раствор массой 900 граммов в масса.
Как мы видим здесь, расчеты, связанные с процентной концентрацией, в основном одинаковы, когда расчет по объему или по массе. Нам просто нужно помнить о метки и единицы измерения, которые мы используем.
Другая проблема, которую мы можем
решить, что связано с процентной концентрацией, вычислить процент
концентрация нового раствора, который получается при смешивании двух растворов
все вместе. Например, мы могли бы начать с
два раствора дезинфицирующего средства для рук: один на 250 миллилитров, что составляет 70 процентов
спирта по объему, а другой — 300-миллилитровый раствор дезинфицирующего средства для рук,
60 процентов спирта по объему.
Например, мы могли бы начать с
два раствора дезинфицирующего средства для рук: один на 250 миллилитров, что составляет 70 процентов
спирта по объему, а другой — 300-миллилитровый раствор дезинфицирующего средства для рук,
60 процентов спирта по объему.
И нам может быть интересно узнать какова процентная концентрация смеси, когда мы добавляем эти два раствора все вместе. Давайте используем переменную 𝑥 для представляют собой процентную концентрацию смеси. Обратимся также к двум растворы добавляются к смеси как раствор A и раствор B.
Используя нашу формулу для расчета
процентная концентрация, мы знаем, что процентная концентрация по объему любого
раствор — это объем растворенного вещества, деленный на объем раствора. Если мы сможем найти эти два значения, мы
можно рассчитать процентную концентрацию смеси. Каков объем раствора
смесь?
Каков объем раствора
смесь?
Итак, смешиваем 250-миллилитровую раствор с 300-миллилитровым раствором. В итоге это даст нам раствор объемом 550 миллилитров. Для другой отсутствующей переменной в наша формула, каков растворенный объем смеси? Ну, мы находим это похожим но чуть более замысловатый способ. Объем растворенного вещества в смеси просто будет объем растворенного вещества в каждом из добавленных отдельных растворов все вместе.
Мы можем найти растворенный объем
решение, взяв объем и умножив его на процент
концентрация. Для раствора А 70 процентов от 250
миллилитров дает нам 175 миллилитров алкоголя. Аналогично для раствора B 60
проценты, умноженные на 300, дают нам 180 миллилитров в качестве объема растворенного вещества. Складываем эти два числа вместе
дает нам объем растворенного вещества для смеси, 355 миллилитров.
Поскольку имеется 355 миллилитров спирта в растворе объемом 550 миллилитров, мы можем разделить 355 миллилитров на 550 миллилитров, чтобы получить процентную концентрацию. Наш окончательный ответ: 64,5. процент. Обратите внимание, что наш ответ, 64,5 процента, находится между двумя исходными концентрациями, с которых мы начали, 60 процентов и 70 процентов. Если рассчитанный процент концентрация смеси была каким-то образом выше, чем более высокая концентрация или ниже, чем более низкая концентрация, мы бы знали, что допустили ошибку в нашем расчеты где-то по пути. Таким образом, при смешивании этих двух растворов процентная концентрация смеси составляет 64,5 процента.
Теперь, когда мы узнали о
процентная концентрация, давайте рассмотрим некоторые ключевые моменты видео. Процентная концентрация указывает
процент растворенного вещества в растворе. Процентная концентрация может быть
концентрация по объему или по массе. Например, 10 процентов по объему означает
что 10% объема всего раствора составляет объем растворенного вещества. С другой стороны, один процент м/м
означает, что один процент массы раствора составляет массу растворенного вещества.
Процентная концентрация может быть
концентрация по объему или по массе. Например, 10 процентов по объему означает
что 10% объема всего раствора составляет объем растворенного вещества. С другой стороны, один процент м/м
означает, что один процент массы раствора составляет массу растворенного вещества.
Формула для расчета процентов
концентрация в процентах, концентрация равна объему растворенного вещества, деленному на раствор
объем, если мы рассчитываем его по объему, или процентная концентрация равна растворенному веществу
массу разделить на массу раствора, чтобы вычислить ее по массе. Мы можем использовать эти формулы или
их измененные версии для решения процентной концентрации, объема растворенного вещества
или масса, или объем раствора, или масса, если заданы два других. И мы можем рассчитать процент
концентрацию смеси двух веществ, найдя общий объем растворенного вещества или
масса и общий объем раствора или масса, а затем их деление.
Процентные решения | Химия для неспециалистов |
Цели обучения
- Определение концентрации.
- Выполнение расчетов с использованием массовых и объемных растворов.
Сколько слишком много?
Изображение FirstPrinciples/Wikimedia Commons.
Существуют культуры, в которых нет числа больше трех. Все, что больше этого, просто упоминается как «много» или «много». Мы понимаем, насколько ограничена эта форма расчета, но делаем то же самое. Существует несколько способов количественного выражения количества растворенного вещества в растворе. концентрация раствора является мерой количества растворенного вещества, растворенного в данном количестве растворителя или раствора. Концентрированный раствор содержит относительно большое количество растворенного вещества. Разбавленный раствор содержит относительно небольшое количество растворенного вещества. Однако эти термины расплывчаты, и нам нужно уметь выражать концентрацию числами.
Однако эти термины расплывчаты, и нам нужно уметь выражать концентрацию числами.
Процентные растворы
Одним из способов описания концентрации раствора является процент растворенного вещества в растворителе. Процент можно дополнительно определить одним из двух способов: (1) отношением массы растворенного вещества к массе раствора или (2) отношением объема растворенного вещества к объему раствора.
Массовые проценты
Когда растворенное вещество в растворе является твердым, удобным способом выражения концентрации является массовый процент, который представляет собой количество граммов растворенного вещества на 100 г раствора.
Предположим, что раствор был приготовлен путем растворения 25,0 г сахара в 100 г воды. Процент по массе можно рассчитать по формуле:
Иногда вам может понадобиться составить определенную массу раствора с заданным процентом по массе и рассчитать, какую массу растворителя использовать. Например, нужно приготовить 3000 г 5% раствора поваренной соли. Вы можете переставить и найти массу растворенного вещества.
Вы можете переставить и найти массу растворенного вещества.
Вам нужно взвесить 150 г NaCl и добавить его в 2850 г воды. Обратите внимание, что необходимо было вычесть массу NaCl (150 г) из массы раствора (3000 г), чтобы вычислить массу воды, которую нужно было добавить.
Объемный процент
Процентное содержание растворенного вещества в растворе легче определить по объему, когда растворяемое вещество и растворитель оба являются жидкостями. Объем растворенного вещества, разделенный на объем раствора, выраженный в процентах, дает объемный процент раствора. Если раствор готовится путем добавления 40 мл этанола к 20 мл воды, процент по объему равен:
Часто на этикетках пищевых продуктов и лекарств количество ингредиентов указывается в процентах (см. рис. ниже).
Резюме
- Описаны методики расчета процентной массовой и объемной концентрации раствора.
Практика
Прочитайте страницы 1-3 материала по ссылке ниже и выполните задачи, связанные с этим разделом.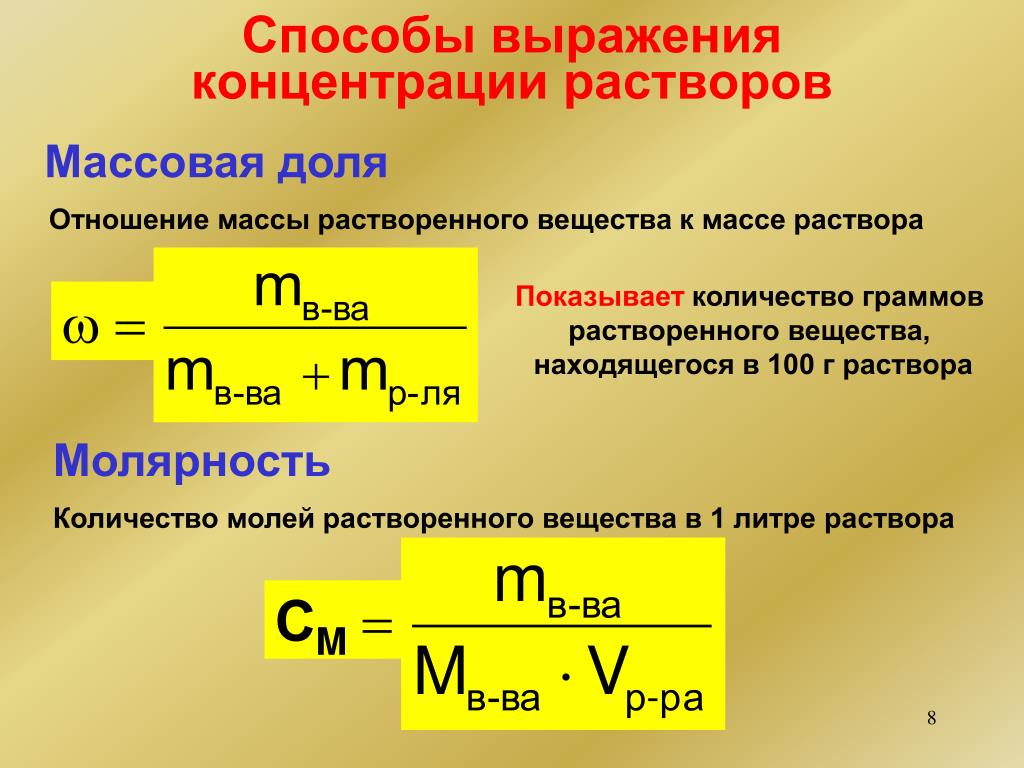 Поработайте над задачами, прежде чем проверять ответы.
Поработайте над задачами, прежде чем проверять ответы.
http://go.hrw.com/resources/go_sc/mc/HUGPS163.PDF
Обзор
- Почему термины «концентрированный» и «разбавленный» не очень полезны?
- В каких случаях следует использовать вычисления объемных процентов?
- Почему вы вычитаете массу растворенного вещества из требуемой общей массы при расчете массовых процентов?
Глоссарий
- концентрированный: Раствор, содержащий относительно большое количество растворенного вещества.
- концентрация: Мера количества растворенного вещества, растворенного в данном количестве растворителя или раствора.
- разбавленный: Раствор, содержащий относительно небольшое количество растворенного вещества.
Лицензии и атрибуты
Лицензионный контент CC, ранее опубликованный
- Химические понятия Средний. Автор: : Calbreath, Baxter, et al.


 Площадь круга
Площадь круга