Лучший ответ по мнению автора | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Посмотреть всех экспертов из раздела Учеба и наука > Химия
| Похожие вопросы |
Решено
Реакция изомеризации пентана.
Во сколько раз изменится скорость…
Найдите объем этилена (н. у.), полученного реакцией дегидрации 230 мл 95%-ого этилового спирта(плотность 0,8 г/мл)
Решено
Ch3Br-CHBr-Ch4+Zn
Для полного восстановления 11,6 г одного из оксидов железа…
Пользуйтесь нашим приложением
Институт неорганической химии СО РАН
Защиты
Брылева Ю.А. (26)
Кабанова Н.А. (17)
Мартынова С.А. (21)
Жданов А.А. (17)
ПОчтарь А.А. (24)
Коротаев Е.В. (19)
Федоренко А.Д. (19)
Федоренко А.Д. (3)
Коротаев Е.В. (4)
Автореферат Чеплаковой А.М. от 24.01.2020г.
Скачать
Уведомление о замене официального оппонента
Скачать
Автореферат Савков Б. Ю. от 28.11.2017г.
Ю. от 28.11.2017г.
Скачать
Автореферат Абрамова П.А. от 4.06.2019г.
Скачать
Автореферат Барсуковой М.О. от 28.03.2018г.
Скачать
Автореферат Баскаковой К.И. от 13.12 2022 г.
Скачать
Автореферат Берёзина А.С. от 16.02.2018г.
Скачать
Автореферат Брылева К.А. от 17.01.2018г.
Скачать
Автореферат Бурлака П.В. от 14.12.2022 г.
Скачать
Автореферат Бушуева М.Б. от 21.02.2019г.
Скачать
Автореферат ВОЛЖЕНИНА А.В. от 10.10.2019г.
Скачать
Автореферат Галлямова М.Р. от 18.10.2017
Скачать
Автореферат Галлямова М.Р. от 18.10.2017г.
Скачать
Автореферат Городецкого Д.В. от 11.01.2019г.
Скачать
Автореферат Колодина А.Н. от 14.03.2018г.
Скачать
Автореферат Колодина А.Н. от 15.03.2018г.
Скачать
Автореферат Колодина Алексея Никитича от 15.03.2018г.
Скачать
Автореферат Купцова А.В. от 19.10.2018г.
Скачать
Автореферат Ластовка А. В. от 24.01.2020г.
В. от 24.01.2020г.
Скачать
Автореферат Лесникова М.К. от 19.04.2019г.
Скачать
Автореферат Литвиновой Ю.М. от 18.10.2018г.
Скачать
Автореферат Лобяка Е.В. от 11.01.2019г.
Скачать
Автореферат Михайлова А.А. от 14.02.2020г.
Скачать
Автореферат Муравьевой В.К. от 27.09.2019г.
Скачать
Автореферат Огиенко Д.С. от 14.04.2018г.
Скачать
Автореферат от 07.04.2017г.
Скачать
Автореферат от 08.04.2016
Скачать
Автореферат от 13.09.2017г.
Скачать
Автореферат от 20.10.2016г.
Скачать
Автореферат от 24.08.2016
Скачать
Автореферат от 24.08.2016г.
Скачать
Автореферат от 28.09.2016г.
Скачать
Автореферат от 29.06.2017г
Скачать
Автореферат от 29.06.2017г
Скачать
Автореферат Пирязева Д.А. от 23.01.2019г.
Скачать
Автореферат Полюхова Д.М. от 01.04.2021г.
Скачать
Автореферат Порываева А.С. от 01.04.2021г.
Скачать
Автореферат Ромадиной Е.И. от 05.10.2022 г.
Скачать
Автореферат Сапьяника А.А. от 28.03.2018г.
Скачать
Автореферат Семериковой А.Н. от 23.01.2019г.
Скачать
Автореферат Сотникова А.В. от 04.02.2019г.
Скачать
Автореферат Сыроквашина М.М. от 10.06.2022г.
Скачать
Автореферат Топчиян П.А. от 14.12.2022 г.
Скачать
Автореферат Трифонова В.А. от 18.10.2017
Скачать
Автореферат Фоменко Я.С. от 17.02.2020г.
Скачать
Автореферат Шамшурина М.В. от 12.10.2022
Скачать
Автореферат Шестопалова М.А. от 19.03.2020г.
Скачать
Диссертация в виде научного доклада Аксенова С.М. от 13.12.2022 г.
Скачать
Закллючение диссертационного совета от 19.02.2020г.
Скачать
Заключение диссертационнного совета от 29.01.2020г.
Скачать
Powered by Phoca Download
Высокоселективное преобразование CO2 в C2H6 на модифицированном графеном хлорофилле Cu посредством многоэлектронного процесса для искусственного фотосинтеза
Высокоселективное преобразование CO
2 в C 2 H 6 на модифицированном графеном хлорофилле Cu посредством многоэлектронного процесса для искусственного фотосинтеза†Тонгшунь Ву, * и Ченг Чжу, б Дунсюэ Хан, ак Чжэньхуэй Кан * б и Ли Ню ак
Принадлежности автора
* Соответствующие авторы
и Центр передовых аналитических наук при Школе химии и химического машиностроения Университета Гуанчжоу, Гуанчжоу 510006, КНР
 edu.cn
edu.cn б Ключевая лаборатория Цзянсу по углеродным функциональным материалам и устройствам, Институт функциональных нано- и мягких материалов (FUNSOM), Сучжоуский университет, 199 Ren’ai Road, Сучжоу, Цзянсу, КНР
Электронная почта: [email protected]
с Государственная ключевая лаборатория электроаналитической химии, c/o Инженерная лаборатория современных аналитических методов, Чанчуньский институт прикладной химии Китайской академии наук, Чанчунь 130022, Цзилинь, Китай
Аннотация
rsc.org/schema/rscart38″> Искусственный фотосинтез является многообещающей стратегией преобразования углекислого газа в углеводородное топливо с помощью солнечной энергии, поскольку он чист, экономичен и безвреден для окружающей среды. Здесь мы разработали селективный и стабильный фотокатализатор для фотокаталитического восстановления CO 2 в C 2 H 6 посредством многоэлектронного пути переноса без внешних жертвенных реагентов. Основной компонент этого составного катализатора был извлечен из экскрементов тутового шелкопряда и модифицирован для получения хлорофилла Cu (Chl-Cu), который содержал порфириновую структуру в качестве антенны для поглощения света и катион Cu в качестве активного центра. Мы обнаружили, что C 2 Углеводороды, такие как C 2 H 2 , C 2 H 4 и C 2 9004 HA 70037. 7 7003777. 777. 777. 77777. 677 7003777777. 67 7. 67677 70037777777. 667 7. 6777777. 667. на хлорофилле-а/графене. После замены катионов Mg 2+ на катионы Cu 2+ в центре порфирина и модификации графеном остается только C 2 H
7 7003777. 777. 777. 77777. 677 7003777777. 67 7. 67677 70037777777. 667 7. 6777777. 667. на хлорофилле-а/графене. После замены катионов Mg 2+ на катионы Cu 2+ в центре порфирина и модификации графеном остается только C 2 H 4 9
0 был обнаружен в 18-часовой реакции. Этот фотокатализатор представил выдающуюся активность и селективность для фотокаталитического CO 2 Снижение (CO 2 RR) с C 2 H 6 . 2 h -1 при облучении видимым светом и кажущейся квантовой эффективностью 1,26% при 420 нм. В этой системе порфириновые кольца возбуждались светом для образования электронно-дырочных пар. Фотоиндуцированные дырки окисляли воду с образованием кислорода, в то время как графен работал как адсорбционный центр и акцептор электронов для CO 9 . 0057 2 сокращение.
0057 2 сокращение.Рассчитайте приблизительную теплоту сгорания этана (C2H6) в …
Проблема
Соответствующее решение
7 м
Воспроизведите видео:
приветствую всех. Нам нужно оценить теплоту сгорания и килл джулей для пропана C три H восемь. Использование падающих ассоциативных энергий связи. Итак, нам нужно начать с записи реакции горения пропана. И мы хотим напомнить, что в реакциях горения участвует наш реагент, которым в данном случае является газообразный пропан, реагирующий с газообразным кислородом, а нашими продуктами всегда будут углекислый газ и вода. И извините, вода здесь просто H 20. Итак, наш следующий шаг — сбалансировать эту реакцию. И, основываясь на атомах в обеих частях нашего уравнения, мы должны добавить коэффициент пять перед нашим кислородом, коэффициент четыре перед водой и коэффициент три перед углекислым газом, чтобы иметь уравновешенную реакцию.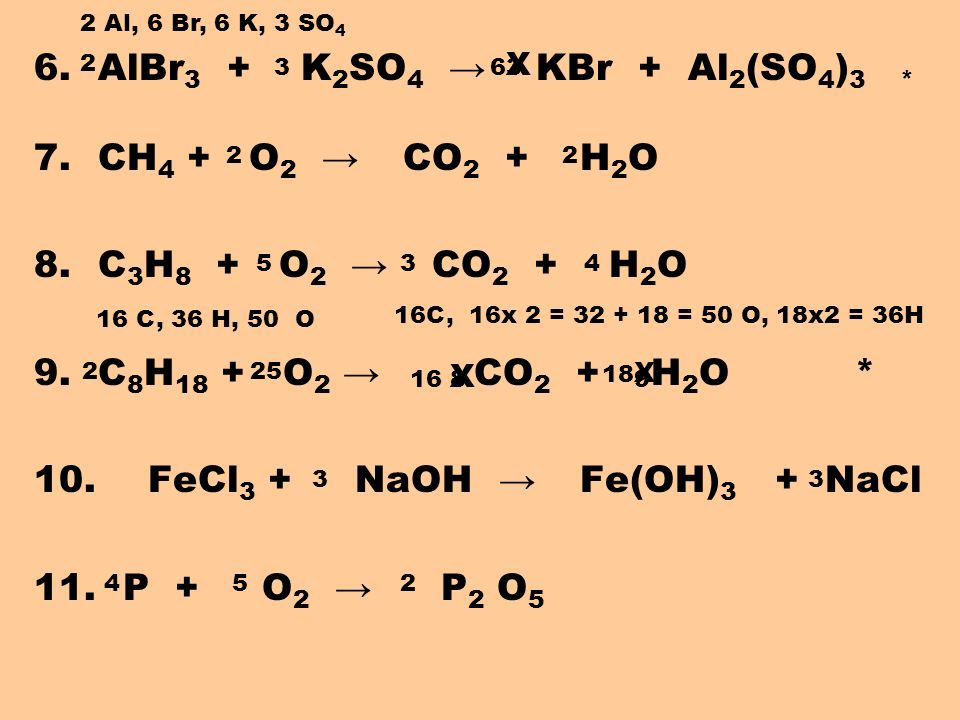 Теперь, когда у нас есть отскочившая реакция, наш следующий эпизод со структурами наших реагентов и продуктов. Итак, начиная с пропана, мы хотим вспомнить, что у нас есть три атома углерода, где у нас есть в общей сложности восемь атомов водорода, окружающих эти атомы углерода, так что, заполняя, мы просто соединим наши атомы здесь. И это наша структура пропана, где мы можем подсчитать, что у нас есть в общей сложности восемь наших углерод-водородных одинарных связей для пропана, и, извините, нам не хватает связи между нашими атомами углерода. Таким образом, у нас есть в общей сложности две наши углерод-углеродные одинарные связи. Теперь рисуя нашу структуру кислорода, мы имеем два атома кислорода, связанных друг с другом, где эти атомы кислорода связаны двойной связью, а наши атомы кислорода имеют два набора неподеленных пар друг с другом. Потому что мы понимаем, что кислород, основываясь на его положении в периодической таблице, расположен в группе шесть А и должен иметь шесть валентных электронов там, где мы должны в этих ковалиновых связях, а затем две другие как неподеленные пары, как мы нарисовали.
Теперь, когда у нас есть отскочившая реакция, наш следующий эпизод со структурами наших реагентов и продуктов. Итак, начиная с пропана, мы хотим вспомнить, что у нас есть три атома углерода, где у нас есть в общей сложности восемь атомов водорода, окружающих эти атомы углерода, так что, заполняя, мы просто соединим наши атомы здесь. И это наша структура пропана, где мы можем подсчитать, что у нас есть в общей сложности восемь наших углерод-водородных одинарных связей для пропана, и, извините, нам не хватает связи между нашими атомами углерода. Таким образом, у нас есть в общей сложности две наши углерод-углеродные одинарные связи. Теперь рисуя нашу структуру кислорода, мы имеем два атома кислорода, связанных друг с другом, где эти атомы кислорода связаны двойной связью, а наши атомы кислорода имеют два набора неподеленных пар друг с другом. Потому что мы понимаем, что кислород, основываясь на его положении в периодической таблице, расположен в группе шесть А и должен иметь шесть валентных электронов там, где мы должны в этих ковалиновых связях, а затем две другие как неподеленные пары, как мы нарисовали. А теперь для наши продукты, рисуя нашу структуру углекислого газа, у нас есть углерод в центре, окруженный двумя атомами кислорода, где у нас есть две связи с углеродом, чтобы дать углероду четыре связи, и затем наши атомы кислорода все еще имеют эти две неподеленные пары на каждом из этих атомы кислорода. Как мы заявили, у нас есть три моля углекислого газа и пять молей кислорода, а это означает, что у нас есть в общей сложности пять наших кислородных связей, связанных двойными связями с кислородом, и три наших, извините поправку, это будет шесть, потому что у нас есть два набора. наших двойных связей кислорода и углерода здесь, так что шесть наших двойных связей кислорода с углеродом. И, наконец, у нас есть второй продукт, вода. Мы знаем, что наша молекула воды — это просто кислород, связанный с двумя атомами водорода одинарными связями, где кислород имеет два набора неподеленных пар. И поскольку у нас есть четыре моля воды в качестве продукта, у нас будет в общей сложности восемь наших кислородно-водородных одинарных связей.
А теперь для наши продукты, рисуя нашу структуру углекислого газа, у нас есть углерод в центре, окруженный двумя атомами кислорода, где у нас есть две связи с углеродом, чтобы дать углероду четыре связи, и затем наши атомы кислорода все еще имеют эти две неподеленные пары на каждом из этих атомы кислорода. Как мы заявили, у нас есть три моля углекислого газа и пять молей кислорода, а это означает, что у нас есть в общей сложности пять наших кислородных связей, связанных двойными связями с кислородом, и три наших, извините поправку, это будет шесть, потому что у нас есть два набора. наших двойных связей кислорода и углерода здесь, так что шесть наших двойных связей кислорода с углеродом. И, наконец, у нас есть второй продукт, вода. Мы знаем, что наша молекула воды — это просто кислород, связанный с двумя атомами водорода одинарными связями, где кислород имеет два набора неподеленных пар. И поскольку у нас есть четыре моля воды в качестве продукта, у нас будет в общей сложности восемь наших кислородно-водородных одинарных связей. Теперь, когда мы перечислили наши структуры и определили количество различных типов связей для наших реагентов в нашей реакции. Теперь мы собираемся определить нашу теплоту сгорания пропана, найдя изменение энтропии нашей реакции, которое, как мы помним, есть дельта H. И мы признаем, что это может быть связано с энергией ассоциации связей наших реагентов, вычтенной из энергия ассоциации связей наших продуктовых связей. Таким образом, упрощая это, мы можем сказать, что наша энтропия нашей реакции равна тому, где мы начинаем наши скобки. У нас есть два моля, умноженные на наши энергии ассоциации наших углерод-углеродных одинарных связей, которые добавляются к восьми молям нашего или извините, восемь молей, умноженные на наши энергии диссоциации связей наших углерод-водородных одинарных связей, затем добавленные к пяти молям, умноженные на энергии диссоциации связи нашей кислородно-кислородной двойной связи. Мы закрыли бы скобки для энергии связи наших реагирующих связей. А теперь начните с вычитания энергий диссоциации наших связей продукта, которые мы будем использовать в фиолетовом цвете.
Теперь, когда мы перечислили наши структуры и определили количество различных типов связей для наших реагентов в нашей реакции. Теперь мы собираемся определить нашу теплоту сгорания пропана, найдя изменение энтропии нашей реакции, которое, как мы помним, есть дельта H. И мы признаем, что это может быть связано с энергией ассоциации связей наших реагентов, вычтенной из энергия ассоциации связей наших продуктовых связей. Таким образом, упрощая это, мы можем сказать, что наша энтропия нашей реакции равна тому, где мы начинаем наши скобки. У нас есть два моля, умноженные на наши энергии ассоциации наших углерод-углеродных одинарных связей, которые добавляются к восьми молям нашего или извините, восемь молей, умноженные на наши энергии диссоциации связей наших углерод-водородных одинарных связей, затем добавленные к пяти молям, умноженные на энергии диссоциации связи нашей кислородно-кислородной двойной связи. Мы закрыли бы скобки для энергии связи наших реагирующих связей. А теперь начните с вычитания энергий диссоциации наших связей продукта, которые мы будем использовать в фиолетовом цвете.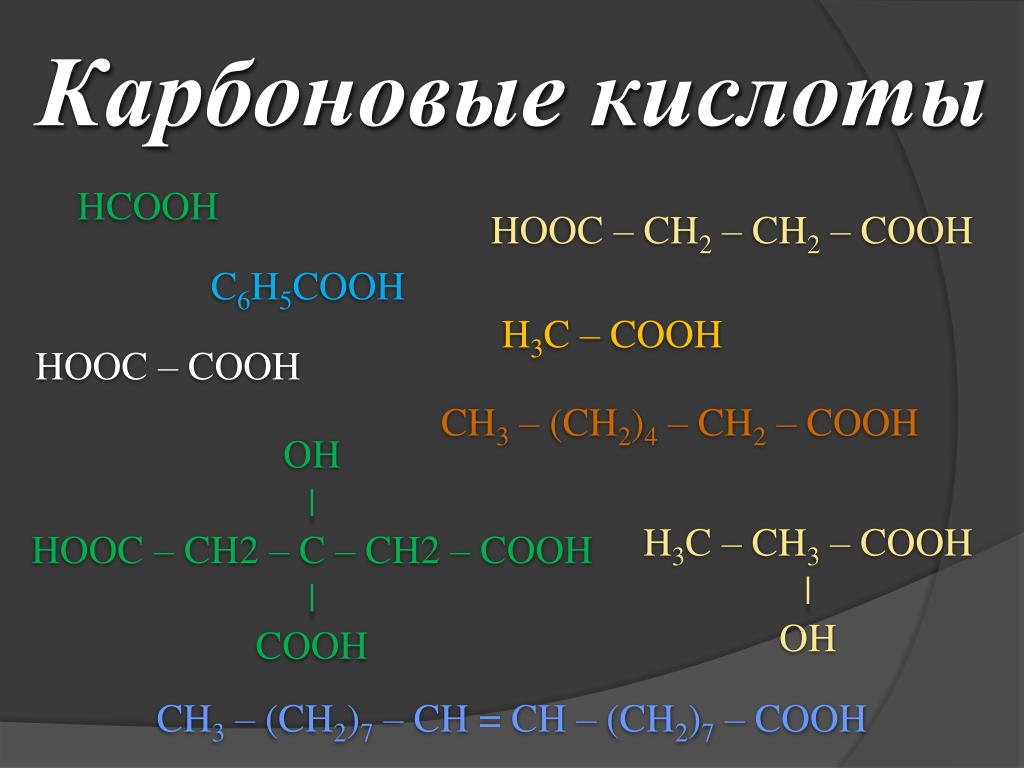 Итак, мы начинаем наши скобки, и у нас есть шесть молей, умноженные на энергию диссоциации связи наших двойных связей углерода и кислорода, добавленных к восьми молям, умноженных на энергию диссоциации связи наших одинарных связей кислорода и водорода, и что мы можем закрыть наши скобки для связи энергия ассоциации наших продуктовых связей. И давайте проясним это, это конец этой скобки. Итак, теперь давайте просто подставим наши значения, полученные из диаграммы, в нашу подсказку. Таким образом, мы можем сказать, что наша энтропия нашей реакции равна началу наших скобок. Два моля, умноженные на энергию связи одинарной углерод-углеродной связи, которая из подсказки дает нам 350 кг джоулей на моль. Затем это добавляется к восьми молям, умноженным на энергии диссоциации наших углерод-водородных одинарных связей, указанные в подсказке как 410 кг джоулей на моль. И затем, добавленный к этому, мы имеем пять молей, умноженных на энергию связи нашего кислорода, двойную связь кислорода, указанную в подсказке как 49.
Итак, мы начинаем наши скобки, и у нас есть шесть молей, умноженные на энергию диссоциации связи наших двойных связей углерода и кислорода, добавленных к восьми молям, умноженных на энергию диссоциации связи наших одинарных связей кислорода и водорода, и что мы можем закрыть наши скобки для связи энергия ассоциации наших продуктовых связей. И давайте проясним это, это конец этой скобки. Итак, теперь давайте просто подставим наши значения, полученные из диаграммы, в нашу подсказку. Таким образом, мы можем сказать, что наша энтропия нашей реакции равна началу наших скобок. Два моля, умноженные на энергию связи одинарной углерод-углеродной связи, которая из подсказки дает нам 350 кг джоулей на моль. Затем это добавляется к восьми молям, умноженным на энергии диссоциации наших углерод-водородных одинарных связей, указанные в подсказке как 410 кг джоулей на моль. И затем, добавленный к этому, мы имеем пять молей, умноженных на энергию связи нашего кислорода, двойную связь кислорода, указанную в подсказке как 49. 8 кг джоулей на моль. Итак, закройте наши скобки и начните с вычитания из них энергий диссоциации связей наших продуктов. У нас есть шесть молей, умноженных на энергию связи нашей двойной связи углерода и кислорода, указанную в подсказке как 804 кг на моль. Который затем добавляется к восьми молям, умноженным на энергию диссоциации связи нашего кислорода, водородных одинарных связей, указанных в подсказке, поскольку извините, мы должны просто убить джоулей на моль. Итак, мы можем закрыть наши скобки. И теперь мы хотим упростить обе скобки, чтобы теперь мы могли иметь в нашей следующей строке, что наша энтропия нашей реакции равна энергии нашей связи связи нашего реагента. Мы должны упростить, чтобы отменить все наши единицы молей. И мы останемся с килограммами драгоценностей. А теперь вычтем это из энергий диссоциации связи наших продуктов, что упростит до значения 8504 кг драгоценных камней. Итак, взяв разницу между этими двумя значениями, мы обнаружим, что наша энтропия нашей реакции равна значению отрицательного 2034 орудия убийства.
8 кг джоулей на моль. Итак, закройте наши скобки и начните с вычитания из них энергий диссоциации связей наших продуктов. У нас есть шесть молей, умноженных на энергию связи нашей двойной связи углерода и кислорода, указанную в подсказке как 804 кг на моль. Который затем добавляется к восьми молям, умноженным на энергию диссоциации связи нашего кислорода, водородных одинарных связей, указанных в подсказке, поскольку извините, мы должны просто убить джоулей на моль. Итак, мы можем закрыть наши скобки. И теперь мы хотим упростить обе скобки, чтобы теперь мы могли иметь в нашей следующей строке, что наша энтропия нашей реакции равна энергии нашей связи связи нашего реагента. Мы должны упростить, чтобы отменить все наши единицы молей. И мы останемся с килограммами драгоценностей. А теперь вычтем это из энергий диссоциации связи наших продуктов, что упростит до значения 8504 кг драгоценных камней. Итак, взяв разницу между этими двумя значениями, мы обнаружим, что наша энтропия нашей реакции равна значению отрицательного 2034 орудия убийства.

 09.14
09.14