Как вычислить удельную теплоемкость: 6 шагов
‘).insertAfter(«#intro»),$(‘
‘).insertBefore(«.youmightalsolike»),$(‘
‘).insertBefore(«#quiz_container»),$(‘
‘).insertBefore(«#newsletter_block_main»),ia(!0),b=document.getElementsByClassName(«scrolltomarker»),a=0;a
В этой статье:
Освойте основы
Вычислите удельную теплоемкость
Дополнительные статьи
Источники
Удельная теплоемкость — это энергия, необходимая для того, чтобы поднять температуру одного грамма чистого вещества на один градус Цельсия. Удельная теплоемкость вещества зависит от его химического состава и агрегатного состояния. Открытие удельной теплоемкости подстегнуло развитие термодинамики, науки о переходах энергии, касающейся теплоты и работы системы. Удельная теплоемкость и термодинамика широко используются в химии, ядерной инженерии и аэродинамики, а также в повседневной жизни для радиаторов и систем охлаждения автомобилей.
Шаги
1
Ознакомьтесь с величинами, которые используются для расчета удельной теплоемкости. Очень важно знать величины, которые используются для расчета удельной теплоемкости. Вы должны знать, как выглядит символ каждой величины, и понимать, что он означает. Далее приведены величины, которые обычно используются в выражении для расчета удельной теплоемкости вещества:
- Дельта, или символ «Δ», подразумевает изменение величины.
- Например, если ваша первая температура (T1) составляет 150 ºC, а вторая (T2) составляет 20 ºC, тогда ΔT, или изменение температуры, составит 150 ºC — 20 ºC = 130 ºC.
- Масса образца обозначается буквой «m».
- Количество теплоты обозначается буквой «Q». Единица измерения количества теплоты — «Дж», или Джоуль.
- «T» — это температура вещества.
- Удельная теплоемкость обозначается буквой «Cp».

- Дельта, или символ «Δ», подразумевает изменение величины.
2
Освойте выражение для определения удельной теплоемкости. Ознакомившись с величинами, которые используются для вычисления удельной теплоемкости, вы должны выучить уравнение для определения удельной теплоемкости вещества. Формула имеет вид: Cp = Q/mΔT.
- Вы можете оперировать этой формулой, если хотите узнать изменение количества теплоты вместо удельной теплоемкости. Вот как это будет выглядеть:
- ΔQ = mCpΔT
Реклама
- Вы можете оперировать этой формулой, если хотите узнать изменение количества теплоты вместо удельной теплоемкости. Вот как это будет выглядеть:
1
Изучите формулу. Сначала вам нужно изучить выражение для того, чтобы понять, что вам нужно сделать, чтобы найти удельную теплоемкость. Давайте рассмотрим следующую задачу:
2
Запишите известные и неизвестные факторы.
 Разобравшись с задачей, вы можете записать все известные и неизвестные переменные, чтобы лучше понять, с чем вы имеете дело. Вот как это делается:
Разобравшись с задачей, вы можете записать все известные и неизвестные переменные, чтобы лучше понять, с чем вы имеете дело. Вот как это делается:- m = 350 г
- Q = 34 700 Дж
- ΔT = 173 ºC — 22 ºC = 151 ºC
- Cp = неизвестно
3
Подставьте неизвестные факторы в уравнение. Известны все значения за исключением «Cpc», поэтому необходимо подставить в исходное уравнение все остальные факторы и найти «C p». Делать это нужно так:
- Исходное уравнение: Cp = Q/mΔT
- c = 34 700 Дж/(350 г x 151 ºC)
4
Найдите ответ. Теперь, после того как вы подставили известные величины в выражение, вам осталось выполнить несколько простейших арифметических действий, чтобы узнать ответ. Удельная теплоемкость — окончательный ответ — составляет 0,65657521286 Дж/(г x ºC).
- Cp = 34,700 Дж/(350 г x 151 ºC)
- Cp = 34,700 Дж/(52850 г x ºC)
- Cp = 0,65657521286 Дж/(г x ºC)
Реклама
Советы
- Металл нагревается быстрее воды из-за низкой удельной теплоемкости.

- При нахождении удельной теплоемкости сокращайте единицы измерения тогда, когда это возможно.
- Удельную теплоемкость многих материалов можно найти в интернете для проверки вашего ответа.
- Иногда для изучения процессе теплопередачи в процессе физических или химических превращений может использоваться калориметр.
- Изменение температуры при прочих равных условиях значительнее для материалов с низкой удельной теплоемкостью.
- Системная единица СИ (Международная система единиц измерения) удельной теплоемкости — джоуль на градус Цельсия на грамм. В странах с британской системой мер она измеряется в калориях на градус Фаренгейта на фунт.
- Изучите формулу расчета удельной теплоемкости пищевых продуктов Cp = 4,180 x w + 1,711 x p + 1,928 x f + 1,547 x c + 0,908 x a — это уравнение для нахождения удельной теплоемкости, где «w» — процентное содержание воды в продукте, «p» — процентное содержание белков, «f» — процентное содержание жиров, «c» — процентное содержание углеводов и «a» — процентное содержание неорганических компонентов.
 Уравнение учитывает массовую долю (x) всех твердых веществ, которые составляют пищу. Расчет удельной теплоемкости приведен в кДж/(кг х K).
Уравнение учитывает массовую долю (x) всех твердых веществ, которые составляют пищу. Расчет удельной теплоемкости приведен в кДж/(кг х K).
Реклама
Источники
- http://www.merriam-webster.com/dictionary/specific%2Bheat
- http://www.grc.nasa.gov/WWW/K-12/airplane/specheat.html
- http://www.chemteam.info/Thermochem/Determine-Specific-Heat.html
Об этой статье
На других языках
Как вычислить удельную теплоемкость — Wiki How Русский
Удельная теплоемкость — это энергия, необходимая для того, чтобы поднять температуру одного грамма чистого вещества на один градус Цельсия. Удельная теплоемкость вещества зависит от его химического состава и агрегатного состояния. Открытие удельной теплоемкости подстегнуло развитие термодинамики, науки о переходах энергии, касающейся теплоты и работы системы. Удельная теплоемкость и термодинамика широко используются в химии, ядерной инженерии и аэродинамики, а также в повседневной жизни для радиаторов и систем охлаждения автомобилей.
Эту страницу просматривали 110 519 раз.
Реклама
| 05.04.2019, 01:42 |
| Вещество | Удельная теплоемкость, кДж/(кг·K) |
|---|---|
| Азот твердый(при t=-250 °С) | 0,46 |
| Бетон (при t=20 °С) | 0,88 |
| Бумага (при t=20 °С) | 1,50 |
| Воздух твердый (при t=-193 °С) | 2,0 |
| Графит | 0,75 |
| Дерево дуб | 2,40 |
| Дерево сосна, ель | 2,70 |
| Каменная соль | 0,92 |
| Камень | 0,84 |
| Кирпич (при t=0 °С) | 0,88 |
Удельная теплоемкость жидкостей
| Вещество | Температура,°C | |
|---|---|---|
| Бензин (Б-70) | 20 | 2,05 |
| Вода | 1-100 | 4,19 |
| Глицерин | 0-100 | 2,43 |
| Керосин | 0-100 | 2,09 |
| Масло машинное | 0-100 | 1,67 |
| Масло подсолнечное | 20 | 1,76 |
| Мед | 20 | 2,43 |
| Молоко | 20 | 3,94 |
| Нефть | 0-100 | 1,67-2,09 |
| Ртуть | 0-300 | 0,138 |
| Спирт | 20 | 2,47 |
| Эфир | 18 | 3,34 |
Удельная теплоемкость металлов и сплавов
| Вещество | Температура,°C | Удельная теплоемкость,к Дж/(кг·K) |
|---|---|---|
| Алюминий | 0-200 | 0,92 |
| Вольфрам | 0-1600 | 0,15 |
| Железо | 0-100 | 0,46 |
| Железо | 0-500 | 0,54 |
| Золото | 0-500 | 0,13 |
| Иридий | 0-1000 | 0,15 |
| Магний | 0-500 | 1,10 |
| Медь | 0-500 | 0,40 |
| Никель | 0-300 | 0,50 |
| Олово | 0-200 | 0,23 |
| Платина | 0-500 | 0,14 |
| Свинец | 0-300 | 0,14 |
| Серебро | 0-500 | 0,25 |
| Сталь | 50-300 | 0,50 |
| Цинк | 0-300 | 0,40 |
| Чугун | 0-200 | 0,54 |
Удельная теплоемкость расплавленных металлов и сжиженных сплавов
| Вещество | Температура,°C | Удельная теплоемкость,к Дж/(кг·K) |
|---|---|---|
| Азот | -200,4 | 2,01 |
| Алюминий | 660-1000 | 1,09 |
| Водород | -257,4 | 7,41 |
| Воздух | -193,0 | 1,97 |
| Гелий | -269,0 | 4,19 |
| Золото | 1065-1300 | 0,14 |
| Кислород | -200,3 | 1,63 |
| Натрий | 100 | 1,34 |
| Олово | 250 | 0,25 |
| Свинец | 327 | 0,16 |
| Серебро | 960-1300 | 0,29 |
Удельная теплоемкость газов и паров
при нормальном атмосферном давлении
| Вещество | Температура,°C | Удельная теплоемкость,к Дж/(кг·K) |
|---|---|---|
| Азот | 0-200 | 1,0 |
| Водород | 0-200 | 14,2 |
| Водяной пар | 100-500 | 2,0 |
| Воздух | 0-400 | 1,0 |
| Гелий | 0-600 | 5,2 |
| Кислород | 20-440 | 0,92 |
| Оксид углерода(II) | 26-200 | 1,0 |
| Оксид углерода(IV) | 0-600 | 1,0 |
| Пары спирта | 40-100 | 1,2 |
| Хлор | 13-200 | 0,50 |
Вода является одним из самых удивительных веществ. Несмотря на широкое распространение и повсеместное использование, она — настоящая загадка природы. Являясь одним из соединений кислорода, вода, казалось бы, должна иметь совсем низкими такие характеристики, как и замерзания, теплота парообразования и т. п. Но этого не происходит. Одна лишь теплоемкость воды, вопреки всему, чрезвычайно высока.
Несмотря на широкое распространение и повсеместное использование, она — настоящая загадка природы. Являясь одним из соединений кислорода, вода, казалось бы, должна иметь совсем низкими такие характеристики, как и замерзания, теплота парообразования и т. п. Но этого не происходит. Одна лишь теплоемкость воды, вопреки всему, чрезвычайно высока.
Вода способна поглощать огромное количество тепла, сама при этом практически не нагреваясь — в этом ее физическая особенность. воды выше теплоемкости песка примерно в пять раз, и в десять раз — железа. Поэтому вода является природным охладителем. Ее свойство накапливать большое количество энергии позволяет сглаживать колебания температуры на поверхности Земли и регулировать тепловой режим в рамках всей планеты, причем происходит это независимо от времени года.
Это уникальное свойство воды позволяет использовать ее в качестве охлаждающего вещества в промышленности и в быту. К тому же вода является общедоступным и сравнительно дешевым сырьем.
Что же понимается под теплоемкостью? Как известно из курса термодинамики, передача тепла происходит всегда от горячего к холодному телу. При этом речь идет о переходе определенного количества тепла, а температура обоих тел, являясь характеристикой их состояния, показывает направление этого обмена. В процессе металлического тела с водой равной массы при одинаковых исходных температурах металл меняет свою температуру в несколько раз больше воды.
Если принять за постулат основное утверждение термодинамики — из двух тел (изолированных от прочих), при теплообмене одно отдает, а другое получает равное количество тепла, то становится ясно, что у металла и воды совершенно разная теплоемкость.
Таким образом, теплоемкость воды (как и любого вещества) — это показатель, характеризующий способность данного вещества отдавать (или получать) какое-то при остывании (нагреве) на единицу температуры.
Удельной теплоемкостью вещества считается количество тепла, требуемое для того, чтобы нагреть единицу этого вещества (1 килограмм) на 1 градус.
Количество тепла, выделяемое или поглощаемое телом, равно произведению величин удельной теплоемкости, массы и разности температур. Измеряется оно в калориях. Одна калория — именно то количество тепла, которого достаточно, чтобы нагреть 1 г воды на 1 градус. Для сравнения: удельная теплоемкость воздуха — 0.24 кал/г ∙°С, алюминия — 0.22, железа — 0.11, ртути — 0.03.
Теплоемкость воды не является константой. С ростом температуры от 0 до 40 градусов она незначительно снижается (от 1,0074 до 0,9980), тогда как у всех остальных веществ в процессе нагревания эта характеристика растет. Кроме того, она может понижаться с ростом давления (на глубине).
Как известно, вода имеет три агрегатных состояния — жидкое, твердое (лед) и газообразное (пар). При этом удельная теплоемкость льда примерно в 2 раза ниже, чем у воды. В этом — основное отличие воды от других веществ, величины удельной теплоемкости которых в твердом и расплавленном состоянии не меняются. В чем же тут секрет?
Дело в том, что лед имеет кристаллическую структуру, которая при нагревании разрушается не сразу. Вода содержит небольшие частицы льда, состоящие из нескольких молекул и именуемые ассоциатами. При нагревании воды часть расходуется на разрушение водородных связей в этих образованиях. Этим и объясняется необычайно высокая теплоемкость воды. Полностью связи между ее молекулами разрушаются только при переходе воды в пар.
Вода содержит небольшие частицы льда, состоящие из нескольких молекул и именуемые ассоциатами. При нагревании воды часть расходуется на разрушение водородных связей в этих образованиях. Этим и объясняется необычайно высокая теплоемкость воды. Полностью связи между ее молекулами разрушаются только при переходе воды в пар.
Удельная теплоемкость при температуре 100° С почти не отличается от таковой у льда при 0° С. Это еще раз подтверждает правильность данного объяснения. Теплоемкость пара, как и теплоемкость льда, в настоящее время изучены гораздо лучше, чем воды, в отношении которой ученые до сих пор не пришли к единому мнению.
Удельная теплоёмкость — это энергия, которая требуется для увеличения температуры 1 грамма чистого вещества на 1°. Параметр зависит от его химического состава и агрегатного состояния: газообразное, жидкое или твёрдое тело. После его открытия начался новый виток развития термодинамики, науки о переходных процессах энергии, которые касаются теплоты и функционирования системы.
Как правило, удельная теплоёмкость и основы термодинамики используются при изготовлении радиаторов и систем, предназначенных для охлаждения автомобилей, а также в химии, ядерной инженерии и аэродинамике. Если вы хотите узнать, как рассчитывается удельная теплоёмкость, то ознакомьтесь с предложенной статьёй.
Перед тем, как приступить к непосредственному расчёту параметра следует ознакомиться с формулой и её компонентами.
Формула для расчёта удельной теплоёмкости имеет следующий вид:
- с = Q/(m*∆T)
Знание величин и их символических обозначений, использующихся при расчёте, крайне важно. Однако необходимо не только знать их визуальный вид, но и чётко представлять значение каждого из них. Расчёт удельной теплоёмкости вещества представлен следующими компонентами:
ΔT – символ, означающий постепенное изменение температуры вещества. Символ «Δ» произносится как дельта.
ΔT = t2–t1, где
- t1 – первичная температура;
- t2 – конечная температура после изменения.

m – масса вещества используемого при нагреве (гр).
Q – количество теплоты (Дж/J)
На основании Цр можно вывести и другие уравнения:
- Q = m*цp*ΔT – количество теплоты;
- m = Q/цр*(t2 — t1) – массы вещества;
- t1 = t2–(Q/цp*m) – первичной температуры;
- t2 = t1+(Q/цp*m) – конечной температуры.
Инструкция по расчёту параметра
- Взять расчётную формулу: Теплоемкость = Q/(m*∆T)
- Выписать исходные данные.
- Подставить их в формулу.
- Провести расчёт и получим результат.
В качестве примера произведём расчёт неизвестного вещества массой 480 грамм обладающего температурой 15ºC, которая в результате нагрева (подвода 35 тыс. Дж) увеличилась до 250º.
Согласно инструкции приведённой выше производим следующие действия:
Выписываем исходные данные:
- Q = 35 тыс. Дж;
- m = 480 г;
- ΔT = t2–t1 =250–15 = 235 ºC.
Берём формулу, подставляем значения и решаем:
с=Q/(m*∆T)=35тыс. Дж/(480 г*235º)=35тыс.Дж/(112800 г*º)=0,31 Дж/г*º.
Дж/(480 г*235º)=35тыс.Дж/(112800 г*º)=0,31 Дж/г*º.
Расчёт
Выполним расчёт C P воды и олова при следующих условиях:
- m = 500 грамм;
- t1 =24ºC и t2 = 80ºC – для воды;
- t1 =20ºC и t2 =180ºC – для олова;
- Q = 28 тыс. Дж.
Для начала определяем ΔT для воды и олова соответственно:
- ΔТв = t2–t1 = 80–24 = 56ºC
- ΔТо = t2–t1 = 180–20 =160ºC
Затем находим удельную теплоёмкость:
- с=Q/(m*ΔТв)= 28 тыс. Дж/(500 г *56ºC) = 28 тыс.Дж/(28 тыс.г*ºC) = 1 Дж/г*ºC.
- с=Q/(m*ΔТо)=28тыс.Дж/(500 гр*160ºC)=28 тыс.Дж/(80 тыс.г*ºC)=0,35 Дж/г*ºC.
Таким образом, удельная теплоемкость воды составила 1 Дж/г *ºC, а олова 0,35 Дж/г*ºC. Отсюда можно сделать вывод о том, что при равном значении подводимого тепла в 28 тыс. Дж олово нагрется быстрее воды, поскольку его теплоёмкость меньше.
Теплоёмкостью обладают не только газы, жидкости и твёрдые тела, но и продукты питания.
Как рассчитать теплоемкость продуктов питания
При расчёте емкости питания уравнение примет следующий вид:
с=(4.180*w)+(1.711*p)+(1.928*f)+(1.547*c)+(0.908 *a), где:
- w – количество воды в продукте;
- p – количество белков в продукте;
- f – процентное содержание жиров;
- c – процентное содержание углеводов;
- a – процентное содержание неорганических компонентов.
Определим теплоемкость плавленого сливочного сыра Viola . Для этого выписываем нужные значения из состава продукта (масса 140 грамм):
- вода – 35 г;
- белки – 12,9 г;
- жиры – 25,8 г;
- углеводы – 6,96 г;
- неорганические компоненты – 21 г.
Затем находим с:
- с=(4.180*w)+(1.711*p)+(1.928*f)+(1.547*c)+(0.908*a)=(4.180*35)+(1.711*12,9)+(1.928*25,8) + (1.547*6,96)+(0.908*21)=146,3+22,1+49,7+10,8+19,1=248 кДж /кг*ºC.
Всегда помните, что:
- процесс нагревания металла проходит быстрее, чем у воды, так как он обладает C P в 2,5 раза меньше;
- по возможности преобразуйте полученные результаты в более высокий порядок, если позволяют условия;
- в целях проверки результатов можно воспользоваться интернетом и посмотреть с для расчётного вещества;
- при равных экспериментальных условиях более значительные температурные изменения будут наблюдаться у материалов с низкой удельной теплоёмкостью.

Количество энергии, которое необходимо сообщить 1 г какого либо вещества, чтобы повысить его температуру на 1°С. По определению, для того чтобы повысить температуру 1 г воды на 1°С, требуется 4,18 Дж. Экологический энциклопедический словарь.… … Экологический словарь
удельная теплоёмкость — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN specific heatSH …
УДЕЛЬНАЯ ТЕПЛОЁМКОСТЬ — физ. величина, измеряемая количеством теплоты, необходимым для нагревания 1 кг вещества на 1 К (см.). Единица удельной темплоёмкости в СИ (см.) на килограмм кельвин (Дж кг∙К)) … Большая политехническая энциклопедия
удельная теплоёмкость — savitoji šiluminė talpa statusas T sritis fizika atitikmenys: angl. heat capacity per unit mass; massic heat capacity; specific heat capacity vok. Eigenwärme, f; spezifische Wärme, f; spezifische Wärmekapazität, f rus. массовая теплоёмкость, f;… … Fizikos terminų žodynas
См. Теплоёмкость … Большая советская энциклопедия
Теплоёмкость … Большая советская энциклопедия
удельная теплоёмкость — удельная теплота … Cловарь химических синонимов I
удельная теплоёмкость газа — — Тематики нефтегазовая промышленность EN gas specific heat … Справочник технического переводчика
удельная теплоёмкость нефти — — Тематики нефтегазовая промышленность EN oil specific heat … Справочник технического переводчика
удельная теплоёмкость при постоянном давлении — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN specific heat at constant pressurecpconstant pressure specific heat … Справочник технического переводчика
удельная теплоёмкость при постоянном объёме — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN specific heat at constant volumeconstant volume specific heatCv … Справочник технического переводчика
Книги
- Физические и геологические основы изучения движения вод в глубоких горизонтах , Трушкин В.
 В.. В целом книга посвящена закону авторегулирования температуры воды с вмещающим телом, открытому автором в 1991 г.
В начале книги проведен обзор состояния изученностипроблемы движения глубоких…
В.. В целом книга посвящена закону авторегулирования температуры воды с вмещающим телом, открытому автором в 1991 г.
В начале книги проведен обзор состояния изученностипроблемы движения глубоких…
Калькулятор удельной теплоемкости + формула (уравнение C = Q /(m ⨉ ΔT))
на
Удельная теплоемкость — это, по сути, мера того, насколько трудно нагреть различных материалов. Чтобы рассчитать удельную теплоемкость (C) любого вещества, вам понадобится формула удельной теплоемкости (уравнение, если хотите).
Далее вы также найдете калькулятор удельной теплоемкости : Просто подключите Q (тепловая энергия) , m (масса) и ΔT (разность температур) , и калькулятор динамически рассчитает для вас удельную теплоемкость. Вот как выглядит калькулятор удельной теплоемкости (скриншот):
Пример расчета: 20 000 Дж тепла нагреют 12 кг вещества на 20°К. Какая удельная теплоемкость? 83,33 Дж/кг×К. Вы можете найти этот калькулятор далее; он будет динамически и автоматически рассчитывать удельную теплоемкость.
Какая удельная теплоемкость? 83,33 Дж/кг×К. Вы можете найти этот калькулятор далее; он будет динамически и автоматически рассчитывать удельную теплоемкость.Сначала рассмотрим формулу удельной теплоемкости. Это довольно простая формула, которую может использовать каждый. В конце приведем также удельные теплоемкости воздуха, воды и некоторых других веществ. Мы также решим несколько простых примеров расчета удельной теплоемкости. Давайте рассмотрим пример, чтобы проиллюстрировать, что на самом деле говорит нам удельная теплоемкость:
Пример: Воздух при комнатной температуре имеет удельную теплоемкость 1012 Дж/кг×К. Вода при комнатной температуре имеет удельную теплоемкость 4181 Дж/кг×К. Это означает, что нам нужно примерно в 4 раза больше тепла, чтобы нагреть килограмм воды, чем килограмм воздуха.
Удельная теплоемкость определяется как количество теплоты, необходимое для повышения температуры 1 кг вещества на 1 К. Чаще всего для этого мы используем единицы СИ (Дж = Джоули, кг = килограммы, К = градусы Кельвина).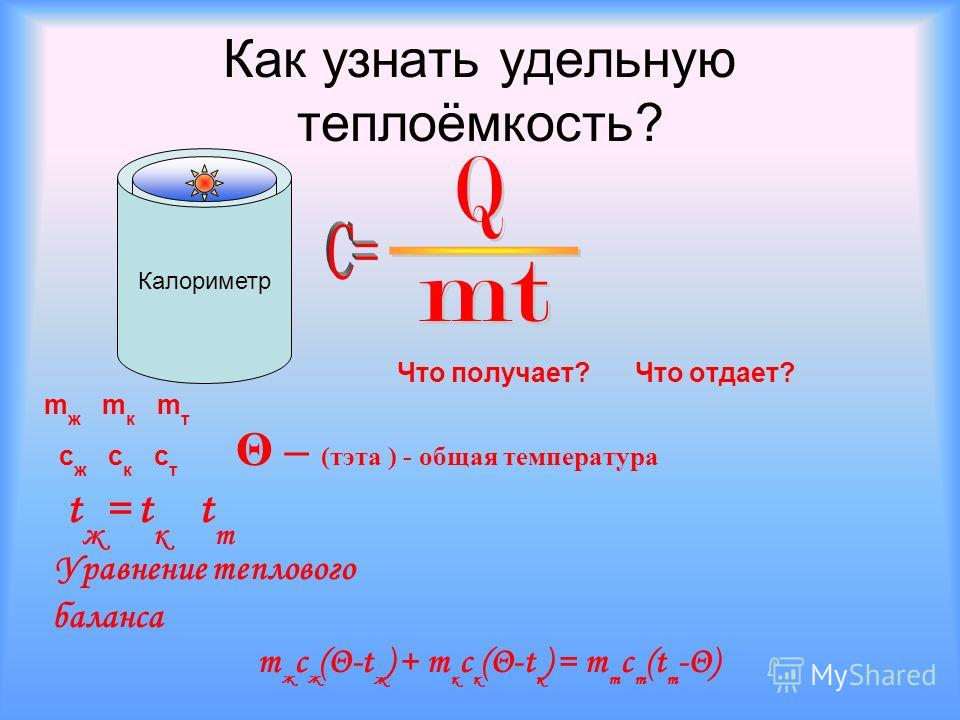
Мы можем аккуратно подставить все эти числа в следующую формулу:
Формула удельной теплоемкости
Удельная теплоемкость обозначается C (C для емкости). Вот уравнение для расчета удельной теплоемкости C:
C = Q ÷ (m×ΔT)
Довольно просто, правда?
- Q — это количество тепла, которое мы подводим к веществу. Может быть 1 Дж, 40 Дж или даже 50 000 Дж, любое количество Джоулей.
- м — это масса вещества, которое мы нагреваем. Вы можете нагреть 1 кг вещества, 20 кг или даже 10 г вещества, подходит любой вес.
- ΔT — это разница температур между начальной и конечной температурами, и она всегда измеряется не в градусах Фаренгейта (°F), не в градусах Цельсия (°C), а в кельвинах (K). Пример: если мы нагреем воду с 68°F или 20°C (это 293K) до 158°F или 70°C (это 343K), разница температур составляет 343K – 293K = 50K.
Вот простой пример: допустим, нам нужно 6000 Дж тепла, чтобы нагреть 3 кг вещества на 10К. Вот как мы рассчитываем удельную теплоемкость, используя приведенное выше уравнение;
Вот как мы рассчитываем удельную теплоемкость, используя приведенное выше уравнение;
C = 6000 Дж ÷ (3 кг × 10 К) = 200 Дж/кг × К
Формула удельной теплоемкости говорит нам, что удельная теплоемкость (C) этого вещества составляет 200 Дж/кг × К.
Чтобы еще больше упростить задачу, вы можете использовать этот калькулятор
Калькулятор удельной теплоемкости
По сути, вы просто вводите Q, m и ΔT, и калькулятор автоматически вычисляет удельную теплоемкость. Конечно, вы также можете немного поиграть с цифрами.
С помощью этого калькулятора можно просто определить, какова удельная теплоемкость вещества без необходимости все вычислять самостоятельно.
Давайте посмотрим на удельные теплоемкости некоторых распространенных газов, жидкостей и твердых тел:
Таблица удельной теплоемкости
| Вещество: | Фаза (газ, жидкость, твердое тело): | Удельная теплоемкость (Дж/кг×К) |
| Воздух при комнатной температуре | Газ | 1012 Дж/кг×К |
| Аргон (Ar) | Газ | 520,3 Дж/кг×К |
| Двуокись углерода (CO2) | Газ | 839Дж/кг×К |
| Гелий (Не) | Газ | 5193,2 Дж/кг×К |
| Водород (h3) | Газ | 14 300 Дж/кг×К |
| Сероводород (h3S) | Газ | 1015 Дж/кг×К |
| Метан при 275K (Ch5) | Газ | 2191/кг×K |
| Азот (N2) | Газ | 1040 Дж/кг×К |
| Неон (Ne) | Газ | 1030,1 Дж/кг×К |
| Кислород (O2) | Газ | 918 Дж/кг×К |
| Аммиак (Nh4) | Жидкость | 4700 Дж/кг×К |
| Этанол (Ch4Ch3OH) | Жидкость | 2440 Дж/кг×К |
| Бензин | Жидкость | 2220 Дж/кг×К |
| Меркурий | Жидкость | 139,5 Дж/кг×К |
| Метанол (Ch4OH) | Жидкость | 2140 Дж/кг×К |
| Вода при 25 °C | Жидкость | 4181,3 Дж/кг×К |
| Алюминий (Al) | Твердый | 897 Дж/кг×К |
| Сурьма | Твердый | 207 Дж/кг×К |
| Мышьяк | Твердый | 328 Дж/кг×К |
| Бериллий | Твердый | 1820 Дж/кг×К |
| Кадмий | Твердый | 231 Дж/кг×К |
| Хром | Твердый | 449 Дж/кг×К |
| Медь | Твердый | 385 Дж/кг×К |
| Алмаз | Твердый | 509,1 Дж/кг×К |
| Стекло | Твердый | 840 Дж/кг×К |
| Золото | Твердый | 129 Дж/кг×К |
| Гранит | Твердый | 790 Дж/кг×К |
| Графит | Твердый | 710 Дж/кг×К |
| Железо | Твердый | 412 Дж/кг×К |
| Свинец | Твердый | 129 Дж/кг×К |
| Литий | Твердый | 3580 Дж/кг×К |
| Магний | Твердый | 1020 Дж/кг×К |
| Полиэтилен | Твердый | 2302,7 Дж/кг×К |
| Силикагель | Твердый | 703 Дж/кг×К |
| Серебро | Твердый | 233 Дж/кг×К |
| Натрий | Твердый | 1230 Дж/кг×К |
| Сталь | Твердый | 466 Дж/кг×К |
| Олово | Твердый | 227 Дж/кг×К |
| Титан | Твердый | 528 Дж/кг×К |
| Уран | Твердый | 116 Дж/кг×К |
| Асфальт | Твердый | 920 Дж/кг×К |
| Кирпич | Твердый | 840 Дж/кг×К |
| Бетон | Твердый | 880 Дж/кг×К |
| Гипс | Газ | 1090 Дж/кг×К |
| Песок | Газ | 835 Дж/кг×К |
| Почва | Газ | 800 Дж/кг×К |
Если у вас есть какие-либо вопросы об удельной теплоемкости, вы можете использовать комментарии ниже, и мы постараемся помочь вам, чем сможем.
Содержание
3.12: Расчеты энергии и теплоемкости
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 47467
Цели обучения
- Связать теплопередачу с изменением температуры.
Тепло — знакомое нам проявление передачи энергии. Когда мы прикасаемся к горячему предмету, энергия течет от горячего предмета к нашим пальцам, и мы воспринимаем эту поступающую энергию как «горячий» предмет. И наоборот, когда мы держим кубик льда в ладонях, энергия течет из нашей руки в кубик льда, и мы воспринимаем эту потерю энергии как «холод». В обоих случаях температура объекта отличается от температуры нашей руки, поэтому можно сделать вывод, что разность температур является конечной причиной теплопередачи.
Удельная теплоемкость вещества может быть использована для расчета изменения температуры данного вещества при нагревании или охлаждении. Уравнение, связывающее теплоту \(\left( q \right)\) с удельной теплоемкостью \(\left( c_p \right)\), массой \(\left( m \right)\) и изменением температуры \(\ слева( \Delta T \right)\) показано ниже.
\[q = c_p \times m \times \Delta T \nonumber \]
Тепло, которое либо поглощается, либо выделяется, измеряется в джоулях. Масса измеряется в граммах. Изменение температуры определяется выражением \(\Delta T = T_f — T_i\), где \(T_f\) — конечная температура, а \(T_i\) — начальная температура.
Каждое вещество имеет характеристическую удельную теплоемкость, которая выражается в единицах кал/г•°C или кал/г•K, в зависимости от единиц, используемых для выражения Δ T . Удельной теплоемкостью вещества называется количество энергии, которое необходимо передать 1 г этого вещества или от него, чтобы изменить его температуру на 1°. \text{o} \text{C} \right)\)»> 0,233
\text{o} \text{C} \right)\)»> 0,233
направление теплового потока не показано в тепле = mc Δ T . Если энергия уходит в объект, то полная энергия объекта увеличивается, а значения теплоты Δ T положительны. Если энергия исходит от объекта, то полная энергия объекта уменьшается, а значения тепла и Δ T отрицательны.
Пример \(\PageIndex{1}\) 9\text{o} \text{C} \nonumber \]
Пример \(\PageIndex{2}\)
Какое количество теплоты передается при нагревании бруска металлического железа массой 150 г с 25,0°C до 73,3°C? Каково направление теплового потока?
Решение
Мы можем использовать теплоту = mc Δ T для определения количества теплоты, но сначала нам нужно определить Δ T . Поскольку конечная температура железа составляет 73,3°С, а начальная температура составляет 25,0°С, Δ T будет следующим: 9\circ C) = 782\: cal} \nonumber \]
Обратите внимание, что грамм и °C сокращаются алгебраически, остается только единица калорий, которая является единицей тепла. Поскольку температура железа увеличивается, энергия (в виде тепла) должна течь в металл.
Поскольку температура железа увеличивается, энергия (в виде тепла) должна течь в металл.
Упражнение \(\PageIndex{1}\)
Какое количество теплоты передается при охлаждении бруска металлического алюминия массой 295,5 г со 128,0°C до 22,5°C? Каково направление теплового потока?
- Ответ
- Тепло покидает алюминиевый блок.
Пример \(\PageIndex{2}\)
Образец красновато-коричневого металла массой 10,3 г выделил 71,7 кал тепла при снижении его температуры с 97,5°C до 22,0°C. Чему равна удельная теплоемкость металла? Можете ли вы определить металл по данным в таблице \(\PageIndex{1}\)?
Решение
Вопрос дает нам теплоту, конечную и начальную температуры и массу образца. Значение Δ T следующее:
Δ T = T окончательная − T начальная = 22,0 °C − 97,5 °C = −75,5 °C
, поэтому значение тепла записывается как отрицательное число, -71,7 кал. \circ C)}}\)
\circ C)}}\)
c = 0,0923 кал/г•°C
Это значение удельной теплоемкости очень близко к значению, указанному для меди в таблице 7.3.
Упражнение \(\PageIndex{2}\)
Кристалл хлорида натрия (NaCl) массой 10,7 г имеет начальную температуру 37,0°C. Какова конечная температура кристалла, если к нему подведено 147 кал теплоты?
- Ответить
Проиллюстрированы расчеты удельной теплоемкости.
ЛИЦЕНЗИЯ ПОД
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Лицензия
- СК-12
- Показать страницу Содержание
- нет на стр.



 Разобравшись с задачей, вы можете записать все известные и неизвестные переменные, чтобы лучше понять, с чем вы имеете дело. Вот как это делается:
Разобравшись с задачей, вы можете записать все известные и неизвестные переменные, чтобы лучше понять, с чем вы имеете дело. Вот как это делается:
 Уравнение учитывает массовую долю (x) всех твердых веществ, которые составляют пищу. Расчет удельной теплоемкости приведен в кДж/(кг х K).
Уравнение учитывает массовую долю (x) всех твердых веществ, которые составляют пищу. Расчет удельной теплоемкости приведен в кДж/(кг х K).


 Возьмем два одинаковых сосуда и,
налив в один из них воду массой 400 г, а в другой — растительное масло
массой 400 г, начнем их нагревать с помощью одинаковых горелок. Наблюдая
за показаниями термометров, мы увидим, что масло нагревается быстрее.
Чтобы нагреть воду и масло до одной и той же температуры, воду следует
нагревать дольше. Но чем дольше мы нагреваем воду, тем большее
количество теплоты она получает от горелки.
Возьмем два одинаковых сосуда и,
налив в один из них воду массой 400 г, а в другой — растительное масло
массой 400 г, начнем их нагревать с помощью одинаковых горелок. Наблюдая
за показаниями термометров, мы увидим, что масло нагревается быстрее.
Чтобы нагреть воду и масло до одной и той же температуры, воду следует
нагревать дольше. Но чем дольше мы нагреваем воду, тем большее
количество теплоты она получает от горелки.


 В.. В целом книга посвящена закону авторегулирования температуры воды с вмещающим телом, открытому автором в 1991 г.
В начале книги проведен обзор состояния изученностипроблемы движения глубоких…
В.. В целом книга посвящена закону авторегулирования температуры воды с вмещающим телом, открытому автором в 1991 г.
В начале книги проведен обзор состояния изученностипроблемы движения глубоких…