Калийное удобрение
|
КАЛИЙНОЕ УДОБРЕНИЕ |
||||||
|
Нормативно-технический документ |
||||||
|
Ts 00203849 –114:2015 |
||||||
|
Химическая формула |
||||||
|
KNO3 |
||||||
|
Номер вещества в реестре CAS |
||||||
|
7757-79-1 |
||||||
|
Общепринятые синонимы |
||||||
|
Калиевая селитра, индийская селитра, соль Петра (Solt of Peter), нитрат калия, калий азотнокислый технический, пищевая добавка Е252 (консервант) |
||||||
|
Коды: |
||||||
ТНВЭД |
2834210000 |
|||||
|
ГНГ |
28342100 |
|||||
|
ЕТСНГ |
483327 |
|||||
|
Номер ООН |
1486 |
|||||
|
Наличие сертификата соответствия (№, дата выдачи, срок действия) |
||||||
|
Сертификат соответствия № UZ. |
||||||
|
Область применения |
||||||
|
Нитрат калия используют для производства порохов, в пиротехнике, в пищевой и стекольной промышленности. Калийные удобрения по значимости для растений стоят на третьем месте после азотных и фосфорных. Агрохимиками доказана устойчивая эффективность калийных удобрений практически на всех культурах и во всех зонах. Достаточный уровень калия в почве способствует значительному ослаблению влияния негативных погодных явлений. Значение калия в жизни растений определяется следующими факторами: ― усиливает процесс фотосинтеза, ассимиляцию СО2 ― сохраняет активность ферментов более значительное время ― благоприятствует образованию белков ― повышает эффективность азота при выращивании культурных растений ― усиливает фиксацию азота бобовыми культурами ― способствует более эффективному использованию растениями воды ― снижает степень поражения растений грибковыми болезнями ― снижает поступления в растения радионуклидов Внесение с калийными удобрениями 1 тонны обеспечивает прибавку с 1га урожая зерна 2-3т, картофеля – 20-33, сахарной свёклы – 35-40, хлопка-сырца – 1-2, льноволокна – 1-1,5, сена сеяных трав –20-33, сена луговых трав – 8-18 тонн. Бесхлорные формы калия способствуют повышению урожайности гречихи, проса и некоторых сортов табака, увеличению содержания сахара в ягодах отдельных сортов винограда, содержанию крахмала в клубнях поздних сортов картофеля и улучшению качества льноволокна. Прямое внесение сульфата и нитрата калия практикуется под такие чувствительные к иону хлора культуры, как табак, цитрусовые, виноград, томаты, морковь, картофель, лён, конопля, гречиха, ягодные, цветы. Особенно они востребованы при выращивании овощей и цветов в тепличных хозяйствах. Бесхлорные формы удобрений необходимы для почв с хлоридным засолением. К преимуществам нитрата калия по сравнению с рядом других удобрений относятся: 1) наличие в его составе двух необходимых растениям элементов – калия и азота 2) отсутствие балласта, что особенно важно при дальних перевозках 3) малая гигроскопичность, благодаря чему удобрение сохраняет сыпучесть |
||||||
|
ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ПРОДУКТА |
||||||
|
Внешний вид |
||||||
|
Безводная кристаллическая соль белого цвета (иногда с желтовато-сероватым оттенком). |
||||||
|
Основные физико-химические свойства |
||||||
|
№ |
Наименование |
Показатель |
||||
|
1. |
Относительная молекулярная масса, а.с.м |
101,1032 |
||||
|
2. |
Молярная масса, г/моль |
101,1032 |
||||
|
3. |
Плотность при16 оС, г/см3 |
2,109 |
||||
|
4. |
Температура плавления, оС |
334 |
||||
|
5. |
Температура кипения, оС |
400 |
||||
|
6. |
Растворимость в воде, г/100 мл: 0 оС 25оС 100оС |
13,3 36 247 |
||||
|
Технические характеристики |
||||||
|
№ |
Наименование |
Норма |
||||
|
1 сорт |
2 сорт |
|||||
|
1. |
Внешний вид |
Белые кристаллы или порошок с желтоватым, розоватым или сероватым оттенком |
||||
|
2. |
Массовая доля калия в пересчете на K2O, %, не менее |
41,0 |
||||
|
3. |
Массовая доля азота, %, не менее |
12,2 |
||||
|
4. |
Массовая доля хлоридов, %, не более |
0,6 |
2,0 |
|||
|
5. |
Массовая доля солей кальция и магния в пересчете на Са, %, не более |
3,7 |
||||
|
6. |
Массовая доля воды, %, не более |
0,2 |
||||
|
Примечание:
|
||||||
|
Упаковка и хранение |
||||||
|
Нитрат калия должен храниться в закрытом складском помещении в упакованном виде. |
||||||
|
Транспортировка |
||||||
|
Нитрат калия технический перевозят в крытых железнодорожных вагонах, в закрытых палубных судах и крытым автотранспортом в соответствии с правилами перевозок грузов, действующих на транспорте данного вида |
||||||
|
Информация о безопасности продукта |
||||||
|
Нитрат калия технический является окислителем, способствует самовозгоранию горючих веществ, по степени воздействия на организм относится к веществам 3-го класса опасности. Не допускается погрузка, разгрузка, перевозка и хранение нитрат калия совместно с горючими веществами, минеральными кислотами, цианистым калием, роданидами, а также смешения с древесными опилками, соломой, углём, торфом и другими органическими веществами во избежание самовозгорания, пожара и взрыва |
||||||
|
Гарантийный срок хранения |
||||||
|
Гарантийный срок хранения – не ограничен |
||||||
Нажмите на кнопку ниже, чтобы прослушать текст Powered by GSpeech
Белорусский государственный университет транспорта — БелГУТ (БИИЖТ)
Электронная очередь на
централизованное тестирование
Как поступить в БелГУТ
Как получить место
в общежитии БелГУТа
ГОРЯЧАЯ ЛИНИЯ
по вопросам приемной кампании
События
Все события
| Пн | Вт | Ср | Чт | Пт | Сб | Вс |
|---|---|---|---|---|---|---|
1 | 2 | 3 | 4 | 5 | 6 | 7 |
8 | 9 | 10 | 11 Дата : 2023-05-11 | 12 | 13 | 14 |
15 | 16 | 17 | 18 | 19 | 20 | 21 |
22 | 23 | 24 | 25 | Дата : 2023-05-26 | 27 | 28 |
29 | 30 Дата : 2023-05-30 | 31 | ||||
Все анонсы
- Поздравление с Днем Победы Председателя Совета Рес.
 ..
.. - С ПРАЗДНИКОМ ВЕЛИКОЙ ПОБЕДЫ!…
- Студсовет поздравляет с Днем Победы…
- 68-я студенческая научно-техническая конференция…
- Фестиваль военно-патриотической песни среди иностр…
- С днем Печати!
- XXXII Международный фестиваль искусств «Славянский…
- Вопросы к собеседованию для прошедших обучение в Н…
- Олимпиада по теории вероятностей…
- Летний оздоровительный лагерь для детей сотруднико…
Анонсы
Университет
Абитуриентам
Студентам
Конференции
Приглашения
Поздравление с Днем Победы Председателя Совета Рес…
С ПРАЗДНИКОМ ВЕЛИКОЙ ПОБЕДЫ!…
Студсовет поздравляет с Днем Победы…
68-я студенческая научно-техническая конференция…
Новости
Университет
Международные связи
Спорт
ИВР
Жизнь студентов
Новости подразделений
- Университет
День Победы!
09 мая 2023
- Воспитательная работа
Праздник ВЕТЕРАНОВ
07 мая 2023
- Воспитательная работа
Как это было . ..
..
06 мая 2023
- Университет
Праздничный концерт и торжественное собрание в ОКЦ…
05 мая 2023
- Университет
Слава Героям — митинг на Аллее Героев
05 мая 2023
- Университет
Макет лагеря «Дулаг-121» выполнен студентами БелГУТа для выставки о ла…
05 мая 2023
- Университет
Поклонимся тем, кто отдал свои жизни за Победу…
05 мая 2023
- Университет
Презентуем патриотический проект «Альбом памяти»…
05 мая 2023
- Студенческая жизнь
Мы помним о тех, кто не вернулся с поля боя. ..
..
05 мая 2023
Другие новости
- Новый номер газеты «Вести БелГУТа»
- Победа в Республиканской Универсиаде по вольной борьбе…
- Наши Первая вице-Мисс и самый харизматичный Мистер Студенчества Гомель…
- Дорогами мира и созидания. Памятник в д. Новоселки…
- Дорогами мира и созидания. Братская могила в деревне Старые Дятловичи…
- Мы тоже должны быть едины и сплочены, как эти братья……
- Парад под окнами… Потапенко Василий Данилович…
- Интерактивный квест по мемориалам г. Гомеля…
- Горек хлебушек блокадный
- Материалы V Международной научно-практической конференции «Научные и м…
- Дорогами мира и созидания. Братская могила в деревне Огородня…
БелГУТ на Доске почета
Достижения университета
КУДА ПОСТУПАТЬ
Все факультеты
Предложения
Все предложения
Видеотека
Все видео
Фотогалерея
Все фото
Отображается соединение Нитрат калия (KNO3) (FDB015409)
Назад к соединениям
| Информация о записи | |||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Версия | 1. 0 0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Дата создания | 08.04.2010 22:11:49 UTC | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Дата обновления. 14 | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вторичные регистрационные номера | Недоступно | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Химическая информация | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| FooDB Наименование | Нитрат калия (KNO3) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Описание | 90 013 Нитрат калия, также известный как нитрат калия или селитра, относится к классу неорганических соединений, известных как нитраты щелочных металлов. . Это неорганические соединения, в которых самым большим оксоанионом является нитрат, а самым тяжелым атомом, не входящим в оксоанион, является щелочной металл. На основе обзора литературы было опубликовано значительное количество статей о нитрате калия.|||||||||||||||||||||||||||||||||||||||||||||||||||||
| Номер CAS | 7757-79-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Структура | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Синонимы | 900 13|||||||||||||||||||||||||||||||||||||||||||||||||||||
| Синоним | Источник |
|---|---|
| Калийнитрат | ЧЭБИ |
| Нитра | ЧЕБИ |
| Азотнокислый калий | ЧЕБИ |
| Азот | ЧЕБИ |
| ЧЕБИ | |
| Селитра | ЧЕБИ |
| Селитра | ЧЕБИ |
| ЧЕБИ | |
| Сенсодин | Кегг |
| Кислота азотная калийная | Генератор | Нитрат, соль калия | Генератор |
| Калий азотнокислый | Генератор |
| Калия нитрат моногидрат | MeSH |
| Калий азотнокислый (kno3) | Генератор |
| Collo-bo | biospider | E252 | db_source |
| KalII nitras | биопаук |
| Нитрат калия | biospider |
| калиевая соль азотной кислоты | biospider |
| калиевая соль азотной кислоты (1:1) | biospider |
| Азотная кислота, калиевая соль, 8CI нитрат ассия (январь/USP) | биопаук |
| нитрат калия [январь] | биопаук |
| Нитрат калия [UN1486] [Окислитель] | биопаук |
| Калий азотнокислый (точка) | биопаук |
| биопаук | |
| Сенсодин (TN) | биопаук |
| Викнайт | биопаук |
| Свойство | Значение | Источник | 9 0009
|---|---|---|
| logP | 0,028 | ChemAxon |
| pKa (сильнейшая кислота) | -1,4 | 900 13 ХимАксон|
| pKa (сильнейший основной) | -6. 1 1 | ChemAxon |
| Physiological Charge | -1 | ChemA xon |
| Подсчет акцепторов водорода | 3 | ChemAxon |
| Подсчет доноров водорода | 0 | ChemAxon |
| Площадь полярной поверхности | 68,88 Ų | ChemAxon |
| Вращающийся счетчик соединений | 0 9 | ChemAxon |
| Поляризуемость | 3,24 ų | ChemAxon |
| Количество колец | 0 | ChemAxon |
| Биодоступность 900 14 | Да | ChemAxon |
| Правило пяти | Да | ChemAxon |
| Фильтр Ghose | № | ХимАксон |
| Правило Вебера | № | ChemAxon |
| Правило, подобное MDDR | № | ChemAxon 9 0014 |
 NO3/c;2-1(3)4/q+1;-1
NO3/c;2-1(3)4/q+1;-1- Неорганические соли
- Оксиды неорганические
- Нитрат щелочного металла
- Неорганический оксид
- Неорганическая соль
- калиевая соль (CHEBI: 63043 )
- неорганическая нитратная соль (CHEBI:63043 )
| Свойство | Значение 900 08 | № по каталогу |
|---|---|---|
| Физическое состояние | Недоступно | |
| Физическое описание | Недоступно | |
| Массовый состав | K 38,67%; Н 13,85%; О 47,47% | ДФК |
| Температура плавления | Т. пл. 334° пл. 334° | ДФХ |
| Температура кипения | Недоступно | Экспериментальная растворимость в воде | Недоступно |
| Экспериментальный logP | Недоступно | |
| Экспериментальная pKa | Нет в наличии | |
| Изоэлектрическая точка | Нет в наличии | |
| Заряд | Недоступно | |
| Оптическое вращение | Недоступно | |
| Спектроскопические УФ-данные | Недоступно 9001 4 | |
| Плотность | Недоступно | |
| Показатель преломления | Недоступно |
| Тип | Описание | Клавиша заставки | Вид |
|---|---|---|---|
| Прогноз ГХ-МС | 9 0013 Нитрат калия (KNO3) , не дериватизированный , Расчетный спектр ГХ-МС — 70 эВ, Положительный всплеск20-0udi-00000-51dd8cb602ed71d15a99 | Спектр |
| Тип | Описание | Ключ-заставка | Просмотр | |
|---|---|---|---|---|
| Расчетный МС/МС | Прогнозируемый спектр ЖХ-МС/МС — 10 В, положительный | splash20-0udi-09 00000000-90cae1f633954557f0b9 | 22. 02.2019 02.2019 | Просмотр спектра |
| Расчетный МС/МС | Прогнозируемый спектр ЖХ-МС/МС — 20 В, положительный 3 22.02.2019 | Просмотр спектра | ||
| Прогноз МС/МС | Прогнозируемый спектр ЖХ-МС/МС — 40 В, положительный | splash20-0udj-9600000000-40c6e2f784462d3dce61 | 22.02.2019 | Просмотр спектра 90 014 |
 Duke ID
Duke ID| Продукты питания | Диапазон содержания | Среднее | Артикул |
|---|---|---|---|
| Продукты питания | 90 955 | Ссылка |
| Ароматизаторы | Цитаты |
|---|---|
| без запаха | 9102 1 Информационный каталог вкусов и ароматов. Информационный каталог вкусов и ароматов. |
Нитрат калия — KNO3, 7757-79-1
Нитрат калия (KNO3) представляет собой белую кристаллическую соль, часто используемую в удобрениях, консервантах и фейерверках. Он также является ключевым ингредиентом некоторых зубных паст для чувствительных зубов.
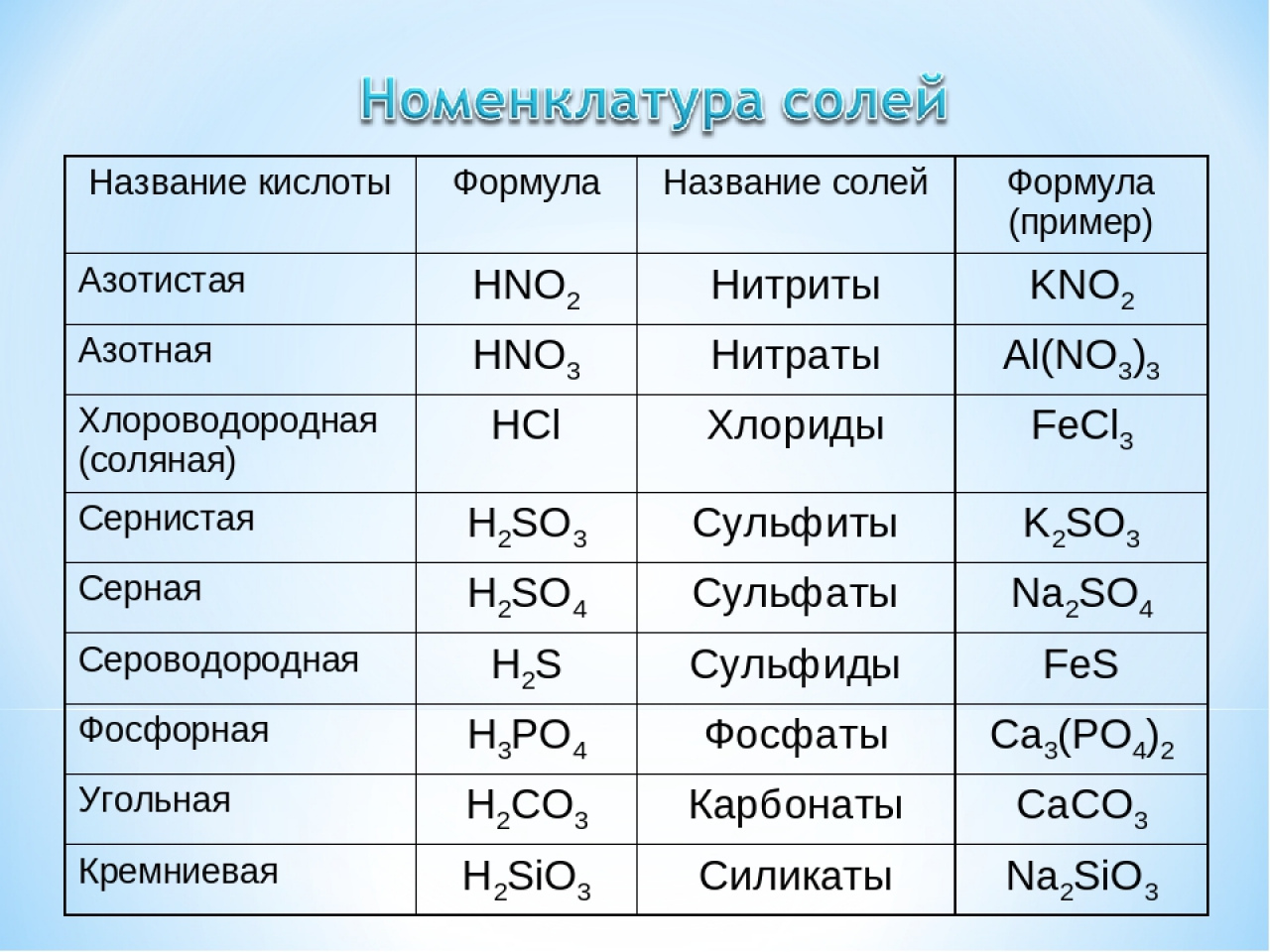
| Название IUPAC | Нитрат калия |
| Молекулярная формула | KNO3 |
| Номер CAS | 7757-79-1 |
| Синонимы | селитра; нитрат калия; селитра; селитра; Е252; китайская селитра; азотная кислота, калиевая соль; Kalii nitras |
| ИнЧИ | ИнЧИ=1S/K. NO3/c;2-1(3)4/q+1;-1 NO3/c;2-1(3)4/q+1;-1 |
Формула нитрата калия
Химическая формула нитрата калия – KNO3. Эта формула показывает, что соединение состоит из одного иона калия, одного иона нитрата и трех ионов кислорода. Формула полезна для расчета количества нитрата калия, необходимого для реакции, а также для определения элементов и ионов, присутствующих в соединении.
Нитрат калия Молярная масса
KNO3 имеет молярную массу 101,1 г/моль. Молярная масса представляет собой массу одного моля вещества и рассчитывается путем суммирования атомных масс всех атомов в соединении. В случае KNO3 молярная масса рассчитывается путем сложения атомной массы одного атома калия, одного атома азота и трех атомов кислорода. Это значение полезно для определения количества KNO3, необходимого для реакции, и для расчета других свойств, таких как концентрация.
Нитрат калия Температура кипения
KNO3 имеет относительно высокую температуру кипения 1336 °C (2437 °F). Это означает, что требуется много энергии, чтобы разорвать связи между атомами в соединении и превратить его из жидкости в газ. Это свойство делает KNO3 полезным в приложениях, требующих высокотемпературных реакций, например, при производстве фейерверков.
Это означает, что требуется много энергии, чтобы разорвать связи между атомами в соединении и превратить его из жидкости в газ. Это свойство делает KNO3 полезным в приложениях, требующих высокотемпературных реакций, например, при производстве фейерверков.
Точка плавления нитрата калия
KNO3 имеет температуру плавления 334 °C (633 °F). Это означает, что при температуре выше 334 °C KNO3 переходит из твердого состояния в жидкое. Это свойство делает KNO3 полезным в таких областях, как производство стекла, где он используется в качестве флюса для снижения температуры плавления кремнезема.
Плотность нитрата калия г/мл
Плотность KNO3 составляет 2,109 г/мл при комнатной температуре. Плотность – это мера массы на единицу объема вещества. Плотность KNO3 важна в таких областях применения, как производство удобрений, где он используется в качестве источника азота и калия. Плотность также полезна для определения количества KNO3, необходимого в данном объеме раствора.
Нитрат калия Молекулярная масса
Молекулярная масса KNO3 составляет 101,1 г/моль. Это значение рассчитывается путем суммирования атомных весов всех атомов в соединении. Молекулярная масса полезна для расчета других свойств KNO3, таких как количество KNO3, необходимое для реакции, или концентрация раствора.
Структура нитрата калия
KNO3 имеет кристаллическую структуру, состоящую из ионов калия, нитрата и кислорода. Ионы калия окружены шестью ионами нитрата, а ионы нитрата окружены шестью ионами калия. Эта структура придает KNO3 его характерные свойства, такие как растворимость, температура плавления и плотность.
| Внешний вид | Белый кристаллический порошок |
| Удельный вес | 2,109г/см³ при 20°C |
| Цвет | Белый |
| Запах | Без запаха |
| Молярная масса 9001 4 | 101,1032 г/моль |
| Плотность | 2,109 г/см³ |
| Температура плавления | 334°C (633°F) |
| Температура кипения | 400°C (752°F) |
| Температура вспышки | Неприменимо |
| Растворимость в воде | 133 г/л при 20°C |
| Растворимость | Растворим в глицерине, аммиаке и воде |
| Давление паров | Незначительно |
| Плотность пара | Неприменимо |
| pKa | 4,75 |
| pH | 6,9 – 7,3 |
KNO3 относительно безопасно при правильном обращении, но может представлять опасность при неправильном обращении. Он классифицируется как окислитель, что означает, что он может усиливать горение других материалов. KNO3 также может раздражать глаза, кожу и дыхательные пути и может быть токсичным при проглатывании или вдыхании в больших количествах. При работе с KNO3 важно надевать защитные средства, такие как перчатки, очки и респиратор, и хранить его в прохладном сухом месте вдали от легковоспламеняющихся материалов. Следует также соблюдать надлежащие методы утилизации, чтобы избежать загрязнения окружающей среды.
Он классифицируется как окислитель, что означает, что он может усиливать горение других материалов. KNO3 также может раздражать глаза, кожу и дыхательные пути и может быть токсичным при проглатывании или вдыхании в больших количествах. При работе с KNO3 важно надевать защитные средства, такие как перчатки, очки и респиратор, и хранить его в прохладном сухом месте вдали от легковоспламеняющихся материалов. Следует также соблюдать надлежащие методы утилизации, чтобы избежать загрязнения окружающей среды.
| Символы опасности | O, Xn |
| Описание техники безопасности | Хранить вдали от источников тепла/искр/открытого огня/горячих поверхностей. Наденьте защитные перчатки/защитные очки/защитную маску для лица. ПРИ ПРОГЛАТЫВАНИИ: При плохом самочувствии обратитесь в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР/к врачу. Прополоскать рот. Не вызывает рвоту. ПРИ ВДЫХАНИИ: Вынести пострадавшего на свежий воздух и обеспечить ему покой в удобном для дыхания положении. Позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР/к врачу. Позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР/к врачу. |
| Идентификаторы ООН | 1486 |
| Код ТН ВЭД | 2834.21.00 |
| Класс опасности | 5.1 |
| Группа упаковки | III |
| Токсичность | Может вызывать раздражение дыхательных путей, кашель и одышку при вдохнул. Может вызвать раздражение глаз и кожи. Проглатывание может вызвать боль в животе, тошноту, рвоту и диарею. Может быть токсичным при проглатывании или вдыхании в больших количествах. |
KNO3 можно синтезировать несколькими методами.
Одним из распространенных методов является реакция между гидроксидом калия и азотной кислотой. В реакционном сосуде два вещества смешиваются и нагреваются до высокой температуры, обычно около 80°C. После этого смесь остывает, и в процессе фильтрации собирается твердый KNO3.
Другим методом является реакция между хлоридом калия и нитратом натрия. Человек смешивает два вещества в реакционном сосуде и нагревает их до высокой температуры, обычно около 600°C.
Человек смешивает два вещества в реакционном сосуде и нагревает их до высокой температуры, обычно около 600°C.
Полученная смесь плавится, а затем затвердевает, образуя кристаллы KNO3.
Третий метод включает окисление аммиака азотной кислотой в присутствии катализатора. Этот метод более сложен и обычно используется в промышленных масштабах.
KNO3 можно добывать из природных источников, таких как пещеры и залежи в земле. Однако этот метод менее распространен из-за низких выходов и наличия примесей в экстрагируемом KNO3.
Использование нитрата калияKNO3 имеет широкий спектр применения в различных отраслях промышленности благодаря своим химическим свойствам. Вот некоторые распространенные области применения KNO3:
- Удобрение – Используется в качестве удобрения из-за высокого содержания азота и калия. Это особенно полезно для культур, требующих высокого уровня калия, таких как фрукты, овощи и табак.

- Консервация пищевых продуктов – также используется в качестве пищевого консерванта, особенно в колбасных изделиях. Подавляет рост бактерий и предотвращает порчу, продлевая срок годности продукта.
- Пиротехника – ключевой компонент в производстве фейерверков и других пиротехнических устройств. Он действует как окислитель, производя кислород для сжигания других материалов. Зубная паста
- — добавляется в некоторые зубные пасты для снижения чувствительности зубов. Он работает, блокируя передачу болевых сигналов от зубного нерва в мозг.
- Использование в медицине – Используется в медицине благодаря своим мочегонным и отхаркивающим свойствам. Он также лечит стенокардию и гипертонию.
- Промышленное применение — также используется в различных промышленных целях, таких как производство стекла, керамики и красителей.
В: Растворяется ли нитрат калия в воде?
О: Да, KNO3 хорошо растворяется в воде. При комнатной температуре в 100 граммах воды может раствориться примерно 37 граммов KNO3.
При комнатной температуре в 100 граммах воды может раствориться примерно 37 граммов KNO3.
В: Для чего используется нитрат калия?
A: KNO3 используется для различных целей, в том числе в качестве удобрения, пищевого консерванта, пиротехнического окислителя, ингредиента зубной пасты, а также в качестве компонента в производстве стекла, керамики и красителей.
В: Что такое нитрат калия?
A: Нитрат калия, также известный как селитра, представляет собой химическое соединение с формулой KNO3. Это ионная соль, состоящая из ионов калия (K+) и ионов нитрата (NO3-).
В: Что нейтрализует нитрат калия?
A: Ионы кальция и магния могут нейтрализовать вредное воздействие чрезмерного потребления KNO3 растениями. У людей не существует известного антидота при отравлении KNO3, и лечение является поддерживающим.
В: Растворяется ли kno3 в воде?
О: Да, KNO3 хорошо растворяется в воде.
В: Что является продуктом электролиза воды, содержащей низкую концентрацию kno3?
A: Продуктами электролиза воды с низкой концентрацией KNO3 являются газообразный водород (h3) и газообразный кислород (O2).

 SMT.01.334.2487499 от 30 сентября 2019 г.
SMT.01.334.2487499 от 30 сентября 2019 г.


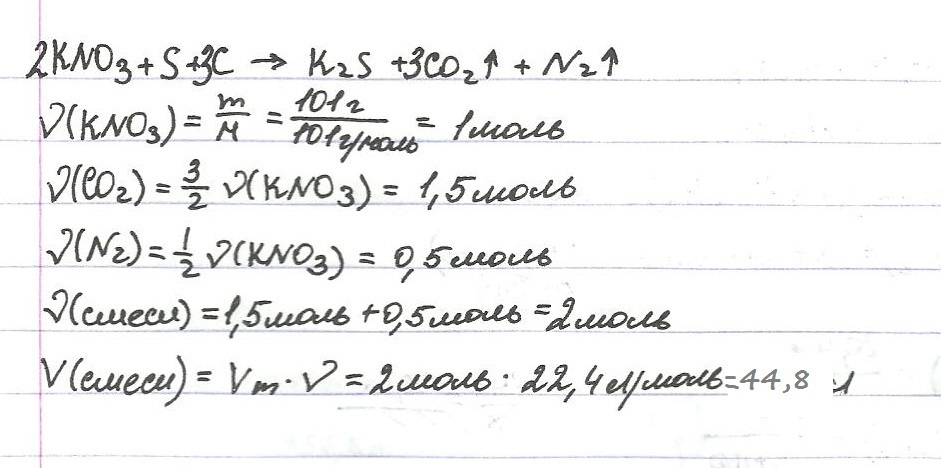
 Нитрат калия упаковывают в полипропиленовые мешки с полиэтиленовым вкладышем. Вес мешка: нетто 50 кг. А также — бумажные, полиэтиленовые мешки или полиэтиленовые мешки-вкладыши, вложенные в бумажные мешки, по нормативно-технической документации, которые обеспечивают сохранность продукции
Нитрат калия упаковывают в полипропиленовые мешки с полиэтиленовым вкладышем. Вес мешка: нетто 50 кг. А также — бумажные, полиэтиленовые мешки или полиэтиленовые мешки-вкладыши, вложенные в бумажные мешки, по нормативно-технической документации, которые обеспечивают сохранность продукции ..
..