Свойства нейтронов
- Главная
- Образование
- Свойства нейтронов
1.1. История нейтронного рассеяния.
В 1935 году профессор Джеймс Чадвик был удостоен Нобелевской премии за открытие нейтронов. Энрико Ферми в 1942 году показал, что нейтроны, которые образуются в результате деления ядра урана, могут поддерживать контролируемую цепную реакцию. Еще раньше, в 1938 году, он был удостоен нобелевской премии за открытие того, что замедленные нейтроны легко взаимодействуют с окружающим веществом и могут быть использованы для определения положений и колебаний атомов вещества.
За прошедшие 50 лет все больше ученых в областях физики, химии, биологии, материаловедения, геологии и многих других обращаются к использованию нейтронного рассеяния в поисках ответов на наиболее сложные проблемы в их областях исследований.
1.2. Источники нейтронов.
В настоящее время рассеяние нейтронов практических уходит от изучения атомной и магнитной структуры и динамики простых кристаллов. Акцент все более делается на изучении наноструктур, разупорядоченных систем, сложных химических реакций, процессов катализа. Расширяется активность в области исследования сложных жидкостей, самоорганизующихся систем, экзотических электронных состояний.
Все эти задачи могут быть поставлены и решены только на современных высокопоточных источниках нейтронов: ядерных реакторах, где используется контролируемая реакция деления ядер урана или плутония, или испарительных источниках на базе протонных ускорителей при бомбардировке тяжелых ядер протонами высоких энергий. Поток нейтронов может быть либо постоянным, либо пульсирующим. При таких процессах производимые нейтроны имеют большие значения энергии, что требует дополнительной установки на источник замедлителей нейтронов. В результате формируется поток нейтронов с длинами волн, сравнимыми с межатомными расстояниями в жидкостях и твердых телах, с кинетическими энергиями, сравнимыми с динамическими процессами в веществе.
Наиболее интенсивные источники нейтронов являются очень дорогими при создании и в обслуживании, и их количество в мире, вообще говоря, мало. В 1950 году был построен первый реактор, предназначенный непосредственно для научных исследований. Его единственной целью было производство как можно большей интенсивности нейтронного излучения. Со временем нейтронные источники превратились в универсальные научно-исследовательские установки, применимые в широком спектре экспериментальных исследований. В настоящее время чуть больше 30 лабораторий в мире оборудованы средне- и высокопоточными нейтронными установками. Научно-исследовательские нейтронные источники являются исключительно источниками нейтронов и неприменимы для каких либо других целей.
1.3. Свойства нейтронов.
Нейтрон является электрически нейтральной элементарной частицей, одной из составных частей ядра атома, с массой почти в 2000 раз тяжелее электрона.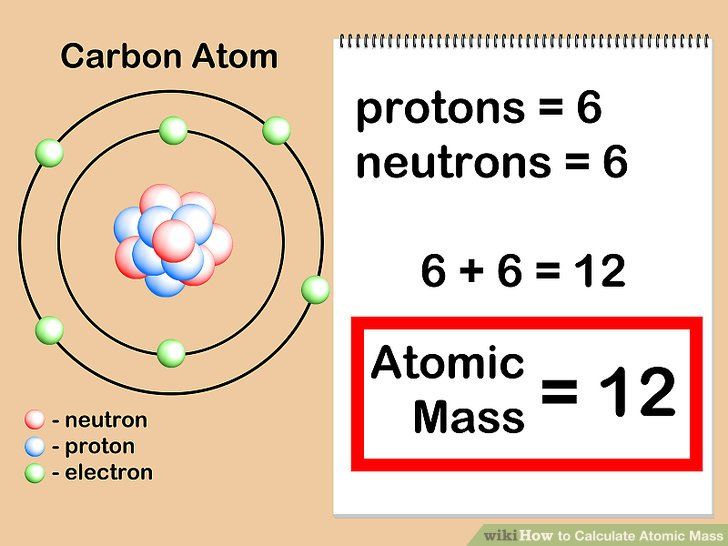 Время жизни нейтрона как свободной частицы около 15 минут, несмотря на то, что в связанном состоянии в ядре атома нейтрон является стабильной частицей.
Время жизни нейтрона как свободной частицы около 15 минут, несмотря на то, что в связанном состоянии в ядре атома нейтрон является стабильной частицей.
Основные свойства нейтронов, применяемые в нейтронном рассеянии:
- Энергия замедленных нейтронов сравнима с энергией атомных и молекулярных движений, и находится в диапазоне от мэВ до эВ.
- Длина волны замедленных нейтронов сравнима с межатомными расстояниями, что позволяет исследовать структуру вещества в диапазоне 10-5 – 105 Å.
- Поскольку нейтроны являются нейтральными частицами, они взаимодействуют с ядрами атомов, а не с диффузными электронными оболочками. Сечение рассеяния нейтронов на близких по массе ядрах может существенно отличаться, это дает возможность «видеть» легкие ядра на фоне тяжелых, эффективно применять метод изотопного замещения, легко различать соседние элементы. Эта особенность является большим преимуществом перед методом рентгеновского рассеяния, в котором излучение рассеивается на электронной оболочке атомов.

- наличие магнитного момента у нейтронов позволяет изучать микроскопическую магнитную структуру и магнитные флуктуации, которые определяют макроскопические параметры вещества.
- Нейтронное излучение является глубоко проникающим вглубь вещества, что позволяет проводить исследования микроскопических свойств, типа микротрещин, промышленных объектов. Подобные исследования невозможно выполнить с помощью оптических методов, рентгеновского рассеяния или электронной микроскопии.
- Нейтроны являются безвредным, неповреджающим излучением даже в случае исследования живых биологических систем.
Основное отличие нейтронного излучения от рентгеновского в том, что рассеяние нейтронов происходит на ядрах атомов. Следовательно, отсутствует необходимость учитывать атомный форм-фактор для описания формы электронного облака атома, кроме того, рассеивающая способность атома не убывает с увеличением угла рассеяния, что наблюдается для рентгеновского рассеяния.
Следует так же указать на одну важную особенность нейтронного излучения. Рентгеновское рассеяние практически нечувствительно к наличию атомов водорода в структуре, в то время как ядра водорода и дейтерия являются сильными рассеивателями для нейтронного излучения. Это означает, что с помощью нейтронов возможно намного более точно определить положение водорода и его тепловые колебания в кристаллической структуре. Более того, длины нейтронного рассеяния водорода и дейтерия имеют противоположные знаки, что позволяет применять технику «вариации контраста». Изменяя изотопный состав буфера образца (варьируя количество водорода и дейтерия), экспериментатор получает возможность менять вклад в рассеяние различных составных частей исследуемого объекта. На практике, тем не менее, не желательно работать с большими концентрациями водорода в образце, поскольку нейтронное рассеяние имеет большую неупругую компоненту при рассеянии на водороде.
Взято из открытых источников.
Ученый-астрофизик об атомах, из которых состоит все, что нас окружает
Так почему же банан и холодильник родственники?
1. А вот почему!
Биологи говорят, что ДНК человека и мыши совпадают на 80% (при определенном способе подсчета). Мы с мышами родственники, как и все млекопитающие, пусть и весьма дальние. Несколько десятков миллионов лет назад на Земле жили наши общие предки. Но это не все.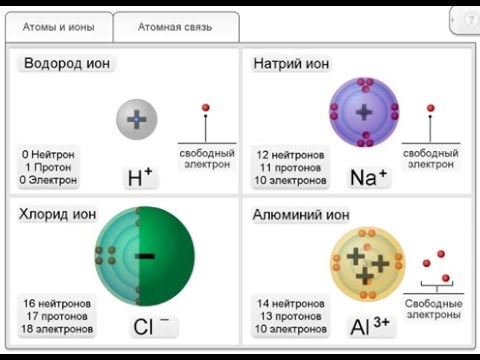 ДНК человека, продолжают биологи, на 50% также совпадает и с ДНК банана! И это тоже логично: ведь и мы, и растение представляем один и тот же мир органической жизни — земной жизни. Поэтому с тем бананом, что, возможно, сейчас хранится в вашем холодильнике, у вас также когда-то был общий предок. И это не метафора, а реальность. Вспомните об этом, когда соберетесь его съесть. Но, с точки зрения астрофизика, все еще гораздо интереснее: у вас был общий предок и с тем самым холодильником! И у банана, получается, тоже. Это тоже не метафора, а научно установленный факт. Попробую это объяснить.
ДНК человека, продолжают биологи, на 50% также совпадает и с ДНК банана! И это тоже логично: ведь и мы, и растение представляем один и тот же мир органической жизни — земной жизни. Поэтому с тем бананом, что, возможно, сейчас хранится в вашем холодильнике, у вас также когда-то был общий предок. И это не метафора, а реальность. Вспомните об этом, когда соберетесь его съесть. Но, с точки зрения астрофизика, все еще гораздо интереснее: у вас был общий предок и с тем самым холодильником! И у банана, получается, тоже. Это тоже не метафора, а научно установленный факт. Попробую это объяснить.
В действительности суть явления довольно проста. Все, что нас окружает, состоит из атомов. А сами атомы, за некоторым исключением, когда-то давно образовались в недрах звезд. Затем были выброшены в межзвездную среду, собрались вместе снова, снова были выброшены, для того чтобы опять стать звездами, планетами, камнями, растениями, разумными существами наконец.
И все бесчисленное разнообразие веществ и предметов нашей вселенной построено лишь на 120 видах различных атомов.
Немного из школьной программы. Каждый атом в общем случае состоит из положительно заряженного ядра, окруженного неким количеством отрицательно заряженных электронов. В свою очередь, ядро атома состоит из протонов (они и несут положительный заряд) и нейтронов (которые заряда не имеют вовсе), вместе называемых нуклонами. В принципе, можно пойти и дальше и рассказать, из чего сделаны нуклоны, но в нашем рассказе это не столь важно. Важно то, что один химический элемент от другого, с точки зрения физика, отличается именно количеством протонов в его ядре. Или, что то же самое, зарядом ядра, который, кстати, соответствует номеру элемента в таблице Менделеева. Так, у водорода — первого элемента — заряд один, и его ядро состоит из единственного протона. Ядро углерода (шестой элемент) — из шести протонов и шести нейтронов, а золота (79-й) — из 79 и 118 соответственно. При этом число нейтронов в атоме может быть различным — ядра с одним и тем же зарядом, но разным количеством нейтронов называют изотопами одного и того же элемента.
close
100%
Однако если электроны в атоме связаны с ядром не очень крепко — посредством электромагнитных сил, — то нуклоны в ядре держатся вместе благодаря сильному (оно так и называется) взаимодействию.
Поэтому оторвать электрон от атома или разделить пару атомов, связанных общим электроном, не так уж и сложно, что регулярно и случается.
А вот разделить на составляющие атомное ядро гораздо сложнее. Для этого необходимо затратить много энергии. Именно поэтому многие атомные ядра сами по себе, единожды образовавшись, могут существовать очень долгое время, на много порядков превышающее современный возраст Вселенной. По сути, вечно. А электроны — дело наживное. Поэтому рассказ об общих предках всего и всех — это рассказ об образовании атомов, а точнее об образовании атомных ядер. Как создавалось химическое разнообразие Вселенной, без которого наш мир был бы совсем не наш?
2. Ядерная кухня
А началось все, как водится, с Большого взрыва еще 13,7 млрд лет назад.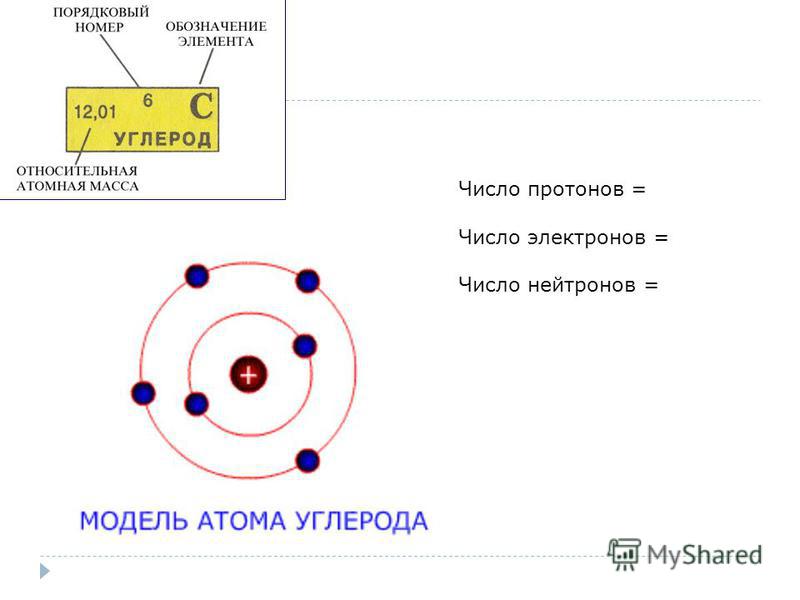 Образование самых первых атомных ядер — первичный нуклеосинтез — завершилось уже в первые 10–20 минут жизни Вселенной. В ту эпоху мир оказался заполнен преимущественно водородом (точнее, протонами), гелием, следующим за водородом элементом, некоторой примесью их изотопов и совсем исчезающе малым количеством чуть более тяжелых элементов, таких как литий и бериллий. Еще в ранней Вселенной были и свободные нейтроны, но их количество быстро уменьшалось, так как эта частица нестабильна и в свободном состоянии живет всего лишь 15 минут.
Образование самых первых атомных ядер — первичный нуклеосинтез — завершилось уже в первые 10–20 минут жизни Вселенной. В ту эпоху мир оказался заполнен преимущественно водородом (точнее, протонами), гелием, следующим за водородом элементом, некоторой примесью их изотопов и совсем исчезающе малым количеством чуть более тяжелых элементов, таких как литий и бериллий. Еще в ранней Вселенной были и свободные нейтроны, но их количество быстро уменьшалось, так как эта частица нестабильна и в свободном состоянии живет всего лишь 15 минут.
При этом нельзя сказать, что все из образовавшихся в первые минуты Вселенной протонов и легких ядер дожили до наших дней. Согласно законам квантовой механики субатомные частицы могут при определенных условиях превращаться друг в друга.
Что впоследствии неоднократно происходило и продолжает случаться по сей день.
Где-то через 500 млн лет после Большого взрыва начали образовываться первые звезды: особенно плотные облака газа первичного водорода начали коллапсировать (падать сами на себя) под действием собственной гравитации. В результате давление и температура в их центре возросли настолько, что отдельные протоны начали сталкиваться, сцепляться и образовывать протон-нейтронные пары (вспомним, что частицы могут превращаться друг в друга). После еще нескольких столкновений из таких пар собиралось ядро гелия, на создание которого, получается, было потрачено четыре протона. То есть запустился механизм синтеза более тяжелых ядер из более легких — термоядерный синтез. «Термо» — потому что он требует очень высоких температур, достижимых только в недрах звезд. И, что важно, этот процесс идет с выделением немалой энергии. Той самой, которая затем излучается звездами. Именно термоядерный синтез «зажигает» звезды, и поэтому говорят, что в их недрах «горят» легкие элементы. Для большинства объектов — водород.
В результате давление и температура в их центре возросли настолько, что отдельные протоны начали сталкиваться, сцепляться и образовывать протон-нейтронные пары (вспомним, что частицы могут превращаться друг в друга). После еще нескольких столкновений из таких пар собиралось ядро гелия, на создание которого, получается, было потрачено четыре протона. То есть запустился механизм синтеза более тяжелых ядер из более легких — термоядерный синтез. «Термо» — потому что он требует очень высоких температур, достижимых только в недрах звезд. И, что важно, этот процесс идет с выделением немалой энергии. Той самой, которая затем излучается звездами. Именно термоядерный синтез «зажигает» звезды, и поэтому говорят, что в их недрах «горят» легкие элементы. Для большинства объектов — водород.
Сборка сложных ядер тяжелых элементов из нескольких более легких есть ключевой механизм возникновения химического разнообразия Вселенной. Но реализовываться он может по-разному.
close
100%
Прямо сейчас в недрах нашего Солнца горит водород и образуется гелий.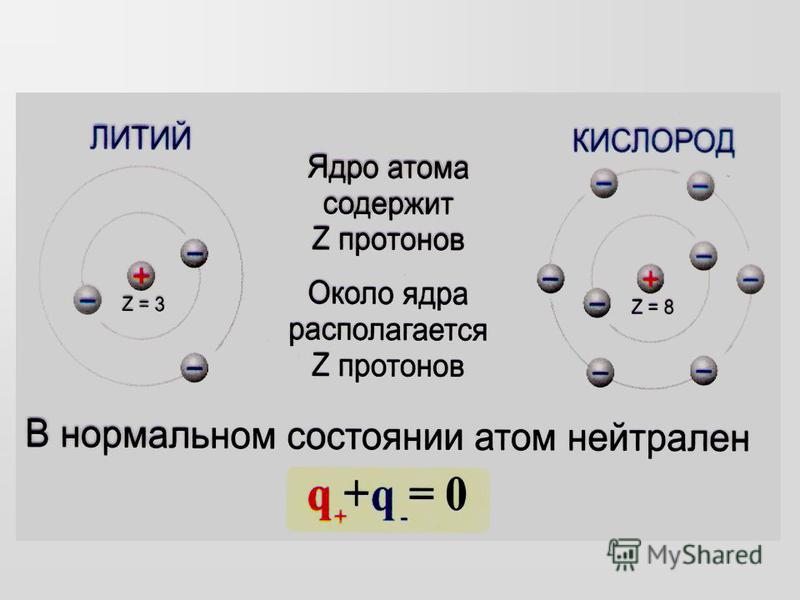 Примерно через 5 млрд лет водород в центре Солнца условно закончится, и эти реакции прекратятся. Но возникнут условия для возгорания образовавшегося гелия, что приведет к возникновению углерода и некоторого количества кислорода. Горение гелия будет продолжаться около 1 млрд лет и оставит после себя углеродное ядро Солнца, окруженное гелиевой и водородной оболочками.
Примерно через 5 млрд лет водород в центре Солнца условно закончится, и эти реакции прекратятся. Но возникнут условия для возгорания образовавшегося гелия, что приведет к возникновению углерода и некоторого количества кислорода. Горение гелия будет продолжаться около 1 млрд лет и оставит после себя углеродное ядро Солнца, окруженное гелиевой и водородной оболочками.
На этом термоядерный синтез в нашей звезде завершится.
Ее массы не хватает для того, чтобы впоследствии зажечь еще углерод. Но у более массивных звезд эти реакции синтеза идут дальше и гораздо быстрее, порождая больше кислорода, натрий, кальций, кремний (да-да, тот самый кремний, благодаря которому вы сейчас читаете с экрана этот текст), вплоть до железа (если масса звезды больше 8–10 солнечных) и никеля. И вот дальше начинаются проблемы. «Горение» железа в рамках термоядерного синтеза идет не с выделением энергии, а, наоборот, с ее поглощением. То есть энергетически невыгодно. И это замечательно! Потому что массивная звезда, в центре которой образовалось железное ядро, не может существовать в состоянии равновесия. Ведь именно давление горящего «термоядерного котла» удерживало их от коллапса. Теперь этот котел начал остывать, что в конечном итоге приводит к коллапсу ядра: за доли секунды оно сжимается в сотни раз до состояния 20-километровой нейтронной звезды (а то и вообще «в точку», то есть образуется черная дыра), а внешние слои звезды со всеми наработанными элементами разлетаются в пространство на скорости в десятки тысяч километров в секунду. Происходит взрыв сверхновой! Наконец-то фабрика по производству химических элементов нашла способ сбыть свою «продукцию». И ее «ассортимент» очень впечатляет. Там и алюминий для наших самолетов, и железо для нашей крови, не говоря уже о жизненно важных углероде и кислороде. Вспышки сверхновой — один из основных источников обогащения межзвездной среды «элементной» базой. Впоследствии эти разлетевшиеся осколки будут участвовать в строительстве новых звезд и планет.
Ведь именно давление горящего «термоядерного котла» удерживало их от коллапса. Теперь этот котел начал остывать, что в конечном итоге приводит к коллапсу ядра: за доли секунды оно сжимается в сотни раз до состояния 20-километровой нейтронной звезды (а то и вообще «в точку», то есть образуется черная дыра), а внешние слои звезды со всеми наработанными элементами разлетаются в пространство на скорости в десятки тысяч километров в секунду. Происходит взрыв сверхновой! Наконец-то фабрика по производству химических элементов нашла способ сбыть свою «продукцию». И ее «ассортимент» очень впечатляет. Там и алюминий для наших самолетов, и железо для нашей крови, не говоря уже о жизненно важных углероде и кислороде. Вспышки сверхновой — один из основных источников обогащения межзвездной среды «элементной» базой. Впоследствии эти разлетевшиеся осколки будут участвовать в строительстве новых звезд и планет.
Среди звезд нового поколения тоже будут массивные, и все повторится вновь.
Однако, напомню, речь пока идет только об элементах не тяжелее железа, которое не может участвовать в термоядерном синтезе.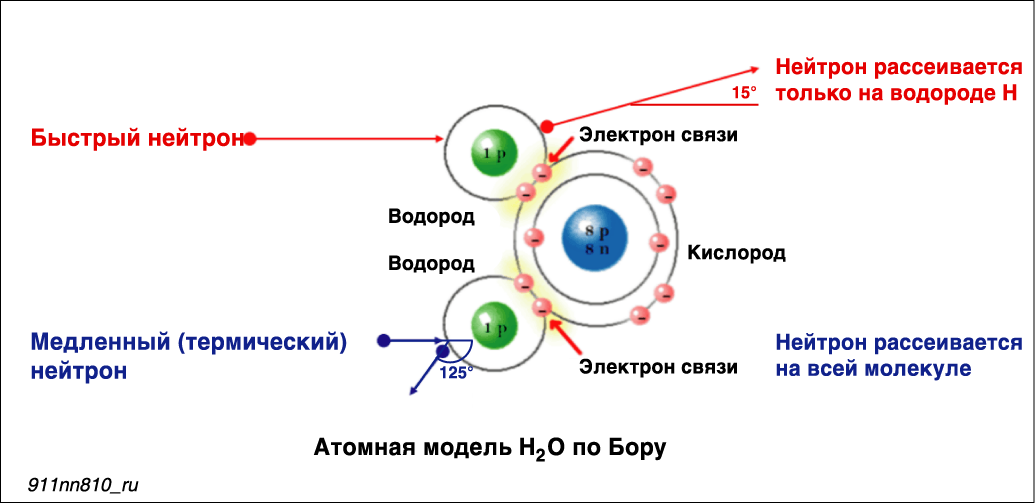 Более тяжелые элементы образуются несколько иначе. Но тоже, разумеется, в звездах.
Более тяжелые элементы образуются несколько иначе. Но тоже, разумеется, в звездах.
3. Не можешь производить — захватывай!
Как же сделать совсем тяжелые элементы? Да, в общем, так же, как и не очень тяжелые: необходимо к атомным ядрам присоединять дополнительные нуклоны. Только в данном случае речь идет не о протонах, а нейтронах. Их к тяжелому ядру (скажем, железа) присоединить порой легче. В ходе взрыва сверхновой разлетающиеся ядра железа, сталкиваясь с многочисленными нейтронами, могут обрастать своего рода шубой из этих частиц. Затем часть нейтронов распадется — превратится в протоны, что увеличит атомный номер ядра, и тем самым возникнет новый, более тяжелый, чем железо, элемент. Такой процесс называется быстрым процессом захвата нейтронов, или r-процессом. Он позволяет образовать ядра атомов вплоть до урана и плутония. То есть атомный взрыв на Земле был возможна благодаря когда-то прогремевшему взрыву сверхновой. Память о последнем все еще также хранят украшения из платины и отчасти из серебра.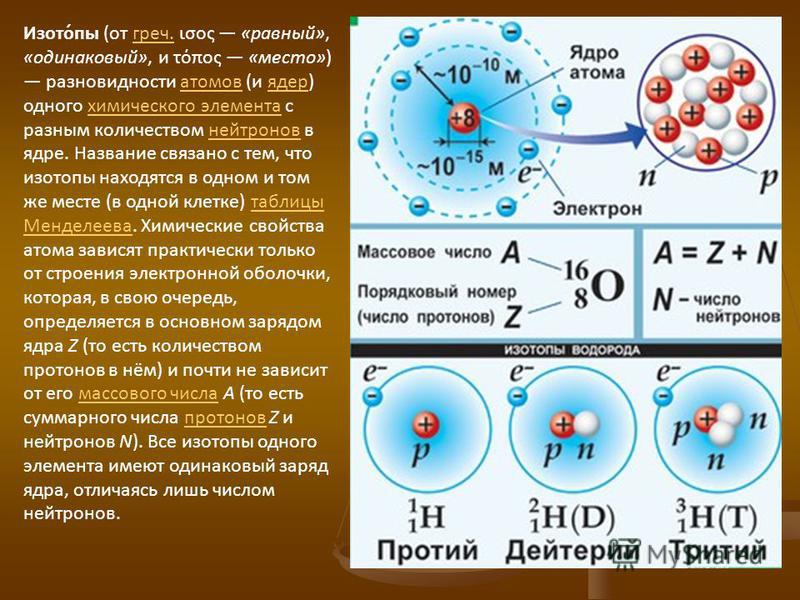 А еще свинец в автомобильном аккумуляторе и некоторые редкоземельные элементы.
А еще свинец в автомобильном аккумуляторе и некоторые редкоземельные элементы.
Кроме быстрого процесса захвата нейтронов существует еще и медленный. Он реализуется в недрах достаточно массивных звезд, пока в них еще идет термоядерных синтез. В отличие от своего «быстрого» аналога, здесь более легкие ядра захватывают нейтроны «по одному», что позволяет создать не самые-самые тяжелые элементы, но те, которые, все-таки тяжелее железа.
Сувениром, доставшимся нам от такого процесса, является, например, медная монета.
Ну или обычная медно-никелевая. Лампочка, заполненная парами ртути, или старая, с вольфрамовой спиралью, также стала возможна благодаря s-процессу захвата нейтронов в одной или нескольких массивных звездах.
В свою очередь, те из звезд, масса которых совсем невелика (вроде нашего Солнца), делятся со Вселенной наработанным материалом не так громко и пафосно, как сверхновые. Но очень красиво: они тихо сбрасывают внешнюю оболочку, порождая то, что мы потом называем планетарной туманностью. Такая судьба ждет и наше Солнце.
Такая судьба ждет и наше Солнце.
close
100%
4. Все то золото
close
100%
Однако на этом не заканчиваются способы создавать в природе химическое многообразие. Атомы некоторых элементов эффективнее всего рождаются в других, нетривиальных и очень красивых астрофизических процессах. Например, золото. Металл, который всегда был на особом счету у человечества. И по сей день он сопутствует нашей жизни не только в виде ювелирных украшений. Начинка гаджета, с которого вы сейчас читаете этот текст, наверняка содержит небольшое количество золота. Поэтому вы сейчас держите в руках (или просто смотрите, в зависимости от размеров гаджета) сувенир, оставшийся после довольно редкого события во Вселенной — слияния нейтронных звезд. Это те самые остатки эволюции массивных звезд, о которых говорилось выше. Звезды ведь часто рождаются двойными. Двойными они эволюционируют и двойными же могут и умирать.
В результате может возникнуть двойная нейтронная звезда (несколько таких мы даже знаем), которая со временем будет терять свой орбитальный момент.
Проще говоря, звезды начнут понемногу приближаться (спираливаться) друг к другу, теряя энергию на излучение гравитационных волн (об открытии которых было объявлено в этом году). И однажды они столкнутся. Столкновение пары сверхплотных, переобогащенных нейтронами тел запускает реакцию синтеза многих тяжелых элементов, разлетающихся в пространство с большими скоростями. В том числе и золота. По существующим оценкам (подтвержденных наблюдениями), в ходе одного такого столкновения может образоваться в 20 раз больше золота, чем масса всей нашей планеты! Так что нам досталась еще только малая часть того, что когда-то образовалось в ходе одного из таких слияний. Кстати, эти события довольно редки, так что по вселенским масштабам любой предмет из золота имеет особую ценность (но только отчасти: этот тяжелый металл также образуется и во вспышках сверхновых).
close
100%
5. Алхимия в природе
Еще один элемент, который в наш век цифровых технологий сопутствует нам даже чаще, чем золото, — это литий. Третий по легкости после водорода и гелия, он оказался очень удобен для производства аккумуляторов, называемых, естественно, литий-ионными. Литий хотя и образуется в звездах, но существует в жестких условиях их недр недолго. Значительная же часть того лития, который сейчас находится у нас на столах и в наших карманах, имеет другую историю. Вернемся опять к вспышке сверхновой звезды. Среди прочего она могла выбросить в межзвездную среду ядро атома свинца, в котором содержится 82 протона и 122 нейтрона.
Третий по легкости после водорода и гелия, он оказался очень удобен для производства аккумуляторов, называемых, естественно, литий-ионными. Литий хотя и образуется в звездах, но существует в жестких условиях их недр недолго. Значительная же часть того лития, который сейчас находится у нас на столах и в наших карманах, имеет другую историю. Вернемся опять к вспышке сверхновой звезды. Среди прочего она могла выбросить в межзвездную среду ядро атома свинца, в котором содержится 82 протона и 122 нейтрона.
Разогнавшись до гигантской скорости, это ядро начало свое путешествие по межзвездной среде.
Такие странствующие потоки частиц называются космическими лучами. Однако их путешествие не может длиться сколь угодно долго: космос не пуст. Его населяют не только звезды, но и газ, то есть одиночные частицы. Двигаясь с большой скоростью, ядро свинца за конечное время столкнется с одной из таких частиц, которая оставит на нем своего рода скол: отколет маленькую часть, состоящую при удаче из трех протонов и четырех нейтронов. Это не что иное, как стабильный изотоп лития, который уже затем попадет в молекулярное облако — прародитель Солнечной системы или просто на Землю. Что интересно, вторым остатком такого космического ДТП станет ядро, содержащее 79 протонов и 118 нейтронов. То есть ядро золота. Таким вот образом в естественной природе протекает реакция превращения свинца в золото.
Это не что иное, как стабильный изотоп лития, который уже затем попадет в молекулярное облако — прародитель Солнечной системы или просто на Землю. Что интересно, вторым остатком такого космического ДТП станет ядро, содержащее 79 протонов и 118 нейтронов. То есть ядро золота. Таким вот образом в естественной природе протекает реакция превращения свинца в золото.
6. Вещества из лаборатории
Для полноты картины стоит упомянуть, что вообще-то не все известные нам химические элементы возникли в астрофизических процессах. Речь идет о тех веществах, которые были созданы человеком в лаборатории в рамках эксперимента.
Метод создания при этом не отличается от природного и заключается в обстреливании ядер тяжелых элементов нуклонами или легкими ядрами с надеждой, что некоторые из них «приживутся».
На сегодняшний день был получен с десяток таких трансплутониевых элементов. Например, америций, эйнштейний или менделевий. Человек примеряет на себя функции звезды.
Впрочем, почему нет? Как, надеюсь, ясно из написанного, все мы и так когда-то уже как минимум один раз были звездами.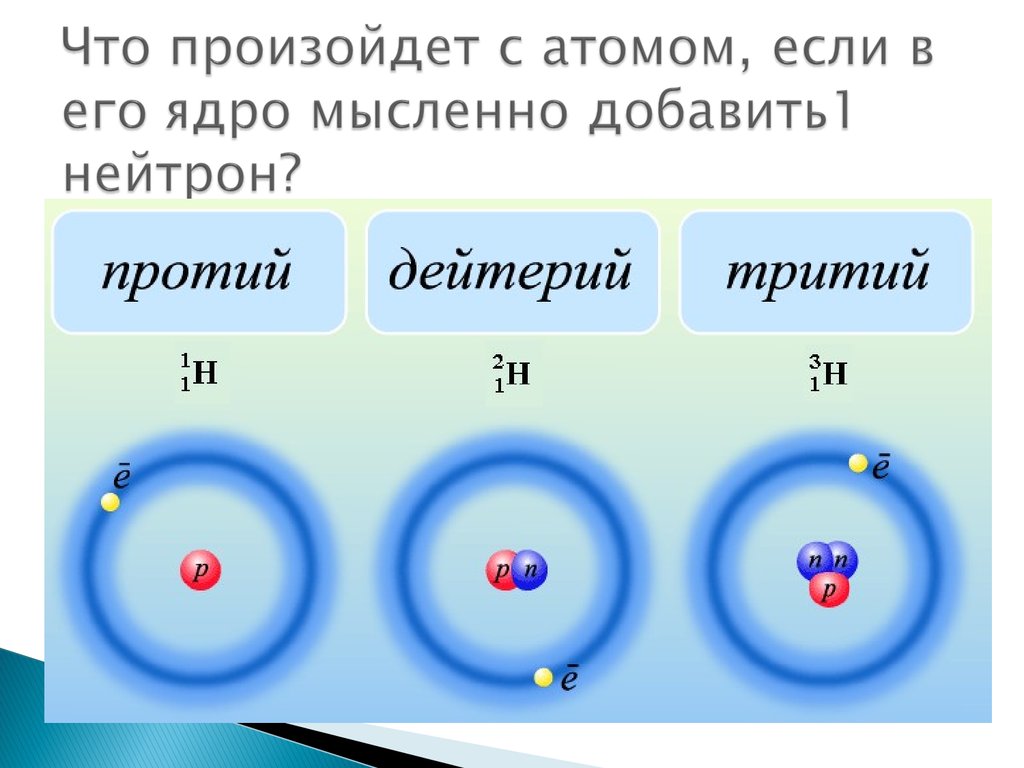 Одной или несколькими. И атомы нашей левой руки вполне могли образоваться в другой части Галактики, нежели атомы правой. И наоборот, наш непримиримый враг когда-то мог составлять с нами единое целое. Скорее всего, конечно, в виде звезды, но, может, и в виде планеты, а то и ее обитателей. У нас друг с другом и с нашим миром гораздо больше общего, чем может показаться на первый взгляд.
Одной или несколькими. И атомы нашей левой руки вполне могли образоваться в другой части Галактики, нежели атомы правой. И наоборот, наш непримиримый враг когда-то мог составлять с нами единое целое. Скорее всего, конечно, в виде звезды, но, может, и в виде планеты, а то и ее обитателей. У нас друг с другом и с нашим миром гораздо больше общего, чем может показаться на первый взгляд.
Что почитать:
http://nuclphys.sinp.msu.ru/astro/astro14.htm
http://physics.info/nucleosynthesis/
Атомная структура
Атомная структураИз чего состоит атом? Атом состоит из тяжелого ядра протонов (положительно заряженные частицы, записываются как p + ) и нейтроны (нейтральные частиц, записываемых как n o ), вокруг которых вращается облако чрезвычайно легкие электроны (отрицательно заряженные частицы, записываются как е — ).
Что определяет элемент?
Количество протонов в ядре каждого
атом.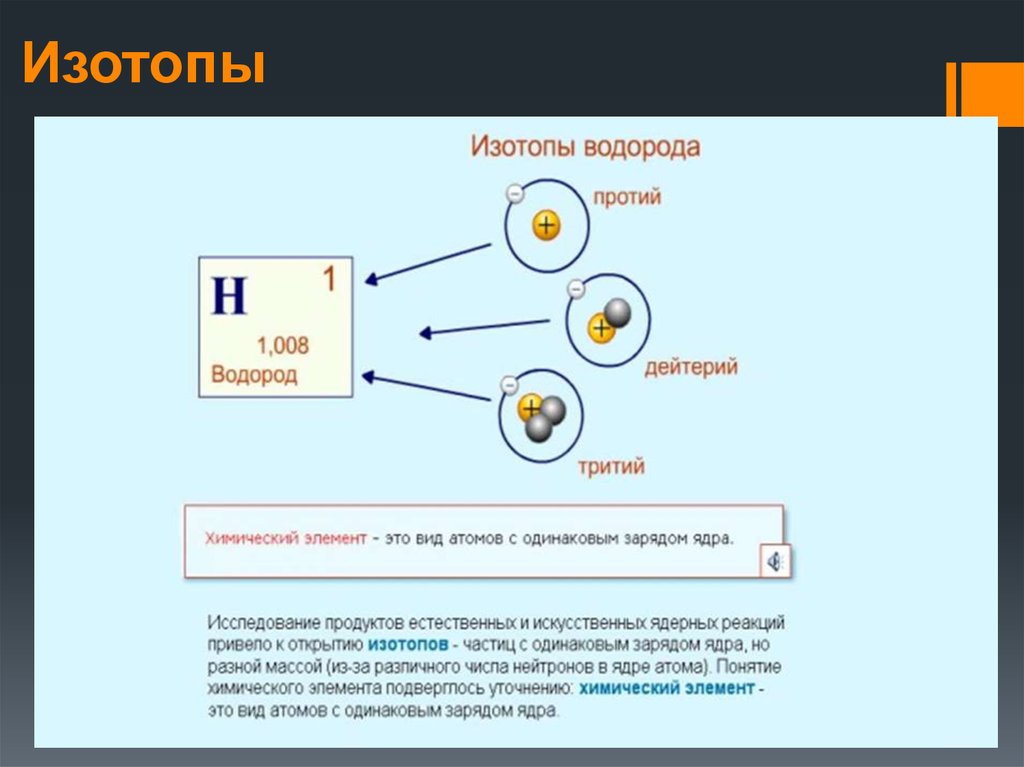
- Атомы водорода (H) имеют 1 протон.
- Атомы водорода с 1 протоном и 1 электроном нейтральны водород ( 1 Н 1 ).
- Атомы водорода с 1 протоном, 1 электроном и 1 нейтроном являются тяжелыми изотоп водорода, называемый дейтерием ( 2 H 1 ).
- Если к водороду добавить протон, мы получим другой элемент — гелий ( 4 He 2 ).
- Номенклатура: Для каждого элемента верхний индекс обозначает количество протоны и нейтроны, а нижний индекс число протонов.
- Сколько нейтронов содержится в нейтральном углероде ( 12 C 6 )?
Всего 12 нуклонов (нейтронов и протонов), и 6 протонов, поэтому должно быть 12 — 6 = 6 нейтронов. - Сколько нейтронов содержится в радиоактивном изотопе называется углерод-14 ( 14 C 6 )?
Всего имеется 14 нуклонов (нейтронов и протонов), и 6 протонов, поэтому должно быть 12 — 6 = 8 нейтронов.
Как строение атома или элемента говорит нам о том, как будет выглядеть его спектр?
- Электроны существуют в стационарных состояниях внутри атомов, каждое из которых определяется формулой дискретный, уникальный уровень энергии. Только определенные энергетические уровни, такие как орбиты с определенными радиусами.
- Свет или излучение, испускаемое или поглощаемое атомами при движении электронов из
одного энергетического уровня на другой можно рассматривать как поток кванты называются фотонами. Каждый фотон несет энергию E = h × v . Мы определяем
эти энергетические уровни следующим образом, говоря, что электрон находится в возбужденное состояние, когда у него есть дополнительная энергия (подумайте о ребенке, отскакивающем от
стены с волнением).
- основное состояние, самый низкий возможный уровень энергии
- Возбужденное состояние 1 st , следующий наивысший допустимый уровень энергии
- 2 nd возбужденное состояние, следующий самый высокий допустимый уровень энергии
- 3 rd возбужденное состояние, следующий наивысший допустимый уровень энергии
- .
 ..
.. - До точки, в которой электрон больше не связан с атомом
- Атом обычно имеет одинаковое количество протонов и электронов. Так как протоны имеют положительный заряд, а электроны — отрицательный, он переносит в этом состоянии нет заряда. Когда атом теряет (или приобретает) электрон, мы говорим что это ионизирует и несет электрический заряд.
Энтропия говорит нам, что все вещи естественным образом тяготеют к минимально возможному энергетическое состояние:
- Бревна и вода катятся вниз по склону.
- Прыгающие мячи замедляются до полной остановки.
- Люди ложатся спать ночью и с трудом встают утром.
- Точно так же атомы водорода склонны находиться в основном состоянии.
- Большинство фотонов пролетают мимо, не взаимодействуя с атомом.
- Но фотоны только с правильной энергией поглощаются атомом.

- В данном случае справа означает, что энергия фотона соответствует
разница энергетических уровней между допускала орбит в водороде
атома, а поглотил означает, что энергия фотона будет
поглощается атомом (оставляя атом в более высоком энергетическом состоянии).
- Фотон с частотой v будет поглощен атомом, если энергия фотона соответствует разнице уровней энергии между разрешенными состояний в атоме.
Что будет дальше?
- Помните, что энтропия ищет самый низкий доступный уровень энергии для всех вещи, так что электрон, поднятый на возбужденную орбиту, будет в конце концов вернуться в основное состояние.
- Сохранение энергии , говорит нам, что разница энергий
между возбужденным состоянием и основным состоянием должно появиться где-то, когда
электрон совершает переход. Он испускается атомом в виде фотона с
ту же энергию, что и исходная, которая была поглощена.

Вот схематическая диаграмма разрешенных орбит в атоме водорода. Если вы можете ответить на вопросы, перечисленные ниже, у вас есть правильная идея!
- Какие переходы соответствуют поглощению фотона? А и Д
- Какой переход соответствует испущенному фотону с самой высокой энергией ? С
- Какой переход соответствует фотонам с самой короткой длиной волны ? С
- Какой переход соответствует самой высокой частоте испускаемого фотона? С
Chem4Kids.com: Атомы: нейтроны
Материя | Атомы | Элементы | Периодическая таблица | Реакции | Биохимия | Все темы
Обзор | Структура | Орбиты | Электроны | Ионы | Нейтроны | Изотопы | Склеивание | Соединения | Составные имена | Радиоактивность и антивещество
Нейтроны — это частицы в атоме, имеющие нейтральный заряд .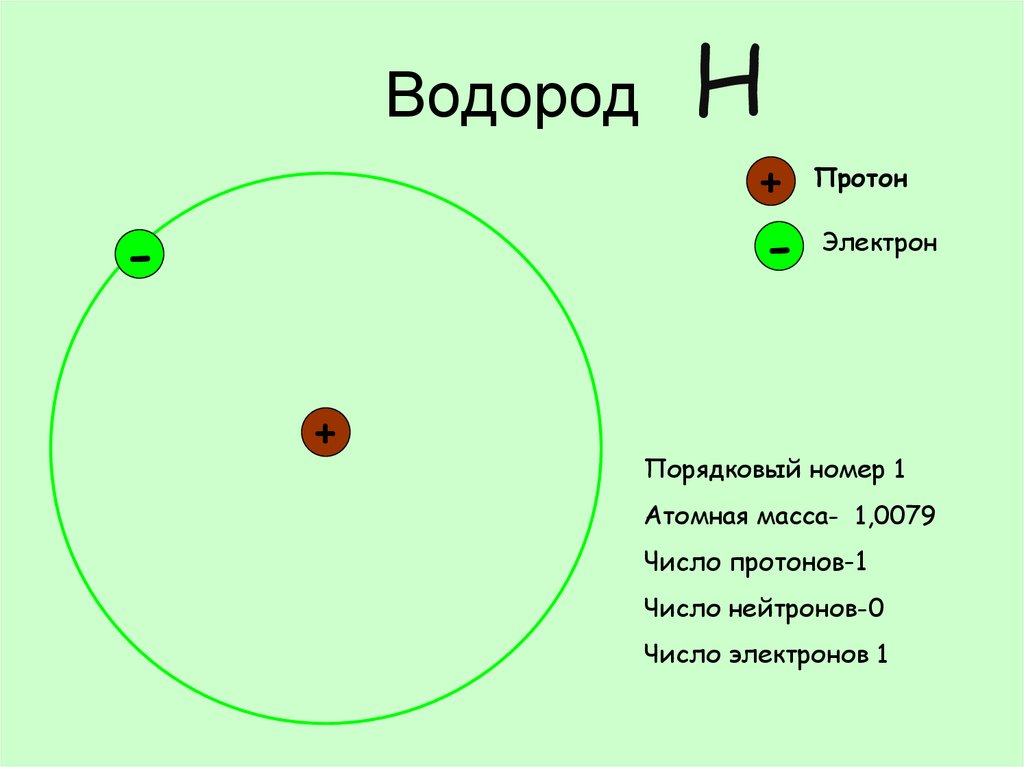 Они не положительны, как протоны. Они не отрицательны, как электроны. Но не начинайте думать, что они не важны. Каждая часть атома имеет огромное значение для того, как атом действует и ведет себя. Нейтроны не исключение.
Они не положительны, как протоны. Они не отрицательны, как электроны. Но не начинайте думать, что они не важны. Каждая часть атома имеет огромное значение для того, как атом действует и ведет себя. Нейтроны не исключение.
Итак, если атом имеет одинаковое количество электронов и протонов, заряды нейтрализуют друг друга, и атом имеет нейтральный заряд. Вы можете добавить в смесь тысячу нейтронов, и заряд не изменится. Однако если вы добавите тысячу нейтронов, вы создадите один сверхрадиоактивный атом. Нейтроны играют главную роль в массе и радиоактивный свойства атомов. Возможно, вы читали страницу об изотопах. Изотопы создаются при изменении нормального количества нейтронов в атоме.
Вы знаете, что нейтроны находятся в ядре атома. В нормальных условиях протоны и нейтроны слипаются в ядре. При радиоактивном распаде они могут быть выбиты оттуда. Нейтронные числа способны изменять массу атомов, потому что они весят примерно столько же, сколько протон и электрон вместе взятые.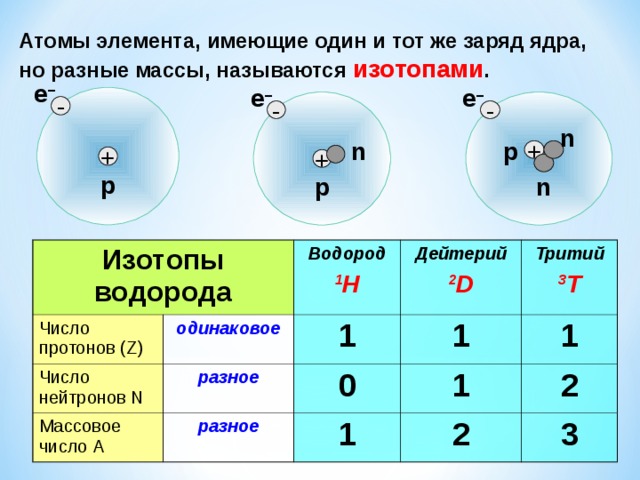 Если есть много атомов элемента, являющихся изотопами, средняя атомная масса этого элемента изменится. Мы говорили об углероде (С), имеющем среднюю массу 12,01. Это не сильно отличается от того, что можно было бы ожидать от атома с 6 протонами и 6 нейтронами. Количество изотопов углерода не сильно меняет атомную массу. По мере того, как вы продвигаетесь выше в таблице Менделеева, вы найдете элементы с гораздо большим количеством изотопов.
Если есть много атомов элемента, являющихся изотопами, средняя атомная масса этого элемента изменится. Мы говорили об углероде (С), имеющем среднюю массу 12,01. Это не сильно отличается от того, что можно было бы ожидать от атома с 6 протонами и 6 нейтронами. Количество изотопов углерода не сильно меняет атомную массу. По мере того, как вы продвигаетесь выше в таблице Менделеева, вы найдете элементы с гораздо большим количеством изотопов.
Разве мы говорили, что все атомы имеют нейтроны? Упс. Все элементы имеют атомы с нейтронами, кроме одного. Обычный атом водорода (H) не имеет нейтронов в своем крошечном ядре. Этот крошечный атом (самый крошечный из всех) имеет только один электрон и один протон. Вы можете убрать электрон и сделать ион, но вы не можете убрать ни одного нейтрона. Особая структура водорода становится очень важной, когда вы узнаете, как водород взаимодействует с другими элементами периодической таблицы. Если вы узнаете о ядерной fusion вы узнаете о дейтерии и тритии.



 ..
..
