Лучший ответ по мнению автора | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Посмотреть всех экспертов из раздела Учеба и наука
| Похожие вопросы |
Построить график функции y=2x-2 и определить проходит ли график через точку:A(10;-20)
Медиана равностороннего треугольника равна 13√3. Найдите его сторону.
Решение плиз
Найдите его сторону.
Решение плиз
Решено
В треугольнике ABC известно, ЧТО AB=5, BC=7, AC=9. Найдите cos угла ABC
Найдите площадь круга и длину ограничивающей его окружности, если сторона правильного треугольника, вписанного в него, равна 5√3 см. Напишите решение плиииз
В треугольнике ABC угол A равен 45 градусов, угол B равен 60 градусов, BC= 6√6. Найдите AC.
Пользуйтесь нашим приложением
что, как сбалансировать и часто задаваемые вопросы —
By Авниш Рават
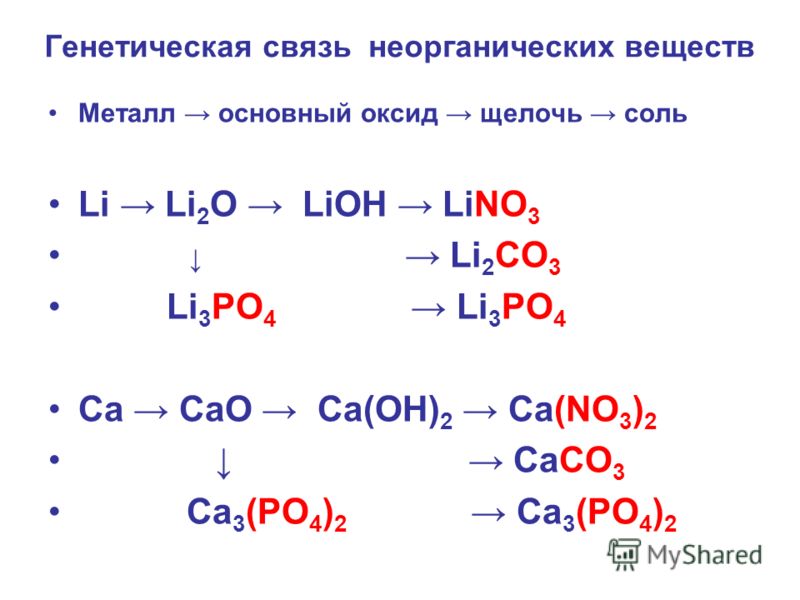
Бромистый водород отвечает за реакции присоединения свободных радикалов, которые присоединяются к алкенам. Сообщите нам о химической активности HBr и Li2O.
HBr обычно используется в качестве реагент в образовании различных бромистых соединений. Реакции с использованием HBr обычно катализируются платиной. Ли2O очень агрессивен по своей природе и поэтому реагирует с водой.
Реакционная способность HBr и Li2O производит осушитель, используемый в системах кондиционирования воздуха. Таким образом, важные характеристики химических веществ, основанные на реакциях, исследуются следующим образом.
Что является продуктом HBr и Li2O?HBr и Li2O взаимодействуют с образованием бромида лития и воды.
HBr + Li2O = LiBr + H2O
Какой тип реакции HBr + Li2O?HBr + Li2О является кислотным основанием нейтрализация реакция, в которой кислота (HBr) и основание (Li2O) реагирует с образованием соли (LiBr) и воды.
Как сбалансировать HBr + Li2O?Чтобы сбалансировать реакцию, можно использовать алгебраическую методологию, описанную ниже.
HBr + Li2O = LiBr + H2O,
- Каждый вид, присутствующий в уравнении, отмечен соответствующей переменной (A, B, C и D), чтобы проиллюстрировать неизвестные коэффициенты.

- А HBr + B Li2O = CLiBr + DH2O
- Затем для решения уравнения применяется подходящая величина, рассматриваемая как коэффициент реагентов и видов продукта.
- Li = 2A = C, O = A = D, H = B = 2D, Br = B = C
- Компания Гауссово исключение методология применяется для установления всех переменных и коэффициентов, и результаты
- А = 1, В = 2, С = 2 и D = 1
- Следовательно, общее сбалансированное уравнение:
- 2 HBr + Li2О= 2 LiBr + H2O
Данная система выполняется как кислотно-основное титрование. Неизвестная концентрация Li2O можно рассчитать титрованием стандартизированным раствором HBr.
АппаратыБюретка, пипетка, коническая колба, воронка, штативы, мерная колба, мензурки.
Фенолфталеин используется как индикатор при титровании лития.2О с HBr.
Процедура- Во-первых, неизвестный раствор HBr стандартизирован для использования в системе титрования.
- Затем стандартизированный раствор HBr пипеткой отбирают в коническую колбу.
- Наполните бюретку неведомой силой ли2O.
- Li2Затем раствор O по каплям добавляют из бюретки в коническую колбу, содержащую стандартный раствор HBr.
- Чтобы узнать конечную точку титрования, в коническую колбу добавляют немного индикатора и продолжают процесс, добавляя Li2O из бюретки до тех пор, пока окраска раствора не станет светло-розовой.
- Сила Ли2Используемый O рассчитывается с использованием M1V1= М2V2
- Где M1 = молярность раствора HBr, В1 = объем раствора HBr, M2 = молярность Li2О раствор, В2 = Объем лития2О решение
Компания чистое ионное уравнение HBr + Li2O is
2 H+ (водн. ) + Li2О (с) = 2 ли+2 (вод) + H2О (л)
) + Li2О (с) = 2 ли+2 (вод) + H2О (л)
- Напишите сбалансированное химическое уравнение и обозначьте соответственно физические состояния реагентов и продуктов
- 2 HBr (водн.) + Li2Операционные системы) = 2 LiBr (с) + H2О (л)
- Итак, сильные кислоты, основания и соли диссоциируют на ионы, тогда как чистые твердые вещества и молекулы не диссоциируют.
- Таким образом, результирующее ионное уравнение имеет вид
- 2 H+ (водн.) + Li2О (с) = 2 ли+2 (вод) + H2О (л)
HBr + Li2O-реакция имеет следующие сопряженные пары:
- Сопряженная пара кислоты HBr представляет собой Br–.
- Сопряженная пара базы Li2О представляет собой LiOH.

Межмолекулярные силы, действующие на HBr и Li2O составляют:
- Молекулы HBr взаимодействуют друг с другом с помощью диполь-дипольного взаимодействия и лондоновских дисперсионных сил.
- Li2O взаимодействует, образуя ионная связь.
HBr + Li2O демонстрирует энтальпия реакции -575.76 кДж/моль.
HBr + Li2О буферный раствор?HBr + Li2O не может сформировать буфер потому что HBr не является слабой кислотой, а Li2O не является солью сопряженного основания HBr.
HBr + Li2О полной реакции?HBr + Li2O является полной реакцией, потому что продукты (LiBr и вода), образующиеся в реакции, очень стабильны.
HBr + Li2O является экзотермической реакцией, поскольку при образовании ионного вещества (LiBr) выделяется тепло.
HBr + Li2О окислительно-восстановительная реакция?HBr + Li2O не окислительно-восстановительная реакция потому что окисление и восстановление не происходят одновременно. Степень окисления H и Li равна +1 как со стороны реагента, так и со стороны продукта.
HBr + Li2О реакция осаждения?HBr + Li2O не реакция осаждения потому что по окончании реакции осадок не образуется. Образовавшийся продукт представляет собой растворимую соль.
HBr + Li2О обратимая или необратимая реакция?HBr + Li2O есть необратимая реакция потому что однажды образовавшиеся продукты не могут быть превращены обратно в исходные реагенты в аналогичных условиях.
HBr + Li2O — это реакция двойного вытеснения поскольку оба анионных компонента реагентов вытесняются соответствующей катионной частью.
ВыводыРеакционная способность HBr + Li2O образуя ионную соль, LiBr представляет собой экзотермическую реакцию с двойным замещением. LiBr является полезным реагентом органического синтеза с широким применением в катализе гидроформилирования. Они используются для очистки простагландинов.
Кинетическое измерение и прогноз выделения водорода из поликристаллической системы LiH/Li2O/LiOH — Страница 25 из 33
PDF-файл: 33 страницы; размер: 4,1 Мбайт
Это артикул входит в состав сборника под названием:
Управление научно-технической информации Технические отчеты и
был предоставлен в Электронную библиотеку ЕНТ
Отделом государственных документов библиотек ЕНТ.
Посмотреть полное описание этой статьи.
Эти элементы управления являются экспериментальными и еще не оптимизированы для пользователей.
яркость
Сброс яркости 0
контраст
Сброс контрастности 0
насыщенность
Сброс насыщенности 0
заточить «/>
Сброс резкости 0
экспозиция
Сброс экспозиции 0
оттенок
Сбросить оттенок 0
гамма
Сброс Гамы 0
Применение фильтров
Предыдущий элемент Следующий элемент
Следующий текст был автоматически извлечен из изображения на этой странице с помощью программного обеспечения для оптического распознавания символов:
(a
F~
-(; - 5 -
:~r5
Это
2 15 р
(д)У
200 м
Рис.
3
Предстоящие страницы
Вот что будет дальше.
Поиск внутри
Эта статья может быть найдена. Примечание: Результаты могут различаться в зависимости от разборчивости текста в документе.
Поиск
Инструменты/Загрузки
Получите копию этой страницы или просмотрите извлеченный текст.
Preview все размеры или…
- Скачать Миниатюра
- Скачать Маленький
- Скачать Medium
- Скачать Большой
- JSON-изображение IIF
- Изображение IIIF
Просмотр извлеченного (OCR) текста
Цитирование и распространение
Основная информация для ссылки на эту веб-страницу. Мы также предоставляем
расширенное руководство по правам использования, ссылкам, копированию или встраиванию.
Мы также предоставляем
расширенное руководство по правам использования, ссылкам, копированию или встраиванию.
Ссылка на текущую страницу этой статьи.
Дин, Л.Н.; Грант, Д.М.; Шильдбах, Массачусетс; Смит, Р.А.; Зикхаус, WJ; Балаш, Б. и соавт. Кинетическое измерение и прогноз выделения водорода из поликристаллической системы LiH/Li2O/LiOH, статья, 6 апреля 2005 г .; Ливермор, Калифорния. (https://digital.library.unt.edu/ark:/67531/metadc874466/m1/25/: по состоянию на 11 марта 2023 г.), Библиотеки Университета Северного Техаса, цифровая библиотека ЕНТ, https://digital.library.unt.edu; зачисление отдела государственных документов библиотек ЕНТ.
Распечатать / поделиться этой страницей
- Скопировать URL
- Встроить средство просмотра
- IIIF
Постоянный URL (эта страница)
Univesal Viewer
International Image Interoperability Framework (эта страница)
Прямое наблюдение in situ за выделением Li2O на богатом литием катодном материале большой емкости, Li[Ni(x)Li((1-2x)/3)Mn((2-x)/3)]O2 (0 ≤ x ≤ 0,5)
. 2014 22 января; 136 (3): 999-1007.
2014 22 января; 136 (3): 999-1007.
doi: 10.1021/ja410137s. Epub 2014 8 января.
Солнечный Хай 1 , Феликс Феликс, Джон Рик, Вей-Ньен Су, Бинг Джо Хван
Принадлежности
принадлежность
- 1 Лаборатория наноэлектрохимии, кафедра химического машиностроения, Тайваньский национальный университет науки и технологии, Тайбэй, Тайвань 10607.
- PMID: 24364760
- DOI: 10.1021/ja410137s
Санни Хай и др.
J Am Chem Soc. .
.
. 2014 22 января; 136 (3): 999-1007.
doi: 10.1021/ja410137s. Epub 2014 8 января.
Авторы
Санни Хай 1 , Феликс Феликс, Джон Рик, Вей-Ньен Су, Бинг Джо Хван
принадлежность
- 1 Лаборатория наноэлектрохимии, кафедра химического машиностроения, Тайваньский национальный университет науки и технологии, Тайбэй, Тайвань 10607.
- PMID: 24364760
- DOI: 10.1021/ja410137s
Абстрактный
Многослойные оксидные катоды с высоким содержанием лития демонстрируют большие перспективы для использования в качестве материалов положительного электрода для перезаряжаемых литий-ионных аккумуляторов. Понимание влияния реакций активации кислорода на поверхности катода во время электрохимического циклирования может привести к улучшению стабильности и производительности. Мы использовали поверхностно-усиленную рамановскую спектроскопию (SERS) in situ для наблюдения поверхностных реакций, связанных с кислородом, которые происходят во время электрохимического циклирования на катодах, богатых литием. Здесь мы демонстрируем прямое наблюдение за образованием Li2O во время расширенного плато и обсуждаем последствия его образования на катоде и аноде. Образование Li2O на катоде приводит к образованию частиц, связанных с образованием h3O вместе с LiOH, и к изменениям внутри электролита, что в конечном итоге приводит к снижению производительности. Защита или смягчение таких разрушительных поверхностных реакций на обоих электродах будет необходимо, чтобы помочь реализовать потенциал катодных материалов высокой емкости (270 мА·ч·г(-1) против 140 мА·ч·г(-1) для LiCoO2) для практического применения.
Понимание влияния реакций активации кислорода на поверхности катода во время электрохимического циклирования может привести к улучшению стабильности и производительности. Мы использовали поверхностно-усиленную рамановскую спектроскопию (SERS) in situ для наблюдения поверхностных реакций, связанных с кислородом, которые происходят во время электрохимического циклирования на катодах, богатых литием. Здесь мы демонстрируем прямое наблюдение за образованием Li2O во время расширенного плато и обсуждаем последствия его образования на катоде и аноде. Образование Li2O на катоде приводит к образованию частиц, связанных с образованием h3O вместе с LiOH, и к изменениям внутри электролита, что в конечном итоге приводит к снижению производительности. Защита или смягчение таких разрушительных поверхностных реакций на обоих электродах будет необходимо, чтобы помочь реализовать потенциал катодных материалов высокой емкости (270 мА·ч·г(-1) против 140 мА·ч·г(-1) для LiCoO2) для практического применения.
Похожие статьи
Роль содержания Mn в электрохимических свойствах богатых никелем слоистых катодов LiNi(0,8-x)Co(0,1)Mn(0,1+x)O₂ (0,0 ≤ x ≤ 0,08) для литий-ионных аккумуляторов.
Чжэн Дж., Кан В.Х., Мантирам А. Чжэн Дж. и др. Интерфейсы приложений ACS. 1 апреля 2015 г .; 7 (12): 6926-34. doi: 10.1021/acsami.5b00788. Epub 2015 19 марта. Интерфейсы приложений ACS. 2015. PMID: 25756196
Катоды из слоистых микросфер с высоким содержанием никеля: разупорядочение лития/никеля и электрохимические характеристики.
Фу К., Ли Г., Луо Д., Ли К., Фан Дж., Ли Л. Фу С и др. Интерфейсы приложений ACS. 24 сентября 2014 г.; 6(18):15822-31. дои: 10.1021/am5030726. Epub 2014 9 сентября. Интерфейсы приложений ACS.
 2014.
PMID: 25203668
2014.
PMID: 25203668Детальные исследования электродного материала большой емкости для аккумуляторных батарей Li2MnO3-LiCo(1/3)Ni(1/3)Mn(1/3)O2.
Ябуучи Н., Йоши К., Мён С.Т., Накаи И., Комаба С. Ябуучи Н. и др. J Am Chem Soc. 2011 30 марта; 133 (12): 4404-19. дои: 10.1021/ja108588y. Epub 2011 4 марта. J Am Chem Soc. 2011. PMID: 21375288
Достижения в области литий-кислородных батарей, основанные на образовании и разложении гидроксида лития.
Чжан С, Донг П, Сун М.К. Чжан X и др. Фронт хим. 2022 1 июля; 10:923936. doi: 10.3389/fchem.2022.923936. Электронная коллекция 2022. Фронт хим. 2022. PMID: 35844634 Бесплатная статья ЧВК. Обзор.
Перспективы литий-ионных аккумуляторов, связанных с электромобильностью: катоды с высокой удельной энергией и химически активные сепараторы.

Сусай Ф.А., Склар Х., Шилина Ю., Пенки Т.Р., Раман Р., Маддукури С., Майти С., Халалай И.С., Луски С., Марковский Б., Аурбах Д. Сусай Ф.А. и соавт. Adv Mater. 2018 Окт;30(41):e1801348. doi: 10.1002/adma.201801348. Epub 2018 17 июля. Adv Mater. 2018. PMID: 30015994 Обзор.
Посмотреть все похожие статьи
Цитируется
Изготовление гетероструктур для повышения структурной стабильности катодов с высоким содержанием лития.
Li Y, Zhao Q, Zhang M, Qiu L, Zheng Z, Liu Y, Sun Y, Zhong B, Song Y, Guo X. Ли Ю и др. АСУ Омега. 2023 13 февраля; 8 (7): 6720-6728. doi: 10.1021/acsomega.2c07313. Электронная коллекция 2023 21 февраля. АСУ Омега. 2023. PMID: 36844563 Бесплатная статья ЧВК.
Микробный пиразиндиамин представляет собой новую добавку к электролиту, которая защищает высоковольтные катоды LiNi 1/3 Co 1/3 Mn 1/3 O 2 .

Гупта А., Бадам Р., Такамори Н., Минакава Х., Масуо С., Такая Н., Мацуми Н. Гупта А. и др. Научный представитель 2022 г., 25 ноября; 12 (1): 19888. doi: 10.1038/s41598-022-22018-1. Научный представитель 2022. PMID: 36434117 Бесплатная статья ЧВК.
Перспективная фаза с высоким содержанием лития на основе молибдена для литий-ионных аккумуляторов.
Ван Ю, Чжоу Х, Цзи Х. Ван Ю и др. RSC Adv. 2019 5 июня; 9 (31): 17852-17855. дои: 10.1039/c9ra03449h. Электронная коллекция 2019 4 июня. RSC Adv. 2019. PMID: 35520583 Бесплатная статья ЧВК.
Последние достижения в разработке катодных материалов для литий-ионных аккумуляторов.
Мохамед Н., Аллам Н.К. Мохамед Н. и др. RSC Adv.


 05.18
05.18

 2014.
PMID: 25203668
2014.
PMID: 25203668