Нейтронные копилки
Алексей Левин
«Популярная механика» №1, 2008
Группе физиков из университета штата Мичиган в Ист-Лансинге удалось получить сверхтяжелые изотопы магния с более чем двойным избытком нейтронов над протонами.
Сейчас известно примерно три сотни стабильных изотопов и вдесятеро больше радиоактивных, в основном полученных в лабораториях. Стабильные изотопы сравнительно легких элементов обычно содержат примерно поровну нуклоны обеих разновидностей — нейтроны и протоны.
Национальная циклотронная лаборатория, расположенная в кампусе Мичиганского университета, располагает двумя ускорителями на сверхпроводящих магнитах, которые обычно работают в тандеме. Первая машина доводит энергию ионов до 40–50 МэВ на нуклон, вторая — примерно до 140 МэВ. Именно они и использовались в эксперименте. В качестве снарядов выступали стабильные ядра кальция-48, имеющего восемь избыточных нейтронов по сравнению с основным изотопом кальцием-40, а мишенью послужила вольфрамовая пластинка примерно миллиметровой толщины. Отдельные ядра кальция при соударениях с ядрами вольфрама захватывали их нейтроны и одновременно теряли собственные протоны. В результате рождались нестабильные нуклонные конгломераты, которые быстро распадались и превращались в ядра магния-40 и алюминия-42, живущие не меньше миллисекунды.
Отдельные ядра кальция при соударениях с ядрами вольфрама захватывали их нейтроны и одновременно теряли собственные протоны. В результате рождались нестабильные нуклонные конгломераты, которые быстро распадались и превращались в ядра магния-40 и алюминия-42, живущие не меньше миллисекунды.
Естественно, такие события происходили нечасто, примерно одно на квадриллион (1015). Во всяком случае, экспериментаторам удалось зарегистрировать три ядра магния-40 и двадцать три ядра алюминия-42. Кроме того, было зарегистрировано одно событие, соответствующее еще более тяжелому алюминию-43. Для извлечения этой информации продукты реакций пришлось дважды отcепарировать и пропустить сквозь систему высокочувствительных детекторов.
Ядра стабильных изотопов легких элементов обычно состоят из примерно равного количества нейтронов и протонов. Так, ядро углерода-12 составлено из шести протонов и шести нейтронов, а кислорода — из восьми. Это правило не вполне универсально, богатый нейтронами кальций-48 обладает особо устойчивым дважды магическим ядром и потому живет практически вечно (его период полураспада почти в миллион раз больше возраста нашей Вселенной).
Однако к более тяжелым элементам оно уже неприменимо. Протоны отталкиваются друг от друга по закону Кулона, и хотя в самых легких ядрах такое отталкивание может быть компенсировано межнуклонным притяжением при равном числе протонов и нейтронов, уже на третьем десятке элементов периодической системы для компенсации нужны дополнительные нейтроны, скрепляющие ядра наподобие клея (а ядерные силы, в отличие от кулоновских, действуют лишь на очень малом расстоянии). Так что по мере возрастания атомного номера в ядрах накапливается избыток нейтронов. У самых тяжелых стабильных изотопов их число превышает число протонов примерно в полтора раза.
Линии жизни
Линия протонной устойчивости прослежена вплоть до очень тяжелых элементов. Нейтронную линию определить сложнее, и сейчас она достоверно выяснена лишь для первых восьми элементов — от водорода до кислорода. Для следующей тройки — фтора, неона и натрия — она определена лишь приблизительно (так, есть основания полагать, что натрий может иметь не более 26 нейтронов).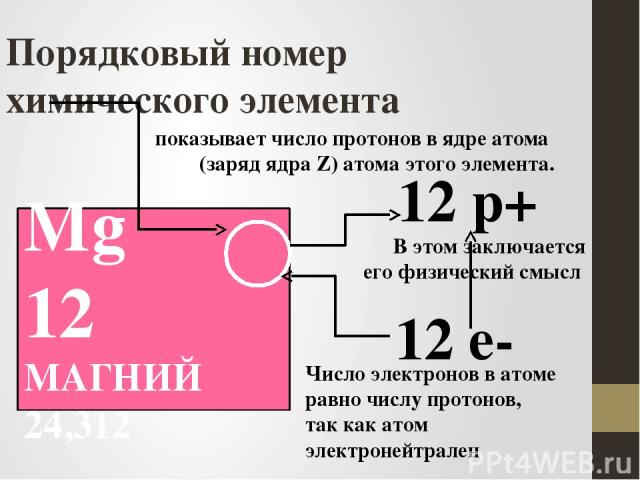 Магний и алюминий занимают двенадцатое и тринадцатое места в таблице Менделеева. Новые эксперименты в Ист-Лансинге показали, что ядро магния «выдерживает» не менее 28 нейтронов. Это куда больше числа нейтронов у трех его стабильных изотопов — 12, 13 и 14. Единственный стабильный изотоп алюминия содержит 14 нейтронов, однако в прошлом физики ухитрились получить множество радиоактивных вариантов этого элемента. Самый легкий из них содержит 9 нейтронов, а самый тяжелый — 28. Теперь же оказалось, что природа разрешает существовать и алюминию-42 с 29 нейтронами, и алюминию-43 — с тридцатью.
Магний и алюминий занимают двенадцатое и тринадцатое места в таблице Менделеева. Новые эксперименты в Ист-Лансинге показали, что ядро магния «выдерживает» не менее 28 нейтронов. Это куда больше числа нейтронов у трех его стабильных изотопов — 12, 13 и 14. Единственный стабильный изотоп алюминия содержит 14 нейтронов, однако в прошлом физики ухитрились получить множество радиоактивных вариантов этого элемента. Самый легкий из них содержит 9 нейтронов, а самый тяжелый — 28. Теперь же оказалось, что природа разрешает существовать и алюминию-42 с 29 нейтронами, и алюминию-43 — с тридцатью.
От первого лица
«Моя группа вот уже лет двадцать занимается экспериментальным определением линии нейтронной устойчивости. Эта работа производится и в других странах, в частности во Франции, — рассказал «ПМ» профессор химии Мичиганского университета Дэвид Морриссей. — Что касается последних экспериментов, то самым большим сюрпризом было рождение алюминия-42. Он содержит нечетные числа протонов и нейтронов, а такие ядра отличаются минимальной устойчивостью. Можно надеяться, что удастся создать и более тяжелые изотопы этого элемента, скажем, алюминий-45, но это очень непросто. Надеюсь, мы продолжим эксперименты будущим летом».
Можно надеяться, что удастся создать и более тяжелые изотопы этого элемента, скажем, алюминий-45, но это очень непросто. Надеюсь, мы продолжим эксперименты будущим летом».
«Наша группа еще в июне прошлого года сообщила о получении тридцатинейтронного кремния-44, — добавляет другой участник эксперимента, сотрудник Лаборатории ядерных реакций дубнинского Объединенного института ядерных исследований Олег Тарасов. — Все эти результаты позволяют уточнить параметры моделей, которые используются для расчета свойств ядер. Кроме этого, они демонстрируют потенциал нашей лаборатории как по части оборудования, то есть ускорителей и спектрометров, так и по части квалификации научных кадров. В 1990-х наилучшими возможностями обладали исследователи, работающие на французском Большом национальном ускорителе тяжелых ионов. Потом пальма первенства перешла к японцам. А теперь — к Мичиганскому университету».
В поисках острова стабильности
А что же сулят эти результаты химикам? Этот вопрос «Популярная механика» задала научному сотруднику Мюнхенского технического университета Александру Якушеву, который вот уже много лет работает с искусственными изотопами сверхтяжелых элементов. «Физики из Дубны в последние годы получили в реакциях слияния актинидных мишеней с всё тем же кальцием-48 около тридцати новых изотопов химических элементов вплоть до элемента 118. Некоторые из них являются долгожителями и распадаются лишь спустя несколько секунд после появления на свет — этого достаточно, чтобы провести анализ их химических свойств. Химиков по-прежнему манит остров стабильности, предсказанный в районе Z = 114 и N = 184, где время жизни ядер должно повыситься еще на несколько порядков, однако высадиться там еще нельзя из-за недостатка нейтронов.
«Физики из Дубны в последние годы получили в реакциях слияния актинидных мишеней с всё тем же кальцием-48 около тридцати новых изотопов химических элементов вплоть до элемента 118. Некоторые из них являются долгожителями и распадаются лишь спустя несколько секунд после появления на свет — этого достаточно, чтобы провести анализ их химических свойств. Химиков по-прежнему манит остров стабильности, предсказанный в районе Z = 114 и N = 184, где время жизни ядер должно повыситься еще на несколько порядков, однако высадиться там еще нельзя из-за недостатка нейтронов.
Пока что нет возможности изыскать такую комбинацию мишени и налетающей частицы, чтобы в сумме получился достаточный нейтронный избыток. Кроме сложных реакций многонуклонной передачи между очень тяжелыми ядрами (такими как столкновение двух ядер урана) альтернативным путем может оказаться бомбардировка мишени радиоактивными нейтроноизбыточными изотопами (конечно, не столь экзотическими, как представленные в работе ученых из Ист-Лансинга). Так что поиск границы нейтронной стабильности идет рука об руку с получением интенсивных пучков нейтроноизбыточных изотопов, столь необходимых для прыжка на остров стабильности».
Так что поиск границы нейтронной стабильности идет рука об руку с получением интенсивных пучков нейтроноизбыточных изотопов, столь необходимых для прыжка на остров стабильности».
Строение атома. Химическая связь. Тест
Категория: Химия.
Строение атома. Химическая связь. Тест
Вариант – I
А1. Каков заряд ядра атома магния?
А) +24 Б) +36 В) +12 Г) -12
А2. Определите элемент, если в его атоме 40 электронов
А) алюминий Б) цирконий В) германий Г) галлий
А3. Чему равняется количество протонов, нейтронов и электронов в атоме фосфора?
А) р=31, n=16, е=31 Б) р=15, n=15, е=15 В) р=15, n=31, е=15 Г) р=15, n=16, е=15
А4. Каков физический смысл порядкового номера элемента
А) это число энергетических уровней в атоме Б) это заряд ядра атома В) это относительная атомная масса Г) это число нейтронов в ядре
А5. Каков физический смысл номера периода таблицы Д. И. Менделеева?
А) это заряд ядра атома Б) это число электронов на внешнем энергетическом уровне В) это число электронов в атоме Г) это число энергетических уровней в атоме
А6.
А) порядковому номеру Б) номеру периода
В) номеру группы Г) числу нейтронов в ядре
А7. Укажите количество электронов на внешнем энергетическом уровне в атоме хлора
А) 2 Б) 5 В) 7 Г) 17
А8. Укажите пару химических элементов, между которыми может возникнуть ковалентная неполярная связь
А) водород и фосфор Б) натрий и фтор В) кислород и натрий Г) азот и азот
А9. Укажите формулу соединения с ковалентной полярной связью
А) O2 Б) CF4 В) KBr Г) P4
А10. Атому, какого химического элемента соответствует электронная формула 1S22S22P2
А) углерод Б) сера В) магний Г) гелий
А11. В ядре атома, какого химического элемента 7 протонов и 8 нейтронов
А) фтор Б) азот В) фосфор Г) кислород
А12. Молекулярная масса вещества с химической формулой H 2SO4
А) 100 Б) 98 В) 56 Г) 124
В1. Установите
соответствие между типом химической связи и формулой соединения
Установите
соответствие между типом химической связи и формулой соединения
Вид химической связи
А) Ковалентная неполярная
Б) Ионная
В) Ковалентная полярная
Г) Металлическая
Химическое соединение
1) N2O5 2) CaCl2
3) Zn 4) O3
5) K3P 6) HF
С1. Найдите массовую долю натрия в составе соды Na2CO3
Вариант – II
А1. Каков заряд ядра атома цинка?
А) -30 Б) +35 В) +65 Г) +30
А2. Определите элемент, если в его атоме 25 электронов
А) титан Б) хром В) марганец Г) бром
А3. Чему равняется количество протонов, нейтронов и электронов в атоме кальция?
А) р=20, n=40, е=20 Б) р=40, n=20, е=40 В) р=20, n=20, е=20 Г) р=40, n=40, е=40
А4. Каков физический смысл порядкового номера элемента
А) это число нейтронов в ядре Б) это число протонов в ядре атома В) это число энергетических уровней в атоме Г) это относительная атомная масса
А5. Каков физический смысл номера периода таблицы
Д. И. Менделеева?
Каков физический смысл номера периода таблицы
Д. И. Менделеева?
А) это заряд ядра атома Б) это число электронов на внешнем энергетическом уровне В) это число электронов в атоме Г) это число энергетических уровней в атоме
А6. Чему равно общее число электронов атома
А) порядковому номеру Б) номеру периода
В) номеру группы Г) числу нейтронов в ядре
А7. Укажите количество электронов на внешнем энергетическом уровне в атоме азота
А) 2 Б) 5 В) 7 Г) 17
А8. Укажите пару химических элементов, между которыми может возникнуть ионная связь
А) водород и кислород Б) фтор и углерод В) литий и хлор Г) хлор и хлор
А9. Укажите формулу соединения с ковалентной неполярной связью
А) O2 Б) CF4 В) KBr Г) P4
А10. Атому, какого химического элемента соответствует электронная формула 1S22S22P63S1
А) литий Б) натрий В) калий Г) кремний
А11. В ядре атома,
какого химического элемента 8 протонов и 8 нейтронов
В ядре атома,
какого химического элемента 8 протонов и 8 нейтронов
А) фтор Б) азот В) фосфор Г) кислород
А12. Молекулярная масса вещества с химической формулой P2O5
А) 142 Б) 64 В) 150 Г) 124
В1. Установите соответствие между типом химической связи и формулой соединения
Вид химической связи
А) Ковалентная неполярная
Б) Ионная
В) Ковалентная полярная
Г) Металлическая
Химическое соединение
1) MgCl2 2) Br2
3) Zn 4) H2
5) Ca 6) HCl
С1. Найдите массовую долю алюминия в составе глинозема Al2O3
М. Д. Скоркина, МБОУ Белогорская СОШ, Кемеровская область
Метки: Химия
Новые измерения экзотического магния предполагают неожиданное изменение формы – Центр новостей
Это оборудование на японском заводе по производству пучков радиоактивных изотопов в Вако, Япония, использовалось в эксперименте по созданию экзотического изотопа магния.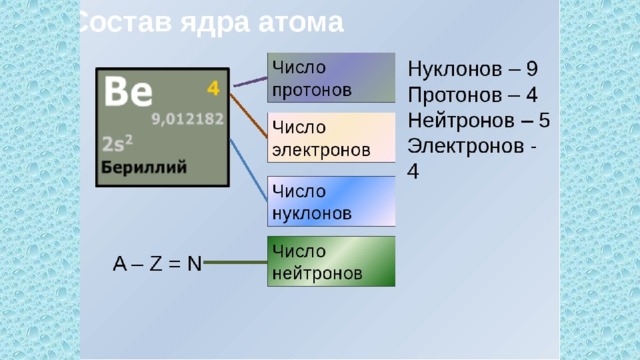 (Источник: Хизер Кроуфорд/Лаборатория Беркли) )
(Источник: Хизер Кроуфорд/Лаборатория Беркли) )
Чуть более десяти лет назад ученые довели атомы магния до новых пределов, запихивая в их ядра дополнительные нейтроны, приближаясь и, возможно, достигнув максимального предела для этого элемента.
Теперь международная группа под руководством ученых из Национальной лаборатории Лоуренса в Беркли Министерства энергетики (Berkeley Lab) воспроизвела эту экзотическую систему, известную как магний-40, и получила новые и удивительные сведения о ее ядерной структуре.
«Магний-40 находится на перекрестке, где возникает много вопросов о том, как он выглядит на самом деле», — сказала Хизер Кроуфорд, штатный научный сотрудник отдела ядерных наук в лаборатории Беркли и ведущий автор этого исследования, опубликованного в Интернете 15 февраля. 7 в журнале Physical Review Letters. «Это чрезвычайно экзотический вид».
В то время как количество протонов (имеющих положительный электрический заряд) в его атомном ядре определяет атомный номер элемента – место в периодической таблице – количество нейтронов (не имеющих электрического заряда) может различаться. Самый распространенный и стабильный тип атома магния, встречающийся в природе, имеет 12 протонов, 12 нейтронов и 12 электронов (имеющих отрицательный заряд).
Самый распространенный и стабильный тип атома магния, встречающийся в природе, имеет 12 протонов, 12 нейтронов и 12 электронов (имеющих отрицательный заряд).
Изображение «коктейля» вторичного пучка, полученного в циклотронном центре в Японии для исследования Mg-40, экзотического изотопа магния. Ось X показывает отношение массы к заряду, а ось Y показывает атомный номер. Это изображение было размещено на обложке журнала Physical Review Letters. (Источник: Х.Л. Кроуфорд и др., Phys. Rev. Lett. 122, 052501, 2019 г.)
Атомы одного и того же элемента с разным числом нейтронов известны как изотопы. Изотоп магния-40 (Mg-40), который изучали исследователи, имеет 28 нейтронов, что может быть максимумом для атомов магния. Для данного элемента максимальное количество нейтронов в ядре называется «линией нейтронного капельного полива» — если вы попытаетесь добавить еще один нейтрон, когда он уже заполнен, лишний нейтрон немедленно «стечет» из ядра. .
«Он чрезвычайно богат нейтронами, — сказал Кроуфорд.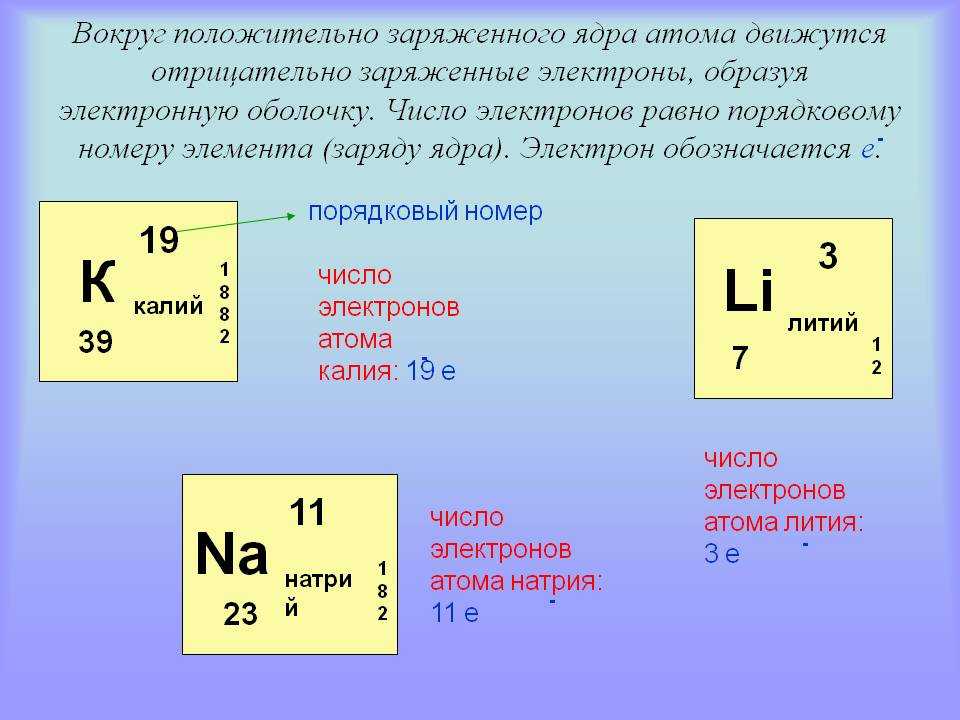 «Неизвестно, находится ли Mg-40 на линии капельного полива, но наверняка очень близко. Это один из самых тяжелых изотопов, который в настоящее время можно экспериментально получить вблизи капельной линии».
«Неизвестно, находится ли Mg-40 на линии капельного полива, но наверняка очень близко. Это один из самых тяжелых изотопов, который в настоящее время можно экспериментально получить вблизи капельной линии».
Форма и структура ядер вблизи границы стока особенно интересны физикам-ядерщикам, потому что они могут научить их фундаментальным вещам о том, как ядра ведут себя в экстремальных условиях существования.
«Интересный вопрос, который постоянно возникает у нас в голове, когда вы подходите так близко к линии капельного полива, звучит так: «Изменяется ли способ расположения нейтронов и протонов?», — сказал Пол Фэллон, старший научный сотрудник отдела ядерных наук лаборатории Беркли. Отдел и соавтор исследования. «Одной из основных целей в области ядерной физики является понимание структуры от ядра элемента до линии капельного полива».
Такое фундаментальное понимание может дать информацию о теориях взрывных процессов, таких как создание тяжелых элементов при слиянии звезд и взрывах, сказал он.
Исследование основано на экспериментах на заводе по производству пучков радиоактивных изотопов (RIBF), расположенном в Центре ускорительных исследований RIKEN Nishina в Вако, Япония. Исследователи объединили мощность трех циклотронов — типа ускорителя частиц, впервые разработанного основателем лаборатории Беркли Эрнестом Лоуренсом в 19 году.31 — для создания пучков частиц очень высокой энергии, движущихся со скоростью около 60 процентов от скорости света.
Исследовательская группа использовала мощный пучок кальция-48, стабильного изотопа кальция с магическим числом протонов (20) и нейтронов (28), чтобы поразить вращающийся диск из углерода толщиной в несколько миллиметров.
Некоторые ядра кальция-48 столкнулись с ядрами углерода, в некоторых случаях образовав изотоп алюминия, известный как алюминий-41. Ядерно-физический эксперимент отделил эти атомы алюминия-41, которые затем были направлены на удары по пластику толщиной в несколько сантиметров (CH 2 ) цель.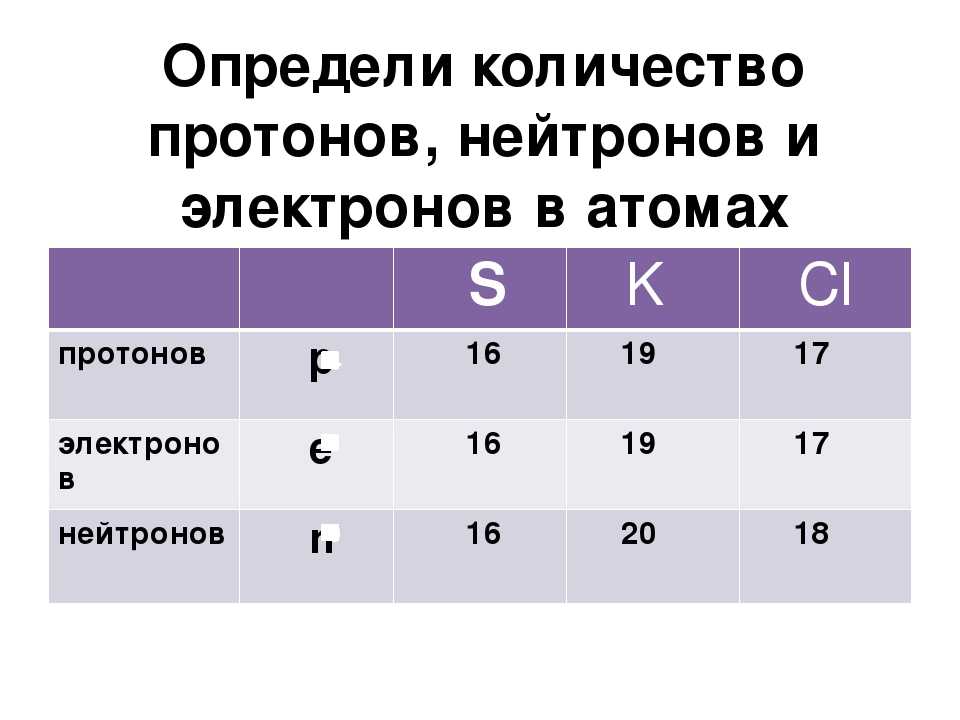 Удар этой вторичной мишенью выбил протон из некоторых ядер алюминия-41, создав ядра Mg-40.
Удар этой вторичной мишенью выбил протон из некоторых ядер алюминия-41, создав ядра Mg-40.
Эта вторая мишень была окружена детектором гамма-излучения, и исследователи смогли исследовать возбужденные состояния Mg-40 на основе измерений гамма-лучей, испускаемых при взаимодействии луча с мишенью.
В дополнение к Mg-40 измерения также зафиксировали энергии возбужденных состояний в других изотопах магния, включая Mg-36 и Mg-38.
«Большинство моделей говорили, что Mg-40 должен быть очень похож на более легкие изотопы, — сказал Кроуфорд. «Но это не так. Когда мы видим что-то, что выглядит совсем по-другому, задача новых теорий состоит в том, чтобы зафиксировать все это».
Поскольку теперь теории расходятся с тем, что было замечено в экспериментах, необходимы новые расчеты, чтобы объяснить, что меняется в структуре ядер Mg-40 по сравнению с Mg-38 и другими изотопами.
Исследование, проведенное лабораторией Беркли, опубликовано на обложке журнала Physical Review Letters. (Источник: Physical Review Letters)
(Источник: Physical Review Letters)
Фэллон сказал, что многие расчеты предполагают, что ядра Mg-40 сильно деформированы и, возможно, имеют форму футбольного мяча, поэтому два добавленных нейтрона в Mg-40 могут жужжать вокруг ядра, формируя так называемое ядро гало, а не встраиваясь в него. форма, которую демонстрируют соседние изотопы магния.
«Мы размышляем о некоторых физических явлениях, но это должно быть подтверждено более подробными расчетами», — сказал он.
Кроуфорд сказал, что дополнительные измерения и теоретическая работа над Mg-40 и соседними изотопами могут помочь точно определить форму ядра Mg-40 и объяснить, что вызывает изменение в ядерной структуре.
Исследователи отметили, что Центр ядерной физики для пучков редких изотопов, новый Центр науки Министерства энергетики США, который строится в Мичиганском государственном университете, в сочетании с массивом отслеживания энергии гамма-излучения (GRETA), строящимся в лаборатории Беркли, позволит дальнейшие исследования других элементов вблизи ядерной границы.
Исследователи Центра Нисина RIKEN и кампуса RIKEN в Сайтаме, Осакского университета, Токийского университета и Токийского технологического института в Японии; Университет Святой Марии и ТРИУМФ в Канаде; Институт ядерной физики во Франции; Йоркский университет в Великобритании; и Центр исследований тяжелых ионов им. Гельмгольца GSI в Германии также участвовали в исследовании.
Эта работа была поддержана Управлением науки Министерства энергетики США, Королевским обществом и Советом по научно-техническим средствам Великобритании.
###
Национальная лаборатория Лоуренса в Беркли, основанная в 1931 году на убеждении, что самые большие научные проблемы лучше всего решаются командами, и ее ученые были отмечены 13 Нобелевскими премиями. Сегодня исследователи из лаборатории Беркли разрабатывают устойчивые энергетические и экологические решения, создают новые полезные материалы, расширяют границы вычислительной техники и исследуют тайны жизни, материи и Вселенной. Ученые со всего мира полагаются на оборудование лаборатории для своих собственных научных открытий. Лаборатория Беркли — это многопрофильная национальная лаборатория, управляемая Калифорнийским университетом для Управления науки Министерства энергетики США.
Ученые со всего мира полагаются на оборудование лаборатории для своих собственных научных открытий. Лаборатория Беркли — это многопрофильная национальная лаборатория, управляемая Калифорнийским университетом для Управления науки Министерства энергетики США.
Управление науки Министерства энергетики США является крупнейшим сторонником фундаментальных исследований в области физических наук в Соединенных Штатах и работает над решением некоторых из самых насущных проблем нашего времени. Для получения дополнительной информации посетите веб-сайт science.energy.gov .
Сколько протонов, нейтронов и электронов содержит атом магния с массовым числом 25?
Ответ
Проверено
222,6 тыс.+ просмотров
Подсказка: Ответ здесь основан на базовой концепции химии, которая использует формулу для нахождения количества протонов, нейтронов и электронов, основанную на периодической таблице. и определяется по формуле: количество протонов = массовое число – количество нейтронов нейтронов.
и определяется по формуле: количество протонов = массовое число – количество нейтронов нейтронов.
Полный пошаговый ответ:
— Мы знакомы с представлениями об атомах, их строении, составе, а также о свойствах из основных понятий химии.
Давайте теперь обновим эти понятия, чтобы мы могли вывести правильный ответ.
— Атом — это мельчайшая частица, которая может существовать, из которой построена вся Вселенная. Он состоит из центрального ядра, состоящего из положительно заряженных частиц, называемых протонами, и нейтральных частиц, называемых нейтронами.
— Отрицательно заряженные электроны вращаются вокруг орбиты ядра.
— Протоны — это не что иное, как тот, который дает атомный номер, и всегда количество протонов равно количеству электронов, и поэтому они равны.
— Нейтроны и протоны вместе составляют массу элемента, и эти присутствующие нейтроны могут быть рассчитаны с использованием массового числа, которое дается формулой: количество протонов = массовое число — количество нейтронов нейтронов.
