Атомная энергия. Том 16, вып. 2. — 1964 — Электронная библиотека «История Росатома»
Атомная энергия. Том 16, вып. 2. — 1964 — Электронная библиотека «История Росатома»Главная → Указатель произведений
ЭлектроннаябиблиотекаИстория Росатома
Ничего не найдено.
Загрузка результатов…
Закладки
Обложка979899100101102103104105106107108109110111112113114115116117118119120121122123124125126127128129130131132133134135136137138139140141142143144145146147148149150151152153154155156157158159160161162163164165166167168169170171172173174175176177178179180181182183184185186187188Обложка (с. 3)
Увеличить/уменьшить масштаб
По ширине страницы
По высоте страницы
Постранично/Разворот
Поворот страницы
Навигация по документу
Закладки
Поиск в издании
Структура документа
Скопировать текст страницы
(работает в Chrome 42+,
Microsoft Internet Explorer и Mozilla FireFox
c установленным Adobe Flash Player)
Добавить в закладки
Текущие страницы выделены рамкой.
Содержание
ОбложкаОбложка
97Титульный лист
98Содержание
99Статьи
99Адамов И. Ю., Душин Л. А., Кононенко В. И., Павличенко О. С.
Микроволновое излучение безэлектродного индукционного разряда 103Бродер Д. Л., Колесов В. Е., Лашук А. И., Садохин И. П., Довбенко А. Г.
Сечения возбуждения уровней Mg, Cr52, Ni58, Ni60 и Nb93 при неупругом рассеянии нейтронов 110Игнатьев К. Г., Кирпичников И. В., Сухоручкин С. И.
Измерение η и парциальных сечений изотопов U235 и Pu239 для нейтронов резонансных энергий 119Франк-Каменецкий А. Д.
Применение метода Монте-Карло для многогруппового расчета реакторов 123Жежерун И. Ф.
Изучение влияния пустых каналов в среде замедлителя на длину диффузии тепловых нейтронов 130Несмеянова Г. М., Викулов А. И.
Влияние некоторых соединений галогенов на окисление U(IV) в сернокислой среде 134Спицын В. И., Дьячкова Р. А.
Концентрирование Pa138Письма в редакцию
138Жилейко Г. И.
И.
Воробьев Г. А.
О работе схемы Аркадьева — Маркса с высокой скважностью 141Брилль О. Д., Панкратов В. М., Рудаков В. П., Рыбаков Б. В.
Сечение реакций T(d, n)He4 и D(d, n)He3 в интервале энергий дейтонов 3—19 Мэв 144Драпчинский Л. В., Коваленко С. С., Петржак К. А., Тютюгин И. И.
Отношение вероятностей тройного деления U235 и U238 нейтронами с различной энергией 145Беда А. Г., Кондратьев Л. Н., Третьяков Е. Ф.
Сечение активации Cd108 тепловыми нейтронами 146Крисюк И. Т.
Оценка вклада изотопов иода и брома в процесс испускания запаздывающих нейтронов 148Малкин Л. З., Алхазов И. Д., Кривохатский А. С., Петржак К. А., Белов Л. М.
Спонтанное деление Cm244 с испусканием длиннопробежной α-частицы 149Зайцев В. В., Каплан С. А.
К теории нестационарного многократного комптоновского рассеяния γ-квантов 151Руденко В. Н.
Дорошенко Г. Г., Филюшкин И. В.
Спектры быстрых нейтронов Po — Be-источника, прошедших водяную защиту 154Отставнов П. С.
Потоки быстрых и замедленных нейтронов в помещениях 155Иохельсон С. В., Попов Д. К.
О содержании Sb125 в почвенном покрове и растениях160Новости науки и техники
160Чувило И. В.
Слабые взаимодействия элементарных частиц 164Усачев Л. Н., Абрамов А. И., Дорохов В. В., Ютландов И. А.
II Международная конференция по нуклидным массам 169Сизов И. В.
Совещание по ядерной физике низких энергий 171Б. Х.
IV Международная конференция по неразрушающим методам контроля 173Гольдин М.
Применение изотопов на Украине 174Синицын В. И.
Применение методов γ-дефектоскопического контроля в некоторых странах — членах СЭВ 176Ю. Т.
Дозиметры и радиометры на выставке приборов ядерной техники стран — членов СЭВ 180Николаева А.
181Патенты
182Библиография
182Новая литература
187Объявление
187Концевая страница
188Объявление
Обложка (с. 3)Contents
Обращаясь к сайту «История Росатома — Электронная библиотека»,
я соглашаюсь с условиями использования представленных там материалов.
Правила сайта (далее – Правила)
- Общие положения
- Настоящие правила определяют порядок и условия использования материалов, размещенных на сайте www.biblioatom.ru (далее именуется Сайт), а также правила использования материалов Сайтом и порядок взаимодействия с Администрацией Сайта.
- Любые материалы, размещенные на Сайте, являются объектами интеллектуальной собственности (объектами авторского права или смежных прав, а также прав на средства индивидуализации). Права Администрации
Сайта на указанные материалы охраняются законодательством о правах на результаты интеллектуальной деятельности.

- Использование материалов, размещенных на Сайте, допускается только с письменного согласия Администрации Сайта или иного правообладателя, прямо указанного на конкретном материале, размещенном на Сайте, или в непосредственной близости от указанного материала.
- Настоящие Правила распространяют свое действие на следующих пользователей: информационные агентства, электронные и печатные средства массовой информации, любые физические и юридические лица, а также
индивидуальные предприниматели (далее — «Пользователи»).

- Использование материалов. Виды использования
- Под использованием материалов Сайта понимается воспроизведение, распространение, публичный показ, сообщение в эфир, сообщение по кабелю, перевод, переработка, доведение до всеобщего сведения и иные способы использования, предусмотренные действующим законодательством Российской Федерации.
- Использование материалов Сайта без получения разрешения от Администрации Сайта не допустимо.
- Внесение каких-либо изменений и/или дополнений в материалы Сайта запрещено.
- Использование материалов Сайта осуществляется на основании договоров с Администрацией Сайта, заключенных в письменной форме, или на основании письменного разрешения, выданного Администрацией Сайта.
- Запрещается любое использование (бездоговорное/без разрешения) фото-, графических, видео-, аудио- и иных материалов, размещенных на Сайте, принадлежащих Администрации Сайта и иным правообладателям
(третьим лицам).

- Стоимость использования каждого конкретного материала или выдача разрешения на его использование согласуется Пользователем и Администрацией Сайта в каждом конкретном случае.
- В случае необходимости использования материалов Сайта, права на которые принадлежат третьим лицам (иным правообладателям, нежели Администрация Сайта, о чем прямо указано на таких материалах либо в непосредственной близости от них), Пользователи обязаны обращаться к правообладателям таких материалов для получения разрешения на использование материалов.
- Обязанности Пользователей при использовании материалов Сайта
- 3.1. При использовании материалов Сайта в любых целях при наличии разрешения Администрации Сайта, ссылка на Сайт обязательна и осуществляется в следующем виде:
- в печатных изданиях или в иных формах на материальных носителях Пользователи обязаны в каждом случае использования материалов указать источник – электронная библиотека «История Росатома»
(www.
 biblioatom.ru)
biblioatom.ru)
- в интернете или иных формах использования в электронном виде не на материальных носителях, Пользователи в каждом случае использования материалов обязаны разместить гиперссылку на Сайт — электронная библиотека «История Росатома» (www.biblioatom.ru), гиперссылка должна являться активной и прямой, при нажатии на которую Пользователь переходит на конкретную страницу Сайта, с которой заимствован материал.
- Ссылка на источник или гиперссылка, указанные в пп. 3.1.1 и 3.1.2. настоящих Правил, должны быть помещены Пользователем в начале используемого текстового материала, а также непосредственно под используемым аудио-, видео-, фотоматериалом, графическим материалом Администрации Сайта.
- в печатных изданиях или в иных формах на материальных носителях Пользователи обязаны в каждом случае использования материалов указать источник – электронная библиотека «История Росатома»
(www.
- Размеры шрифта ссылки на источник или гиперссылки не должны быть меньше размера шрифта текста, в котором используются материалы Сайта, либо размера шрифта текста Пользователя, сопровождающего аудио-,
видео-, фотоматериалы и графические материалы Сайта, а также цвет ссылки должен быть идентичен цветам ссылок на Сайте и должен быть видимым Пользователю.

- Использование материалов с Сайта, полученных из вторичных источников (от иных правообладателей, нежели Администрация Сайта, о чем прямо указано на таких материалах либо в непосредственной близости от них), возможно только со ссылкой на эти источники и, в случае необходимости, установленной такими источниками (правообладателями), — с их разрешения.
- Не допускается переработка оригинального материала (произведения), взятого с Сайта, в том числе сокращение материала, иная его переработка, в том числе приводящая к искажению его смысла.
- 3.1. При использовании материалов Сайта в любых целях при наличии разрешения Администрации Сайта, ссылка на Сайт обязательна и осуществляется в следующем виде:
- Права на материалы третьих лиц, урегулирование претензий
- Материалы, права на которые принадлежат третьим лицам, размещенные на Сайте, размещены либо с разрешения правообладателя, полученного Администрацией Сайта, либо, в случае, если таковое использование
прямо не запрещено правообладателем, в соответствии с Законодательством РФ в информационных целях с обязательным указанием имени автора, материал которого используется, и источника заимствования.

- В случае, если в обозначении авторства материалов в соответствии с п. 4.1. настоящих Правил содержится ошибка, или в случае использования материала с предполагаемым или реальным нарушением прав
третьих лиц, или в иных спорных случаях использования объектов интеллектуальной собственности, размещенных на Сайте, в том числе в случае, когда права третьего лица тем или иным образом нарушаются с
использованием Сайта, применяется следующая схема урегулирования претензий третьих лиц к Администрации Сайта:
- в адрес Администрации Сайта по электронной почте на адрес [email protected] направляется претензия, содержащая информацию об объекте интеллектуальной собственности, права на который
принадлежат
заявителю и который используется незаконно посредством Сайта или с нарушением правил использования, или иным образом права заявителя как обладателя исключительного права на объект интеллектуальной
собственности, размещенный на Сайте, нарушены посредством Сайта, с приложением документов, подтверждающих правомочия заявителя, данные о правообладателе и копия доверенности на действия от лица
правообладателя, если лицо, направляющее претензию, не является руководителем компании правообладателя или непосредственно физическим лицом — правообладателем.
 В претензии также указывается адрес
страницы
Сайта, которая содержит данные, нарушающие права, и излагается полное описание сути нарушения прав;
В претензии также указывается адрес
страницы
Сайта, которая содержит данные, нарушающие права, и излагается полное описание сути нарушения прав;
- Администрация Сайта обязуется рассмотреть надлежаще оформленную претензию в срок не менее 5 (пяти) рабочих дней с даты ее получения по электронной почте. Администрация Сайта обязуется уведомить заявителя о результатах рассмотрения его заявления (претензии) посредством отправки письма по электронной почте на адрес, указанный заявителем, а также направить ответ в письменном виде на адрес, указанный заявителем (в случае неуказания такового адреса отправки, обязательство по предоставлению письменного ответа на претензию с Администрации Сайта снимается). В том числе, Администрация Сайта вправе запросить дополнительные документы, свидетельства, данные, подтверждающие законность предъявляемой претензии. В случае признания претензии правомерной, Администрация Сайта примет все возможные меры, необходимые для прекращения нарушения прав заявителя и урегулирования претензии;
- Администрация Сайта в любом случае предпринимает все возможные меры к скорейшему удовлетворению обоснованных претензий третьих лиц и стремиться к максимально скорому урегулированию всех
спорных
вопросов.

- в адрес Администрации Сайта по электронной почте на адрес [email protected] направляется претензия, содержащая информацию об объекте интеллектуальной собственности, права на который
принадлежат
заявителю и который используется незаконно посредством Сайта или с нарушением правил использования, или иным образом права заявителя как обладателя исключительного права на объект интеллектуальной
собственности, размещенный на Сайте, нарушены посредством Сайта, с приложением документов, подтверждающих правомочия заявителя, данные о правообладателе и копия доверенности на действия от лица
правообладателя, если лицо, направляющее претензию, не является руководителем компании правообладателя или непосредственно физическим лицом — правообладателем.
- Материалы, права на которые принадлежат третьим лицам, размещенные на Сайте, размещены либо с разрешения правообладателя, полученного Администрацией Сайта, либо, в случае, если таковое использование
прямо не запрещено правообладателем, в соответствии с Законодательством РФ в информационных целях с обязательным указанием имени автора, материал которого используется, и источника заимствования.
- Прочие условия
- Администрация Сайта оставляет за собой право изменять настоящие Правила в одностороннем порядке в любое время без уведомления Пользователей. Любые изменения будут размещены на Сайте. Изменения вступают в силу с момента их опубликования на Сайте.
- По всем вопросам использования материалов Сайта Пользователи могут обращаться к Администрации Сайта по следующим координатам: [email protected]
- Во всем, что не урегулировано настоящими Правилами в отношении вопросов использования материалов на Сайте, стороны руководствуются положениями Законодательства РФ.
СогласенНе согласен
ФГБОУ ВО ПГФА Минздрава России
Пермская государственная
фармацевтическая академия
Для слабовидящих
Осторожно: грипп!!!
…
Грипп — симптомы и профилактика
…
еще …
Наши новости
Пять вузов Пермского края вошли в рейтинг лучших в стране
15 октября 2022
Электронные образовательные ресурсы ПГФА
11 октября 2022
еще …
Наши события
Визит генерального консула Республики Узбекистан
14 октября 2022
Иностранные студенты ПГФА посетили Пермский оперный театр и Музей Аптекарского двора
10 октября 2022
еще . ..
..
Конференции, олимпиады, форумы…
Федеральный проект «Платформа университетского технологического предпринимательства»
20 октября 2022
Приглашение к участию во Всероссийском студенческом онлайн-конкурсе «Контур.Старт»
13 октября 2022
О конкурсах Ассоциации по улучшению состояния здоровья и качества жизни населения «Здоровые города, районы и поселки»
10 октября 2022
еще …
Новости спорта
Всероссийские соревнования «Кубок памяти» по дартс
20 октября 2022
Команда ПГФА в турнире «Mobile Paradise» по дисциплине Brawl Stars
12 октября 2022
Фестиваль спорта в парке Балатово
10 октября 2022
еще …
Button
Ученый совет
Научный полк
Обращение советов ректоров вызов Пермского края
Мисс Фармация-2019
Галерея новостей
День открытых дверей
Информация об аккредитации специалистов
Видеообзор — введение в профессию
Ректор ПГФА Алексей Юрьевич Турышев рассказывает о перспективах специальности и приёме в 2019 году
В ПГФА имеется 200 бюджетных мест для абитуриентов. Трудоустройство выпускников ПГФА почти 100 %. ПГФА обеспечивает половину кадровой потребности отрасли. Провизоры — аналитики, технологи, организаторы. Обеспечивается полный цикл обучения от создания молекулы до разработки лекарственной формы. Эфир 26 февраля 2019 года
Трудоустройство выпускников ПГФА почти 100 %. ПГФА обеспечивает половину кадровой потребности отрасли. Провизоры — аналитики, технологи, организаторы. Обеспечивается полный цикл обучения от создания молекулы до разработки лекарственной формы. Эфир 26 февраля 2019 года
Смотреть все видеообзоры о професии
Условия проживания студентов в общежитии № 2 (более новое первое общежитие не показано). Съёмка 2016 года.
Имеющиеся у ПГФА два общежития неизменно входят в десятку лучших общежитий образовательных учреждений города Перми. В общежитиях имеются столовая, кухни на каждом этаже, библиотека, спортзал, бытовая, душевая и постирочная комнаты (общежитие № 1 новее).
Первокурсники на лабораторных занятиях по физике в ПГФА. Съёмка 25 февраля 2019 года
На первом курсе студенты изучают биологию, физиологию, математику, физику, неорганическую химию, физическую химию, латинский язык, информатику, экономическую теорию, историю. Основной предмет — химия. За годы учёбы её будет 9 видов.
Впечатления первокурсника
после двух месяцев учёбы в 2018 году.
Ректор
Проректоры
Помощник ректора по воспитательной работе
Ученый совет
Административно — управленческие подразделения
Ведущий юрисконсульт
Учебные подразделения
Кафедры
Научные подразделения
Корпуса и общежития
Отдел качества
Региональный испытательный центр «Фарматест»
Полиграфический отдел
Стоматологическая клиника
Столовая
Здравпункт
Музей
Профком сотрудников
Профком студентов
Социально-психологическая служба
WebElements Periodic Table » Натрий » фторид натрия
- Формула: NaF
- Формула системы Хилла: F 1 Na 1
- Регистрационный номер CAS: [7681-49-4]
- Масса формулы: 41,988
- Класс: фторид №
- Цвет: белый
- Внешний вид: кристаллическое твердое вещество
- Температура плавления: 996°C
- Температура кипения: 1695°С; 1704°С
- Плотность: 2780 кг·м -3
Ниже приведены некоторые синонимы фторида натрия :
- фторид натрия
- фторид натрия(I)
Степень окисления натрия во фториде натрия составляет 1 .
Синтез
Одним из способов получения фторида натрия является взаимодействие гидроксида с плавиковой кислотой. Полученную соль затем можно очистить перекристаллизацией.
NaOH(водн.) + HF(водн.) → NaF(водн.) + H 2 O(л)
Хотя это и не является обычным способом получения из-за дороговизны, металлический натрий энергично реагирует со всеми галогенами с образованием галогенидов натрия. Итак, горит фтором, F 2 , с образованием фторида натрия (I), NaF.
2Na(т) + F 2 (г) → 2NaF(т)
Твердотельная структура
- Геометрия натрия: 6 координата: октаэдрическая
- Прототип структуры: NaCl (каменная соль)
Элементный анализ
В таблице показано процентное содержание элементов для NaF (фторид натрия).
| Элемент | % |
|---|---|
| Ф | 45,25 |
| Нет данных | 54,75 |
Изотопная схема NaF
На приведенной ниже диаграмме показана рассчитанная изотопная картина для формулы NaF с наиболее интенсивным ионом, установленным на 100%.
Каталожные номера
Данные на страницах этих соединений собраны и адаптированы из основной литературы и нескольких других источников, включая следующие.
- Р.Т. Сандерсон в Chemical Periodicity , Reinhold, New York, USA, 1960.
- Н.Н. Гринвуд и А. Эрншоу в Chemistry of the Elements , 2-е издание, Butterworth, UK, 1997.
- Ф.А. Коттон, Г. Уилкинсон, К.А. Мурильо и М. Бохманн, в Advanced Inorganic Chemistry , John Wiley & Sons, 1999.
- А. Ф. Тротман-Дикенсон, (редактор) в Комплексная неорганическая химия , Пергамон, Оксфорд, Великобритания, 1973.
- Р.В.Г. Wyckoff, в Crystal Structures , том 1, Interscience, John Wiley & Sons, 1963.
- A.R.West в Базовая химия твердого тела Химия , John Wiley & Sons, 1999.
- А. Ф. Уэллс в Структурная неорганическая химия , 4-е издание, Оксфорд, Великобритания, 1975.
- Дж.Д.Х. Донней, (ред.
 ) в Определяющие таблицы данных о кристаллах , монография ACA № 5, Американская кристаллографическая ассоциация, США, 1963.
) в Определяющие таблицы данных о кристаллах , монография ACA № 5, Американская кристаллографическая ассоциация, США, 1963. - Д.Р. Лиде, (редактор) в справочнике по химии и физике компании Chemical Rubber Company , CRC Press, Бока-Ратон, Флорида, США, 77-е издание, 1996.
- Дж.В. Меллор в Всеобъемлющий трактат по неорганической и теоретической химии , тома 1–16, Longmans, Лондон, Великобритания, 1922–1937.
- Дж. Э. Макинтайр (редактор) в Словаре неорганических соединений , тома 1-3, Chapman & Hall, Лондон, Великобритания, 1992.
Исследуйте периодические свойства по этим ссылкам
Число окисления – определение, правила, расчет, примеры
Окислительно-восстановительный потенциал – это химический процесс, связанный с изменением степени окисления атомов. Фактический или формальный перенос электронов между химическими веществами определяется окислительно-восстановительными реакциями, которые обычно включают одно вещество (восстановитель), подвергающееся окислению (теряя электроны), в то время как другое вещество (окислитель) подвергается восстановлению (приобретает электроны). Химические соединения, потерявшие электрон, называются окисленными, а химические соединения, получившие электрон, — восстановленными. Другими словами:
Химические соединения, потерявшие электрон, называются окисленными, а химические соединения, получившие электрон, — восстановленными. Другими словами:
Потеря электронов или увеличение степени окисления атома, иона или отдельных атомов в молекуле называется окислением .
Прирост электронов или понижение степени окисления атома, иона или отдельных атомов в молекуле называется восстановлением (снижение степени окисления).
Номера окисления
Мы можем идентифицировать окисленный материал, восстановленное вещество, а также восстановители и окислители в химической реакции. Согласно понятию окислительно-восстановительной реакции, такую идентификацию можно провести, определив, какой материал передает электроны другим соединениям. С другой стороны, это объяснение с точки зрения потери и присоединения электронов применимо только к ионным соединениям с полным переносом электронов и исключает другие реакции, такие как:
N 2 +O 2 → 2NO
H 2 +CL 2 → 2HCl
«Когда все остальные атомы в оставшихся молекуле.
остаточный заряд, который есть у атома или кажется, что он есть».
Термины степень окисления и степень окисления обычно взаимозаменяемы. Это потому, что периодическое качество электроотрицательности основано на стандартных обозначениях степеней окисления. Оценивая свое окружение, атом в молекуле может присвоить отрицательную, положительную или нулевую степень окисления. В некоторых случаях степени окисления могут быть даже дробными.
Правила присвоения степеней окисления элементам:
Знание следующих критериев может быть использовано для расчета степени окисления элементов в соединениях.
Правило 1: Сумма всех атомов в степенях окисления молекулы равна нулю.
напр. В KMnO 4 степень окисления K равна +1, степень окисления Mn равна +7, а степень окисления кислорода равна -2.
Правило 2: Степень окисления атома всегда равна 0 в его основной форме.
напр. Степень окисления H ,O ,N ,P ,S ,Se ,Cu, Ag в их элементных формах составляет H 2 ,O 2 ,N 2 ,P 4 ,S 8 , Se 8 ,Cu,Ag соответственно равен нулю.
Правило 3: Щелочные металлы (Li, Na, K, Rb, Cs) в своих соединениях имеют степень окисления +1.
напр. В NaCl степень окисления Na равна +1.
Правило 4: Щелочноземельные металлы (Be, Mg, Ca, Sr, Ba) в своих соединениях обычно имеют степень окисления +2.
напр. Степень окисления Mg в MgO равна +2.
Правило 5: За исключением гидридов металлов, степень окисления Н в его соединении всегда +1.
напр. В HCl степень окисления H равна +1, а в NaH (гидрид натрия) степень окисления H равна -1.
Правило 6: Степень окисления фтора равна 1 во всех его соединениях.
напр. В NaF степень окисления F равна -1.
Правило 7: За исключением перекиси, супероксидов, оксифторидов и озонидов, кислород имеет степень окисления -2 в большинстве своих оксидов.
напр. В Na 2 O степень окисления O равна -2.
Исключительные случаи:
- Пероксиды: Степень окисления кислорода в пероксидах равна 1. Примеры, H 2 O 2 , Na 2 O 2 .
Степень окисления кислорода в соединениях фтора равна +2. Примеры F 2 O или OF 2 и т. д.
- Супероксиды: Степень окисления кислорода в супероксидах составляет –1/2.
- Озониды: Каждый атом кислорода в озониде имеет степень окисления –1/3.
Правило 8: Заряд ионного соединения равен сумме степеней окисления всех атомов.
напр. В SO 2 –4 степень окисления серы равна +6. Степень окисления кислорода равна -2.
Правило 9: За исключением кислорода и фтора, максимальная степень окисления любого элемента равна номеру его группы.
напр. Количество окисления серы в H 2 S 2 O 8 , K 2 S 2 O 8 , S 2 O –2 8 и H 010 2 SO 5 равен +6 из-за наличия перекисной связи.
Правило 10: Возможно, что не все атомы одного и того же элемента имеют одинаковую степень окисления в определенных соединениях. Мы получаем средний результат, когда вычисляем степень окисления этого элемента в таких компонентах.
напр. Один атом серы в Na 2 S 2 O 3 имеет степень окисления +6, тогда как другие атомы серы имеют степень окисления -2. В результате средняя степень окисления серы в Na 2 S 2 O 3 +2.
В результате средняя степень окисления серы в Na 2 S 2 O 3 +2.
Правило 11: Углерод в органических молекулах может иметь любую степень окисления от -4 до +4.
напр. в HCHO степень окисления углерода равна нулю.
Правило 12: Общая степень окисления элемента эквивалентна его номеру группы от IA до IV A. Формула (номер группы –8) дает общую степень окисления любого элемента от VA до VIII-A.
напр.
- Степень окисления элементов I А группы =+1.
- Степень окисления элементов II А группы =+2.
- Степень окисления элементов III А группы =+3.
- Степень окисления элементов IV А группы =+4.
- Степень окисления элементов группы V A =–3.
- Степень окисления элементов VI А группы =–2.
- Степень окисления элементов VII А группы =–1.
- Степень окисления элементов VIII А группы =0.

Правило 13: C, N, P и S имеют степени окисления 4, –3, –3 и –2 во всех карбидах, нитридах, фосфидах и сульфидах соответственно.
напр. В Mg 3 N 2 степень окисления азота равна -3.
Правило 14: Во всех карбонилах металлов степень окисления металлов равна нулю.
напр. В Ni(CO) 4 степень окисления Ni равна нулю.
Расчет степеней окисления
- Степень окисления серы в H 2 SO 4
Пусть степень окисления серы в h3SO4 равна X
Степень окисления водорода 9050 =+1 9050 =–2
2(+1)+(X)+4×(–2)=0
2+X–8=0
X = 8–2=+6.
Степень окисления серы в H 2 SO 4 равна +6.
- Степень окисления хрома в Cr 2 O 2– 7 ион.
Степень окисления кислорода =–2
Степень окисления хрома =X
2X+7(–2)=–2
2X–14=–2
2X=–2+14 =12
Следовательно, X=+6.
Степень окисления хрома в Cr 2 O 2– 7 равна +6.
- Число окисления азота в нитрите аммония
Нитрит аммония представляет собой ионное соединение, содержащее ионы NH+4 и NO–2.
Степень окисления азота в NH + 4 ион =–3
Степень окисления азота в NO – 2 =+3.
Таким образом, один атом азота в нитрите аммония находится в степени окисления а–3 –, а другой атом азота – в степени окисления а+3.
Примеры вопросов
Вопрос 1: Какова общепринятая степень окисления инертных газов?
Ответ:
Инертные газы имеют нулевую степень окисления.
Вопрос 2: Каковы правила для степеней окисления?
Ответ:
Правила для степеней окисления:
- Сумма всех атомов в степенях окисления молекулы равна нулю.
- Степень окисления атома в его самой основной форме всегда равна нулю.
- В их соединениях степень окисления щелочных металлов (Li, Na, K, Rb, Cs) всегда +1.
- В их соединениях степень окисления щелочноземельных металлов (Be, Mg, Ca, Sr, Ba) всегда +2.
- За исключением гидридов металлов, степень окисления Н в его соединении всегда +1.
- Фтор имеет степень окисления 1 во всех своих соединениях.
- За исключением перекиси, супероксидов, оксифторидов и озонидов, степень окисления кислорода в большинстве его оксидов равна -2.
- Углерод в органических молекулах может иметь любую степень окисления от -4 до +4.
Вопрос 3: Какова степень окисления ртути в амальгаме.
Ответ:
Амальгама ртути имеет нулевую степень окисления. Каждый элемент в сплаве или амальгаме имеет нулевую степень окисления.
Вопрос 4: Какова степень окисления кислорода в O 3 и в MgO?
Ответ:
Степень окисления O в O3=0
Степень окисления O в MgO=–2
Вопрос 5: Какова степень окисления Chromium2O2–7 в Crion2O2–7 ?
Ответ:
Степень окисления кислорода =–2
Степень окисления хрома =X
2X+7(–2)=–2
2X–905–3 –2+14=12
Следовательно, X=+6.




 biblioatom.ru)
biblioatom.ru)


 В претензии также указывается адрес
страницы
Сайта, которая содержит данные, нарушающие права, и излагается полное описание сути нарушения прав;
В претензии также указывается адрес
страницы
Сайта, которая содержит данные, нарушающие права, и излагается полное описание сути нарушения прав;

 ) в Определяющие таблицы данных о кристаллах , монография ACA № 5, Американская кристаллографическая ассоциация, США, 1963.
) в Определяющие таблицы данных о кристаллах , монография ACA № 5, Американская кристаллографическая ассоциация, США, 1963.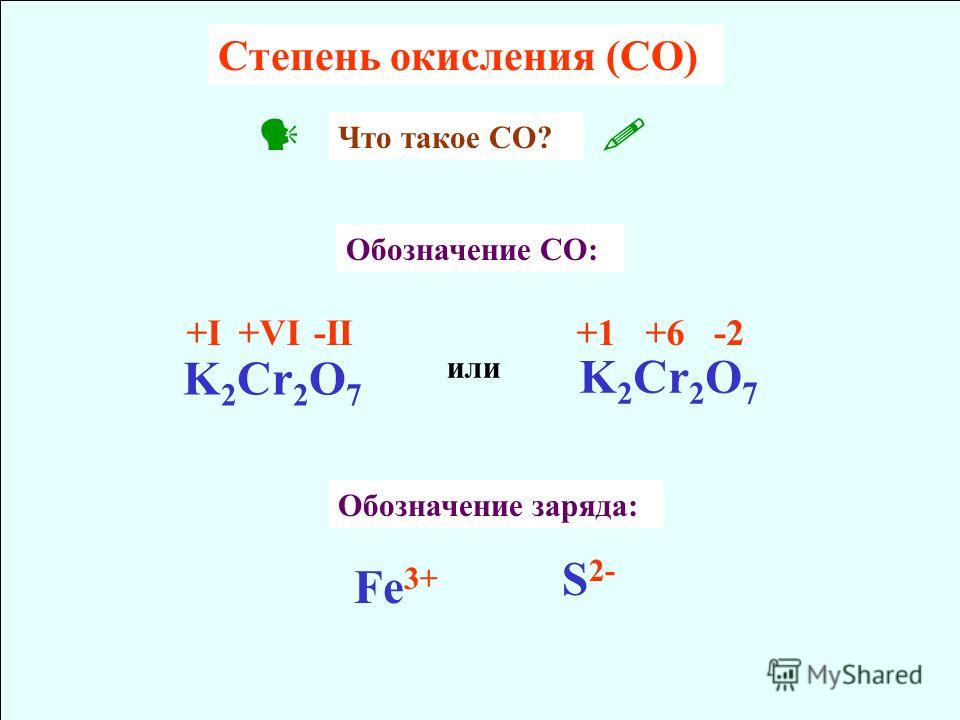 остаточный заряд, который есть у атома или кажется, что он есть».
остаточный заряд, который есть у атома или кажется, что он есть».

