Лучший ответ по мнению автора | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Посмотреть всех экспертов из раздела Учеба и наука > Химия
Решено
Помогите пожалуйста. .. Установите пространственную структуру следующих молекул и ионов, определите в каждом случае тип гибридизации центрального атома, сигма-и и пи-связь СlF3,CHF3.
.. Установите пространственную структуру следующих молекул и ионов, определите в каждом случае тип гибридизации центрального атома, сигма-и и пи-связь СlF3,CHF3.
Решено
1,000 г металла Х растворили в избытке раствора азотной кислоты. Образовавшуюся соль выделили и прокалили до постоянной массы. Масса образовавшегося
Решено
CO2+4h3=Ch5+2h3O(г) Рассчитать энтальпию, энтропию, энергию Гиббса для данной реакции и ответить на вопросы
Взаимодействует ли плавиковая кислота с оксидом кремния (IV) и почему? Ведь кислотный оксид не взаимодействует с кислотой.
При растворении в воде гидроксид-ионы образует вещество с формулой 1) Zn(OH)2 2) Ca(OH)2 3) Fe(OH)3 4) Al(OH)3
Пользуйтесь нашим приложением
Эквивалентные массы реагирующих веществ | Задачи 439
Задача 439.
Имеется раствор, в 1 л которого содержится 18,9 г HNO3, и раствор, содержащий в 1 л 3,2 г NaOH. В каком объемном отношении нужно смешать эти растворы для получения раствора, имеющего нейтральную реакцию?
Решение:
Уравнение реакции нейтрализации гидроксида натрия азотной кислотой имеет вид:
HNO3 + NaOH = NaNO3 + H2O
Вещества реагируют в эквивалентных отношениях 1 : 1, что указывает на то, что эквивалентные массы реагирующих друг с другом веществ численно равны их молекулярным массам:
M(NaOH) = 40г/моль;
Найдём количество HNO3 и NaOH в литровых растворах:
NaOH взят в недостатке, поэтому нужно некоторое количество его для нейтрализации HNO3. Обозначим объём раствора NaOH через x. Тогда общее количество раствора NaOH можно записать как 0,08х. Количество HNO3 должно быть равно количеству NaOH, Поскольку по уравнению реакции количества NaOH и HNO3 равны, то можно записать:
Можно составить пропорцию:
Ответ: 1 : 3,75.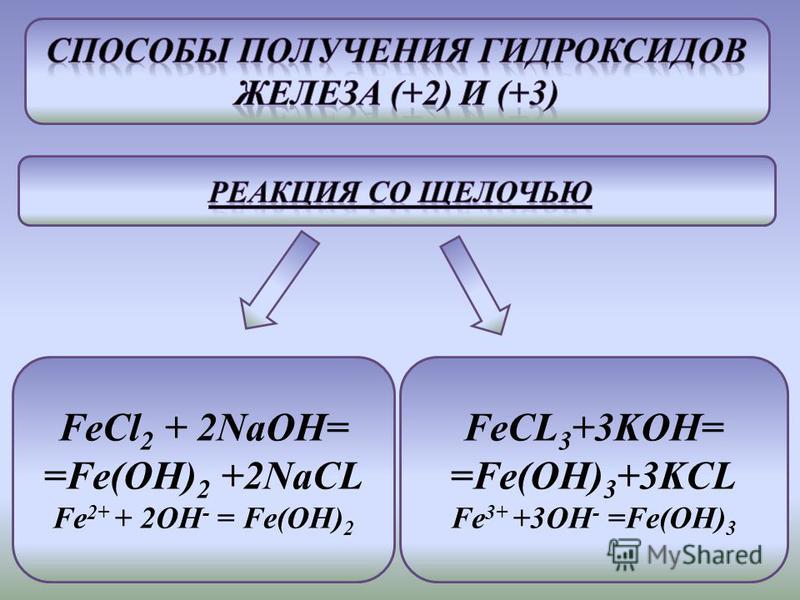
Задача 440.
Какой объем 0,2н. раствора щелочи потребуется для осаждения в виде Fe(OH)3 всего железа, содержащегося в 100 мл 0, 5 н. раствора FeCl3?
Решение:
В 100 мл 0,5 н раствора содержится 0,05 эквивалента FeCl3
Ответ: 0,25л.
Задача 441.
Сколько граммов СаСО3 выпадает в осадок, если к 400 мл 0,5 н. раствора СаСI2 прибавить избыток раствора соды?
Решение:
Уравнение реакции имеет вид:
СаСI2 + Na2CO3 ⇔ CaCO3 + 2NaCl
Из уравнения реакции следует, что на получение 1 моля СаСО3 требуется 1 моль СаСI2. Находим количество эквивалентов СаСО3 в 400 мл 0,5 Н раствора:
Находим количество эквивалентов СаСО3 в 400 мл 0,5 Н раствора:
0,4 . 0,5 = 0,2 Н
Такое же количество СаСО
МЭ(В) — молярная масса эквивалента соли, г/моль; М(В) — молярная масса соли; n — коэффициент при атоме металла; А — валентность металла.
Отсюда
Теперь рассчитаем массу выпавшего осадка CaCO3 : 0,2 . 50 = 10г.
Ответ: 10г.
Задача 442. Для нейтрализации 20 мл 0,1Н. раствора кислоты потребовалось 8 мл раствора NaOН. Сколько граммов содержит 1 л этого раствора?
Решение:
Для вычисления нормальности раствора NaOH используем математическое выражение следствия из закона эквивалентности (так называемое правило пропорциональности):
CЭ(А) . V(A) = C Э(B) . V(B),
V(A) = C Э(B) . V(B),
где
CЭ(А) и CЭ(B) — нормальные концентрации эквивалентов веществ А и В, моль/л; V(A) и V(B) — объёмы растворов веществ А и В.
По условию задачи известны V(щелочи), V(кислоты) и СЭ(кислоты), то нетрудно вычислить СЭ(щелочи) по формуле:
Эквивалентная масса NaOH равна его молярной массе, т.е. 40 г/моль. Тогда массу NaOH, содержащегося в 1 л раствора можно определить по формуле:
m(NaOH) = M(NaOH) . СЭ(NaOH) = 40 . 0,25 = 10 г.
Ответ: 10 г.
| 1 | Найдите количество нейтронов | Х | |
| 2 | Найдите массу 1 моля | Н_2О | |
| 3 | Баланс | H_2(SO_4)+K(OH)→K_2(SO_4)+H(OH) | |
| 4 | Найдите массу 1 моля | Х | |
| 5 | Найдите количество нейтронов | Фе | |
| 6 | Найдите количество нейтронов | ТК | |
| 7 | Найдите электронную конфигурацию | Х | |
| 8 | Найдите количество нейтронов | Са | |
| 9 | Баланс | CH_4+O_2→H_2O+CO_2 | |
| 10 | Найдите число нейтронов | С | |
| 11 | Найдите число протонов | Х | |
| 12 | Найдите количество нейтронов | О | |
| 13 | Найдите массу 1 моля | СО_2 | |
| 14 | Баланс | C_8H_18+O_2→CO_2+H_2O | |
| 15 | Найдите атомную массу | Х | |
| 16 | Определить, растворимо ли соединение в воде | Н_2О | |
| 17 | Найдите электронную конфигурацию | Нет | |
| 18 | Найдите массу отдельного атома | Х | |
| 19 | Найдите количество нейтронов | № | |
| 20 | Найдите количество нейтронов | Золото | |
| 21 | Найдите количество нейтронов | Мн | |
| 22 | Найдите количество нейтронов | Ру | |
| 23 | Найдите электронную конфигурацию | О | |
| 24 | Найдите массовые проценты | Н_2О | |
| 25 | Определить, растворимо ли соединение в воде | NaCl | |
| 26 | Найдите эмпирическую/простейшую формулу | Н_2О | |
| 27 | Найти степени окисления | Н_2О | |
| 28 | Найдите электронную конфигурацию | К | |
| 29 | Найдите электронную конфигурацию | Мг | |
| 30 | Найдите электронную конфигурацию | Са | |
| 31 | Найдите количество нейтронов | Рх | |
| 32 | Найдите количество нейтронов | Нет | |
| 33 | Найдите количество нейтронов | Пт | |
| 34 | Найдите количество нейтронов | Быть | Быть |
| 35 | Найдите количество нейтронов | Кр | |
| 36 | Найдите массу 1 моля | Н_2SO_4 | |
| 37 | Найдите массу 1 моля | HCl | |
| 38 | Найдите массу 1 моля | Фе | |
| 39 | Найдите массу 1 моля | С | |
| 40 | Найдите количество нейтронов | Медь | |
| 41 | Найдите количество нейтронов | С | |
| 42 | Найдите степени окисления | Х | |
| 43 | Баланс | CH_4+O_2→CO_2+H_2O | |
| 44 | Найдите атомную массу | О | |
| 45 | Найдите атомный номер | Х | |
| 46 | Найдите количество нейтронов | Пн | |
| 47 | Найдите количество нейтронов | ОС | |
| 48 | Найдите массу 1 моля | NaOH | |
| 49 | Найдите массу 1 моля | О | |
| 50 | Найдите электронную конфигурацию | Фе | |
| 51 | Найдите электронную конфигурацию | С | |
| 52 | Найдите массовые проценты | NaCl | |
| 53 | Найдите массу 1 моля | К | |
| 54 | Найдите массу отдельного атома | Нет | |
| 55 | Найдите число нейтронов | Н | |
| 56 | Найдите количество нейтронов | Ли | |
| 57 | Найдите количество нейтронов | В | |
| 58 | Найдите число протонов | № 92О | |
| 60 | Упростить | ч*2р | |
| 61 | Определить, растворимо ли соединение в воде | Х | |
| 62 | Найдите плотность на STP | Н_2О | |
| 63 | Найти степени окисления | NaCl | |
| 64 | Найдите атомную массу | Он | Он |
| 65 | Найдите атомную массу | Мг | |
| 66 | Найдите количество электронов | Х | |
| 67 | Найдите число электронов | О | |
| 68 | Найдите число электронов | С | |
| 69 | Найдите число нейтронов | Пд | |
| 70 | Найдите количество нейтронов | рт.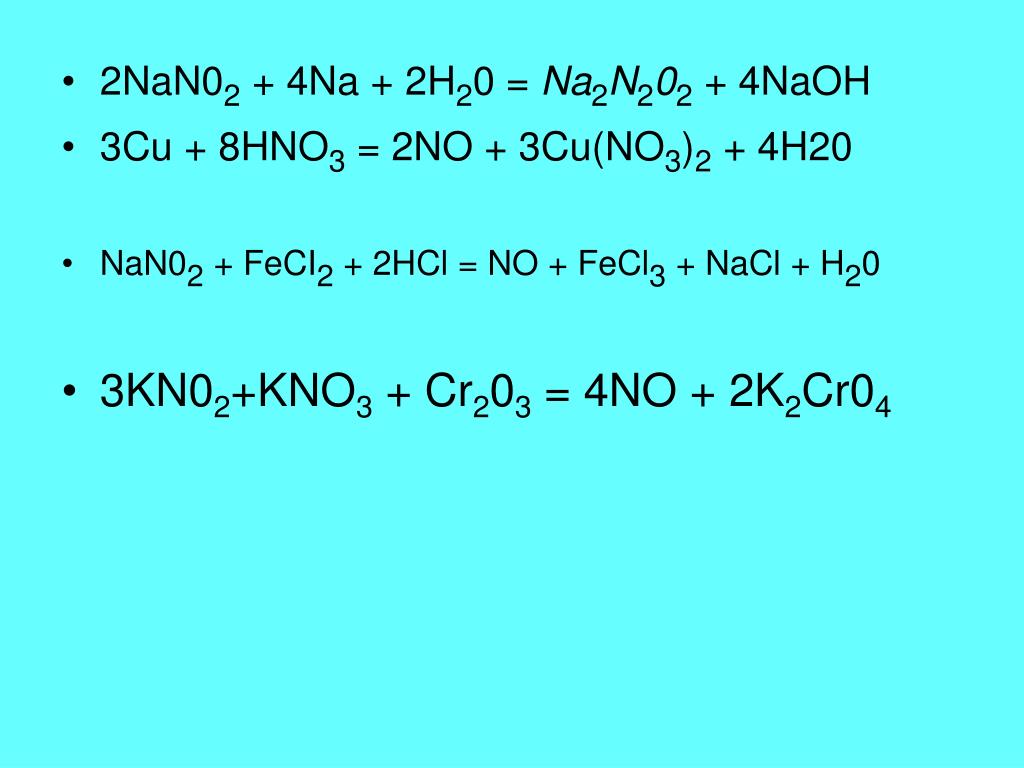 ст. ст. | |
| 71 | Найдите количество нейтронов | Б | |
| 72 | Найдите массу отдельного атома | Ли | |
| 73 | Найдите эмпирическую формулу | Н=12%, С=54%, N=20 | , , |
| 74 | Найдите число протонов | Быть | Быть |
| 75 | Найдите массу 1 моля | На | |
| 76 | Найдите электронную конфигурацию | Со | |
| 77 | Найдите электронную конфигурацию | С | |
| 78 | Баланс | C_2H_6+O_2→CO_2+H_2O | |
| 79 | Баланс | Н_2+О_2→Н_2О | |
| 80 | Найдите электронную конфигурацию | Р | |
| 81 | Найдите электронную конфигурацию | Пб | |
| 82 | Найдите электронную конфигурацию | Ал | |
| 83 | Найдите электронную конфигурацию | Ар | |
| 84 | Найдите массу 1 моля | О_2 | |
| 85 | Найдите массу 1 моля | Н_2 | |
| 86 | Найдите количество нейтронов | К | |
| 87 | Найдите количество нейтронов | Р | |
| 88 | Найдите число нейтронов | Мг | |
| 89 | Найдите количество нейтронов | Вт | |
| 90 | Найдите массу отдельного атома | С | |
| 91 | Упростить | н/д+кл | |
| 92 | Определить, растворимо ли соединение в воде | Н_2SO_4 | |
| 93 | Найдите плотность на STP | NaCl | |
| 94 | Найти степени окисления | C_6H_12O_6 | |
| 95 | Найти степени окисления | Нет | |
| 96 | Определить, растворимо ли соединение в воде | C_6H_12O_6 | |
| 97 | Найдите атомную массу | Кл | |
| 98 | Найдите атомную массу | Фе | |
| 99 | Найдите эмпирическую/самую простую формулу | СО_2 | |
| 100 | Найдите количество нейтронов | Мт |
Усиленный ферментативный гидролиз Pennisetum alopecuroides с помощью предварительной обработки разбавленной кислотой, щелочью и хлоридом железа
1. Caruso M.C., Braghieri A., Capece A., Napolitano F., Romano P., Galgano F., Altieri G., Genovese F. Последние обновления по использованию агропищевых отходов для производства биогаза. заявл. науч. 2019;9:1217. doi: 10.3390/app17. [CrossRef] [Google Scholar]
Caruso M.C., Braghieri A., Capece A., Napolitano F., Romano P., Galgano F., Altieri G., Genovese F. Последние обновления по использованию агропищевых отходов для производства биогаза. заявл. науч. 2019;9:1217. doi: 10.3390/app17. [CrossRef] [Google Scholar]
2. You Z., Zhang S., Kim H., Chiang P.C., Sun Y., Guo Z., Xu H. Влияние кукурузной соломы, предварительно обработанной NaOH и CaO, на анаэробные процессы. переваривание свиного навоза и кукурузной соломы. заявл. науч. 2019;9:123. doi: 10.3390/app23. [Перекрестная ссылка] [Академия Google]
3. Cheng X.Y., Zhong C. Влияние соотношения корма и инокулята, совместного сбраживания и предварительной обработки на производство биогаза при анаэробном сбраживании стеблей хлопчатника. Энергетическое топливо. 2014; 28:3157–3166. doi: 10.1021/ef402562z. [CrossRef] [Google Scholar]
4. Cheng X.Y., Liu C.Z. Улучшенное совместное производство водорода и метана из стеблей кукурузы с помощью трехэтапного процесса анаэробной ферментации, объединенного с щелочным гидролизом. Биоресурс. Технол. 2012; 104: 373–379. doi: 10.1016/j.biortech.2011.10.082. [PubMed] [CrossRef] [Академия Google]
Биоресурс. Технол. 2012; 104: 373–379. doi: 10.1016/j.biortech.2011.10.082. [PubMed] [CrossRef] [Академия Google]
5. Cheng X.Y., Li Q., Liu C.Z. Совместное производство водорода и метана посредством анаэробной ферментации отходов стеблей кукурузы в реакторе непрерывного действия с мешалкой, интегрированном с восходящим слоем анаэробного ила. Биоресурс. Технол. 2012; 114:327–333. doi: 10.1016/j.biortech.2012.03.038. [PubMed] [CrossRef] [Google Scholar]
6. Кан С.Х., Сунь Ю.М., Ли Л.Х., Конг С.Ю., Юань З.Х. Улучшение производства метана в результате анаэробного сбраживания Pennisetum Hybrid путем предварительной щелочной обработки. Биоресурс. Технол. 2018; 255:205–212. doi: 10.1016/j.biortech.2017.12.001. [PubMed] [CrossRef] [Академия Google]
7. Camesasca L., Ramı’rez M.B., Guigou M., Ferrari MD, Lareo C. Оценка предварительной обработки разбавленными кислотами и щелочами, ферментативный гидролиз и ферментация травы мятлика для производства топливного этанола. Биомасса Биоэнергетика. 2015;74:193–201. doi: 10.1016/j.biombioe.2015.01.017. [CrossRef] [Google Scholar]
Биомасса Биоэнергетика. 2015;74:193–201. doi: 10.1016/j.biombioe.2015.01.017. [CrossRef] [Google Scholar]
8. Ван С.Д., Чен Дж.Х., Ян Г.Х., Гао В.Х., Чен К.Ф. Эффективное преобразование Hybrid Pennisetum в глюкозу путем предварительной обработки кислородно-водной щелочной ионной жидкой средой в благоприятных условиях. Биоресурс. Технол. 2017; 243:335–338. doi: 10.1016/j.biortech.2017.06.134. [PubMed] [CrossRef] [Академия Google]
9. Tsai M.H., Lee W.C., Kuan W.C., Sirisansaneeyakul S., Savarajara A. Оценка различных видов предварительной обработки травы Napier для ферментативного осахаривания и производства этанола. Энергетика наук. англ. 2018; 6: 683–692. doi: 10.1002/ese3.243. [CrossRef] [Google Scholar]
10. Скордиа Д., Косентино С.Л., Джеффрис Т.В. Эффективность предварительной обработки разбавленной щавелевой кислотой биомассы Miscanthus×giganteus для производства этанола. Биомасса Биоэнергетика. 2013; 59: 540–548. doi: 10.1016/j.biombioe. 2013.090,011. [CrossRef] [Google Scholar]
2013.090,011. [CrossRef] [Google Scholar]
11. Ким Д. Физико-химическая конверсия лигноцеллюлозы: эффекты ингибиторов и стратегии детоксикации: мини-обзор. Молекулы. 2018;23:309. doi: 10,3390/молекулы23020309. [Статья бесплатно PMC] [PubMed] [CrossRef] [Google Scholar]
12. Кумари Д., Сингх Р. Предварительная обработка лигноцеллюлозных отходов для производства биотоплива: критический обзор. Продлить. Поддерживать. Энергия. 2018; 90:877–891. doi: 10.1016/j.rser.2018.03.111. [Перекрестная ссылка] [Академия Google]
13. Bensah E.C., Mensah M. Химические методы предварительной обработки для производства целлюлозного этанола: технологии и инновации. Междунар. Дж. Хим. англ. 2013;2013:1–21. doi: 10.1155/2013/719607. [CrossRef] [Google Scholar]
14. Латика Б., Соня Дж., Румана А. Экономические и экологические перспективы производства этанола из возобновляемых сельскохозяйственных отходов: обзор. АМБ Экспресс. 2012;2:65. doi: 10.1186/2191-0855-2-65. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
15. Кухарска К., Рыбарчик П., Холовач И., Лукайтис Р., Глинка М., Камински М. Предварительная обработка лигноцеллюлозных материалов в качестве субстратов для ферментации процессы. Молекулы. 2018;23:2937. doi: 10.3390/молекулы23112937. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Кухарска К., Рыбарчик П., Холовач И., Лукайтис Р., Глинка М., Камински М. Предварительная обработка лигноцеллюлозных материалов в качестве субстратов для ферментации процессы. Молекулы. 2018;23:2937. doi: 10.3390/молекулы23112937. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Fu S.F., Chen KQ, Zhu R., Sun WX, Zou H., Guo RB Улучшение показателей анаэробного сбраживания Miscanthus floridulus за счет различной предварительной обработки методы и предварительный экономический анализ. Энерг. Конверс. Управление 2018; 159:120–128. doi: 10.1016/j.enconman.2018.01.014. [CrossRef] [Google Scholar]
17. Элиана С., Хорхе Р., Хуан П., Луис Р. Влияние метода предварительной обработки на ферментативный гидролиз и ферментируемость этанолом целлюлозной фракции травы слона. Топливо. 2014; 118:41–47. doi: 10.1016/j.fuel.2013.10.055. [Перекрестная ссылка] [Академия Google]
18. Сабанджи К., Буюккиледжи А.К. Сравнение обработок жидкой горячей водой, очень разбавленной кислотой и щелочью для повышения ферментативной усвояемости остатков обрезки деревьев фундука. Биоресурс. Технол. 2018; 261:158–165. doi: 10.1016/j.biortech.2018.03.136. [PubMed] [CrossRef] [Google Scholar]
Биоресурс. Технол. 2018; 261:158–165. doi: 10.1016/j.biortech.2018.03.136. [PubMed] [CrossRef] [Google Scholar]
19. Саху Д., Уммалима С.Б., Окрам А.К., Пандей А., Санкар М., Сукумаран Р.К. Влияние предварительной обработки разбавленной кислотой травы дикого риса ( Zizania latifolia ) из озера Локтак на ферментативный гидролиз. Биоресурс. Технол. 2018; 253: 252–255. doi: 10.1016/j.biortech.2018.01.048. [PubMed] [CrossRef] [Академия Google]
20. Пандей А.К., Неги С. Влияние предварительной обработки ПАВ кислотой и щелочью на лигноцеллюлозную структуру листвы сосны и оптимизация параметров ее осахаривания с использованием методологии поверхности отклика. Биоресурс. Технол. 2015;192:115–125. doi: 10.1016/j.biortech.2015.04.054. [PubMed] [CrossRef] [Google Scholar]
21. Li K.N., Wan J.M., Wang X., Wang J.F., Zhang J.H. Сравнение предварительной обработки разбавленной кислотой и щелочью при производстве ферментируемых сахаров из бамбука: эффект Tween 80. Ind. Crops Products. 2016; 83: 414–422. doi: 10.1016/j.indcrop.2016.01.003. [Перекрестная ссылка] [Академия Google]
Crops Products. 2016; 83: 414–422. doi: 10.1016/j.indcrop.2016.01.003. [Перекрестная ссылка] [Академия Google]
22. Cheng X.Y., Liu C.Z. Улучшенное производство биогаза из остатков процесса экстракции трав за счет предварительной щелочной обработки с помощью микроволновой печи. Дж. Хим. Технол. Биотехнолог. 2010; 85: 127–131. doi: 10.1002/jctb.2278. [CrossRef] [Google Scholar]
23. Liu C.Z., Cheng X.Y. Улучшенное производство водорода посредством термофильной ферментации кукурузной соломы путем предварительной обработки кислотой в микроволновой печи. Междунар. Дж. Водородная энергия. 2010;35:8945–8952. doi: 10.1016/j.ijhydene.2010.06.025. [Перекрестная ссылка] [Академия Google]
24. Menegol D., Schol A.L., Dillon A.J., Camassola M. Влияние различных химических препаратов на траву слона ( Pennisetum purpureum, Schum ), используемую в качестве субстрата для производства целлюлазы и ксиланазы при глубинном культивировании. Биопроцесс Биосист. англ. 2016;39:1455–1464. doi: 10.1007/s00449-016-1623-8. [PubMed] [CrossRef] [Google Scholar]
doi: 10.1007/s00449-016-1623-8. [PubMed] [CrossRef] [Google Scholar]
25. Камиредди С.Р., Ли Дж.Б., Такер М., Дегенштейн Дж., Джи Ю. Влияние и механизм солей хлоридов металлов на предварительную обработку и ферментативную усвояемость кукурузной соломы. Инд.Инж. хим. Рез. 2013;52:1775–1782. doi: 10.1021/ie3019609. [CrossRef] [Google Scholar]
26. Кан К.Э., Пак Д.Х., Чон Г.Т. Влияние неорганических солей на предварительную обработку соломы Miscanthus . Биоресурс. Технол. 2013; 132:160–165. doi: 10.1016/j.biortech.2013.01.012. [PubMed] [CrossRef] [Google Scholar]
27. Чжан Х.Д., Лю Г.Дж., Чжан А.П., Ли С., Се Дж. Влияние предварительной обработки хлоридом железа и поверхностно-активными веществами на производство сахара из жома сахарного тростника. Биоресурс. Технол. 2018; 265:93–101. doi: 10.1016/j.biortech.2018.05.111. [PubMed] [CrossRef] [Академия Google]
28. Мэн С., Фостон М., Лейзен Дж., Демартини Дж., Вайман С.Е., Рагаускас А.Дж. Определение пористости лигноцеллюлозной биомассы до и после предварительной обработки с использованием методов окраски Саймонса и ЯМР. Биоресурс. Технол. 2013; 144:467–476. doi: 10.1016/j.biortech.2013.06.091. [PubMed] [CrossRef] [Google Scholar]
Биоресурс. Технол. 2013; 144:467–476. doi: 10.1016/j.biortech.2013.06.091. [PubMed] [CrossRef] [Google Scholar]
29. Brienzo M., Fikizolo S., Benjamin Y., Tyhoda L., Görgens J. Влияние жесткости предварительной обработки на структурные изменения, содержание лигнина и ферментативный гидролиз образцов жома сахарного тростника . Продлить. Энергия. 2017; 104: 271–280. doi: 10.1016/j.renene.2016.12.037. [Перекрестная ссылка] [Академия Google]
30. Wang W.H., Zhang C.Y., Tong S.S., Cui Z.Y., Liu P. Усиленный ферментативный гидролиз и структурные особенности кукурузной соломы с помощью комбинированной предварительной обработки NaOH и озона. Молекулы. 2018;23:13:00. doi: 10,3390/молекулы23061300. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
31. Li H., Chen X., Wang C., Sun S., Sun R. Оценка двухэтапной обработки ионными жидкостями и щелочью для усиления ферментативного гидролиза эвкалипта: химические и анатомические изменения. Биотехнолог. Биотопливо. 2016;9:166. doi: 10.1186/s13068-016-0578-y. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
doi: 10.1186/s13068-016-0578-y. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
32. Yan YH, Zhang CH, Lin QX, Wang XH, Cheng BG, Li HL, Ren JL Предварительная обработка щавелевой кислотой в микроволновой печи для усиления фермента гидролиз при производстве ксилозы и арабинозы из багассы. Молекулы. 2018;23:862. doi: 10.3390/молекулы23040862. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
33. Джин С., Чжан Г., Чжан П., Ли Ф., Ван С., Фан С., Чжоу С. Щелочная предварительная обработка с помощью микроволновой печи для усиления ферментативного осахаривания опилок катальпы. Биоресурс. Технол. 2016; 221:26–30. doi: 10.1016/j.biortech.2016.090,033. [PubMed] [CrossRef] [Google Scholar]
34. Ван З.Н., Хоу С.Ф., Сунь Дж., Ли М., Чен З.Ю., Гао З.З. Сравнение ионной жидкости с помощью ультразвука и предварительной обработки щелочью Eucalyptus для усиления ферментативного осахаривания. Биоресурс. Технол. 2018; 254:145–150. doi: 10.1016/j. biortech.2018.01.021. [PubMed] [CrossRef] [Google Scholar]
biortech.2018.01.021. [PubMed] [CrossRef] [Google Scholar]
35. Shimizu F.L., Monteiro P.Q., Ghiraldi P.H.C., Melati R.B., Pagnocca F.C., Souza W., Sant’Anna C., Brienzo M. Предварительная обработка кислотой, щелочью и пероксидом увеличивает доступность целлюлозы и выход глюкозы из псевдостебля банана. Инд. Культуры Прод. 2018; 115:62–68. doi: 10.1016/j.indcrop.2018.02.024. [Перекрестная ссылка] [Академия Google]
36. Томас Х.Л., Сейра Дж., Эскуди Р., Каррер Х. Предварительная обработка мискантуса известью: влияние на bmp и периодическое сухое совместное переваривание с навозом крупного рогатого скота. Молекулы. 2018;23:1608. doi: 10,3390/молекулы23071608. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
37. Duque A., Manzanares P., Gonzalez A., Ballesteros M. Изучение применения щелочной экструзии для предварительной обработки биомассы Eucalyptus в качестве Первый шаг в процессе производства биоэтанола. Энергии. 2018;11:2961. doi: 10.3390/en11112961. [CrossRef] [Google Scholar]
[CrossRef] [Google Scholar]
38. Ximenes E., Kim Y., Mosier N., Dien B., Ladisch M. Деактивация целлюлаз фенолами. Фермент. микроб. Технол. 2011;48:54–60. doi: 10.1016/j.enzmictec.2010.09.006. [PubMed] [CrossRef] [Google Scholar]
39. Ximenes E., Kim Y., Mosier N., Dien B., Ladisch M. Ингибирование целлюлаз фенолами. Фермент. микроб. Технол. 2010;46:170–176. doi: 10.1016/j.enzmictec.2009.11.001. [CrossRef] [Академия Google]
40. Мишлен М., Хименес Э., де Лурдес Тейшейра де Мораес Полизели М., Ладиш М.Р. Влияние фенольных соединений из предварительно обработанного багассы сахарного тростника на целлюлозолитическую и гемицеллюлозолитическую активность. Биоресурс. Технол. 2016; 199: 275–278. doi: 10.1016/j.biortech.2015.08.120. [PubMed] [CrossRef] [Google Scholar]
41. Monlau F., Sambusiti C., Barakat A., Quéméneur M., Trably E., Steyer J.P., Carrère H. Фурановые и фенольные соединения лигноцеллюлозы и биомассы водорослей гидролизат ингибирует анаэробные смешанные культуры: всесторонний обзор. Биотехнолог. Доп. 2014;32:934–951. doi: 10.1016/j.biotechadv.2014.04.007. [PubMed] [CrossRef] [Google Scholar]
Биотехнолог. Доп. 2014;32:934–951. doi: 10.1016/j.biotechadv.2014.04.007. [PubMed] [CrossRef] [Google Scholar]
42. Имман С., Арнтонг Дж., Бурапатана В., Чампред В., Лаосириподжана Н. Влияние промоторов кислоты и щелочи на предварительную обработку рисовой соломы сжатой жидкостью и горячей водой. Биоресурс. Технол. 2014; 171:29–36. doi: 10.1016/j.biortech.2014.08.022. [PubMed] [CrossRef] [Google Scholar]
43. Ривера О.М.П., Молдес А.Б., Торрадо А.М., Домингес Дж.М. Производство молочной кислоты и биосурфактантов из гидролизованных дистиллированных виноградных выжимок. Процесс биохим. 2007;42:1010–1020. doi: 10.1016/j.procbio.2007.03.011. [Перекрестная ссылка] [Академия Google]
44. Макинтош С., Ванков Т. Оптимизация предварительной обработки разбавленной щелочью для ферментативного осахаривания пшеничной соломы. Биомасса Биоэнергетика. 2011;35:3094–3103. doi: 10.1016/j.biombioe.2011.04.018. [CrossRef] [Google Scholar]
45. Meng X.Z., Wells T., Sun Q.N. , Huang F., Ragauskas A. Анализ влияния предварительной обработки разбавленной кислотой, горячей водой или щелочью на доступную для целлюлозы площадь поверхности и общее состояние пористость Populus . Зеленый хим. 2015;17:4239–4246. дои: 10.1039/C5GC00689A. [CrossRef] [Google Scholar]
, Huang F., Ragauskas A. Анализ влияния предварительной обработки разбавленной кислотой, горячей водой или щелочью на доступную для целлюлозы площадь поверхности и общее состояние пористость Populus . Зеленый хим. 2015;17:4239–4246. дои: 10.1039/C5GC00689A. [CrossRef] [Google Scholar]
46. Obeng A.K., Premjet D., Premjet S. Производство ферментируемого сахара из кожуры двух сортов дуриана ( Durio zibethinus Murr. ) путем предварительной обработки фосфорной кислотой. Ресурсы. 2018;7:60. doi: 10.3390/resources7040060. [CrossRef] [Google Scholar]
47. Phitsuwan P., Sakka K., Ratanakhanokchai K. Структурные изменения и ферментативный ответ травы Napier ( Pennisetum purpureum ), вызванные предварительной щелочной обработкой. Биоресурс. Технол. 2016; 218: 247–256. doi: 10.1016/j.biortech.2016.06.089. [PubMed] [CrossRef] [Google Scholar]
48. Jiao X.X., Jin HY, Wang M.M. Прогресс исследований в области предварительной обработки соломы для анаэробной ферментации с получением биогаза в Китае. Китай Биогаз. 2011;29:29–39. [Google Scholar]
Китай Биогаз. 2011;29:29–39. [Google Scholar]
49. Yu Y., Zheng P., Chen X.G., Cai J. Три типичных режима использования энергии биомассы при ферментации. Бык. науч. Технол. 2009; 25: 854–859. doi: 10.3969/j.issn.1001-7119.2009.06.031. (На китайском языке) [CrossRef] [Google Scholar]
50. Морено Дж., Дюфур Дж. Оценка жизненного цикла лигноцеллюлозного биоэтанола: воздействие на окружающую среду и энергетический баланс. Продлить. Поддерживать. Энергия. Ред. 2015; 42:1349–1361. doi: 10.1016/j.rser.2014.10.097. [CrossRef] [Google Scholar]
51. Du J. Novozymes ускоряет коммерциализацию целлюлозного этанола. Китайская трибуна ВТО. 2010;10:81. doi: 10.3969/j.issn.1672-1160.2010.10.019. (На китайском языке) [CrossRef] [Google Scholar]
52. Duque S.H., Cardona C.A., Moncada J. Технико-экономический и экологический анализ производства этанола из агропромышленных отходов в Колумбии. Энергетическое топливо. 2015;29:775–783. doi: 10.1021/ef5019274. [Перекрестная ссылка] [Академия Google]
53. Човау С., Деграу Д., Ван дер Брюгген Б. Критический анализ технико-экономических оценок себестоимости производства лигноцеллюлозного биоэтанола. Продлить. Поддерживать. Energy Rev. 2013; 26:307–321. doi: 10.1016/j.rser.2013.05.064. [CrossRef] [Google Scholar]
Човау С., Деграу Д., Ван дер Брюгген Б. Критический анализ технико-экономических оценок себестоимости производства лигноцеллюлозного биоэтанола. Продлить. Поддерживать. Energy Rev. 2013; 26:307–321. doi: 10.1016/j.rser.2013.05.064. [CrossRef] [Google Scholar]
54. Gubicza K., Nieves I.U., Sagues W.J., Barta Z., Shanmugam K.T., Ingram L.O. Технико-экономический анализ производства этанола из жмыха сахарного тростника с использованием сжижения и одновременного процесса осахаривания и коферментации. Биоресурс. Технол. 2016; 208:42–48. doi: 10.1016/j.biortech.2016.01.093. [PubMed] [CrossRef] [Google Scholar]
55. Денис Б., Марк М.В., Роберт Б. Больше, чем этанол: технико-экономический анализ завода по биопереработке этанола из кукурузной соломы, интегрированного с процессом гидротермального сжижения для преобразования лигнин в биохимические вещества. Биотопливо. Биопрод. Биор. 2018;12:497–509. doi: 10.1002/bbb.1866. [CrossRef] [Google Scholar]
56. Chen Y.Q., Guo X. D., Liu J.J., Zhang Z.J. Оценка маргинального земельного потенциала для энергетических установок в Китае. Земля Девелопмент. англ. Рез. 2017; 2:1–7. (на китайском языке) [Google Scholar]
D., Liu J.J., Zhang Z.J. Оценка маргинального земельного потенциала для энергетических установок в Китае. Земля Девелопмент. англ. Рез. 2017; 2:1–7. (на китайском языке) [Google Scholar]
57. Миллер Г.Л. Применение реагента динитросалициловой кислоты для определения редуцирующих сахаров. Анальный. хим. 1959; 31: 426–428. doi: 10.1021/ac60147a030. [CrossRef] [Google Scholar]
58. Государственное управление охраны окружающей среды Китая (SEPAC) Методы мониторинга и анализа воды и сточных вод. 4-е изд. Китайское издательство экологических наук; Пекин, Китай: 2002. [Google Scholar]
59. APHA . Стандартные методы исследования воды и сточных вод. 20-е изд. Американская ассоциация общественного здравоохранения; Вашингтон, округ Колумбия, США: 1998. [Google Scholar]
60. Геринг Х. К., Ван-Соест П. Дж. Сельскохозяйственный справочник № 379. Анализ кормовой клетчатки, аппаратура, реагенты, процедуры и некоторые приложения. Министерство сельского хозяйства США; Вашингтон, округ Колумбия, США: 1970.

 11.20
11.20