Pb(No3)2+2KI ионно молекулярное уравнение — Знания.site
Последние вопросы
Химия
7 минут назад
Сколько кг карбоната аммония вступит в реакцию с нитратом кальция, чтобы получить 1 кг нитрата аммонияХимия
12 минут назад
Кусочек металлического натрия массой 4,6 г опустили в стаканчик с 30 мл воды и, когда реакция закончилась, в стакан прилили 86 мл 20%-ного раствора серной кислоты. Какая соль и каким количеством вещества получилась при этом?Химия
1 час назад
СРОЧНО ДАЮ 20 БАЛОВ!!! які сульфурвмісні та нітрогенвмісні сполуки викидають в повітря та воду промисловості машини тощо.
Химия
1 час назад
Расположите перечисленные спирты в ряд по возрастанию кислотности: этиловый, изобутиловый, бутиловый, трет-бутиловый. Дайте краткое обоснование.Химия
3 часа назад
Здравствуйте, помогите пожалуйста с химией.Химия
3 часа назад
17.Розрахувати масу K2Cr2O7 в 150 мл 0,1025 н. розчину дихромату каліюХимия
3 часа назад
1. Обери тип реакцiй, характерних для алканів. А Обміну; Б заміщення; В приєднання; Г полімеризації.
А Обміну; Б заміщення; В приєднання; Г полімеризації.Химия
4 часа назад
Помогите с химией плизХимия
4 часа назад
прошу, помогите ! 1. Формальдегид объемом 67,2 л растворили в 300 г воды. Рассчитайте массовую долю альдегида в раствореХимия
4 часа назад
ZnCl2 + 2NН4ОН = Zn(OH)2↓ + 2NН4Cl уравнения) в молекулярной, полной исокращенной ионной формах.Химия
4 часа назад
очень, надо!! помогите пожалуйста!! 3. Составить уравнения реакций для метаналя – окисление, восстановление и получения метаналя из спирта
Составить уравнения реакций для метаналя – окисление, восстановление и получения метаналя из спиртаХимия
4 часа назад
1. Осуществить превращение: Этан→бромэтан→этанол→хлорэтан→бутан→этан→уксусный альдегид→уксусная кислота→бутиловый эфир уксусной кислотыХимия
4 часа назад
2.Яка вода має більше домішок: річкова чи джерельна? Поясни чому.-
Химия
4 часа назад
2Mn(OH)2↓ + О2 = 2h3MnO3 ионное и сокращённо ионное уравнение Химия
4 часа назад
4. Для речовини октін-2 Напишіть два гомолога і два
ізомера. Назвіть всі речовини.
Для речовини октін-2 Напишіть два гомолога і два
ізомера. Назвіть всі речовини.
Все предметы
English
United States
Polski
Polska
Bahasa Indonesia
Indonesia
English
India
Türkçe
Türkiye
English
Philippines
Español
España
Português
Brasil
Русский
Россия
How much to ban the user?
1 hour 1 day
ki agno3 — Google Suche
AlleBilderVideosNewsMapsShoppingBücher
Suchoptionen
Tipp: Begrenze die Suche auf deutschsprachige Ergebnisse. Du kannst deine Suchsprache in den Einstellungen ändern.
Du kannst deine Suchsprache in den Einstellungen ändern.
AgNO3 + KI → AgI + KNO3 | Chemische Gleichungen online!
chemequations.com › s=AgNO3+++KI+=+AgI+++KNO3
Gelöste und ausgeglichene chemische Gleichung AgNO3 + KI → AgI + KNO3 mit kompletten Produkten. Anwendung zur vervollständigung on Produkten und …
KI + AgNO3 → KNO3 + AgI | Chemische Gleichungen online!
chemequations.com › s=KI+++AgNO3+=+KNO3+++AgI
Gelöste und ausgeglichene chemische Gleichung KI + AgNO3 → KNO3 + AgI mit kompletten Produkten. Anwendung zur vervollständigung on Produkten und …
KI + AgNO3 = KNO3 + AgI — Chemischer Gleichungs-Ausgleicher
www.chemicalaid.com › tools › equationbalancer › equation=KI+++AgNO…
Gleiche die chemische Gleichung oder Reaktion KI + AgNO3 = KNO3 + AgI mit Hilfe dieses Rechners aus!
What happens when AgNO3 react with KI? ? | Precipitation reaction
www.youtube.com › watch
10.04.2022 · This video is the practical demonstration of the reaction of potassium iodide (KI) with sodium . ..
..
Dauer: 1:57
Gepostet: 10.04.2022
How to Write the Net Ionic Equation for AgNO3 + KI = AgI + KNO3
www.youtube.com › watch
07.04.2020 · There are three main steps for writing the net ionic equation for AgNO3 + KI = AgI + KNO3 …
Dauer: 3:11
Gepostet: 07.04.2020
Forming ppt AgNO3 and KI — YouTube
www.youtube.com › watch
06.08.2020 · Forming ppt AgNO3 and KI. Watch later. Share. Copy link. Info. Shopping. Tap to unmute. If …
Dauer: 0:24
Gepostet: 06.08.2020
Determine whether a mixture of AgNO3 and KI will … — Study.com
homework.study.com › … › Precipitation (chemistry)
Silver nitrate and potassium iodide are both soluble salt compounds in water. Mixing them together in a single aqueous solution creates the following two …
In neutralization of KI by AgNO3 positive charge is due to absorption of
www.toppr.com › … › Surface Chemistry › Catalysis
Click here to get an answer to your question ✍️ In neutralization of KI by AgNO3 positive charge is due to absorption of.
1)AgNO3+KI = AgI(стрелка — Школьные Знания.com
znanija.com › Химия › 10 — 11 классы
Найди ответ на свой вопрос: Помогите составить полное и сокращенное ионное уравнение: 1)AgNO3+KI = AgI(стрелка вниз)+KNO3 2)AgNO3+KCl = AgCl(стрелка …
Can anyone help me complete this reaction: KCl + AgNO3 + KI — Quora
www.quora.com › Can-anyone-help-me-complete-this-reaction-KCl-AgNO…
Actually, AgNO3 can cause the precipitation of both AgCl and AgI from a solution containing both KCl and KI. These reactions, very easy to write, …
Ähnliche Suchanfragen
ki + agno3 precipitate
ki + agno3 reaction
agno3 + nh5scn
ki + agno3 balanced equation
ki + agno3 complete ionic equation
ki + agno3 spectator ions
agno3 + ki precipitate color
agno3 + ki product
2 КИ (водн.) + Pb(NO3)2 (водн.) → PbI2 (тв.) + 2 KNO3 (водн.) Раствор с йодидом калия содержит 0,500 г KI. Раствор, содержащий нитрат свинца содержит 0,500 г Pb(NO3)2.
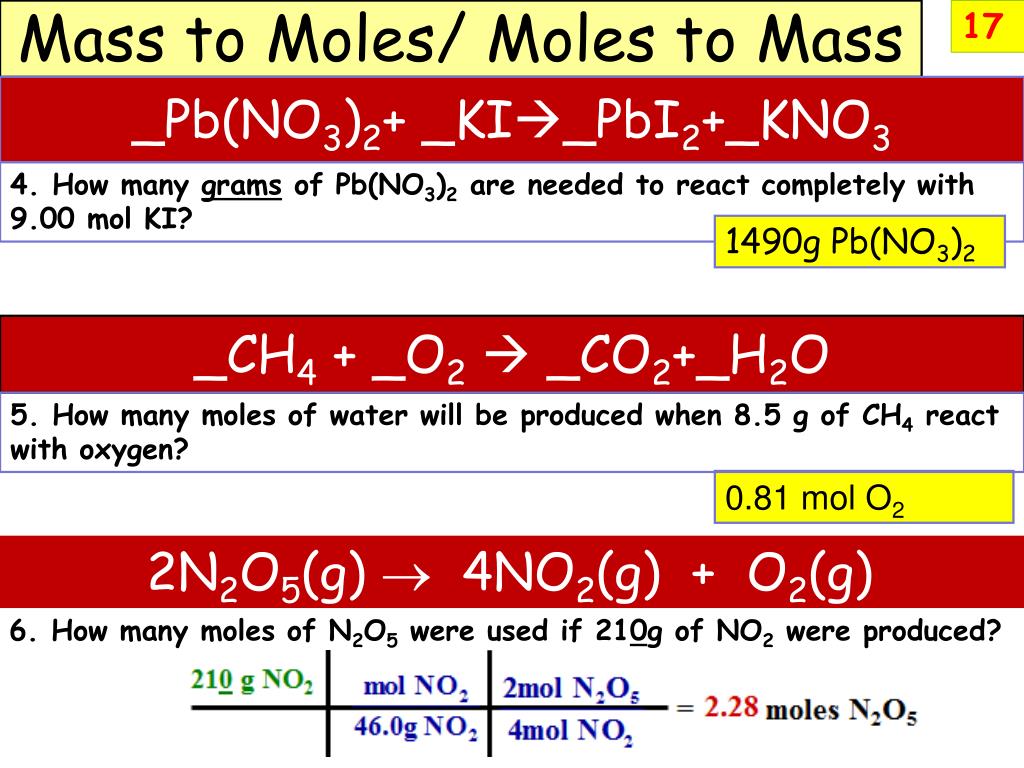 Когда
вы смешиваете их, вы формируете преципитат PbI2. Как
образуется много граммов PbI2 и какова ваша
лимитирующий реагент?
Когда
вы смешиваете их, вы формируете преципитат PbI2. Как
образуется много граммов PbI2 и какова ваша
лимитирующий реагент?Вопрос
Пошаговый ответ
2 KI (aq) + Pb(NO3)2 (водн.) → PbI2 (тв.) + 2 KNO3 (водн.) Раствор с йодидом калия содержит 0,500 г KI. Раствор, содержащий нитрат свинца содержит 0.…
2 КИ (водн.) + Pb(NO3)2 (водн.) → PbI2 (тв.) + 2 KNO3 (водн.) Раствор с йодидом калия содержит 0,500 г KI. Раствор, содержащий нитрат свинца содержит 0,500 г Pb(NO3)2. Когда вы смешиваете их, вы формируете преципитат PbI2. Как образуется много граммов PbI2 и какова ваша лимитирующий реагент?
Видеоответ:
Решено проверенным экспертом
Вопрос о лучшем совпадении:
2 KI (aq) + Pb(NO3)2 (водн.) → PbI2 (тв.) + 2 KNO3 (водн.) Раствор с йодидом калия содержит 0,500 г KI. Раствор, содержащий нитрат свинца содержит 0,500 г Pb(NO3)2. Когда вы смешиваете их, вы формируете преципитат PbI2. Как образуется много граммов PbI2 и какова ваша лимитирующий реагент?
Рекомендуемые видео
Стенограмма
Итак, у нас есть йодид калия, а затем нитрат свинца. А затем они пройдут двойную реакцию замещения с образованием йодистого свинца и нитрата калия. Раствор содержит 0,5 г йодида калия. Также раствор содержит 0,5 г нитрата свинца. Итак, когда мы смешаем эти два вещества вместе, сколько йодида свинца может образоваться, ммм, сколько граммов. Итак, чтобы понять это, нам нужно выяснить, что такое лимитирующий реагент. Итак, у нас есть одинаковое количество массы каждого продукта или, простите, каждого реагента. Хм, а затем один из них будет полностью израсходован. И затем, как только он полностью израсходуется, наша реакция прекратится. Гм. Итак, это будет наша ограничивающая область. Это ограничивает нас и мешает нам продолжать нашу реакцию и создавать больше продукта, это все равно, что сделать бутерброд, а у вас кончился хлеб. Даже если у вас остались лишние, понимаете, мясо и сыр, вы больше не сможете делать бутерброды. Ты ограничивающий реагент — твой хлеб. И как только вы сядете на хлеб, вы больше не сможете делать бутерброды. Типа такая же ситуация.
А затем они пройдут двойную реакцию замещения с образованием йодистого свинца и нитрата калия. Раствор содержит 0,5 г йодида калия. Также раствор содержит 0,5 г нитрата свинца. Итак, когда мы смешаем эти два вещества вместе, сколько йодида свинца может образоваться, ммм, сколько граммов. Итак, чтобы понять это, нам нужно выяснить, что такое лимитирующий реагент. Итак, у нас есть одинаковое количество массы каждого продукта или, простите, каждого реагента. Хм, а затем один из них будет полностью израсходован. И затем, как только он полностью израсходуется, наша реакция прекратится. Гм. Итак, это будет наша ограничивающая область. Это ограничивает нас и мешает нам продолжать нашу реакцию и создавать больше продукта, это все равно, что сделать бутерброд, а у вас кончился хлеб. Даже если у вас остались лишние, понимаете, мясо и сыр, вы больше не сможете делать бутерброды. Ты ограничивающий реагент — твой хлеб. И как только вы сядете на хлеб, вы больше не сможете делать бутерброды. Типа такая же ситуация.

 Итак, молярная масса иодида свинца. Гм Мой поводок, мы уже посмотрели Собирается быть что 207,2 г и мой я умер. Гм, он посмотрел ранее, будет 186,9. Но в моем комплексе их двое. Так что я возьму два раза и добавлю их вместе. Итак, когда я получил все это вместе, я получил 461 0,0 г на один моль моего йодида калия. Так что это все мои молярные массы, и все они будут важны. Хм, по мере того, как мы продвигаемся вперед, пытаясь решить, какая из моих устраненных областей, потому что какой бы ни была, когда мы делаем нашу историю геометрии и соотношений молей и всего размерного анализа. Тот, кто производит наименьшее количество, является моим живым реагентом. Потому что, опять же, мы можем заработать только наименьшую сумму. Итак, еще раз подумайте о моей аналогии с хлебом. Гм Чего бы ни было меньше, если бы у меня было меньше хлеба или если бы у меня было меньше мяса, гм Что бы ни было, у меня его недостаточно, чтобы сделать больше. Эм, это мой ограничивающий реагент. Это ограничивает нашу способность производить больше продукции.
Итак, молярная масса иодида свинца. Гм Мой поводок, мы уже посмотрели Собирается быть что 207,2 г и мой я умер. Гм, он посмотрел ранее, будет 186,9. Но в моем комплексе их двое. Так что я возьму два раза и добавлю их вместе. Итак, когда я получил все это вместе, я получил 461 0,0 г на один моль моего йодида калия. Так что это все мои молярные массы, и все они будут важны. Хм, по мере того, как мы продвигаемся вперед, пытаясь решить, какая из моих устраненных областей, потому что какой бы ни была, когда мы делаем нашу историю геометрии и соотношений молей и всего размерного анализа. Тот, кто производит наименьшее количество, является моим живым реагентом. Потому что, опять же, мы можем заработать только наименьшую сумму. Итак, еще раз подумайте о моей аналогии с хлебом. Гм Чего бы ни было меньше, если бы у меня было меньше хлеба или если бы у меня было меньше мяса, гм Что бы ни было, у меня его недостаточно, чтобы сделать больше. Эм, это мой ограничивающий реагент. Это ограничивает нашу способность производить больше продукции.
 165,998. И так я получаю число умноженное на два. Итак, 331 996. А затем я делю верх на низ, чтобы вычислить, сколько граммов йодида свинца я создаю. Итак, когда я беру верхние 2 30, деленные на 331. Хм, я получаю 3310,6 94 грамма моего, не так ли? Вот сколько продукта я получаю, используя 0,5 г йодида калия. Итак, теперь давайте посмотрим на мой нитрат свинца. Я собираюсь получить 0,5 г 0,500 г нитрата свинца. А затем я хочу отменить граммы нитрата свинца и преобразовать их в моли. Так что я знаю за каждый моль нитрата свинца. Гм мы подсчитали, что я получаю 200 и 83 3211 г. Итак, 283 0,2 грамма нитрата свинца. Тогда я должен использовать свой многомольный коэффициент. Итак, коэффициент 11. Так что у меня есть еще один мой нитрат свинца на каждый моль моей идеи. И я знаю, что на каждый моль йодистого свинца я получаю то же число, что и на 461 000 г йодистого свинца. Итак, я возьму числа, умножив их сверху, Итак, 0,5 умножить на один раз 1 умножить на 4 61. Эм, и это будет верхнее число.
165,998. И так я получаю число умноженное на два. Итак, 331 996. А затем я делю верх на низ, чтобы вычислить, сколько граммов йодида свинца я создаю. Итак, когда я беру верхние 2 30, деленные на 331. Хм, я получаю 3310,6 94 грамма моего, не так ли? Вот сколько продукта я получаю, используя 0,5 г йодида калия. Итак, теперь давайте посмотрим на мой нитрат свинца. Я собираюсь получить 0,5 г 0,500 г нитрата свинца. А затем я хочу отменить граммы нитрата свинца и преобразовать их в моли. Так что я знаю за каждый моль нитрата свинца. Гм мы подсчитали, что я получаю 200 и 83 3211 г. Итак, 283 0,2 грамма нитрата свинца. Тогда я должен использовать свой многомольный коэффициент. Итак, коэффициент 11. Так что у меня есть еще один мой нитрат свинца на каждый моль моей идеи. И я знаю, что на каждый моль йодистого свинца я получаю то же число, что и на 461 000 г йодистого свинца. Итак, я возьму числа, умножив их сверху, Итак, 0,5 умножить на один раз 1 умножить на 4 61. Эм, и это будет верхнее число. Так что я все это делаю. У меня 230,5. А потом я брал цифры по дну. Так до 83.211 раз один раз один. Так что я получу там то же число, потому что я умножаю на единицу. Итак, чтобы получить 83,211, возьмите верх, разделенный на низ. И поэтому, когда я это делаю, у меня остаются граммы йодистого калия. При подсчетах я получаю 0,814 граммов йодистого калия. Итак, глядя на эти два числа, это число является моим меньшим числом, которое говорит мне, что это мой ограниченный свободный агент, потому что как только весь мой йодид калия израсходован, реакция останавливается. Так что это весь продукт, который я могу сделать из 0,5 г каждого продукта или а на каждый реактор. Так что это мой ограничивающий реагент, и это то, сколько йодида свинца я могу получить из моего .69.4
Так что я все это делаю. У меня 230,5. А потом я брал цифры по дну. Так до 83.211 раз один раз один. Так что я получу там то же число, потому что я умножаю на единицу. Итак, чтобы получить 83,211, возьмите верх, разделенный на низ. И поэтому, когда я это делаю, у меня остаются граммы йодистого калия. При подсчетах я получаю 0,814 граммов йодистого калия. Итак, глядя на эти два числа, это число является моим меньшим числом, которое говорит мне, что это мой ограниченный свободный агент, потому что как только весь мой йодид калия израсходован, реакция останавливается. Так что это весь продукт, который я могу сделать из 0,5 г каждого продукта или а на каждый реактор. Так что это мой ограничивающий реагент, и это то, сколько йодида свинца я могу получить из моего .69.4Поделиться вопросом
Добавить в плейлист
Хммм, похоже, у вас нет плейлистов. Пожалуйста, добавьте свой первый плейлист.
`
2KI + Pb(NO3)2 = 2KNO3 + PbI2
| Поиск |
иодид калия + нитрат свинца(ii) = нитрат калия + иодид свинца |
Новости Только 5% НАСЕЛЕНИЯ знают
Реклама
Содержание
Нажмите, чтобы увидеть более подробную информацию и рассчитать вес/моль >>
| jpg» substance-weight=»166.00277 ± 0.00013″> 2KI | + | Pb(NO 3 ) 2 | → | 2KNO 3 | + | PbI 2 | |
| йодид калия | нитрат свинца(ii) | нитрат калия | Иодид свинца; дииодид свинца; иодид свинца(II); Lead(II) diiodide | ||||
| 2 | 1 | 2 | 1 | Хо Со | |||
| Nguyên — Phân tử khối (g/mol) | |||||||
| Số mol | |||||||
| Хой лунг (г) |
Реклама
Дополнительная информация об уравнении 2KI + Pb(NO
3 ) 2 → 2KNO 3 + PbI 2В каких условиях KI (йодид калия) реагирует с Pb(NO3)2 (нитратом свинца(ii)) ?
Для этого химического уравнения не найдено информации
Объяснение: идеальные условия окружающей среды для реакции, такие как температура, давление, катализаторы и растворитель. Катализаторы — это вещества, которые ускоряют темп (скорость) химической реакции, не потребляясь и не становясь частью конечного продукта.
Катализаторы не влияют на равновесные ситуации.
Катализаторы — это вещества, которые ускоряют темп (скорость) химической реакции, не потребляясь и не становясь частью конечного продукта.
Катализаторы не влияют на равновесные ситуации.
Как могут происходить реакции с образованием KNO3 (нитрат калия) и PbI2 (йодид свинца; дииодид свинца; йодид свинца(II); дийодид свинца(II) ?
В полном предложении вы также можете сказать, что KI (йодид калия) реагирует с Pb(NO3)2 (нитратом свинца(ii)) и производит KNO3 (нитрат калия) и PbI2 (йодид свинца; дийодид свинца; йодид свинца(II); Дииодид свинца(II)
Явление после взаимодействия KI (иодида калия) с Pb(NO3)2 (нитрат свинца(ii))
Это уравнение не несет никакой конкретной информации о явлении.
В этом случае вам просто нужно наблюдать, чтобы убедиться, что вещество продукта PbI2 (Иодид свинца; Дииодид свинца; Иодид свинца(II); Дииодид свинца(II)), появляющийся в конце реакции.
Или если какое-либо из следующих реагентов Pb(NO3)2 (нитрат свинца(ii)), исчезает
Какую другую важную информацию вы должны знать о реакции
У нас нет дополнительной информации об этой химической реакции.
Категории уравнения
Другие вопросы, связанные с химическими реакциями 2KI + Pb(NO
3 ) 2 → 2KNO 3 + PbI 2Вопросы, связанные с химическим веществом и
KI (калий) Характеристика KI (йодида калия)? В каких химических реакциях используется KI (йодид калия) в качестве реагента?
Вопросы, связанные с реагентом Pb(NO3)2 (нитрат свинца(ii))
Каковы химические и физические характеристики Pb(NO3)2 (нитрат свинца(ii))? NO3)2 (нитрат свинца(ii)) в качестве реагента?
Вопросы, связанные с продуктом KNO3 (нитрат калия)
Каковы химические и физические характеристики KNO3 (нитрат свинца(ii))?Каковы химические реакции, в которых KNO3 (нитрат калия) является продуктом?
Вопросы, связанные с продуктом PbI2 (йодид свинца; дииодид свинца; йодид свинца(II); дийодид свинца(II))
Каковы химические и физические характеристики PbI2 (нитрата свинца(ii))?Каковы химические реакции которые содержат PbI2 (йодид свинца; дииодид свинца; йодид свинца(II); дийодид свинца(II))?
Essentt — Товары, подобранные вручную
Продукты, подобранные вручную Необходимы для работы из дома!
Уравнения с KI в качестве реагента
калия йодид
KI + CH 3 CH(Br)CH 2 (Br) → KBr + IBr + CH 2 =CHCH 3 H 2 O + 2KI + O 72 I 3 + 2KOH + O 2 2KI + SO 3 → I 2 + K 2 SO 3 Просмотреть все уравнения с KI в качестве реагента
Уравнения с Pb(NO3)2 в качестве реагента
нитрат свинца(ii)
2Pb(NO 3 ) 2 → 4NO 2 + 4O 2 + 2PbO H 2 S + Pb(NO 3 ) 2 → 2HNO 3 + PbS Na 2 SO 4 + Pb(NO 3 ) 2 → 2NaNO 3 + PbSO 4 Просмотреть все уравнения с Pb(NO3)2 в качестве реагента
Реклама
Уравнения с Pb(NO3)2 в качестве продукта
нитрат свинца(ii)
2HNO 3 + Pb → H 2 O + Pb(NO 3 ) 2 6HNO 3 + 2Mn(NO 3 ) 2 + 5PbO 2 → 2H 2 O + 5PB (NO 3 ) 2 + 2HMNO 4 2HNO 3 + PB (OH) 2 → 2H 2 O + PB (№ 3 ) 2 333.


 А Обміну; Б заміщення; В приєднання; Г полімеризації.
А Обміну; Б заміщення; В приєднання; Г полімеризації. Составить уравнения реакций для метаналя – окисление, восстановление и получения метаналя из спирта
Составить уравнения реакций для метаналя – окисление, восстановление и получения метаналя из спирта Для речовини октін-2 Напишіть два гомолога і два
ізомера. Назвіть всі речовини.
Для речовини октін-2 Напишіть два гомолога і два
ізомера. Назвіть всі речовини.