2.NaOH күшті негіз (к.н.) және HCl күштіқышқыл (к.қ.) әрекеттескенде түзілетін тұз.
NaCl —> Na(+)+ CI(-)
НОН —> Н(+) +ОН(-)
Жақсы Жауап
ЖЖ таңдарсың )
Ұқсас сұрақтар
1 жауап
NaOH+HNO3-> Cu(OH)2+HCL-> Cu(oH)2-> Fe(OH)3-> ….+….->KOH+h3 реакция теңдеулерін аяқтау керек
нурболовнаХимия 5.02.2013 сұрақ қойды | 3.1k қаралды
- реакция теңдеуі
- ақпарат
- химия
1 жауап
Na2CO3+HCL=? NaOH+HCL=? Fe(OH)3+HNO3=? Mg+h3SO4=?
Белгісіз Химия 17.02.2013 сұрақ қойды | 1.8k қаралды
- реакция теңдеуі
- ақпарат
- химия
1 жауап
Мына заттардың қайсысы натрий гидроксидімен әрекеттеседі: HCL, CaO, h3SO4, CO,KCL, CuO
нурболовнаХимия 5.02.2013 сұрақ қойды | 6.9k қаралды
- реакция теңдеуі
- ақпарат
2 жауап
NaOH+HCL->NaCL+h3O Тауып берсеңіздер АЛЛАНЫҢ НҰРЫ жаусын!
Белгісіз
Химия
16. 02.2013
сұрақ қойды
|
1.6k қаралды
02.2013
сұрақ қойды
|
1.6k қаралды
- реакция теңдеуі
- ақпарат
- қазақша сұрақ
1 жауап
Na2CO3+HCL=? КӨМЕК КӨМЕК КӨМЕК КӨМЕК
Белгісіз Химия 17.02.2013 сұрақ қойды | 970 қаралды
- реакция теңдеуі
- ақпарат
- химия
- Санаттар
- Мектеп сұрақтары
29.3k
- Мектеп 9.0k
- Қазақ тілі 5.7k
- Математика 3.1k
- Химия 2.5k
- Информатика 627
- Аспан әлемі, Ғарыш 191
- Геометрия 1.4k
- Физика 2.6k
- Биология 903
- Психология 197
- География 823
- ҰБТ жайлы 988
- Үй тапсырмасы 1.1k
- Серпін-2050 жобасы 73
- Университет, колледж 4.1k
- Тарих сұрақтары 2.0k
- Компьютер, Интернет 16.5k
- Авто 1.1k
- Қаржы, Бизнес 2.1k
- Саясат, Мемлекет 1.7k
- Заң 2.0k
- Өмір, Тіршілік
4.
 9k
9k - Тағам, Аспаздық 990
- Жұмыс 1.4k
- Экология, Табиғат 1.4k
- Денсаулық 6.5k
- Спорт 3.1k
- Танысу, Махаббат 2.7k
- Көңіл-көтеру 1.7k
- Өнер 1.5k
- Қыдыру, Демалыс 453
- Кітап, Әдебиет 3.4k
- Құрылыс, Жобалау 392
- Музыка, Ән 5.8k
- Ұялы телефон 5.3k
- Әлеуметтік желі 1.6k
- Кино, Теледидар 3.1k
- Сурет, Видео 1.4k
- Тұлға, Адам 3.0k
- Салт-дәстүр 1.0k
- Логикалық сұрақтар 3.3k
- Жалпы сұрақ 14.0k
- Онлайн конференция 16
напишите реакции аминоуксусной кислоты с NaOH,HCI,h3SO4 — Знания.site
Последние вопросы
Химия
17 минут назад
Химия. Химический диктант по теме: «Углерод и его соединения»Химия
23 минут назад
Реакція оцтової кислоти з нерозчинною основою (амфотерним гідроксидом) Налийте в пробірку 1 мл розчину лугу і додайте стільки ж розчину купрум(II) сульфату або виданого вам розчину іншої солі. Що спостерігаєте? Перемішайте суміш з осадом і долийте до неї 2 мл розчину оцтової кислоти. Що відбувається в пробірці?
Що спостерігаєте? Перемішайте суміш з осадом і долийте до неї 2 мл розчину оцтової кислоти. Що відбувається в пробірці?Химия
28 минут назад
Яку масу нітратної кислоти потрібно використати для повного розчинення осаду купрум (ІІ) гідроксиду масою 9,8 г ? *Химия
42 минут назад
Решите задачу по химииХимия
43 минут назад
Вычисли массу кислорода, который содержится в порции фосфорной кислоты массой 40 г. В промежуточных расчётах результат округляй до сотых, ответ — до целых.Химия
43 минут назад
Обчисліть об’єм газу Н2S кількістю речовини 4 моль.
48 минут назад
Химия 8 классХимия
48 минут назад
— Рассчитайте массу (кг) стеарата натрия, который можно получить при щелочном гидролизе триглицерида массой 1,55 т с массовой долей тристеарата глицерина, равной 95 %, если практический выход стеарата составляет 80 % (М 890 г/моль) напишите пожалуйста подробное решениеХимия
53 минут назад
пожалуйста, помогите мне 3-methylpentene-1Химия
1 час назад
Реакція оцтової кислоти з основним (амфотерним) оксидом Помістіть у пробірку трохи порошку купрум(II) оксиду або іншого виданого вам оксиду і налийте 2 мл i розчину оцтової кислоти. Що спостерігаєте? За потре- би нагрійте вміст пробірки, але не до кипіння.
Що спостерігаєте? За потре- би нагрійте вміст пробірки, але не до кипіння.Химия
1 час назад
Хімія 8 клас. Будь ласка, швидше. Буду дуже вдячна!Напишіть рівняння реакцій, за допомогою яких можна здійснити такі перетворення: 1. Барій — барій оксид — барій гідроксид — барій сульфат. 2. Фосфор — фосфор(V) оксид → ортофосфатна кислота.Химия
1 час назад
1. Укажите ряд, в котором представлены электронные конфигура- ции, соответствующие основному состоянию атомов неметаллов VIIA- и VIA-групп соответственно: a) 1s22s22p5 и 1s22s22p63s2; 6) 1s²2s²2p³ и 1s²2s²2p63s²3p³; og в) 1s22s22p63s23р³ и 1s²2s22p63s1; г) 1s22s22p63s23p³ и 1s22s22p4.Химия
1 час назад
Помогите с заданием по химии пожалуйстаХимия
1 час назад
яка речовина утвориться під час пропускання водню через рідкий жирХимия
1 час назад
6. Під час спалювання 112 г фосфіну(РН,) утворилося 233 г
фосфор(V) оксид та 89 г води. Знайдіть масу кисню та запишіть
хiмiчне рiвняння.
Під час спалювання 112 г фосфіну(РН,) утворилося 233 г
фосфор(V) оксид та 89 г води. Знайдіть масу кисню та запишіть
хiмiчне рiвняння.
Все предметы
Выберите язык и регион
English
United States
Polski
Polska
Português
Brasil
English
India
Türkçe
Türkiye
English
Philippines
Español
España
Bahasa Indonesia
Indonesia
Русский
Россия
How much to ban the user?
1 hour 1 day 100 years
кислотно-щелочное — Выбор между окислительно-восстановительными реакциями и реакциями нейтрализации для смеси HCl, h3SO4 и NaOH
Как мы с Клаусом упоминали, первые реакции кажутся очень странными с химической точки зрения, даже если они правильно сбалансированы.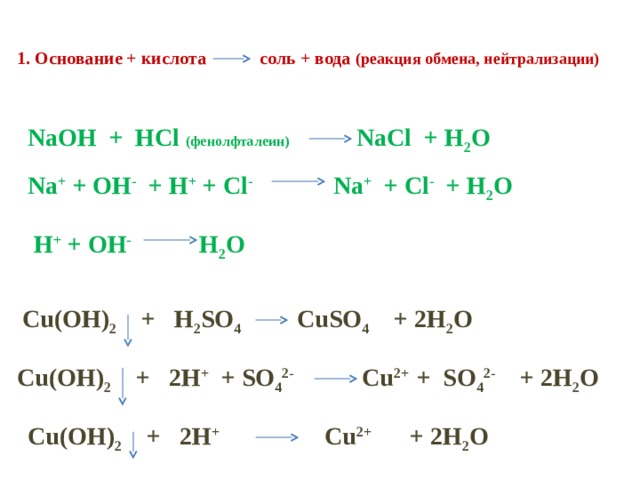
Это предназначено только как качественный способ сравнения реакций, так как я предполагаю стандартные условия для реакций, которые не обязательно верны. Кроме того, для нескольких видов я не нашел правильных значений в этих двух источниках [1] [2]. $\ce{SCl2}$ и $\ce{S2Cl2}$, вероятно, не могут быть найдены в таблице для водной фазы из-за их склонности к гидролизу, поэтому я использовал свободные энергии образования для газовой и твердой фаз соответственно. Я также не нашел источника для водного $\ce{Na2SO4}$, поэтому вместо этого использовал данные для твердого декагидрата $\ce{Na2SO4. 10 ч3О(с)}$. Результаты, которые я получил: 9{-1}}\\ \hline \текст{А} и +440 \\ \text{B} & +1940 \\ \текст{С} и +590 \\ \text{D} и \mathbf{-2610} \\ \hline \конец{массив} $$
Как видите, несмотря на то, что расчет был очень грубым, огромная разница в значениях свободной энергии говорит о том, что первые три реакции полностью подавляются последней, так что из четырех перечисленных возможностей только последняя любой шанс возникновения. Строго говоря, это не означает, что происходит последняя реакция, а только то, что она гораздо более благоприятна, чем другие представленные; может быть незарегистрированная реакция, которая даже более благоприятна, чем все четыре, упомянутые в вопросе. Однако эмпирические данные подтверждают, что последняя реакция, простая реакция нейтрализации, является основным при смешивании $\ce{HCl}$, $\ce{h3SO4}$ и $\ce{NaOH}$ практически в любых условиях.
Строго говоря, это не означает, что происходит последняя реакция, а только то, что она гораздо более благоприятна, чем другие представленные; может быть незарегистрированная реакция, которая даже более благоприятна, чем все четыре, упомянутые в вопросе. Однако эмпирические данные подтверждают, что последняя реакция, простая реакция нейтрализации, является основным при смешивании $\ce{HCl}$, $\ce{h3SO4}$ и $\ce{NaOH}$ практически в любых условиях.
Видео с вопросами: Расчет объема серной кислоты, который полностью нейтрализует заданный объем и концентрацию гидроксида натрия
Стенограмма видео
Какой объем 0,5-молярной серной кислоты полностью нейтрализует 125 миллилитров 0,1-молярного гидроксида натрия?
Чтобы ответить на этот вопрос, нам нужно использовать объем и концентрацию гидроксида натрия, данные вместе с концентрацией серной кислоты, чтобы определить объем серной кислоты, необходимый для полной нейтрализации раствора гидроксида натрия. Эта проблема может быть решена в несколько шагов. Чтобы связать два разных вещества друг с другом, участвующие в химической реакции, нам нужно знать количество молей одного из веществ и их молярное соотношение. Поскольку вопрос дает нам две части информации о гидроксиде натрия и только одну информацию о серной кислоте, мы начнем с определения количества молей гидроксида натрия в 125 миллилитрах 0,1-молярного раствора.
Чтобы связать два разных вещества друг с другом, участвующие в химической реакции, нам нужно знать количество молей одного из веществ и их молярное соотношение. Поскольку вопрос дает нам две части информации о гидроксиде натрия и только одну информацию о серной кислоте, мы начнем с определения количества молей гидроксида натрия в 125 миллилитрах 0,1-молярного раствора.
Для этого воспользуемся уравнением 𝑛 равно 𝑐𝑉, где 𝑛 представляет количество в молях, 𝑐 — концентрация в молях на литр, а 𝑉 — объем в литрах. Нам дана концентрация гидроксида натрия в молях, которая совпадает с концентрацией в молях на литр. Объем указан в миллилитрах. Но чтобы использовать уравнение, объем должен быть в литрах. Один литр равен 1000 миллилитров. Мы можем преобразовать 125 миллилитров в литры, умножив на один литр на 1000 миллилитров. Единица миллилитры сократится, и мы получим значение 0,125 литра.
Теперь мы можем определить количество молей гидроксида натрия. Литровые единицы сократятся, и мы получим значение 0,0125 моль. Теперь, когда мы знаем количество молей гидроксида натрия, нам нужно знать молярное отношение гидроксида натрия к серной кислоте. Итак, нам нужно написать сбалансированное химическое уравнение. Химическая формула серной кислоты – h3SO4, а химическая формула гидроксида натрия – NaOH.
Теперь, когда мы знаем количество молей гидроксида натрия, нам нужно знать молярное отношение гидроксида натрия к серной кислоте. Итак, нам нужно написать сбалансированное химическое уравнение. Химическая формула серной кислоты – h3SO4, а химическая формула гидроксида натрия – NaOH.
Когда серная кислота, сильная кислота, реагирует с гидроксидом натрия, образуется сильное основание, соль и вода. Вода получается из иона водорода из кислоты и иона гидроксида из основания. Это означает, что соль должна образовываться, когда ион сульфата из кислоты соединяется с ионом натрия из основания. Ионы натрия имеют заряд один плюс, а ионы сульфата — два минус. Чтобы соединение имело общий нейтральный заряд, на каждый ион сульфата должно приходиться два иона натрия.
Мы записали произведения этого химического уравнения, но уравнение не уравновешено. Мы видим, что на стороне продукта два атома натрия, а на стороне реагента только один атом натрия. Поэтому нам нужно поставить коэффициент два перед гидроксидом натрия. С учетом этого коэффициента мы видим, что на стороне реагента имеется четыре атома водорода и только два атома водорода на стороне продукта. Таким образом, нам нужно разместить коэффициент два перед водой.
С учетом этого коэффициента мы видим, что на стороне реагента имеется четыре атома водорода и только два атома водорода на стороне продукта. Таким образом, нам нужно разместить коэффициент два перед водой.
Теперь, когда у нас есть сбалансированное химическое уравнение, мы можем видеть, что молярное отношение серной кислоты к гидроксиду натрия составляет один к двум. Мы можем использовать меньшее соотношение для расчета количества молей серной кислоты из количества молей гидроксида натрия. В реакции участвовало 0,0125 моль гидроксида натрия. Мы можем умножить это значение на молярное отношение, записанное в виде дроби с молями гидроксида натрия в знаменателе, так что единицы сокращаются. Выполнение расчета дает нам значение 0,00625 моль серной кислоты.
Теперь мы наконец можем рассчитать объем серной кислоты. Еще раз, мы будем использовать уравнение 𝑛 равно 𝑐𝑉. Концентрация была указана в вопросе, а мы просто подсчитали количество молей серной кислоты. Таким образом, мы можем подставить эти значения в уравнение.

 9k
9k Що спостерігаєте? Перемішайте суміш з осадом і долийте до неї 2 мл розчину оцтової кислоти. Що відбувається в пробірці?
Що спостерігаєте? Перемішайте суміш з осадом і долийте до неї 2 мл розчину оцтової кислоти. Що відбувається в пробірці?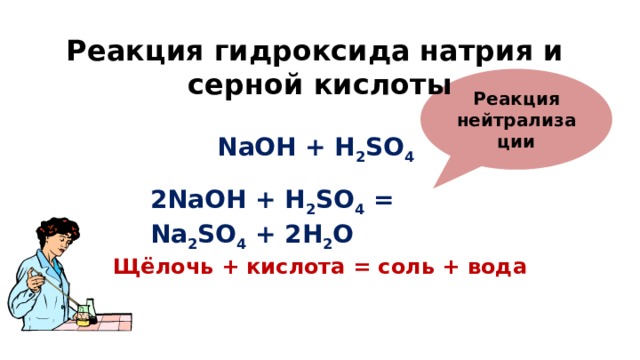
 Що спостерігаєте? За потре- би нагрійте вміст пробірки, але не до кипіння.
Що спостерігаєте? За потре- би нагрійте вміст пробірки, але не до кипіння. Під час спалювання 112 г фосфіну(РН,) утворилося 233 г
фосфор(V) оксид та 89 г води. Знайдіть масу кисню та запишіть
хiмiчне рiвняння.
Під час спалювання 112 г фосфіну(РН,) утворилося 233 г
фосфор(V) оксид та 89 г води. Знайдіть масу кисню та запишіть
хiмiчне рiвняння.