«Почему у водорода нет нейтрона?» — Яндекс Кью
Популярное
Сообщества
Мисс Элих
·
14,0 K
ОтветитьУточнитьПавел Васильев
11
Химик-аналитик, информационные технологии (на уровне любителя). · 5 янв 2021
Это обусловлено строением атома элемента. Атом любого элемента обычно состоит из протонов, нейтронов и электронов. В атоме обычного водорода содержится один протон и один электрон. Иногда ион H+ (обратите внимание, речь об ионе, а не об атоме; это разные понятия) так и называют — протон.
По одной из версий нейтрона в обычном атоме водорода действительно нет. А если он появляется, свойства очень сильно меняются, поэтому оба стабильных изотопов имеют свои названия дейтерий (один нейтрон) и тритий (2 нейтрона).
По другой версии атом обычного водорода содержит один протон, один электрон и один нейтрон. А изотопы дейтерий (2 нейтрона) и тритий (3 нейтрона) содержат ещё и 2 электрона и 2 протона; и 3 электрона и 3 протона соответственно для каждого помимо указанного для каждого числа нейтронов. Т.е. обычный ион водорода (не путайте с атомом, он всегда электрически нейтрален, т.е. заряда никогда не имеет; ион же всегда имеет какой-либо заряд («+» или «-«)) будет H+ , ион дейтерия h3+ (ион водорода с зарядом 2+), а ион трития h4+ (ион водорода с зарядом 3+). Это в корне неверная теория, она противоречит истинному строению атома водорода и его изотопов.
На основании последних исследований всё больше современных учёных и исследователей склоняются к первой версии как к наиболее верной и правильной.
Сейчас в современных источниках информации всё больше ссылок на первую версию и именно её авторы источников предлагают принять как единственно правильную и достоверную, а также всё больше и больше использовать её для изучения и различных расчётов.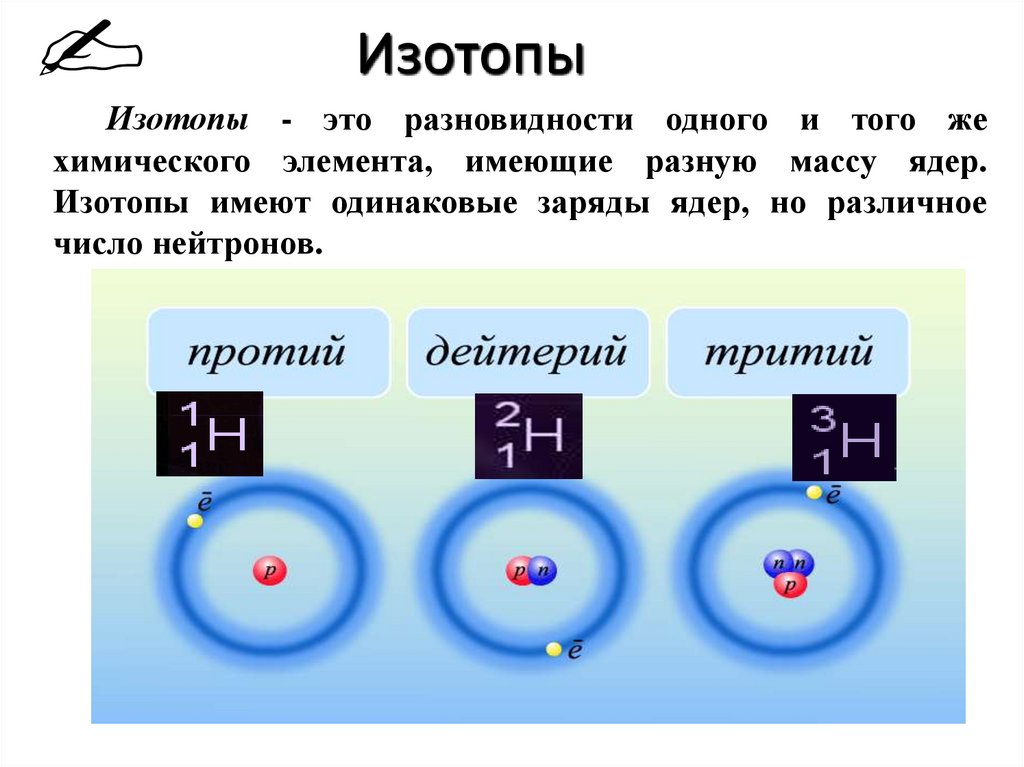
В самых старых источниках информации верной и единственно правильной принято считать вторую версию. Хотя, на основании многолетних исследований атома водорода доподлинно известно, что ион обычного водорода имеет степень окисления (заряд) +1. В свете всех выше изложенных фактов первая теория выглядит всё же более состоятельнее и ближе к истине, нежели вторая.
Водород пока изучен не в полной мере. Учёные до сих пор спорят не только по поводу данных теорий, но даже о том, к какой группе в Периодической таблице (системе) химических элементов Дмитрия Ивановича Менделеева можно окончательно отнести водород: к первой или всё же к седьмой. Поэтому водород пока принадлежит к обоим группам Периодической таблицы. Это решение было принято на основании последних данных о свойствах и электронном строении атома этого загадочного элемента, а также свойствах его изотопов и данных об электронном строении атомов данных изотопов водорода, учитывая все известные особенности электронного строения и свойств и атомов, и ионов, и молекул, и самих свободных веществ как обычного водорода, так и всех его изотопов, включая нестабильные; с учётом всех физико-химических свойств этих свободных веществ, а также и целого ряда других не менее важных факторов.
Подведём итоги.
Атом любого вещества состоит из ядра и электронов (отрицательно заряженных частиц), движущихся по орбитам вокруг него. Ядро атома содержит положительно заряженные частицы — протоны, и частицы с нейтральным зарядом — нейтроны. В обычном атоме число электронов и протонов совпадает, а вот количество нейтронов может отличаться. В этом случае элементы, имеющие разное число нейтронов в ядре, называются изотопами элемента. Ион водорода имеет заряд +1, в атоме обычного водорода содержится один электрон и один протон. Его изотопы — протий, дейтерий и тритий. Слово «протий» образовано от греческого слова «первый». Этот элемент имеет лишь один протон в ядре. По сути, он представляет собой привычный нам водород. Дейтерий означает «второй». В его ядре имеется один протон и один нейтрон. А тритий переводится как «третий» и содержит в ядре опять же один протон, но два нейтрона.
Николай Семенов
5 января 2021
можно ссылку где ион водорода(не путать с атомом) обычно нейтральный, а ион трития имеет заряд т+3?
Комментировать ответ…Комментировать…
Михаил Реутин
Медицина
8,9 K
врач-педиатр · 27 мая 2018
Не совсем понял ваш вопрос. Протон вполне себе есть. Я даже больше скажу — на жаргоне ион H+ так и называется — протон.
Протон вполне себе есть. Я даже больше скажу — на жаргоне ион H+ так и называется — протон.
А вот нейтрона в обычном водороде нет. А если он появляется, свойства меняются очень сильно, поэтому оба стабильны изотопов имеют свои названия дейтерий (один нейтрон) и тритий (2 нейтрона).
ТРИКСТЕР
3 декабря
А в молекуле Н2 есть ли нейтроны!?!
И что тогда обращует массу молекулы водорода, если нет нейтронов??!
Комментировать ответ…Комментировать…
Вы знаете ответ на этот вопрос?
Поделитесь своим опытом и знаниями
Войти и ответить на вопрос
| 1 | Найти число нейтронов | H | |
| 2 | Найти массу одного моля | H_2O | |
| 3 | Баланс | H_2(SO_4)+K(OH)→K_2(SO_4)+H(OH) | |
| 4 | Найти массу одного моля | H | |
| 5 | Найти число нейтронов | Fe | |
| 6 | Найти число нейтронов | Tc | |
| 7 | Найти конфигурацию электронов | H | |
| 8 | Найти число нейтронов | ||
| 9 | Баланс | CH_4+O_2→H_2O+CO_2 | |
| 10 | Найти число нейтронов | C | |
| 11 | Найти число протонов | H | |
| 12 | Найти число нейтронов | O | |
| 13 | Найти массу одного моля | CO_2 | |
| 14 | Баланс | C_8H_18+O_2→CO_2+H_2O | |
| 15 | Найти атомную массу | H | |
| 16 | Определить, растворима ли смесь в воде | H_2O | |
| 17 | Найти конфигурацию электронов | Na | |
| 18 | Найти массу одного атома | H | |
| 19 | Найти число нейтронов | Nb | |
| 20 | Найти число нейтронов | Au | |
| 21 | Найти число нейтронов | Mn | |
| 22 | Найти число нейтронов | Ru | |
| 23 | Найти конфигурацию электронов | ||
| 24 | Найти массовую долю | H_2O | |
| 25 | Определить, растворима ли смесь в воде | NaCl | |
| 26 | Найти эмпирическую/простейшую формулу | H_2O | |
| 27 | Найти степень окисления | H_2O | |
| 28 | Найти конфигурацию электронов | K | |
| 29 | Найти конфигурацию электронов | Mg | |
| 30 | Найти конфигурацию электронов | Ca | |
| 31 | Найти число нейтронов | Rh | |
| 32 | Найти число нейтронов | Na | |
| 33 | Найти число нейтронов | Pt | |
| 34 | Найти число нейтронов | Be | Be |
| 35 | Найти число нейтронов | Cr | |
| 36 | Найти массу одного моля | H_2SO_4 | |
| 37 | Найти массу одного моля | HCl | |
| 38 | Найти массу одного моля | Fe | |
| 39 | Найти массу одного моля | C | |
| 40 | Найти число нейтронов | Cu | |
| 41 | Найти число нейтронов | S | |
| 42 | Найти степень окисления | H | |
| 43 | Баланс | CH_4+O_2→CO_2+H_2O | |
| 44 | Найти атомную массу | O | |
| 45 | Найти атомное число | H | |
| 46 | Найти число нейтронов | Mo | |
| 47 | Найти число нейтронов | Os | |
| 48 | Найти массу одного моля | NaOH | |
| 49 | Найти массу одного моля | O | |
| 50 | Найти конфигурацию электронов | Fe | |
| 51 | Найти конфигурацию электронов | C | |
| 52 | Найти массовую долю | NaCl | |
| 53 | Найти массу одного моля | ||
| 54 | Найти массу одного атома | Na | |
| 55 | Найти число нейтронов | N | |
| 56 | Найти число нейтронов | Li | |
| 57 | Найти число нейтронов | V | |
| 58 | Найти число протонов | N | |
| 59 | Упростить | H^2O | |
| 60 | Упростить | h*2o | |
| 61 | Определить, растворима ли смесь в воде | H | |
| 62 | Найти плотность при стандартной температуре и давлении | H_2O | |
| 63 | Найти степень окисления | NaCl | |
| 64 | Найти атомную массу | He | He |
| 65 | Найти атомную массу | Mg | |
| 66 | Найти число электронов | H | |
| 67 | Найти число электронов | O | |
| 68 | Найти число электронов | S | |
| 69 | Найти число нейтронов | Pd | |
| 70 | Найти число нейтронов | Hg | |
| 71 | Найти число нейтронов | B | |
| 72 | Найти массу одного атома | Li | |
| 73 | Найти эмпирическую формулу | H=12% , C=54% , N=20 | , , |
| 74 | Найти число протонов | Be | Be |
| 75 | Найти массу одного моля | Na | |
| 76 | Найти конфигурацию электронов | Co | |
| 77 | Найти конфигурацию электронов | S | |
| 78 | Баланс | C_2H_6+O_2→CO_2+H_2O | |
| 79 | Баланс | H_2+O_2→H_2O | |
| 80 | Найти конфигурацию электронов | P | |
| 81 | Найти конфигурацию электронов | Pb | |
| 82 | Найти конфигурацию электронов | Al | |
| 83 | Найти конфигурацию электронов | Ar | |
| 84 | Найти массу одного моля | O_2 | |
| 85 | Найти массу одного моля | H_2 | |
| 86 | Найти число нейтронов | K | |
| 87 | Найти число нейтронов | P | |
| 88 | Найти число нейтронов | Mg | |
| 89 | Найти число нейтронов | W | |
| 90 | Найти массу одного атома | C | |
| 91 | Упростить | na+cl | |
| 92 | Определить, растворима ли смесь в воде | H_2SO_4 | |
| 93 | Найти плотность при стандартной температуре и давлении | NaCl | |
| 94 | Найти степень окисления | C_6H_12O_6 | |
| 95 | Найти степень окисления | Na | |
| 96 | Определить, растворима ли смесь в воде | C_6H_12O_6 | |
| 97 | Найти атомную массу | Cl | |
| 98 | Найти атомную массу | Fe | |
| 99 | Найти эмпирическую/простейшую формулу | CO_2 | |
| 100 | Найти число нейтронов | Mt |
Сколько нейтронов в водороде?
Обновлено 15 марта 2018 г.
Автор John Papiewski
В природе у подавляющего большинства атомов водорода нет нейтронов; эти атомы состоят только из одного электрона и одного протона и являются самыми легкими из возможных атомов. Однако у редких изотопов водорода, называемых дейтерием и тритием, есть нейтроны. У дейтерия один нейтрон, а у неустойчивого и не встречающегося в природе трития — два.
TL;DR (слишком длинный; не читал)
Большинство атомов водорода не имеют нейтрона. Однако редкие изотопы водорода, называемые дейтерием и тритием, имеют один и два нейтрона соответственно.
Элементы и изотопы
Большинство элементов периодической таблицы имеют несколько изотопов – «кузенов» элемента, которые имеют одинаковое количество протонов, но разное количество нейтронов. Изотопы очень похожи друг на друга и имеют схожие химические свойства. Например, наряду с изотопом углерода-12 практически во всех живых существах можно найти небольшое количество радиоактивного углерода-14.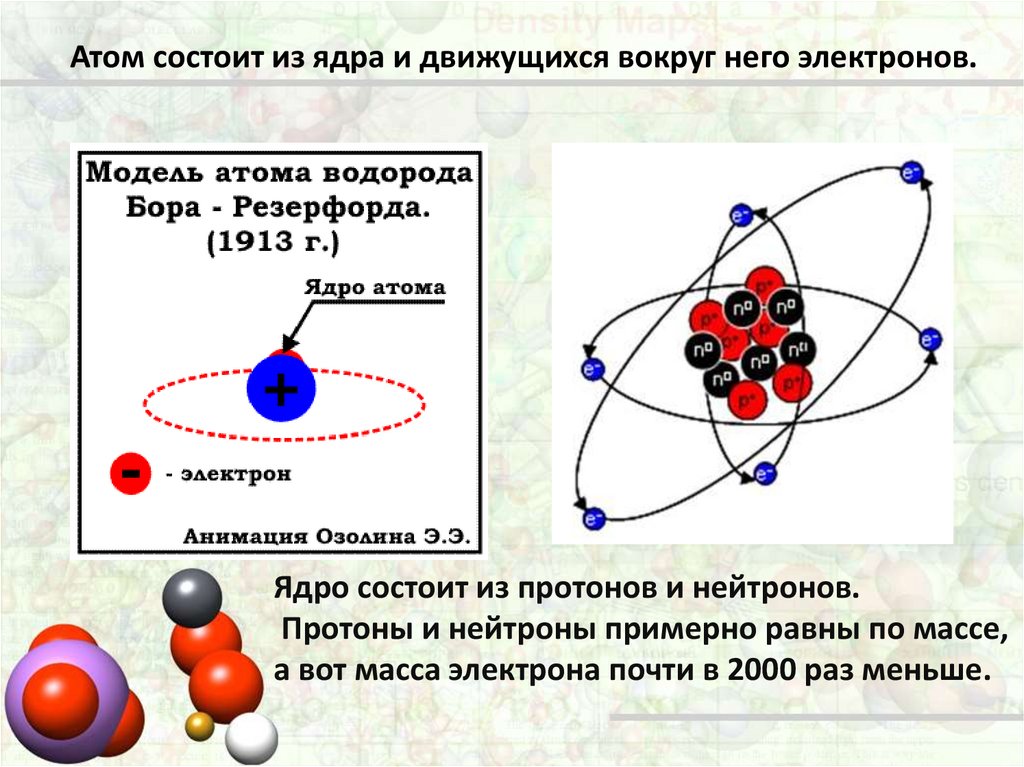 Однако, поскольку нейтроны имеют массу, веса изотопов немного отличаются. Ученые могут обнаружить разницу с помощью масс-спектрометра и другого специализированного оборудования.
Однако, поскольку нейтроны имеют массу, веса изотопов немного отличаются. Ученые могут обнаружить разницу с помощью масс-спектрометра и другого специализированного оборудования.
Использование водорода
Водород — самый распространенный элемент во Вселенной. На Земле вы редко найдете водород сам по себе; гораздо чаще он соединяется с кислородом, углеродом и другими элементами в химических соединениях. Вода, например, представляет собой водород, соединенный с кислородом. Водород играет важную роль в углеводородах, таких как масла, сахара, спирты и другие органические вещества. Водород также служит «зеленым» источником энергии; при горении на воздухе; он выделяет тепло и чистую воду, не производя CO 2 или другие вредные выбросы.
Использование дейтерия
Хотя дейтерий, также известный как «тяжелый водород», встречается в природе, он менее распространен, составляя один из каждых 6420 атомов водорода.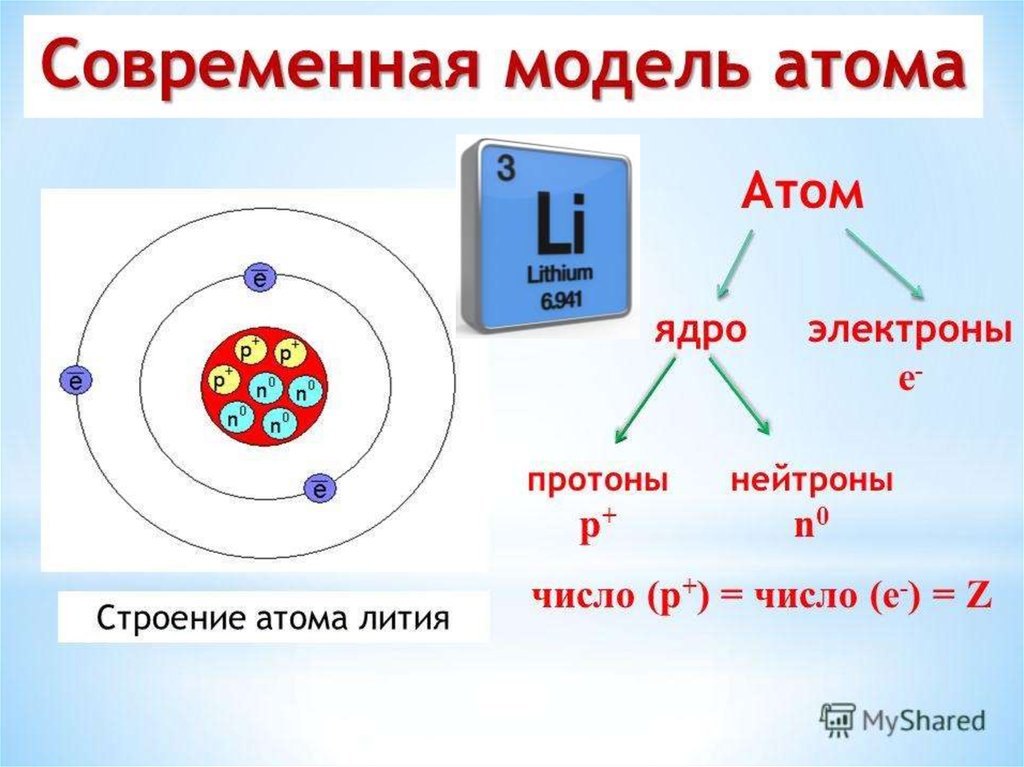 Подобно водороду, он соединяется с кислородом, образуя «тяжелую воду», вещество, которое выглядит и ведет себя так же, как обычная вода, но немного тяжелее и имеет более высокую температуру замерзания, 3,8 градуса Цельсия (38,4 градуса по Фаренгейту), по сравнению с 0 градусов. Цельсия (32 градуса по Фаренгейту). Дополнительные нейтроны делают тяжелую воду полезной для защиты от радиации и других применений в научных исследованиях. Будучи редкой, тяжелая вода также намного дороже, чем обычная. Его дополнительный вес делает его химически несколько странным по сравнению с водой. При нормальных концентрациях беспокоиться не о чем; однако количество более 25 процентов повредит кровь, нервы и печень, а очень высокие концентрации могут быть смертельными.
Подобно водороду, он соединяется с кислородом, образуя «тяжелую воду», вещество, которое выглядит и ведет себя так же, как обычная вода, но немного тяжелее и имеет более высокую температуру замерзания, 3,8 градуса Цельсия (38,4 градуса по Фаренгейту), по сравнению с 0 градусов. Цельсия (32 градуса по Фаренгейту). Дополнительные нейтроны делают тяжелую воду полезной для защиты от радиации и других применений в научных исследованиях. Будучи редкой, тяжелая вода также намного дороже, чем обычная. Его дополнительный вес делает его химически несколько странным по сравнению с водой. При нормальных концентрациях беспокоиться не о чем; однако количество более 25 процентов повредит кровь, нервы и печень, а очень высокие концентрации могут быть смертельными.
Использование трития
Дополнительные два нейтрона, содержащиеся в тритии, делают его радиоактивным, период полураспада которого составляет 12,28 года. Без естественных запасов трития его необходимо производить в ядерных реакторах. Хотя его излучение несколько опасно, в небольших количествах и при осторожном обращении и хранении тритий может быть полезным. Таблички «Выход», изготовленные из трития, излучают мягкое свечение, которое остается видимым до 20 лет; поскольку им не нужно электричество, они обеспечивают безопасное освещение во время отключения электроэнергии и других чрезвычайных ситуаций. Тритий имеет и другие применения в исследованиях, например, для отслеживания потока воды; он также играет роль в некоторых видах ядерного оружия.
Хотя его излучение несколько опасно, в небольших количествах и при осторожном обращении и хранении тритий может быть полезным. Таблички «Выход», изготовленные из трития, излучают мягкое свечение, которое остается видимым до 20 лет; поскольку им не нужно электричество, они обеспечивают безопасное освещение во время отключения электроэнергии и других чрезвычайных ситуаций. Тритий имеет и другие применения в исследованиях, например, для отслеживания потока воды; он также играет роль в некоторых видах ядерного оружия.
Сколько нейтронов содержит стандартный атом водорода в ядре?
Ответить
Проверено
209,1 тыс.+ просмотров
Подсказка: Атомный номер водорода равен 1. Всего у водорода три изотопа. Это протий, дейтерий и тритий. Все три изотопа имеют одинаковые атомные номера, но отличаются друг от друга массовым числом.
Полный пошаговый ответ:
Водород — это химический элемент, представленный в периодической таблице, который представлен символом H. 1H$ 93H$
1H$ 93H$
Число нейтронов в протии рассчитывается, как показано ниже.
$\Rightarrow Количество нейтронов = 1 — 1$
$\Rightarrow Количество нейтронов = 0$
Количество нейтронов в дейтерии рассчитывается, как показано ниже.
$\Rightarrow Количество нейтронов = 2 — 1$
$\Rightarrow Количество нейтронов = 1$
Количество нейтронов в тритии рассчитывается, как показано ниже.
$\Rightarrow Количество нейтронов = 3 — 1$
$\Rightarrow Количество нейтронов = 2$
Итак, количество нейтронов в протии равно 0, дейтерию равно 1 и тритию равно 2.
Примечание:
Изотоп протия также известен как изотоп водорода. Атомный номер атома равен числу протонов. Массовое число – это сумма протонов и нейтронов.
Недавно обновленные страницы
Большинство эубактериальных антибиотиков получено из биологии ризобий класса 12 NEET_UG
Саламиновые биоинсектициды были извлечены из биологии класса 12 А0003
Канализационные или городские канализационные трубы не должны быть непосредственно очищены от микробов класса 12 по биологии NEET_UG
Очистка сточных вод осуществляется микробами A.