Оксид марганца(IV), MnO2, химические свойства, получение
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
ФосфорФосфор
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
КриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИридийИридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Марганец. Строение атома, степени окисления. Оксиды, гидроксиды, соли. Перманганат калия
φ°(Mn2+/Mn) = –1,18 В.
Mn + 2h3O = Mn(OH)2 + h3↑.
Mn + 4HNO3 = Mn(NO3)2 + 2NO2↑ + 2h3O.
Э + 7HNO3 = HЭO4 + 7NO2↑ + 3h3O, где Э = Tc, Re.
Соединения марганца(II) MnO, Mn(OH)2 и соли катионного типа
При нагревании:
MnCO3 = MnO + CO2,
MnO + h3O = Mn(OH)2↓,
MnSO4 + 2NaOH = Mn(OH)2↓ + Na2SO4,
2MnSO4 + 2h3O = (MnOH)2SO4 + h3SO4.
Восстановительные свойства:
2Mn(OH)2 + O2 = 2MnO2 + 2h3O,
2Mn(NO3)2 + 5NaBiO3 + 16HNO3 = 2HMnO4 + 5Bi(NO3)3 + 5NaNO3 + 7h3O,
3MnSO4 + 2KMnO4 + 2h3O = 5MnO2 + K2SO4 + 2h3SO4.
Mn2O3, слабое основание Mn(OH)3 и соли. Соединения марганца(III) легко диспропорционируют:
Соединения марганца(IV)
MnO2 – чёрно-бурый, Mn(SO4)2, Na2MnO3 (манганит натрия).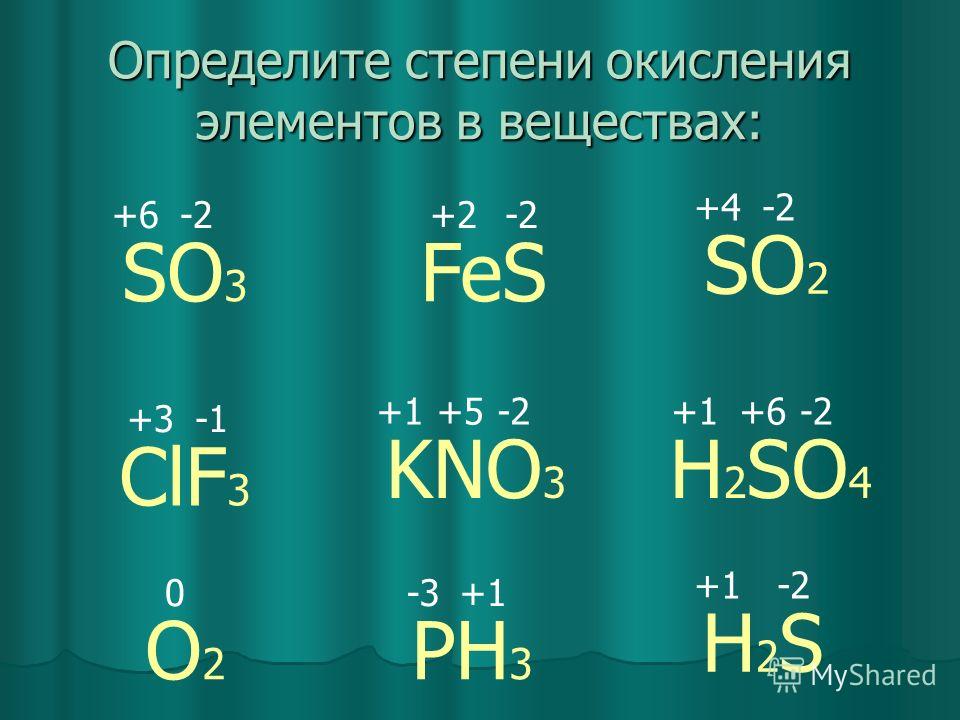
Окислительные свойства MnO2:
MnO2 + 4H+ + 2ē = Mn2+ + 2h3O; φ° = 1,23 В.
MnO2 + 4HCl = MnCl2 + Cl2↑ + 2h3O,
MnO2 + 2KBr + h3SO4 = MnSO4 + Br2 + K2SO4 + h3O.
Восстановительные свойства MnO2 (при сплавл.):
Гидролиз:
При сплавлении:
Гидролиз:
Соли марганцовистой кислоты (h3MnO4) – манганаты.
Получение.
При сплавлении:
2KMnO4 + 2KOH + KNO2 = 2K2MnO4 + KNO3 + h3O,
MnSO4 + 4KOH + 2KNO3 = K2MnO4 + 2KNO2 + K2SO4 + 2h3O,
MnSO4 + 2Br2 + 8NaOH = Na2MnO4 + 4NaBr + Na2SO4 + 4h3O.
Диспропорционирование:
Окислительные свойства:
Восстановительные свойства:
Разложение при нагревании (500 °C):
Mn2O7, HMnO4 и её соли перманганаты.
Получение:
2MnSO4 + 5NaBiO3 + 16HNO3 = 2HMnO4 + 5Bi(NO3)3 + NaNO3 + 2Na2SO4 + 7h3O.
2MnSO4 + 5K2S2O8 + 8h3O = 2HMnO4 + 5K2SO4 + 7h3SO4.
2KMnO4 + h3SO4(конц.) = Mn2O7 + K2SO4 + h3O.
Сильные окислители, особенно в кислой среде:
MnO4 — + 2h3O + 3ē = MnO2 + 4OH– ; φ° = +0,60 В;
MnO4 — + ē = MnO4 2- ; φ° = +0,56 В;
MnO4 — + 8H+ + 5 ē = Mn2+ + 4h3O; φ° = +1,51 В.
Окислительные свойства:
2KMnO4 + 6KI + 4h3O = 2MnO2 + 3I2 + 8KOH,
6KMnO4 + KI + 6KOH = 6K2MnO4 + KIO3 + 3h3O,
2KMnO4 + 10KI + 8h3SO4 = 2MnSO4 + 5I2 + 6K2SO4 + 8h3O.
Термическое разложение (выше 250 °C):
Водные растворы неустойчивы:
Разложение Mn2O7:
Mn(OH)2, Mn(OH)3, Mn(OH)4, (h3MnO4), HMnO4.
Основные свойства ослабевают, а кислотные свойства усиливаются в ряду выше.
Ионная проводимость одного пористого мезостержня MnO2 при контролируемых степенях окисления
Тимоти Плетт, и Тревор Гэмбл, и Элеонора Джилетт, б Санг Бок Ли б и Зузанна С. Сивы* ак
Принадлежности автора
* Соответствующие авторы
и Факультет физики, Калифорнийский университет, Ирвин, Ирвин, Калифорния 92697-4575, США
Электронная почта: zsiwy@uci. edu
edu
Факс: +1 9498242174
Тел.: +1 9498246911
б Кафедра химии и биохимии, Мэрилендский университет, Колледж-Парк, Мэриленд 20742, США
Факс: +1 3013149121
Тел.: +1 3013149121
с Кафедра химии, Калифорнийский университет, Ирвин, Ирвин, Калифорния 92697-2025, США
Факс: +1 9498248571
Тел.: +1 9498244097
Аннотация
rsc.org/schema/rscart38″> Ионная проводимость пористого MnO 2 в наномасштабе изучена недостаточно, несмотря на возможную важность в процессах зарядки/разрядки аккумуляторов. Здесь показано, что MnO 2 в различных степенях окисления проявляет различную ионную проводимость и характеристики поверхностного заряда, которые исследуются измерениями обратного потенциала.Какова степень окисления марганца в Mno2
IIT JAM UGC CSIR NET GATE CHEMISTRY
Что такое степень окисления марганца в Mno2 . Степень окисления обозначает степень окисления элемента в соединении, установленную в соответствии с набором правил, сформулированных на основе этого электрона. Web 6) какова степень окисления марганца в mno2?
IIT JAM UGC CSIR NET GATE CHIMISTRY
Интернет-ответ (1 из 2): Интернет, какова степень окисления марганца в перманганат-ионе (mno2 )? Паутина в процессе зарядки для элемента цинка / щелочи / диоксида марганца, разряженный положительный активный материал, оксигидроксид марганца (mnooh), окисляется до марганца. Таким образом, мы получаем степень окисления марганца как + 4. Твердое олово помещают в следующие растворы. Степень окисления обозначает степень окисления элемента в соединении, установленную в соответствии с набором правил, сформулированных на основе этого электрона. Ответ заключается в том, что степень окисления марганца (mn) может варьироваться от +2 до +7 в зависимости от соединения, однако в этом случае марганец должен был бы. Причина существования такого. Он твердый и очень хрупкий, трудно плавится, но легко окисляется. Здесь оксид марганца является нейтральным соединением, которое имеет свои.
Таким образом, мы получаем степень окисления марганца как + 4. Твердое олово помещают в следующие растворы. Степень окисления обозначает степень окисления элемента в соединении, установленную в соответствии с набором правил, сформулированных на основе этого электрона. Ответ заключается в том, что степень окисления марганца (mn) может варьироваться от +2 до +7 в зависимости от соединения, однако в этом случае марганец должен был бы. Причина существования такого. Он твердый и очень хрупкий, трудно плавится, но легко окисляется. Здесь оксид марганца является нейтральным соединением, которое имеет свои.
Металлический марганец и его обычные ионы. Веб-степень окисления марганца в mno2 составляет 4+. Так как сумма степеней окисления должна быть. Что из перечисленного может быть окислено mno2? Ответ заключается в том, что степень окисления марганца (mn) может варьироваться от +2 до +7 в зависимости от соединения, однако в этом случае марганец должен был бы. Web в mno, степень окисления марганца +2, что означает, что степень окисления низкая, поэтому это основной оксид. Диоксид марганца Web не имеет запаха. Веб какая степень окисления марганца в mno2? В каком растворе будет a. Какое утверждение правильно описывает степень окисления атома марганца (mn) в mnl2 и mno2? Веб-ответ (1 из 2):
Диоксид марганца Web не имеет запаха. Веб какая степень окисления марганца в mno2? В каком растворе будет a. Какое утверждение правильно описывает степень окисления атома марганца (mn) в mnl2 и mno2? Веб-ответ (1 из 2):
Как найти степень окисления Mn в ионе MnO2 2 . (манганат
Web 6) какая степень окисления марганца у mno2? Так как сумма степеней окисления должна быть. Какое утверждение правильно описывает степень окисления атома марганца (mn) в mnl2 и mno2? 2 — акцептор водородной связи для mno2. Веб-число /a > c6h5no2 степень окисления марганца в mno2 составляет +4, оксид представляет собой 4 подходы # шаг 1 kmno4 ) общая степень окисления mn 4+ /mn 3+. Веб-степень окисления марганца в mno2 составляет 4+. Твердое олово помещают в следующие растворы. A) +5 b) +6 c)+7 d) +8 7. Web в mno, степень окисления марганца +2, что означает низкую степень окисления, поэтому это основной оксид. Веб-ответ (1 из 2):
марганца Ив/химическая формула окиси марганца
В каком растворе будет a. Ответ заключается в том, что степень окисления марганца (mn) может варьироваться от +2 до +7 в зависимости от соединения, однако в этом случае марганец должен был бы. О марганец имеет степень окисления. Степень окисления mno2 равна +4. Web 6) какова степень окисления марганца в mno2? Сеть марганца существует в 6 различных степенях окисления, т.е. здесь оксид марганца является нейтральным соединением, которое имеет свою. Веб-степень окисления марганца в mno2 составляет 4+. Диоксид марганца Web не имеет запаха. Число сложности двуокиси марганца составляет 18,3.
Ответ заключается в том, что степень окисления марганца (mn) может варьироваться от +2 до +7 в зависимости от соединения, однако в этом случае марганец должен был бы. О марганец имеет степень окисления. Степень окисления mno2 равна +4. Web 6) какова степень окисления марганца в mno2? Сеть марганца существует в 6 различных степенях окисления, т.е. здесь оксид марганца является нейтральным соединением, которое имеет свою. Веб-степень окисления марганца в mno2 составляет 4+. Диоксид марганца Web не имеет запаха. Число сложности двуокиси марганца составляет 18,3.
Примеры степеней окисления Online Chemistry Tutor
Web какова степень окисления марганца в перманганат-ионе (mno2 )? Веб-число /a > c6h5no2 степень окисления марганца в mno2 составляет +4, оксид представляет собой 4 подходы # шаг 1 kmno4 ) общая степень окисления mn 4+ /mn 3+. Степень окисления марганца зависит от частн. Причина существования такого. Металлический марганец и его обычные ионы.
