Железо и его соединения — презентация онлайн
Похожие презентации:
Сложные эфиры. Жиры
Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Газовая хроматография
Хроматографические методы анализа
Искусственные алмазы
Титриметрические методы анализа
Биохимия гормонов
Антисептики и дезинфицирующие средства. (Лекция 6)
Клиническая фармакология антибактериальных препаратов
Биохимия соединительной ткани
элемент
4- ого периода
элемент №
26
ставшее
международным,
латинское
название
«Ferrum», от
греко-латинского
«быть твердым»
элемент
8 группы
побочной
подгруппы
четвертый по
распространенности в
земной коре, второй среди
металлов
Fe
2е
8е 14е
2е
2
2
6
2
6
6
2
1S 2S 2P 3S 3P 3D 4S
возможные степени окисления
+2 и +3
Нахождение в природе
В земной коре на долю железа
земной коры (4-е место среди всех
элементов, 2-е среди металлов).

Известно большое число руд и
минералов, содержащих железо.
Оно бывает в виде различных
соединений: оксидов, гидроксидов и
солей.
В свободном виде железо находят в
метеоритах, изредка встречается
самородное железо (феррит) в земной
коре как продукт застывания магмы.
Первое металлическое железо,
попавшее в руки человека,
имело, явно, метеоритное
происхождение.
Руды железа широко
распространены и часто
встречаются даже на
поверхности Земли
Железные изделия из
метеоритного железа
найдены в захоронениях,
относящихся к очень давним
временам (IV — V
тысячелетиях до н.э.), в
Египте и Месопотамии
бурый железняк
(лимонит Fe2О3*пН2О;
содержит до
65% Fe)
Наиболее
распространенные
и добываемые
руды и минералы
железный шпат
(сидерит – FeCO3
содержит до 48% Fe)
красный железняк
(гематит — Fe2O3;
содержит до 70 %
Fe)
магнитный железняк
(магнетит — Fe3O4;
содержит 72,4 % Fe),
История
получения железа
Люди впервые овладели железом в 4-3 тысячелетиях
до н.
 э., подбирая упавшие с неба камни — железные
э., подбирая упавшие с неба камни — железныеметеориты, и превращая их в украшения, орудия труда и
охоты. Их и сейчас находят у жителей Северной и
Южной Америки, Гренландии и Ближнего Востока, а
также при археологических раскопках на всех
континентах.
Самый древний способ получения железа основывается на
его восстановлении из оксидных руд. В 19 веке были
разработаны современные способы: мартеновские печи,
электросталеплавильные процессы и другие методы…
серебристосерый
Физические
свойства железа
тугоплавкий
(Т пл.=15350C)
Тяжелый
(плотность=7,8 г\см3 )
ковкий;
обладает
свойствами
Химические свойства
Реакции с простыми веществами
Железо сгорает в чистом кислороде
при нагревании:4Fe +3O2=2Fe2O3
Реагирует с порошком серы при
нагревании:Fe +S = FeS
Реагирует с галогенами при
нагревании:2Fe + 3CL2=2FeCL3
Химические свойства
Реакции со сложными веществами
С кислотами:
А) с соляной кислотой
2HCL + Fe = FeCL2 + h3
Б) с серной кислотой
h3SO4 + Fe = FeSO4 + h3
С солями:
Fe + CuSO4= Cu + FeSO4
С водой(при высокой температуре):
3Fe + 4h3O=Fe3O4 +4h3
(железная окалина)
Железо разрушается под действием окружающей среды, т.
 е.
е.подвергается коррозии – «ржавлению».
При этом на поверхности образуется «ржавчина».
4Fe + 2Н2О + ЗО2 = 2(Fe2O3•Н2О)
оксиды:
FeO, Fe2O3
Fe3O4
гидроксиды:
Fe(OH)2
Fe(OH)3
Соли (+2) (+3)- растворимые и нерастворимые:
Fe(NO3)2, FeCL3, Fe2(SO4)3 , FeS…..
FeO — основный оксид
Fe3O4смешанный оксид
(FeO и Fe2O3)
Fe2O3- слабовыраженный
амфотерный оксид
Химические свойства FeO
1) с кислотами:
FeO + 2HCL=FeCL2 + h3O
2) с более активными металлами:
3FeO + 2Al = 3Fe + Al2O3
Химические свойства Fe3O4
1) с кислотами
Fe3O4 + 8HCL=FeCL2 +2FeCL3 + 4h3O
2) также с более активными металлами
Fe3O4 +4 Zn=4 ZnO +3Fe
Химические свойства Fe2O3
1) с кислотами:
Fe2O3 + 3h3SO4=Fe2(SO4)3 + 3h3O
2) с более активными металлами
Fe2O3 + 3Mg=3MgO +2Fe
Fe(OH)2 и Fe(OH)3
Окисление:
4Fe(OH)2+ O2 +2h3O=4Fe(OH)3
Fe(OH)2 и Fe(OH)3
1)Реагируют с кислотами:
Fe(OH)2 + 2HNO3= Fe(NO3)2 + 2h3O
Fe(OH)3 + 3HCL=FeCl3+3h3O
2)Разлагаются при нагревании:
2Fe(OH)3 = Fe2O3+3h3O
Fe(OH)2=FeO + h3O
Fe(OH)3 реагирует с конц.

щелочами
Fe(OH)3 + 3NaOH=Na3(Fe(OH)6)
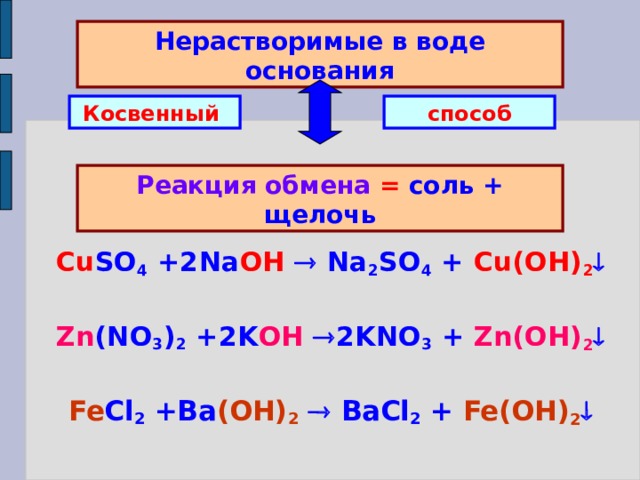
Реагируют с щелочами:
FeCL2 + 2NaOH= Fe(OH)2 + 2 NaCL
Реагируют с более активными металлами:
FeCL2 + Mg= MgCL2+ Fe
Реагируют с другими солями:
Fe2(SO4)3 + 3BaCL2=3BaSO4 + 2FeCL3
Реагируют с кислотами:
FeS + 2HCl=FeCL2 + h3S
FeCl2 + 2NaOH=
=Fe(OH)2 +2NaCL
Fe2+ +2CL- + 2Na+ + 2OH=Fe(OH)2 + 2Na+ + 2OHFe2+ + 2OH- = Fe(OH)2
FeCL3+3KOH=
=Fe(OH)3+3KCL
Fe3+ +3CL- +3K+ +3OH=Fe(OH)3 +3K+ +3OHFe3+ +3OH- =Fe(OH)3
Fe(OH)2 -осадок
темно-зеленого
цвета
FeCL2
NaOH
FeCl3
Fe(OH)3 — осадок
коричневого
цвета
Железо в виде ионов присутствует в организмах всех
растений и животных и, конечно же, человека, но в
растениях и животных в малых количествах (в среднем
0,02%).
Основная биологическая функция железа – участие в
транспорте кислорода ко всем органам и окислительных
процессах.
В организме человека с массой тела прниблизительно70 кг
содержится 4,2 г железа, а в 1 л крови – 450 мг.
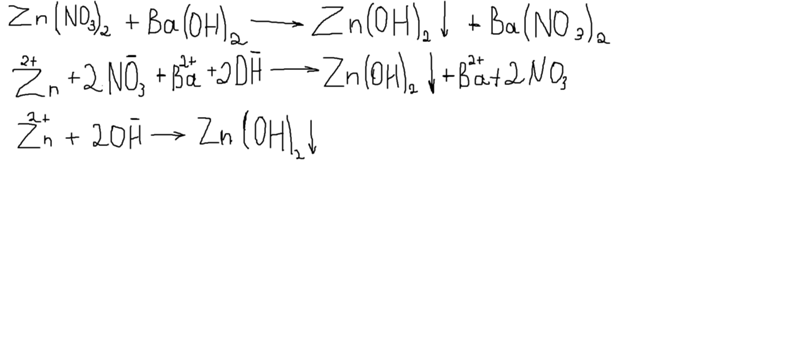
При недостатке железа в организме развивается железистая
анемия.
Перенос железа в организме осуществляет важнейший белок
–гемоглобин, в котором находится больше половины всего
железа организма.
Почти 60%, поступающего в
организм железа расходуется на
синтез гемоглобина.
Некоторое количество (примерно
20%) — откладывается в мышцах,
костном мозге, печени и селезенке.
Еще 20% его используется для
синтеза различных ферментов.
Основная роль железа в организме –
участие в «рождении» красных
(эритроцитов) и белых (лимфоцитов)
кровяных клеток.
Эритроциты содержат гемоглобин переносчик кислорода, а лимфоциты
ответственны за иммунитет.
гречка
печень
говядина
белая капуста
и черный хлеб
бобы и курага
мясо кур
орехи
яблоки
Будьте внимательны к своему здоровью: наличие
достаточного количества гемоглобина – это наша
жизнь!!!
При анемии (недостатке гемоглобина) увеличьте в своем
рационе количество нежирного говяжьего мяса и печени,
красной икры, а также яичных желтков.

При анемии, для приготовления пищи, рекомендуется
использовать чугунную посуду.
Как показали эксперименты, приготовление и кипячение
соуса на протяжении 20 минут в такой посуде,
способствует увеличению количества железа в 9 раз.
Людям с пониженным гемоглобином необходимо чаще
бывать на свежем воздухе.
Чистое железо имеет довольно
ограниченное применение.
Его используют при изготовлении
сердечников электромагнитов, как
катализатор химических процессов,
для некоторых других целей.
Находят широкое применение и
многие соединения железа. Так,
сульфат железа (III) используют при
водоподготовке, оксиды и цианид
железа служат пигментами при
изготовлении красителей и так далее.
Но сплавы железа — чугун и сталь
— составляют основу современной
техники
Чугун
Сталь
Fe — 90-93%
C — 2-4,5%
хрупкость
Fe — 95-97%
C — 0,3-1,7%
ковкость
Гидроэлектростанции и опоры
линий
электропередач
Железо
сегодня
Автомобили ,
Тракторы,
Подводные лодки,
Бытовые приборы,
Другие предметы
Трубопроводы
для воды,
нефти и газа
С чем будет реагировать железо?
(найдите три кубика с возможными соединениями)
h3SO4
CuSO4
O2
HCL
MgO
Na
CuSO4
CL2
HCL
AL
ALCL3
Br2
HgSO4
h3O
S
KOH
MgCL2
O2
С какими веществами будут реагировать
оба оксида — FeO и Fe2O3
AL
Mg
HCL
O2
h3SO4
Дана соль : Сульфат железа (III)
С какими веществами она реагирует?
KOH
HCl
AL(OH)3
BaCL2
NaNO3
AL
ССЫЛКИ НА ИСТОЧНИКИ ИНФОРМАЦИИ И ИЗОБРАЖЕНИЙ:
http://www.
 ukzdor.ru/ferrum.html
ukzdor.ru/ferrum.htmlhttp://termist.com/bibliot/popular/mezenin/mezenin_046.htm
Учебник для общеобразовательных учреждений , 9 класс,
Г.Е. Рудзитис ,Ф .Г. Фельдман
http://im4-tub-ru.yandex.net/i?id=64602315-02-72&n=21
http://im0-tub-ru.yandex.net/i?id=151351830-48-72&n=21
http://im5-tub-ru.yandex.net/i?id=132804891-18-72&n=21
http://im0-tub-ru.yandex.net/i?id=389614815-46-72&n=21
http://im3-tub-ru.yandex.net/i?id=152691363-60-72&n=21
http://im5-tub-ru.yandex.net/i?id=375112224-26-72&n=21
http://img0.liveinternet.ru/images/attach/c/7/94/310/94310832_nygooset06.jpg
http://im8-tub-ru.yandex.net/i?id=72487700-14-72&n=21
http://im0-tub-ru.yandex.net/i?id=148759345-57-72&n=21
http://cdn.elec.ru/_fitbox/200×200/offers/orig/8796471298.jpg
http://im3-tub-ru.yandex.net/i?id=97587139-26-72&n=21
http://im8-tub-ru.yandex.net/i?id=26227792-59-72&n=21
English Русский Правила
(+))# Обратите внимание, что эта реакция производит ионов гидроксония. Это говорит вам о том, что баланс, который существует между катионами гидроксония и анионами гидроксида в нейтральном растворе , будет нарушен, поскольку теперь у вас есть на больше катионов гидроксония, чем анионов гидроксида #-># раствор кислый .
Это говорит вам о том, что баланс, который существует между катионами гидроксония и анионами гидроксида в нейтральном растворе , будет нарушен, поскольку теперь у вас есть на больше катионов гидроксония, чем анионов гидроксида #-># раствор кислый .
Это именно то, что предлагает ваша книга, но делается это немного по-другому.
Вот что там происходит. Вы можете представить нитрат цинка как 9(+)#), поэтому полученный раствор
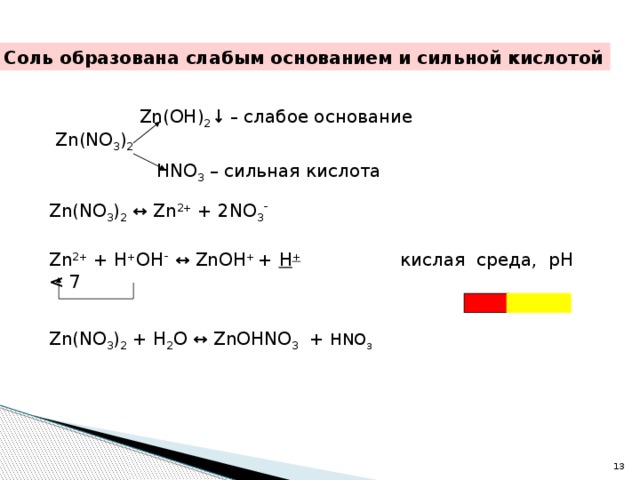
Характерные реакции ионов цинка (Zn²⁺)
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 97279
- Джеймс П. Бирк
- Университет штата Аризона
- Наиболее распространенные степени окисления: +2
- М.