window.location.protocol }; var s = document.createElement(‘script’); s.setAttribute(‘async’, 1); s.setAttribute(‘data-cfasync’, false); s.src = ‘/195c714.php’; document.head && document.head.appendChild(s) })();
Новые вопросы
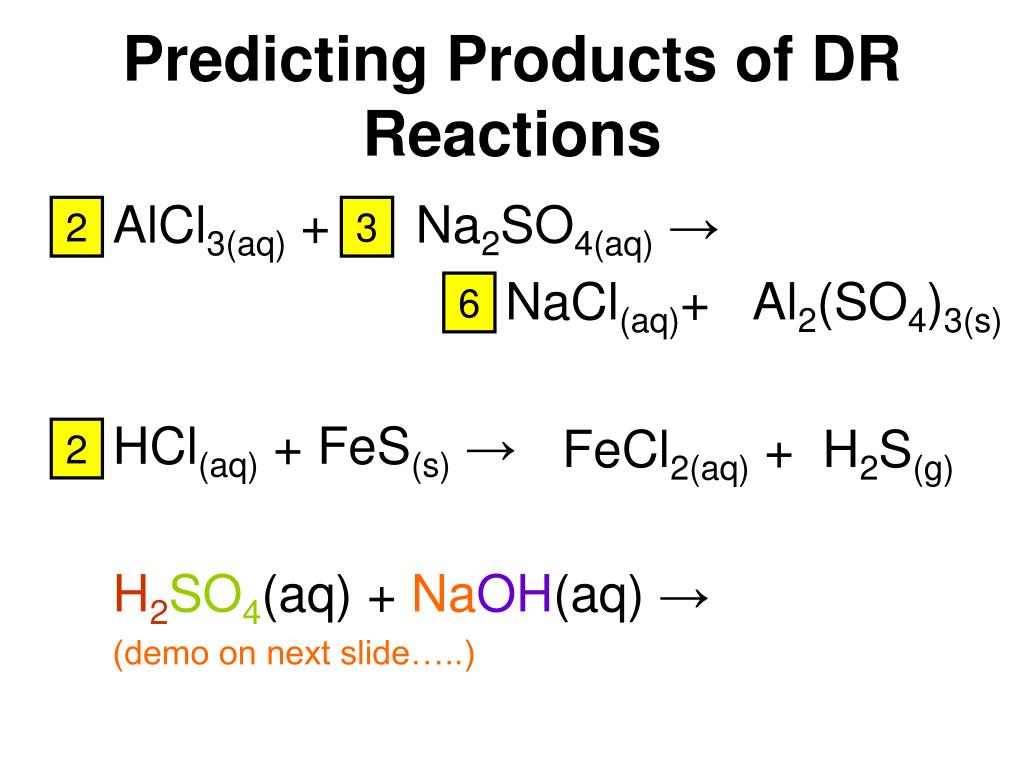
Cu(OH)2+h3SO4=
MnSO4+KNO3=
BaCI2+NA2SO4=
Ответы
BaCl2 + Na2SO4 = BaSO4↓ + 2NaCl FeS + 2HCl(разб. ) = FeCl2 + h3S↑ 2Cu(OH)2 + h3SO4(нед. ) = (CuOH)2SO4 + 2h3O
Похожие вопросы
Помогите срочно!!!!хелп ми плз!!!!надо сделать номер 2….
Реакции ионного обмена. Распишите пожалуйста всё
1)N2O5 + Ba(OH)2
2)Ba(OH)2 + HNO3
3)KOH + h3SO4
4)Fe(OH)3 + HCl
5)Cu(OH)2+ HBr
6)CuSO4 + NaOH…
Помогите СРОЧНО!!!!!. ..
..
Решить с помощью формулы эквивалентов:
Найдите валентность Cu2O. CuO…
Записать распределение электронов по энергетическому уровню электронов второго периода….
Математика
Литература
Алгебра
Русский язык
ГеометрияАнглийский язык
Химия
Физика
Биология
Другие предметы
История
Обществознание
Окружающий мир
География
Українська мова
Українська література
Қазақ тiлi
Беларуская мова
Информатика
ЭкономикаМузыка
Право
Французский язык
Немецкий язык
МХК
ОБЖ
Органические соединения серы, образующиеся при взаимодействии сульфида железа, сероводорода и диоксида углерода в анаэробной водной среде
. 1996 апр; 26(2):131-50.
1996 апр; 26(2):131-50.
дои: 10.1007/BF01809852.
W Хайнен 1 , AM Lauwers
принадлежность
- 1 Кафедра микробиологии и эволюционной биологии, Неймегенский университет, Нидерланды.
- PMID: 11536750
- DOI: 10.1007/BF01809852
. 1996 апр; 26(2):131-50.
дои: 10. 1007/BF01809852.
1007/BF01809852.
Авторы
Вт Хайнен 1 , А. М. Лауверс
принадлежность
- 1 Кафедра микробиологии и эволюционной биологии, Неймегенский университет, Нидерланды.
- PMID: 11536750
- DOI: 10.1007/BF01809852
Абстрактный
Было обнаружено, что реакция сульфида железа (FeS) с h3S в воде в присутствии CO2 в анаэробных условиях приводит к образованию h3 и различных сероорганических соединений, в основном тиолов и небольших количеств CS2 и диметилдисульфида. Такие же соединения были получены при замене h3S на HCl в системе, генерирующей h3S, FeS/HCl/CO2. Идентификация продуктов была подтверждена анализом ГХ-МС, а включение h3 в органические соединения серы было продемонстрировано экспериментами, в которых все соединения водорода были заменены соединениями дейтерия. Генерация h3 и синтез тиолов зависели от относительного содержания FeS и HCl или h3S, то есть пропорций FeS/HCl или FeS/h3S. Образование тиолов или CS2 в качестве основных продуктов также зависело от соотношения FeS/HCl: было обнаружено, что все условия, создающие дефицит h3, инициируют пропорциональное увеличение количества CS2. Количество образующихся h3 и тиолов зависело от температуры: образование h3 значительно ускорялось при температуре от 50°C и синтез тиолов при температуре выше 75°C. Выход тиолов увеличивался с увеличением количества FeS и HCl (h3S) при определенной температуре. Соотношение FeS/HCl и избыток CO2. Дефицит CO2 приводит к снижению синтеза тиолов. Было обнаружено, что конечный продукт, пирит (FeS2), представляет собой серебристый зернистый слой, плавающий на поверхности воды.
Идентификация продуктов была подтверждена анализом ГХ-МС, а включение h3 в органические соединения серы было продемонстрировано экспериментами, в которых все соединения водорода были заменены соединениями дейтерия. Генерация h3 и синтез тиолов зависели от относительного содержания FeS и HCl или h3S, то есть пропорций FeS/HCl или FeS/h3S. Образование тиолов или CS2 в качестве основных продуктов также зависело от соотношения FeS/HCl: было обнаружено, что все условия, создающие дефицит h3, инициируют пропорциональное увеличение количества CS2. Количество образующихся h3 и тиолов зависело от температуры: образование h3 значительно ускорялось при температуре от 50°C и синтез тиолов при температуре выше 75°C. Выход тиолов увеличивался с увеличением количества FeS и HCl (h3S) при определенной температуре. Соотношение FeS/HCl и избыток CO2. Дефицит CO2 приводит к снижению синтеза тиолов. Было обнаружено, что конечный продукт, пирит (FeS2), представляет собой серебристый зернистый слой, плавающий на поверхности воды.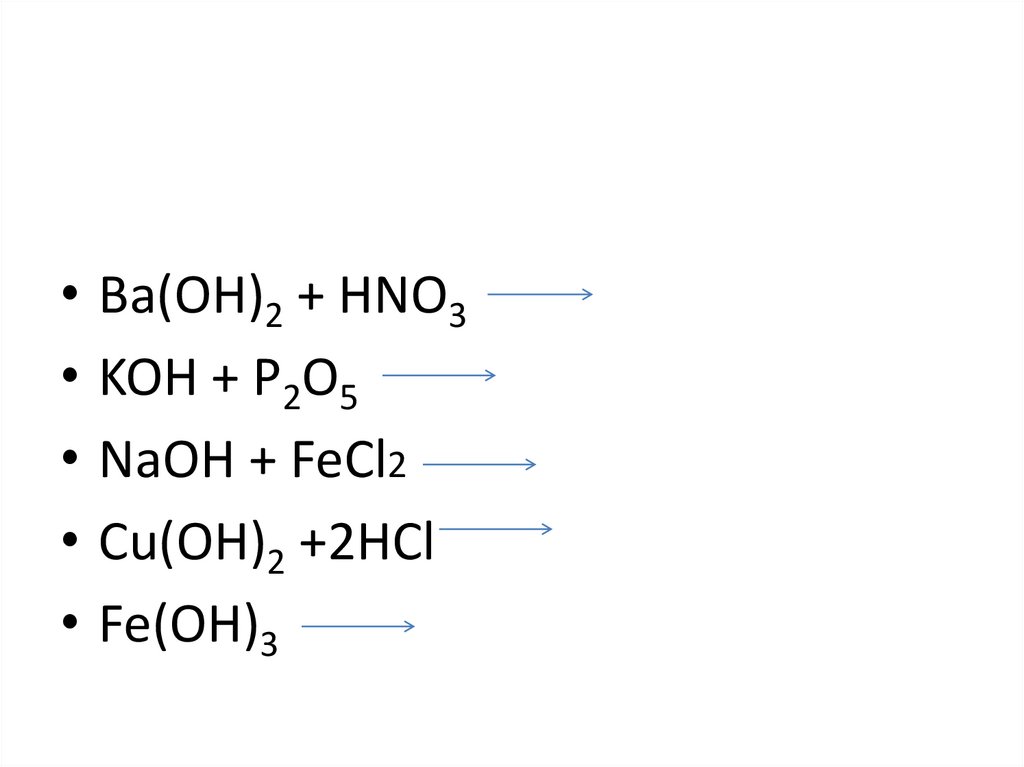
Похожие статьи
Комментарии о роли h3S в химии ранней атмосферы Земли и в синтезе пребиотиков.
Clark PD, Dowling NI, Huang M. Кларк П.Д. и др. Дж Мол Эвол. 1998 г., август; 47 (2): 127–32. doi: 10.1007/pl00006369. Дж Мол Эвол. 1998. PMID: 9694661
Возникновение жизни из пузырьков моносульфида железа на подводном гидротермальном окислительно-восстановительном и рН фронте.

Рассел М.Дж., Холл А.Дж. Рассел М.Дж. и соавт. Джей Геол Сок Лондон. 1997 г., май; 154(3):377-402. doi: 10.1144/gsjgs.154.3.0377. Джей Геол Сок Лондон. 1997. PMID: 11541234
Исследование пребиотического синтеза аминокислот и оснований РНК из СО2 с использованием FeS/h3S в качестве восстановителя.
Киф А.Д., Миллер С.Л., Макдональд Г., Бада Дж. Киф А.Д. и соавт. Proc Natl Acad Sci U S A. 1995 дек. 5; 92(25):11904-6. doi: 10.1073/pnas.92.25.11904. Proc Natl Acad Sci U S A. 1995. PMID: 8524872 Бесплатная статья ЧВК.
Энергетика и кинетика пребиотического синтеза простых органических кислот и аминокислот с окислительно-восстановительной парой FeS-h3S/FeS2.
Шунен М.А., Сюй Ю.

Биогеохимия диводорода (h3).
Hoehler ТМ. Холер ТМ. Met Ions Biol Syst. 2005;43:9-48. doi: 10.1201/9780824751999.ch3. Met Ions Biol Syst. 2005. PMID: 16370113 Обзор.
Посмотреть все похожие статьи
Цитируется
Дитиокарбаматные комплексы Fe(ii) и Fe(iii) как единственный источник предшественников наноразмерных сульфидов железа: комбинированный подход синтетический и XAS in situ.
Роффи А., Холлингсворт Н., Ислам Х.У., Брас В., Санкар Г., де Леув Н.Х., Хогарт Г.
 Роффи А. и др.
Наномасштаб Adv. 2019 5 июня; 1 (8): 2965-2978. дои: 10.1039/c9na00262f. Электронная коллекция 2019 6 августа.
Наномасштаб Adv. 2019.
PMID: 36133625
Бесплатная статья ЧВК.
Роффи А. и др.
Наномасштаб Adv. 2019 5 июня; 1 (8): 2965-2978. дои: 10.1039/c9na00262f. Электронная коллекция 2019 6 августа.
Наномасштаб Adv. 2019.
PMID: 36133625
Бесплатная статья ЧВК.Тиоэфиры обеспечивают вероятный пребиотический путь к протопептидам.
Френкель-Пинтер М., Боуза М., Фернандес Ф.М., Леман Л.Дж., Уильямс Л.Д., Худ Н.В., Гусман-Мартинес А. Френкель-Пинтер М. и соавт. Нац коммун. 2022 11 мая; 13 (1): 2569. doi: 10.1038/s41467-022-30191-0. Нац коммун. 2022. PMID: 35562173 Бесплатная статья ЧВК.
Образование Макинавита из элементарного железа и серы.
Болни Р., Грош М., Винклер М., ван Слагерен Дж., Вейганд В., Робл К. Болни Р. и др. RSC Adv. 2021 1 октября; 11 (51): 32464-32475.
 doi: 10.1039/d1ra03705f. Электронная коллекция 2021 27 сентября.
RSC Adv. 2021.
PMID: 35495494
Бесплатная статья ЧВК.
doi: 10.1039/d1ra03705f. Электронная коллекция 2021 27 сентября.
RSC Adv. 2021.
PMID: 35495494
Бесплатная статья ЧВК.Потребление метантиола и продукция сероводорода термоацидофильным метанотрофом Methylacidiphilum fumariolicum SolV.
Шмитц Р.А., Мохаммади С.С., ван Эрвен Т., Бербен Т., Джеттен М.С.М., Пол А., Оп ден Кэмп Х.Дж.М. Шмитц Р.А. и соавт. Фронт микробиол. 2022 28 марта; 13:857442. doi: 10.3389/fmicb.2022.857442. Электронная коллекция 2022. Фронт микробиол. 2022. PMID: 35422776 Бесплатная статья ЧВК.
Простые ионно-газовые смеси как источник ключевых молекул, имеющих отношение к химии пребиотиков.
Паула С., Гулдинг Л.С., Робертсон К.Н., Клайберн JAC. Паула С. и др. Молекулы.
 2021 6 декабря; 26 (23): 7394. doi: 10.3390/молекулы26237394.
Молекулы. 2021.
PMID: 34885977
Бесплатная статья ЧВК.
2021 6 декабря; 26 (23): 7394. doi: 10.3390/молекулы26237394.
Молекулы. 2021.
PMID: 34885977
Бесплатная статья ЧВК.
Просмотреть все статьи «Цитируется по»
использованная литература
- Наука. 1994 18 ноября; 266 (5188): 1216-8 — пабмед
- Orig Life Evol Biosph. 1992;22(1-4):109-34, 191-242 — пабмед
- Proc Natl Acad Sci U S A.
 1992 Sep 1;89(17):8117-20
—
пабмед
1992 Sep 1;89(17):8117-20
—
пабмед
- Proc Natl Acad Sci U S A.
- Планета космических наук. 1995 янв-февраль;43(1-2):153-9 — пабмед
- Натурвиссеншафтен. 1992 август; 79 (8): 361-5 — пабмед
термины MeSH
вещества
= | Сбалансированное уравнение химической реакции
| Поиск |
Результаты поиска по химическому уравнению
Новости Только 5% НАСЕЛЕНИЯ знают
Рекламное объявление
1 результатов найдено
Отображение уравнения от 1 до 1 Страница 1 — Пожалуйста, прокрутите до конца, чтобы увидеть больше результатов
Уравнение Результат #1
Нажмите, чтобы увидеть более подробную информацию и рассчитать вес/моль >>
120609000000-22866. png» substance-weight=»126.7510″> FeCl 2 png» substance-weight=»126.7510″> FeCl 2 | + | Рекламное объявлениеДополнительная информация об уравнении FeCl2 + H 2 S → FeS + 2HClВ каких условиях FeCl2 (хлорид железа(ii)) реагирует с h3S (сероводород) ?Для этого химического уравнения не найдено информации Объяснение: идеальные условия окружающей среды для реакции, такие как температура, давление, катализаторы и растворитель. |


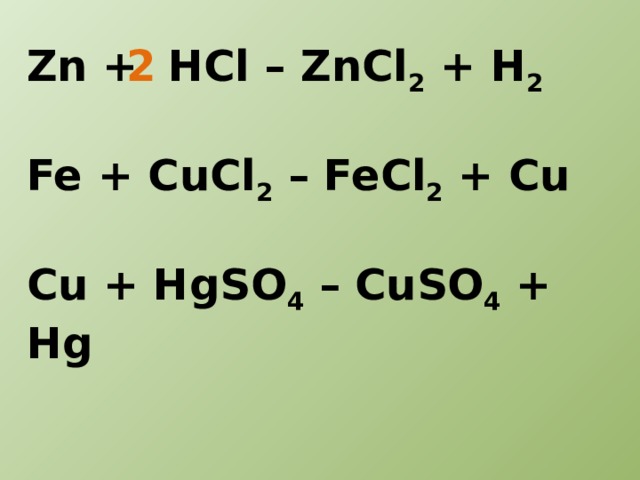
 Роффи А. и др.
Наномасштаб Adv. 2019 5 июня; 1 (8): 2965-2978. дои: 10.1039/c9na00262f. Электронная коллекция 2019 6 августа.
Наномасштаб Adv. 2019.
PMID: 36133625
Бесплатная статья ЧВК.
Роффи А. и др.
Наномасштаб Adv. 2019 5 июня; 1 (8): 2965-2978. дои: 10.1039/c9na00262f. Электронная коллекция 2019 6 августа.
Наномасштаб Adv. 2019.
PMID: 36133625
Бесплатная статья ЧВК. doi: 10.1039/d1ra03705f. Электронная коллекция 2021 27 сентября.
RSC Adv. 2021.
PMID: 35495494
Бесплатная статья ЧВК.
doi: 10.1039/d1ra03705f. Электронная коллекция 2021 27 сентября.
RSC Adv. 2021.
PMID: 35495494
Бесплатная статья ЧВК. 2021 6 декабря; 26 (23): 7394. doi: 10.3390/молекулы26237394.
Молекулы. 2021.
PMID: 34885977
Бесплатная статья ЧВК.
2021 6 декабря; 26 (23): 7394. doi: 10.3390/молекулы26237394.
Молекулы. 2021.
PMID: 34885977
Бесплатная статья ЧВК. 1992 Sep 1;89(17):8117-20
—
пабмед
1992 Sep 1;89(17):8117-20
—
пабмед