Ответы | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Посмотреть всех экспертов из раздела Учеба и наука > Химия
| Похожие вопросы |
В цилиндре под поршнем находится воздух при давлении 250 кПа и температуре 27 °C.
Определить количество вагонов-думпкаров ВС-85 для тягового агрегата ОПЭ-1
Здравствуйте! Мне нужна помощь в решении контрольной по алгебре, 11 класс. Тема: Показательная и логарифмическая функции. Буду очень признательна!
Автомобиль, с колесами радиуса R, движется со скоростью v по горизонтальной дороге, причем v2Rg, где g-ускорение свободного падения. На какую
Решено
Знайдіть модуль напруженості електричного поля точкового заряду q=-36 нКл на відстані 2 см від нього. Заряд знаходиться у воді
Пользуйтесь нашим приложением
Ответы | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Посмотреть всех экспертов из раздела Учеба и наука > Химия
| Похожие вопросы |
Гидролиз NA3PO4
CaC2->C2h3->C6H6->C6H6-NO2->C6H6-Nh3
количественные характеристики растворов
Из предложенного ряда формул выпишите.
Решено
Реакция изомеризации пентана.
Пользуйтесь нашим приложением
Характеристические реакции ионов магния (Mg²⁺)
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 97272
- Джеймс П. Бирк
- Университет штата Аризона
- Наиболее распространенная степень окисления: +2
- М.П. 650º
- л.н. 1120º
- Плотность 1,74 г/см 3
- Характеристики: Магний — металл серебристого цвета, весьма активный, медленно реагирующий с кипящей (но не холодной) водой с образованием водорода и довольно нерастворимого гидроксида магния \(\ce{Mg(OH)2}\).
 Он легко соединяется с кислородом и при высоких температурах реагирует с такими неметаллами, как галогены, сера и даже азот. 9{2-}}\)
Он легко соединяется с кислородом и при высоких температурах реагирует с такими неметаллами, как галогены, сера и даже азот. 9{2-}}\)Эта страница под названием «Характерные реакции ионов магния (Mg²⁺)» распространяется по незаявленной лицензии, автором, ремиксом и/или куратором которой является Джеймс П. Бирк.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Автор
- Джеймс Бирк
- Показать страницу TOC
- № на стр.
- Теги
- Магний
- реактив магния
Магний (Mg) и вода
- Домашний
- Периодическая таблица
- Элементы и вода
- Магний в воде (Mg + h3O)
Магний присутствует в морской воде в количестве около 1300 ppm.  После натрия это наиболее часто встречающийся катион в океанах. Реки содержат около 4 частей на миллион магния, морские водоросли 6000-20 000 частей на миллион, а устрицы 1200 частей на миллион. Голландская питьевая вода
После натрия это наиболее часто встречающийся катион в океанах. Реки содержат около 4 частей на миллион магния, морские водоросли 6000-20 000 частей на миллион, а устрицы 1200 частей на миллион. Голландская питьевая вода
содержит от 1 до 5 мг магния на литр.
Магний и другие щелочноземельные металлы отвечают за жесткость воды. Вода, содержащая большое количество ионов щелочноземельных металлов, называется жесткой водой, а вода с низким содержанием этих ионов называется мягкой водой.
Как и в какой форме магний взаимодействует с водой?Металлы магния не подвержены влиянию воды при комнатной температуре. Магний обычно является медленно реагирующим элементом, но его реакционная способность увеличивается с повышением уровня кислорода. Кроме того, магний реагирует с парами воды с образованием гидроксида магния и газообразного водорода:
Mg (т) + 2H 2 O(г) -> Mg(OH) 2 (водн.) + H 2 (г)
Пожары магния нельзя потушить водой.
 Магний продолжает гореть после истощения кислорода. Затем он реагирует с азотом из воздуха с образованием нитрида магния (Mg 3 N 2 ). Когда предпринимаются попытки потушить огонь магния водой, магний агрессивно реагирует с газообразным водородом. Чтобы предотвратить какие-либо повреждения, огонь магния должен быть покрыт песком.
Магний продолжает гореть после истощения кислорода. Затем он реагирует с азотом из воздуха с образованием нитрида магния (Mg 3 N 2 ). Когда предпринимаются попытки потушить огонь магния водой, магний агрессивно реагирует с газообразным водородом. Чтобы предотвратить какие-либо повреждения, огонь магния должен быть покрыт песком.
Примером соединения магния является фосфид магния (Mg 3 P 2 ), твердое вещество серого цвета с запахом. Когда это соединение вступает в контакт с водой или влажным воздухом, оно разлагается и образуется фосфин (PH 3 ). Это токсичное соединение, а также очень легко воспламеняется на воздухе.
Растворимость магния и соединений магнияМагний в основном присутствует в виде Mg 2+ (водн.) в водных растворах, а также в виде MgOH + (водн.) и Mg(OH) 2 (водн. ). В морской воде его также можно найти в виде MgSO 4 .
Водорастворимость гидроксида магния составляет 12 мг/л. Другие соединения магния явно более растворимы в воде, например, карбонат магния (600 мг/л). Сульфат магния придает воде горьковатый вкус и имеет растворимость в воде 309.г/л при 10 o C.
Другие соединения магния явно более растворимы в воде, например, карбонат магния (600 мг/л). Сульфат магния придает воде горьковатый вкус и имеет растворимость в воде 309.г/л при 10 o C.
Почему магний присутствует в воде?Большое количество минералов содержит магний, например доломит (карбонат кальция-магния; CaMg(CO 3 ) 2 ) и магнезит (карбонат магния; MgCO 3 ). Магний вымывается из горных пород и впоследствии попадает в воду.
Магний имеет множество различных назначений и, следовательно, может попасть в воду разными путями. Химическая промышленность добавляет магний в пластмассы и другие материалы в качестве противопожарной меры или в качестве наполнителя. Он также попадает в окружающую среду в результате внесения удобрений и корма для скота. Сульфат магния применяется на пивоваренных заводах, а гидроксид магния применяется в качестве флокулянта на очистных сооружениях. Магний также является мягким слабительным. Магниевые сплавы применяются в кузовах автомобилей и самолетов.
Магниевые сплавы применяются в кузовах автомобилей и самолетов.
Во время Второй мировой войны магний применялся в зажигательных бомбах, вызывающих крупные пожары в городах. При разработке этих бомб использовался метод извлечения магния из морской воды.
Каково воздействие магния в воде на окружающую среду?Магний является диетическим минералом для любого организма, кроме насекомых. Это центральный атом молекулы хлорофилла, поэтому он необходим для фотосинтеза растений. Магний можно найти не только в морской воде, но и в реках и дождевой воде, что приводит к его естественному распространению в окружающей среде.
В природе встречаются три изотопа магния, все они стабильны и, следовательно, не радиоактивны. Есть также восемь нестабильных изотопов.
Рекомендации по содержанию магния в питьевой воде маловероятны, поскольку не ожидается отрицательного воздействия на здоровье людей и животных.
Экологические проблемы, косвенно вызванные магнием в воде, вызваны применением умягчителей. Как было описано ранее, жесткость частично обусловлена магнием. Ионы кальция и магния (особенно кальций) отрицательно влияют на очищающую способность моющих средств, так как образуют с мылом практически нерастворимые соли. Следовательно, в мыло добавляется около 40% смягчителя. Раньше это были фосфаты, но было обнаружено, что они практически не поддаются биологическому разложению и вызывают эвтрофикацию. Сегодня применяются альтернативные химикаты, в основном комплексообразователи, такие как цитрат натрия, ЭДТА и НТА, или ионообменники, такие как цеолит А. Эти вещества не вызывают эвтрофикацию и не токсичны. Нитрилоуксусная кислота (NTA) может быть мутагенной, и ее трудно удалить во время очистки воды. Цеолит А увеличивает количество шлама. Кроме того, другие комплексообразователи, такие как этилендиаминтетрауксусная кислота (ЭДТА), обладают смелостью удалять металлы из соединений, которые в противном случае трудно разлагаются. Подвижные тяжелые металлы могут попасть в водные пути, потому что ЭДТА трудно удалить на очистных сооружениях.
Как было описано ранее, жесткость частично обусловлена магнием. Ионы кальция и магния (особенно кальций) отрицательно влияют на очищающую способность моющих средств, так как образуют с мылом практически нерастворимые соли. Следовательно, в мыло добавляется около 40% смягчителя. Раньше это были фосфаты, но было обнаружено, что они практически не поддаются биологическому разложению и вызывают эвтрофикацию. Сегодня применяются альтернативные химикаты, в основном комплексообразователи, такие как цитрат натрия, ЭДТА и НТА, или ионообменники, такие как цеолит А. Эти вещества не вызывают эвтрофикацию и не токсичны. Нитрилоуксусная кислота (NTA) может быть мутагенной, и ее трудно удалить во время очистки воды. Цеолит А увеличивает количество шлама. Кроме того, другие комплексообразователи, такие как этилендиаминтетрауксусная кислота (ЭДТА), обладают смелостью удалять металлы из соединений, которые в противном случае трудно разлагаются. Подвижные тяжелые металлы могут попасть в водные пути, потому что ЭДТА трудно удалить на очистных сооружениях. В отличие от кальция магний не связывается с цеолитами в условиях промывки.
В отличие от кальция магний не связывается с цеолитами в условиях промывки.
Жесткость воды может различаться в зависимости от региона, поэтому добавление смягчителей к моющим средствам не требуется для регионов, где используется только мягкая вода. В регионах с жесткой водой можно применять более высокие дозы моющего средства, чтобы добавить больше смягчителя. Это приводит к тому, что другие вещества в моющих средствах дозируются слишком высоко, что усложняет процесс очистки сточных вод. Возможным решением этой проблемы является самостоятельное дозирование различных соединений в моющих средствах.
Как магний в воде влияет на здоровье?Человеческое тело содержит около 25 г магния, из которых 60 % находится в костях, а 40 % — в мышцах и других тканях. Это диетический минерал для человека, один из микроэлементов, отвечающих за функции мембран, передачу нервных стимуляторов, сокращение мышц, построение белков и репликацию ДНК. Магний входит в состав многих ферментов.


 12.13
12.13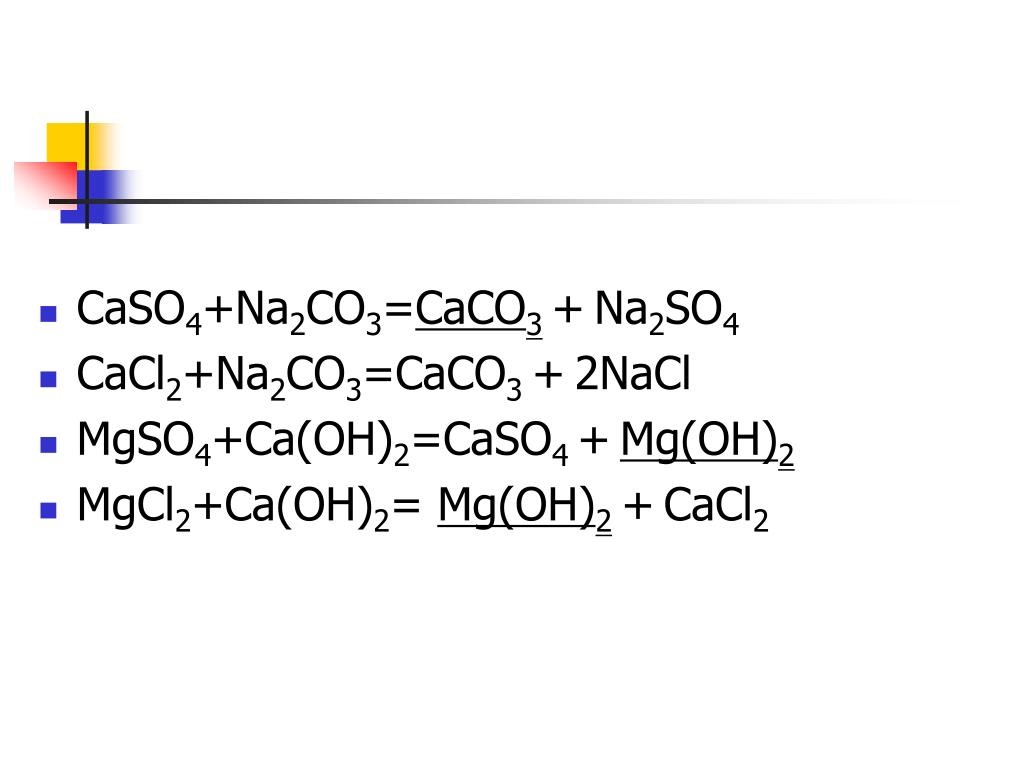 11.14
11.14 Он легко соединяется с кислородом и при высоких температурах реагирует с такими неметаллами, как галогены, сера и даже азот. 9{2-}}\)
Он легко соединяется с кислородом и при высоких температурах реагирует с такими неметаллами, как галогены, сера и даже азот. 9{2-}}\) После натрия это наиболее часто встречающийся катион в океанах. Реки содержат около 4 частей на миллион магния, морские водоросли 6000-20 000 частей на миллион, а устрицы 1200 частей на миллион. Голландская питьевая вода
После натрия это наиболее часто встречающийся катион в океанах. Реки содержат около 4 частей на миллион магния, морские водоросли 6000-20 000 частей на миллион, а устрицы 1200 частей на миллион. Голландская питьевая вода  Магний продолжает гореть после истощения кислорода. Затем он реагирует с азотом из воздуха с образованием нитрида магния (Mg 3 N 2 ). Когда предпринимаются попытки потушить огонь магния водой, магний агрессивно реагирует с газообразным водородом. Чтобы предотвратить какие-либо повреждения, огонь магния должен быть покрыт песком.
Магний продолжает гореть после истощения кислорода. Затем он реагирует с азотом из воздуха с образованием нитрида магния (Mg 3 N 2 ). Когда предпринимаются попытки потушить огонь магния водой, магний агрессивно реагирует с газообразным водородом. Чтобы предотвратить какие-либо повреждения, огонь магния должен быть покрыт песком.  Другие соединения магния явно более растворимы в воде, например, карбонат магния (600 мг/л). Сульфат магния придает воде горьковатый вкус и имеет растворимость в воде 309.г/л при 10 o C.
Другие соединения магния явно более растворимы в воде, например, карбонат магния (600 мг/л). Сульфат магния придает воде горьковатый вкус и имеет растворимость в воде 309.г/л при 10 o C. Магниевые сплавы применяются в кузовах автомобилей и самолетов.
Магниевые сплавы применяются в кузовах автомобилей и самолетов.  Как было описано ранее, жесткость частично обусловлена магнием. Ионы кальция и магния (особенно кальций) отрицательно влияют на очищающую способность моющих средств, так как образуют с мылом практически нерастворимые соли. Следовательно, в мыло добавляется около 40% смягчителя. Раньше это были фосфаты, но было обнаружено, что они практически не поддаются биологическому разложению и вызывают эвтрофикацию. Сегодня применяются альтернативные химикаты, в основном комплексообразователи, такие как цитрат натрия, ЭДТА и НТА, или ионообменники, такие как цеолит А. Эти вещества не вызывают эвтрофикацию и не токсичны. Нитрилоуксусная кислота (NTA) может быть мутагенной, и ее трудно удалить во время очистки воды. Цеолит А увеличивает количество шлама. Кроме того, другие комплексообразователи, такие как этилендиаминтетрауксусная кислота (ЭДТА), обладают смелостью удалять металлы из соединений, которые в противном случае трудно разлагаются. Подвижные тяжелые металлы могут попасть в водные пути, потому что ЭДТА трудно удалить на очистных сооружениях.
Как было описано ранее, жесткость частично обусловлена магнием. Ионы кальция и магния (особенно кальций) отрицательно влияют на очищающую способность моющих средств, так как образуют с мылом практически нерастворимые соли. Следовательно, в мыло добавляется около 40% смягчителя. Раньше это были фосфаты, но было обнаружено, что они практически не поддаются биологическому разложению и вызывают эвтрофикацию. Сегодня применяются альтернативные химикаты, в основном комплексообразователи, такие как цитрат натрия, ЭДТА и НТА, или ионообменники, такие как цеолит А. Эти вещества не вызывают эвтрофикацию и не токсичны. Нитрилоуксусная кислота (NTA) может быть мутагенной, и ее трудно удалить во время очистки воды. Цеолит А увеличивает количество шлама. Кроме того, другие комплексообразователи, такие как этилендиаминтетрауксусная кислота (ЭДТА), обладают смелостью удалять металлы из соединений, которые в противном случае трудно разлагаются. Подвижные тяжелые металлы могут попасть в водные пути, потому что ЭДТА трудно удалить на очистных сооружениях.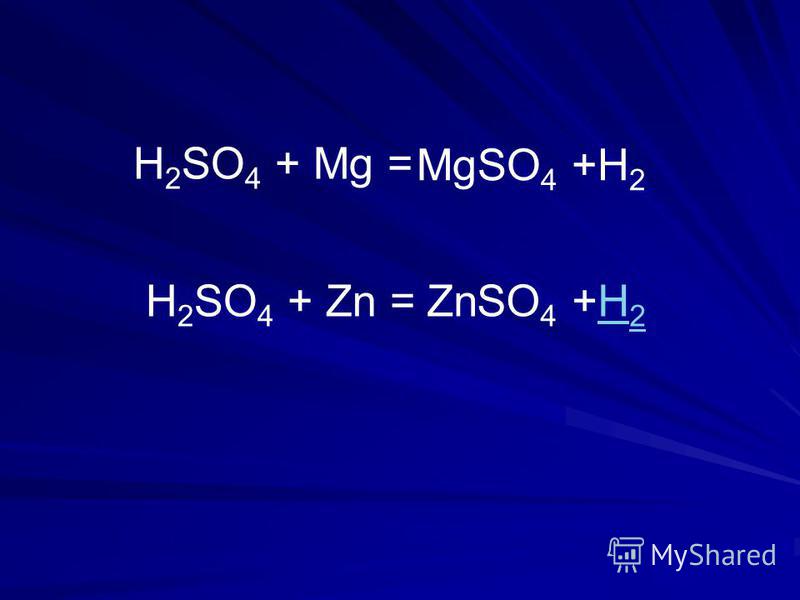 В отличие от кальция магний не связывается с цеолитами в условиях промывки.
В отличие от кальция магний не связывается с цеолитами в условиях промывки. 