| 1 | Найти число нейтронов | H | |
| 2 | Найти массу одного моля | H_2O | |
| 3 | Баланс | H_2(SO_4)+K(OH)→K_2(SO_4)+H(OH) | |
| 4 | Найти массу одного моля | H | |
| 5 | Найти число нейтронов | Fe | |
| 6 | Найти число нейтронов | Tc | |
| 7 | Найти конфигурацию электронов | H | |
| 8 | Найти число нейтронов | Ca | |
| 9 | Баланс | CH_4+O_2→H_2O+CO_2 | |
| 10 | Найти число нейтронов | C | |
| 11 | Найти число протонов | H | |
| 12 | Найти число нейтронов | O | |
| 13 | Найти массу одного моля | CO_2 | |
| 14 | Баланс | C_8H_18+O_2→CO_2+H_2O | |
| 15 | Найти атомную массу | H | |
| 16 | Определить, растворима ли смесь в воде | H_2O | |
| 17 | Найти конфигурацию электронов | Na | |
| 18 | Найти массу одного атома | H | |
| 19 | Найти число нейтронов | Nb | |
| 20 | Найти число нейтронов | Au | |
| 21 | Найти число нейтронов | Mn | |
| 22 | Найти число нейтронов | Ru | |
| 23 | Найти конфигурацию электронов | ||
| 24 | Найти массовую долю | H_2O | |
| 25 | Определить, растворима ли смесь в воде | NaCl | |
| 26 | Найти эмпирическую/простейшую формулу | H_2O | |
| 27 | Найти степень окисления | H_2O | |
| 28 | Найти конфигурацию электронов | K | |
| 29 | Найти конфигурацию электронов | Mg | |
| 30 | Найти конфигурацию электронов | Ca | |
| 31 | Найти число нейтронов | Rh | |
| 32 | Найти число нейтронов | Na | |
| 33 | Найти число нейтронов | Pt | |
| 34 | Найти число нейтронов | Be | Be |
| 35 | Найти число нейтронов | Cr | |
| 36 | Найти массу одного моля | H_2SO_4 | |
| 37 | Найти массу одного моля | HCl | |
| 38 | Найти массу одного моля | Fe | |
| 39 | Найти массу одного моля | C | |
| 40 | Найти число нейтронов | Cu | |
| 41 | Найти число нейтронов | S | |
| 42 | Найти степень окисления | H | |
| 43 | Баланс | CH_4+O_2→CO_2+H_2O | |
| 44 | Найти атомную массу | O | |
| 45 | Найти атомное число | H | |
| 46 | Найти число нейтронов | Mo | |
| 47 | Найти число нейтронов | Os | |
| 48 | Найти массу одного моля | NaOH | |
| 49 | Найти массу одного моля | O | |
| 50 | Найти конфигурацию электронов | Fe | |
| 51 | Найти конфигурацию электронов | C | |
| 52 | Найти массовую долю | NaCl | |
| 53 | Найти массу одного моля | ||
| 54 | Найти массу одного атома | Na | |
| 55 | Найти число нейтронов | N | |
| 56 | Найти число нейтронов | Li | |
| 57 | Найти число нейтронов | V | |
| 58 | Найти число протонов | N | |
| 59 | Упростить | H^2O | |
| 60 | Упростить | h*2o | |
| 61 | Определить, растворима ли смесь в воде | H | |
| 62 | Найти плотность при стандартной температуре и давлении | H_2O | |
| 63 | Найти степень окисления | NaCl | |
| 64 | Найти атомную массу | He | He |
| 65 | Найти атомную массу | Mg | |
| 66 | Найти число электронов | H | |
| 67 | Найти число электронов | O | |
| 68 | Найти число электронов | S | |
| 69 | Найти число нейтронов | Pd | |
| 70 | Найти число нейтронов | Hg | |
| 71 | Найти число нейтронов | B | |
| 72 | Найти массу одного атома | Li | |
| 73 | Найти эмпирическую формулу | H=12% , C=54% , N=20 | , , |
| 74 | Найти число протонов | Be | Be |
| 75 | Найти массу одного моля | Na | |
| 76 | Найти конфигурацию электронов | Co | |
| 77 | Найти конфигурацию электронов | S | |
| 78 | Баланс | C_2H_6+O_2→CO_2+H_2O | |
| 79 | Баланс | H_2+O_2→H_2O | |
| 80 | Найти конфигурацию электронов | P | |
| 81 | Найти конфигурацию электронов | Pb | |
| 82 | Найти конфигурацию электронов | Al | |
| 83 | Найти конфигурацию электронов | Ar | |
| 84 | Найти массу одного моля | O_2 | |
| 85 | Найти массу одного моля | H_2 | |
| 86 | Найти число нейтронов | K | |
| 87 | Найти число нейтронов | P | |
| 88 | Найти число нейтронов | Mg | |
| 89 | Найти число нейтронов | W | |
| 90 | Найти массу одного атома | C | |
| 91 | Упростить | na+cl | |
| 92 | Определить, растворима ли смесь в воде | H_2SO_4 | |
| 93 | Найти плотность при стандартной температуре и давлении | NaCl | |
| 94 | Найти степень окисления | C_6H_12O_6 | |
| 95 | Найти степень окисления | Na | |
| 96 | Определить, растворима ли смесь в воде | C_6H_12O_6 | |
| 97 | Найти атомную массу | Cl | |
| 98 | Найти атомную массу | Fe | |
| 99 | Найти эмпирическую/простейшую формулу | CO_2 | |
| 100 | Найти число нейтронов | Mt |
Строение атома брома (Br), схема и примеры
Онлайн калькуляторы
На нашем сайте собрано более 100 бесплатных онлайн калькуляторов по математике, геометрии и физике.
Справочник
Основные формулы, таблицы и теоремы для учащихся. Все что нужно, чтобы сделать домашнее задание!
Заказать решение
Не можете решить контрольную?!
Мы поможем! Более 20 000 авторов выполнят вашу работу от 100 руб!
Общие сведения о строении атома брома
Относится к элементам p-семейства. Неметалл. Обозначение – Br. Порядковый номер – 35. Относительная атомная масса – 79,904 а.е.м.
Электронное строение атома брома
Атом брома состоит из положительно заряженного ядра (+35), внутри которого есть 35 протонов и 45 нейтронов, а вокруг, по четырем орбитам движутся 35 электронов.
Рис.1. Схематическое строение атома брома.
Распределение электронов по орбиталям выглядит следующим образом:
+35Br)2)8)18)7;
1s22s22p63s23p63d104s24p5.
Внешний энергетический уровень атома брома содержит 7 электронов, которые являются валентными. Энергетическая диаграмма основного состояния принимает следующий вид:
Каждый валентный электрон атома брома можно охарактеризовать набором из четырех квантовых чисел: n (главное квантовое), l (орбитальное), ml (магнитное) и s (спиновое):
|
Подуровень |
n |
l |
ml |
s |
|
s |
4 |
0 |
0 |
+1/2 |
|
s |
4 |
0 |
0 |
-1/2 |
|
p |
4 |
1 |
-1 |
+1/2 |
|
p |
4 |
1 |
-1 |
-1/2 |
|
p |
4 |
1 |
0 |
+1/2 |
|
|
4 |
1 |
0 |
-1/2 |
|
p |
4 |
1 |
1 |
+1/2 |
Наличие одного неспаренного электрона свидетельствует о том, что степень окисления брома может быть равна -1 или +1. Так как на четвертом уровне есть вакантные орбитали 4d-подуровня, то для атома брома характерно наличие возбужденного состояния:
Так как на четвертом уровне есть вакантные орбитали 4d-подуровня, то для атома брома характерно наличие возбужденного состояния:
Именно поэтому для брома также характерна степень окисления +3. Известно, что в своих соединениях бром также способен проявлять степени окисления +5 и +7.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
Сколько протонов, нейтронов и электронов имеет бром?
Бром является классифицированным галогеном и имеет символ «Br». Бром является 35-м элементом периодической таблицы, поэтому его атомный номер равен 35. Атомный номер элемента равен количеству протонов и электронов в этом элементе.
Следовательно, атом брома имеет тридцать пять протонов и тридцать пять электронов. Количество нейтронов в атоме можно определить по разнице между массой атома и количеством протонов.
Разница между массовым числом атома брома и числом протонов составляет сорок пять. Следовательно, атом брома имеет сорок пять нейтронов. Количество нейтронов зависит от изотопа элемента. Атом брома имеет два стабильных изотопа.
| Element Name | Bromine |
| Symbol | Br |
| Atomic number | 35 |
| Atomic weight (average) | 79.904 |
| Protons | 35 |
| Neutrons | 45 |
| Electrons | 35 |
| Group | 17 |
| Period | 4 |
| Block | p-блок |
| Электроны на оболочку | 2, 8, 18, 7 |
| Электронная конфигурация | [Ar] 3d 10 4p 2 0084 5 |
| Степени окисления | +5, +1, -1 |
В этой статье подробно обсуждалось, как легко найти количество протонов, нейтронов и электронов в броме атом.
Также обсуждаются положение электронов, протонов и нейтронов в атоме, число атомных масс и изотопы брома. Надеюсь, после прочтения этой статьи вы узнаете подробности по этой теме.
Содержание
Где в атоме расположены электроны, протоны и нейтроны?
Атом – это мельчайшая частица элемента, которая не существует самостоятельно, но непосредственно участвует в химических реакциях как мельчайшая единица. Атомы настолько малы, что их невозможно увидеть даже под мощным микроскопом.
Диаметр атома водорода равен 0,1 нм (1,0 нм = 10 -9 м). Таким образом, если 1000 миллионов атомов водорода расположить рядом друг с другом, его длина составит 1 метр.
Атомная структура атомаОднако стало возможным обнаружить атомы, увеличив зрение очень мощного электронного микроскопа в два миллиона раз. В атоме существует множество постоянных и временных частиц.
Электроны, протоны и нейтроны находятся в атоме как постоянные частицы. Также нейтрино, антинейтрино, позитрон и масон находятся в атоме как временные частицы.
Атомы обычно можно разделить на две части. Один — ядро, а другой — орбита. Эксперименты разных ученых показали, что ядро атома содержит протоны и нейтроны.
Единственным исключением является водород, в ядре которого есть только протоны, но нет нейтронов. Электроны вращаются вокруг ядра по определенной орбите.
Как легко найти количество электронов, протонов и нейтронов в атоме брома?
Ученый Генри Гвинн Джеффрис Мосл исследовал рентгеновский спектр различных элементов с 1913 по 1914 год. Результаты его экспериментов показывают, что каждый элемент имеет уникальное целое число, равное количеству положительных зарядов в ядре этого элемента.
Он назвал это число порядком атомов. Таким образом, количество положительных зарядов, присутствующих в ядре элемента, называется атомным номером этого элемента. Атомный номер элемента обозначается буквой «Z».
Этот номер равен порядковому номеру таблицы Менделеева. Мы знаем, что протоны находятся в ядре атома в виде положительного заряда.
То есть атомный номер это общее количество протонов. Атом в целом нейтрален по заряду. Следовательно, количество отрицательно заряженных электронов, обращающихся по своей орбите, равно количеству положительно заряженных протонов в ядре.
Атомный номер (Z) = количество зарядов в ядре (p)
Сколько протонов имеет атом брома?
Протоны — постоянные частицы ядра атома. Он находится в центре или ядре атома. Когда атом водорода удаляет электрон со своей орбиты, оставшаяся положительно заряженная частица называется протоном. Следовательно, протон выражается H + .
Относительная масса протонов равна 1, что примерно равно массе водорода (1,00757 а.е.м.). Однако фактическая масса протона составляет 1,6726 × 10 9 .0084 −27 кг. То есть масса протона примерно в 1837 раз больше массы электрона.
Протон — положительно заряженная частица. Его фактический заряд составляет +1,602 × 10 −19 кулонов. Диаметр протонной частицы составляет около 2,4 × 10 -13 см.
В таблице Менделеева 118 элементов, 35-й из них — бром. Элементы в периодической таблице расположены в соответствии с их атомным номером. Поскольку бром является 35-м элементом периодической таблицы, атомный номер брома равен 35.
Мы всегда должны помнить, что атомный номер и число протонов элемента равны. Следовательно, атом брома содержит тридцать пять протонов.
Сколько электронов у атома брома?
Электроны — постоянные частицы ядра атома. Он находится на определенной орбите атома и вращается вокруг ядра. Свойства элементов и их соединений зависят от электронной конфигурации.
В 1897 году ученый Дж. Дж. Томсон открыл существование электронов с помощью электронно-лучевого исследования. Наименьшая из частиц постоянного ядра атома — это электрон. Его масса составляет примерно 1/1836 массы атома водорода.
Фактическая масса электрона составляет 9,1085 × 10 −28 г или 9,1093 × 10 −31 кг. Массой электрона часто пренебрегают, потому что эта масса слишком мала. Электроны всегда дают отрицательный заряд.
Электроны всегда дают отрицательный заряд.
Выражается e – . Заряд электронов составляет –1,609 × 10 –19 кулонов, а относительный заряд – –1. То есть заряд электрона равен заряду протона, но наоборот.
Мы также должны помнить, что количество протонов и электронов в элементе одинаково. Следовательно, атом брома содержит на своей орбите тридцать пять электронов.
Сколько нейтронов у атома брома?
Ученый Чедвик открыл нейтрон в 1932 году. Он находится в ядре в центре атома. Нейтрон является частицей с нейтральным зарядом и выражается через n.
Заряд нейтрона равен нулю, и относительный заряд также равен нулю. Масса нейтрона 1,674×10 −27 кг. Количество электронов и протонов в атоме одинаково, но количество нейтронов разное.
Мы уже знаем, что ядро находится в центре атома. В ядре есть два типа частиц. Один из них представляет собой положительно заряженный протон, а другой — нейтрон с нейтральным зарядом.
Почти вся масса атома сосредоточена в ядре. Поэтому массу ядра называют атомной массой. Ядро состоит из протонов и нейтронов. Следовательно, атомная масса относится к общей массе протонов и нейтронов.
Атомная масса (A) = Масса ядра = Суммарная масса протонов и нейтронов (p + n)
Опять же, масса каждого протона и нейтрона составляет около 1 а.е.м. Поэтому общее число протонов и нейтронов называется атомным массовым числом. То есть число атомной массы (А) равно p + n
Таким образом, число нейтронов в элементе получается из разницы между числом атомных масс и числом атомов. То есть число нейтронов (n) = атомное массовое число (A) – атомное число (Z)
| Mass number (A) | Atomic number (Z) | Neutron number = A – Z |
| 79.904 | 35 | 45 |
Мы знаем, что атомный номер брома равен 35, а среднее атомное массовое число около 80. Нейтрон = 80 – 35 = 45. Следовательно, атом брома имеет сорок пять нейтронов.
Нейтрон = 80 – 35 = 45. Следовательно, атом брома имеет сорок пять нейтронов.
Основываясь на атомном номере, массовом числе и числе нейтронов элемента, можно рассмотреть три вещи. Это изотоп, изобар и изотон. Количество нейтронов зависит от изотопа атома.
Количество протонов, электронов, нейтронов для брома (Br)Как определить количество нейтронов по изотопам брома?
Атомы, имеющие одинаковое количество протонов, но разные массовые числа, называются изотопами друг друга. Английский химик Фредерик Соди впервые выдвинул идею изотопов в 1912 году, а ученый Астон в 1919 году определил два атома неона с разными массами ( 20 Ne, 22 Ne).
Он назвал атомы с разными массами одного и того же элемента изотопами этого элемента. Количество протонов в атоме изотопа не меняется, но меняется количество нейтронов. Всего у атома брома тридцать два изотопа.
| Isotope | Mass number (A) | Atomic number (Z) | Neutron number = A – Z |
| 68 Br | 67.95836 | 35 | 33 |
| 69 Br | 68.95011 | 35 | 34 |
| 70 Br | 69.94479 | 35 | 35 |
| 71 Br | 70. 93874 93874 | 35 | 36 |
| 72 Br | 71.93664 | 35 | 37 |
| 73 Br | 72.93169 | 35 | 38 |
| 74 Br | 73.929891 | 35 | 39 |
| 75 Br | 74.925776 | 35 | 40 |
| 76 Br | 75.924541 | 35 | 41 |
| 77 Br | 76.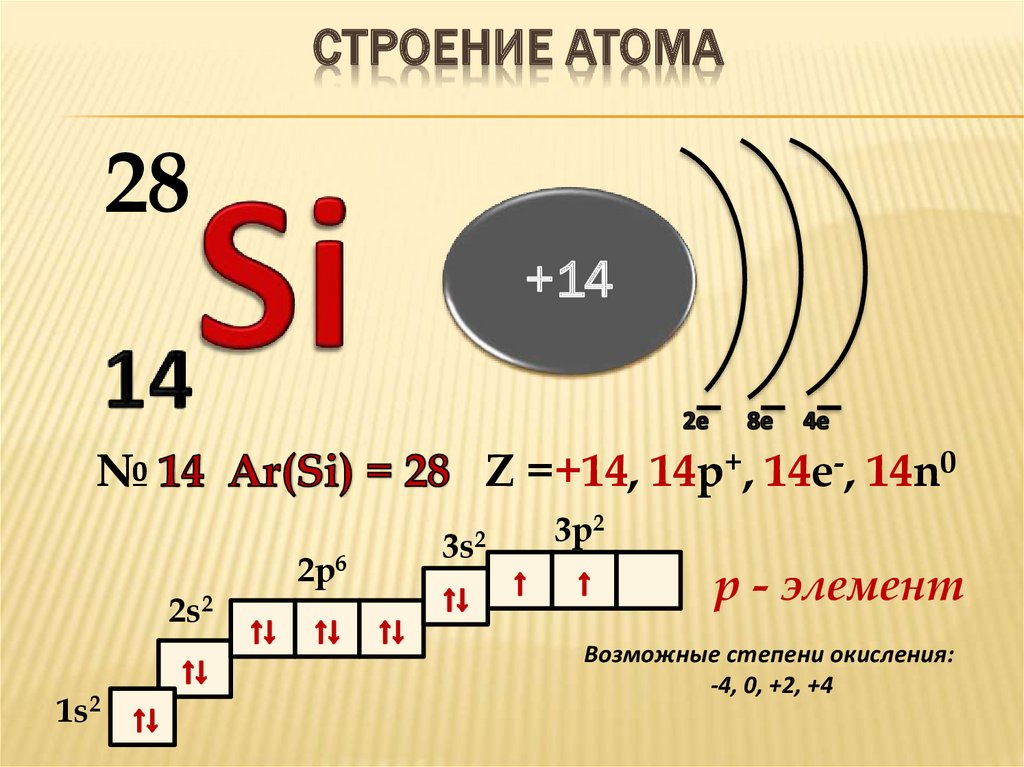 921379 921379 | 35 | 42 |
| 78 Br | 77.921146 | 35 | 43 |
| 79 Br | 78.9183371 | 35 | 44 |
| 80 Br | 79.9185293 | 35 | 45 |
| 81 Br | 80.9162906 | 35 | 46 |
| 82 Br | 81.9168041 | 35 | 47 |
| 83 Br | 82. 915180 915180 | 35 | 48 |
| 84 Br | 83.916479 | 35 | 49 |
| 85 Br | 84.915608 | 35 | 50 |
| 86 Br | 85.918798 | 35 | 51 |
| 87 Br | 86.920711 | 35 | 52 |
| 88 Br | 87.92407 | 35 | 53 |
| 89 Br | 88. 92639 92639 | 35 | 54 |
| 90 Br | 89.93063 | 35 | 55 |
| 91 Br | 90.93397 | 35 | 56 |
| 92 Br | 91.93926 | 35 | 57 |
| 93 Br | 92.94305 | 35 | 58 |
| 94 Br | 93.94868 | 35 | 59 |
| 95 Br | 94. 95287 95287 | 35 | 60 |
| 96 Br | 95.95853 | 35 | 61 |
| 97 Br | 96.96280 | 35 | 62 |
| 98 Br | 35 | 63 | |
| 101 Br | 35 | 66 |
Среди изотопов бром-79 и бром-81 стабильны и образуются естественным путем. Остальные изотопы брома очень нестабильны, а их периоды полураспада очень короткие.
Из 32 радиоизотопов брома самым долгоживущим является бром-77 с периодом полураспада 57,036 часов. Все остальные меньше минуты, большинство меньше секунды. Масса стабильного брома-79 составляет около 79, а брома-81 — около 81.
Все остальные меньше минуты, большинство меньше секунды. Масса стабильного брома-79 составляет около 79, а брома-81 — около 81.
Сколько протонов, нейтронов и электронов имеет ион брома (Br
– )?Когда атом несет отрицательный или положительный заряд, принимая или отталкивая электроны, он называется ионом. Ионные свойства элементов зависят от обмена электронами.
В атомарном ионе изменяется только число электронов, но не изменяется число протонов и нейтронов. У брома на последней орбите всего семь электронов.
Атомный номер брома, атомный вес и зарядПри образовании связи последняя оболочка брома получает электрон и превращается в бромид-ион (Br–). В этом случае атом брома несет отрицательный заряд.
Br + e – → Br –
Здесь электронная конфигурация бромид-иона (Br — ) IS 1S 2 2S 2 2P 6 3S 2 3P 6 3D 10 4S 2 4P 6 . Этот ион брома (Br – ) имеет тридцать пять протонов, сорок пять нейтронов и тридцать шесть электронов.
Этот ион брома (Br – ) имеет тридцать пять протонов, сорок пять нейтронов и тридцать шесть электронов.
| Bromide ion | Protons | Neutrons | Electrons |
| Br – | 35 | 45 | 36 |
| Название | Символ | Относительная масса (AMU) | Относительная плата | Фактическая масса (KG) | Фактическая масса (KG) | Фактическая масса (KG) | Фактическая масса (KG) | Фактическая масса (KG) | Фактическая масса (KG)0014| Actual Charge(C) | Location | |
| Proton | p | 1. 00757 00757 | +1 | 1.672×10 −27 | 1.602×10 −19 | Inside the nucleus | |||||
| Neutron | n | 1.0089 | 0 | 1.674×10 −27 | 0 | Inside the nucleus | |||||
| Electron | e – | 5.488×10 −4 | –1 | 9.109×10 −31 | –1.6×10 –19 | Outside the nucleus |
Почему нам важно знать количество электронов и протонов?
Атомный номер — это число, которое несет в себе свойства элемента. Количество электронов и протонов в элементе определяется атомным номером. Также определяется точное положение элемента в периодической таблице.
Количество электронов и протонов в элементе определяется атомным номером. Также определяется точное положение элемента в периодической таблице.
Свойства элемента можно определить по электронной конфигурации. Кроме того, валентность, валентные электроны и ионные свойства элементов определяются электронной конфигурацией.
Чтобы определить свойства элемента, необходимо расположить электроны этого элемента. И чтобы расположить электроны, вы должны знать количество электронов в этом элементе.
Чтобы узнать количество электронов, вам нужно знать атомный номер этого элемента. Мы знаем, что в ядре элемента находится равное количество протонов с атомным номером, а электроны, равные протонам, находятся на орбите вне ядра.
Атомный номер (Z) = Количество электронов
Мы уже знаем, что атомный номер брома равен 35. То есть в атоме элемента брома тридцать пять электронов. Итак, по электронной конфигурации можно определить свойства брома.
Электронная конфигурация брома показывает, что последняя оболочка брома имеет семь электронов. Следовательно, валентных электронов брома семь.
Следовательно, валентных электронов брома семь.
Последний электрон брома переходит на р-орбиталь. Следовательно, это элемент p-блока. Чтобы знать эти свойства брома, нужно знать число электронов и протонов брома.
Ссылка
Википедия
Chem4Kids.com: Атомы: изотопы
Материя | атомов | Элементы | Периодическая таблица | Реакции | Биохимия | Все темы
Обзор | Структура | Орбиты | Электроны | Ионы | Нейтроны | Изотопы | Склеивание | Соединения | Составные имена | Радиоактивность и антиматерия
Мы уже узнали, что ионы — это атомы, у которых либо отсутствуют, либо есть лишние электроны. Скажем, атому не хватает нейтрона или есть лишний нейтрон.
Например, во Вселенной много атомов углерода (C). Нормальные — углерод-12. Эти атомы имеют 6 нейтронов. Есть несколько отстающих атомов, у которых нет 6. Эти странные атомы могут иметь 7 или даже 8 нейтронов. Когда вы узнаете больше о химии, вы, вероятно, услышите об углероде-14. Углерод-14 на самом деле имеет 8 нейтронов (2 лишних). С-14 считается изотопом углерода.
Если вы заглядывали в периодическую таблицу, то могли заметить, что атомная масса элемента редко бывает четным числом. Это происходит из-за изотопов. Если вы атом с дополнительным электроном, в этом нет ничего страшного. Электроны не имеют большой массы по сравнению с нейтроном или протоном.
Атомные массы рассчитываются путем определения количества каждого типа атома и изотопа во Вселенной. У углерода много атомов С-12, пара атомов С-13 и несколько атомов С-14. Когда вы усредняете все массы, вы получаете число, которое немного превышает 12 (вес атома C-12). средняя атомная масса элемента на самом деле равна 12,011. Поскольку вы никогда не знаете, какой атом углерода вы используете в расчетах, вы должны использовать среднюю массу атома.
Бром (Br) с атомным номером 35 имеет большее разнообразие изотопов. Атомная масса брома (Br) равна 79,90. Есть два основных изотопа 79 и 81, которые в среднем составляют 79,90 а.е.м. 79 имеет 44 нейтрона, а 81 — 46 нейтронов. Хотя это не изменит среднюю атомную массу, ученые создали изотопы брома с массами от 68 до 9.7. Все дело в количестве нейтронов. По мере того, как вы переходите к более высоким атомным номерам в периодической таблице, вы, вероятно, найдете еще больше изотопов для каждого элемента.
Если мы еще раз посмотрим на атом C-14, мы обнаружим, что C-14 не существует вечно. Наступает время, когда он теряет лишние нейтроны и становится С-12. Потеря этих нейтронов называется радиоактивным распадом . Этот распад происходит регулярно, как часы. Для углерода распад происходит за несколько тысяч лет (5730 лет). Некоторым элементам требуется больше времени, а другие имеют распад, который происходит в течение нескольких минут. Археологи могут использовать свои знания о радиоактивном распаде, когда им нужно узнать дату раскопанного объекта. C-14, запертый в объекте несколько тысяч лет назад, будет распадаться с определенной скоростью. Обладая знаниями в области химии, археологи могут определить, сколько тысяч лет тому или иному объекту. Этот процесс называется радиоуглеродный анализ .
► СЛЕДУЮЩАЯ СТРАНИЦА ПО АТОМАМ
► СЛЕДУЮЩАЯ ОСТАНОВКА НА ОБЪЕКТЕ ОБЪЕКТА
► ВИКТОРИНА ПО СТРУКТУРЕ АТОМА
► ВЕРНУТЬСЯ НА НАЧАЛО СТРАНИЦЫ
► Или выполните поиск на сайтах.
