Помощь студентам в учёбе от Людмилы Фирмаль
Здравствуйте!
Я, Людмила Анатольевна Фирмаль, бывший преподаватель математического факультета Дальневосточного государственного физико-технического института со стажем работы более 17 лет. На данный момент занимаюсь онлайн обучением и помощью по любыми предметам. У меня своя команда грамотных, сильных бывших преподавателей ВУЗов. Мы справимся с любой поставленной перед нами работой технического и гуманитарного плана. И не важно: она по объёму на две формулы или огромная сложно структурированная на 125 страниц! Нам по силам всё, поэтому не стесняйтесь, присылайте.
Срок выполнения разный: возможно онлайн (сразу пишите и сразу помогаю), а если у Вас что-то сложное – то от двух до пяти дней.
Для качественного оформления работы обязательно нужны методические указания и, желательно, лекции. Также я провожу онлайн-занятия и занятия в аудитории для студентов, чтобы дать им более качественные знания.
Моё видео:
youtube.com/embed/4sKc0lcxi7g» frameborder=»0″ allow=»accelerometer; autoplay; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»/>Вам нужно написать сообщение в Telegram . После этого я оценю Ваш заказ и укажу срок выполнения. Если условия Вас устроят, Вы оплатите, и преподаватель, который ответственен за заказ, начнёт выполнение и в согласованный срок или, возможно, раньше срока Вы получите файл заказа в личные сообщения.
Сколько может стоить заказ?Стоимость заказа зависит от задания и требований Вашего учебного заведения. На цену влияют: сложность, количество заданий и срок выполнения. Поэтому для оценки стоимости заказа максимально качественно сфотографируйте или пришлите файл задания, при необходимости загружайте поясняющие фотографии лекций, файлы методичек, указывайте свой вариант.
Какой срок выполнения заказа?Минимальный срок выполнения заказа составляет 2-4 дня, но помните, срочные задания оцениваются дороже.
Сначала пришлите задание, я оценю, после вышлю Вам форму оплаты, в которой можно оплатить с баланса мобильного телефона, картой Visa и MasterCard, apple pay, google pay.
Какие гарантии и вы исправляете ошибки?В течение 1 года с момента получения Вами заказа действует гарантия. В течении 1 года я и моя команда исправим любые ошибки в заказе.
Качественно сфотографируйте задание, или если у вас файлы, то прикрепите методички, лекции, примеры решения, и в сообщении напишите дополнительные пояснения, для того, чтобы я сразу поняла, что требуется и не уточняла у вас. Присланное качественное задание моментально изучается и оценивается.
Теперь напишите мне в Telegram или почту и прикрепите задания, методички и лекции с примерами решения, и укажите сроки выполнения. Я и моя команда изучим внимательно задание и сообщим цену.
Если цена Вас устроит, то я вышлю Вам форму оплаты, в которой можно оплатить с баланса мобильного телефона, картой Visa и MasterCard, apple pay, google pay.
Мы приступим к выполнению, соблюдая указанные сроки и требования. 80% заказов сдаются раньше срока.
После выполнения отправлю Вам заказ в чат, если у Вас будут вопросы по заказу – подробно объясню. Гарантия 1 год. В течении 1 года я и моя команда исправим любые ошибки в заказе.
youtube.com/embed/g4ioDc7sLwU» frameborder=»0″ allow=»accelerometer; autoplay; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»/>
youtube.com/embed/zW5JhiZ4140″ frameborder=»0″ allow=»accelerometer; autoplay; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»/>
Можете смело обращаться к нам, мы вас не подведем. Ошибки бывают у всех, мы готовы дорабатывать бесплатно и в сжатые сроки, а если у вас появятся вопросы, готовы на них ответить.
Ошибки бывают у всех, мы готовы дорабатывать бесплатно и в сжатые сроки, а если у вас появятся вопросы, готовы на них ответить.
В заключение хочу сказать: если Вы выберете меня для помощи на учебно-образовательном пути, у вас останутся только приятные впечатления от работы и от полученного результата!
Жду ваших заказов!
С уважением
Пользовательское соглашение
Политика конфиденциальности
Ответы | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||
|
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Посмотреть всех экспертов из раздела Учеба и наука
| Похожие вопросы |
Решено
Периметр прямоугольника 150дм. Длинна его больше ширины на 150см.Вычислидлины сторон прямоугольника.
Длинна его больше ширины на 150см.Вычислидлины сторон прямоугольника.
Медиана равностороннего треугольника равна 13√3.Найдите его сторону. Решение плиз
В треугольнике ABC известно, что AC=6, BC=8, угол C равен 90°. Найдите радиус описанной около этого треугольника окружность. На пишите пожалуйста решение
Среднее арифметическое трех чисел 6.найдите эти числа,если первое число в 2,5 раза больше, а второе в 1,5 раза больше третьего
1) Найдите хорду, стягивающую дугу в 90 градусов, если радиус окружности равен 5 см.
Пользуйтесь нашим приложением
h3s -> ? -> so2 -> ? -> h3so4 -> mgso4 с последним
Химия, 2021-12-31 00:47:21, mirankov
Ответ
Ответ разместил: exampllee1
2h3S+3O2 = 2SO2 + 2h3O
2SO2 + O2 = 2SO3
SO3+h3O = h3SO4
h3SO4 + Mg = MgSO4 + h3
Ответ
Ответ разместил: KoTuK405
1-2
2-3
3-4
4-4
5-3
6-1
7-1
8-3
9-1
10-2
11-3
12-3
13-2
14-2
15-3
16-4
17-3
18-3
19-4
20-CaO+h3O=Ca(OH)2
Ca(OH)2+2HCI=CaCI2+2h3O
Ca(2+) +2OH(-) +2H(+)+2CI(-)=Ca(2+)2CI(-)+2h3O
2H(+)+2OH(-)=2h3O
21 Ba(OH)2+h3SO4=BaSO4+2h3O
m(Ba(OH)2)=50*1/100=5г
M(Ba(OH)2)=171г/моль
n(Ba(OH)2)=5/171=0,3моль
n(BaSO4)=0,3моль
M(BaSO4)=233г/моль
m(BaSO4)=O,3*233=69,9г
Ответ
Ответ разместил: bogoslowskaia
1-4
2- хщ
3-1
4-4
5-3
6-3
7-3
8-3
Ответ
Ответ разместил: Killer3D
1-4
2-4
3-2
4-2
5-1
8-2
9-4
10-4
В2:1)Е 2)Б 3)Г 4)Д
остальные ленюсь
Ответ
Ответ разместил: Mimishichka
1. 4
4
2. 3
3. 1
4. 4
5. 2
6. 1
7. 3
8. 2
9. 3
10. 2
11. 2
12. 3
13. 4
14. 4
15.4
16. 1
17. 1
18. 3
19. m(p-pa) = m(щелочи) + m(h3O) = 10 + 30 = 40 г
W(щелочи) = [m(щелочи)/m(p-pa)]x100% = [10/40]x100% = 25 %
20. 4Al + 3O2 = 2Al2O3
Al(0) — 3e = Al(+3) восстановитель
O2(0) + 4e = 2O(-2) окислитель
Общий коэффициент равен 12: 4Al(0) + 3O2(0) = 4Al(+3) + 6O(-2)
Al2O3 + 6HCl = 2AlCl3 + 3h3O
AlCl3 + 3NaOH = Al(OH)3 + 3NaCl
Al(3+) + 3Cl(-) + 3Na(+) + 3OH(-) = Al(OH)3 + 3Na(+) + 3Cl(-)
Al(3+) + 3OH(-) = Al(OH)3
21. Na2SiO3 + 2HNO3 = 2NaNO3 + h3SiO3 (осадок)
m(Na2SiO3) = m(p-pa)xW(p-pa) = 50×0,2 = 10 г
n(Na2SiO3) = m/M = 10/122 = 0,082 моль = n(h3SiO3)
m(h3SiO3) = nxM = 0,082×78 = 6,4 г
Ответ
Ответ разместил: liza901283
1. Иод
2. Кислород
3. Ослабевают
4. h3SO4
5. Оксид натрия
6. Ba(OH)2, NaNO3, HNO3
7. ZnO + h3SO4 = ZnSO4 + h3O
ZnO + h3SO4 = ZnSO4 + h3O
8. 3
9. 2AlCl3 и 3h3
10. с кислотами и кислотными оксидами
11. CO2
12. h3CO3
13. соляной кислоте
14. серной кислоты
15. Na2CO3 + 2HNO3 = 2NaNO3 + CO2 + h3O
16. хлоридами
17. 40%
18. 128 г
19. 25%
20.
2Сu+O2=2CuO
электронный баланс:
2 | Сu(0)-2e=Cu(2+)
1 | O2+4e=2O(2-)
CuO+2HCl=CuCl2+h3O
полное ионное
CuO+2H(+)+2Cl(-)=Cu(2+)+2Cl(-)+h3O
сокращенное ионное
CuO+2H(+)=Cu(2+)+h3O
CuCl2+2NaOH=Cu(OH)2+2NaCl
полное ионное
Cu(2+)+2Cl(-)+2Na(+)+2OH(-)=Cu(OH)2+2Na(+)+2Cl(-)
сокращенное ионное
Cu(2+)+2OH(-)=Cu(OH)2
21.
NaOH+HNO3=NaNO3+h3O
m(NaOH)=m(р-ра) *w(NaOH)=50*12/100=6 г
n(NaOH)=m(NaOH)/M(NaOH)=6/(23+16+1)=6/40=0,15 моль
n(NaNO3)=n(NaOH)=0,15 моль
m(NaNO3)=n(NaNO3)*M(NaNO3)=0,15*(23+14+3*16)=0,15*85=12,75 г
Ответ
Ответ разместил: egor22832
1. К простым веществам относится 2) фосфор
2.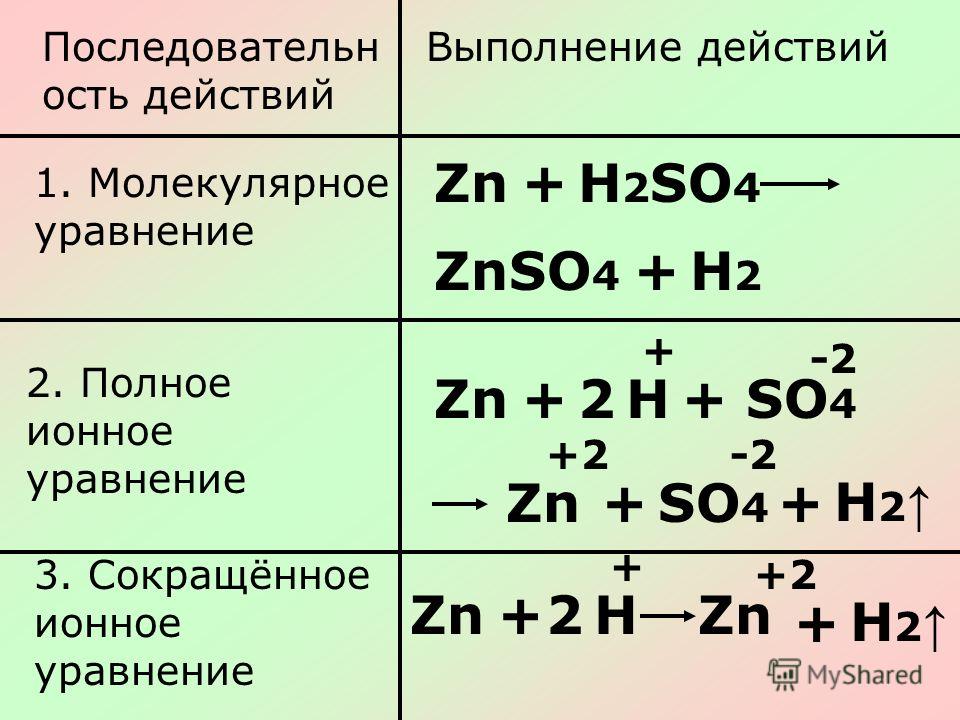 Ряд чисел 2,8,5 соответствует распределению электронов по энергетическим уровням атома 3) фосфора
Ряд чисел 2,8,5 соответствует распределению электронов по энергетическим уровням атома 3) фосфора
3. Наиболее ярко неметаллические свойства выражены у 4) С
4. Степень окисления хрома в оксиде CrO3 равна 4) + 6
5. Химическая связь в молекуле брома Br2 3) ковалентная неполярная
6. Формулы оксида, основания, соли соответственно 1) BaO, Fe(OH)2, NaNO3
7. Уравнение реакции замещения1) Zn + 2HCl = ZnCl2 + h3
8. Коэффициент перед формулой углекислого газа в уравнении реакции горения этана, схема которой 2C2H6 + O2––> CO2 + 6h3O 3) 4
9. Соль и водород образуются при взаимодействии соляной кислоты с1) металлами (не всеми)
10. Гидроксид меди(II) реагирует c 2) HNO3
11.Оксид кальция реагирует с 3) HNO3
12. Формула вещества X в схеме превращений FeO ––> X ––> FeCl2 3) Fe
13. Фенолфталеин изменяет окраску при добавлении к 2) NaOH (р-р )
14. К электролитам относится каждое из веществ в ряду 2) CuCl2, HCl, Na2SO4
15. К реакциям ионного обмена относится 3) NaCl + AgNO3 = NaNO3 + AgCl
16. В соответствии с сокращенным ионным уравнением Cu2+ + 2OH– = Cu(OH)2 взаимодействуют электролиты 2) CuCl2 и KOH
В соответствии с сокращенным ионным уравнением Cu2+ + 2OH– = Cu(OH)2 взаимодействуют электролиты 2) CuCl2 и KOH
17. Массовая доля кислорода в серной кислоте h3SO4 равна приблизительно 3) 65%
18. Количество водорода, выделившегося при взаимодействии 325 г цинка с соляной кислотой, равно 3) 5 моль
19. Для приготовления 5%-ного раствора необходимо 2 г сахара растворить в воде, массой 3) 38 г
Запишите полностью ход решения
20. Напишите уравнения реакций, с которых можно осуществить превращения кальций ––> оксид кальция ––> X ––> хлорид кальция. В первом уравнении расставьте коэффициенты методом электронного баланса, а для последнего запишите полное и сокращенное ионные уравнения.
·2 восстановитель полуреакция окисления
·1 окислитель полуреакция восстановления
21. Определите массу осадка, образовавшегося при взаимодействии 50 г 18%-ного раствора гидроксида бария с серной кислотой.
1) =50 · 0,18 = 9 г
2) моль
3) По уравнению реакции моль
4) =0,0526 · 233=12,2558 г ≈12,26 г
ответ: 12,26 г
Ответ
Ответ разместил: GoRussia228
1. К простым веществам относится 2)фосфор.
К простым веществам относится 2)фосфор.
2. 3)фосфор.
3.Наиболее ярко неметаллические свойства выражены у 4) С.
4.+6.
5.3) ковалентная неполярная.
6. 1)
7. 1)
8.3) 4
9.1)
10.2)
11.3)
12.3)
13.2)
14.2)
15.3)
16.2)
17.3)
18.3)
19.3)
20.2Ca+O2=2CaO
2I Ca(0) -2e->Ca(2+) востановитель окисление
1I O2(0)+4e->2O(-2)окислитель востановление
CaO+h3O=Ca(OH)2
Ca(OH)2+2HCl=CaCl2+2h3O
Ca(2+) +2OH(-) + 2H(+) +2Cl(-) = Ca(2+) +2Cl(-) +2h3O
OH(-) + H(+) = h3O
21.НЕзнаю
Ответ
Ответ разместил: santchkaakimowa
KOH гидроксид калия
Ba(OH)2 гидроксид бария(II)
Fe(OH)3 гидроксид железа(III)
NaOH гидроксид натрия
Ответ
Ответ разместил: aruka996
а) 2HCl+Mg—> MgCl2 + h3 (стрелка вверх)
б) h3SO4+Zn—> ZnSO4 + h3
В)Pb(no3)2+h3SO4—> PbSO4 (стрелка вниз, малорастворимая моль) + 2HNO3
г) HCl+Al—>
д) ZnO+2HCl—> ZnCl2 + h3O
2. а)Fe(OH)3+HCl= FeCl3 + 3h3O
а)Fe(OH)3+HCl= FeCl3 + 3h3O
б) Al(OH)3+Naoh= основание с основанием не может взаимодействовать
в) Cu(OH)2+h3SO4=CuSO4 + 2h3O
Ответ
Ответ разместил: 8AnnaMur8
ответ: s+h3=h3s
n(h3)=2.5 моль
m(h3)=2.5*2=5
v(h3)=2.5*22.4=56
n(s)=2.5 моль
m(s)=2.5*32=80
объяснение: всё ясно и понятно
Ответ
Ответ разместил: milanavornik
сложи все коэффиценты.ответ г
Другие вопросы по: Химия
Опубликовано: 27.02.2019 18:30
Основанием прямой призмы авса1в1с1 является равнобедренный треугольник, в котором ав=ас=2sqrt(2), вс=2.высота призмы равна 1. найдите градусную меру угла между ребром ас и диагонал…
Ответов: 3
Опубликовано: 28.02.2019 04:20
Написати усмішку(гумористичний твір)…
Ответов: 2
Опубликовано: 02. 03.2019 07:00
03.2019 07:00
Вчетырехугольнике abcd точки m, n,k, l являются серединами ab, bc, cd, ad соответственно прямые mkи ln пересекаются в oдоказать чтосумма векторов oa+ob+oc+od=0…
Ответов: 3
Опубликовано: 03.03.2019 22:50
Найти объем кислорода для сжигания 51 г аммиака…
Ответов: 2
Опубликовано: 04.03.2019 09:20
2. определите молекулярную формулу органического вещества, которое содержит 62,1% углерода и 10,3% водорода, плотность его паров по гелию 14,5. органическое вещество дает реакцию «…
Ответов: 3
Опубликовано: 06.03.2019 21:20
Арифметическая прогрессия задана формулой аn=98-5n найдите сумму положительных членов данной прогрессии…
Ответов: 1
Популярные вопросы
Опубликовано: 27.02.2019 09:10
 найдитеего углы! №2 стороныпрямоугольника равна12,4и26. №3 диагоналиромберавны4,73и2,94.найдит еего углырешите…
найдитеего углы! №2 стороныпрямоугольника равна12,4и26. №3 диагоналиромберавны4,73и2,94.найдит еего углырешите…Ответов: 1
Опубликовано: 01.03.2019 06:30
Первый станок отштампует требуемое число деталей за 5 часов, а второй-за 7 часов. сколько деталей в час штампует первый станок, если второй штампует в час на 100 деталей меньше, че…
Ответов: 3
Опубликовано: 01.03.2019 08:00
На первой полке на18 книг меньше ,чем на второй. после того как число книг на первой полке удвоили ,оно составило 80% от числа книг на второй полке. сколько книг стояло на каждой п…
Ответов: 2
Опубликовано: 01.03.2019 10:30
Найти слова с использования слов с уменьшительно ласкательными суффиксами…
Ответов: 1
Опубликовано: 01.03.2019 17:50
Как решить уравнения: а)(3х+5х)*18=144; б)(7у-3у): 8=17; в)(6а+а): 13=14; г)48: (9b-b)=2;. ..
..
Ответов: 1
Опубликовано: 01.03.2019 20:00
Даны четыре последовательных чётных числа. произведение двух первых из них на 232 меньше произведения двух последующих. найдите эти числа….
Ответов: 2
Опубликовано: 02.03.2019 19:20
Найдите углы треугольника, если внешние его углы пропорциональны числам 3, 7 и 8….
Ответов: 3
Опубликовано: 03.03.2019 03:50
Втреугольнике авс угол в в 2 раза больше угла а и в 3 раза меньше угла с, найдите угол в…
Ответов: 1
Опубликовано: 03.03.2019 08:50
Радиусы оснований усеченного конуса равны 5 дм и 10 дм , а образующая -13дм найти высоту и площадь его осевого сечения…
Ответов: 1
Опубликовано: 04.03.2019 02:10
Идеальный газ переводится из состояния а в в тремя в каком случае совершиться большая работа? почему? какому состоянию соответствует наибольшая температура?. ..
..
Ответов: 2
Больше вопросов по предмету: Химия Случайные вопросы
Популярные вопросы
Гидролиз диоксида серы в малых кластерах серной кислоты: механистическое и кинетическое исследование
. 2015 17 ноября; 49(22):13112-20.
doi: 10.1021/acs.est.5b02977. Epub 2015 26 октября.
Цзинцзин Лю 1 , Шэн Фан 1 , Чжисю Ван 1 , Венцай Йи 1 , Фу-Мин Тао 2 , Цзин-Яо Лю 1
Принадлежности
- 1 Институт теоретической химии Цзилиньского университета, Чанчунь 130023, Китайская Народная Республика.

- 2 Кафедра химии и биохимии Калифорнийского государственного университета, Фуллертон, Калифорния 92834, США.
- PMID: 26450714
- DOI: 10.1021/acs.est.5b02977
Jingjing Liu et al. Технологии экологических наук. .
. 2015 17 ноября; 49(22):13112-20.
doi: 10.1021/acs.est.5b02977. Epub 2015 26 октября.
Авторы
Цзинцзин Лю 1 , Шэн Фан 1 , Чжисю Ван 1 , Венцай Йи 1 , Фу-Мин Тао 2 , Цзин-Яо Лю 1
Принадлежности
- 1 Институт теоретической химии Цзилиньского университета, Чанчунь 130023, Китайская Народная Республика.

- 2 Кафедра химии и биохимии Калифорнийского государственного университета, Фуллертон, Калифорния 92834, США.
- PMID: 26450714
- DOI: 10.1021/acs.est.5b02977
Абстрактный
Реакция осаждения и гидролиза SO2 + h3O в малых кластерах серной кислоты и воды изучена путем теоретических расчетов молекулярных кластеров SO2-(h3SO4)n-(h3O)m (m = 1,2; n = 1,2) . Серная кислота оказывает резкое каталитическое действие на реакцию гидролиза SO2, поскольку она снижает энергетический барьер более чем на 20 ккал/моль. Реакция с моногидратированной серной кислотой (SO2 + h3O + h3SO4 — h3O) имеет наименьший энергетический барьер 3,83 ккал/моль, при которой изначально на входном канале образуется кластер h3SO4-(h3O)2.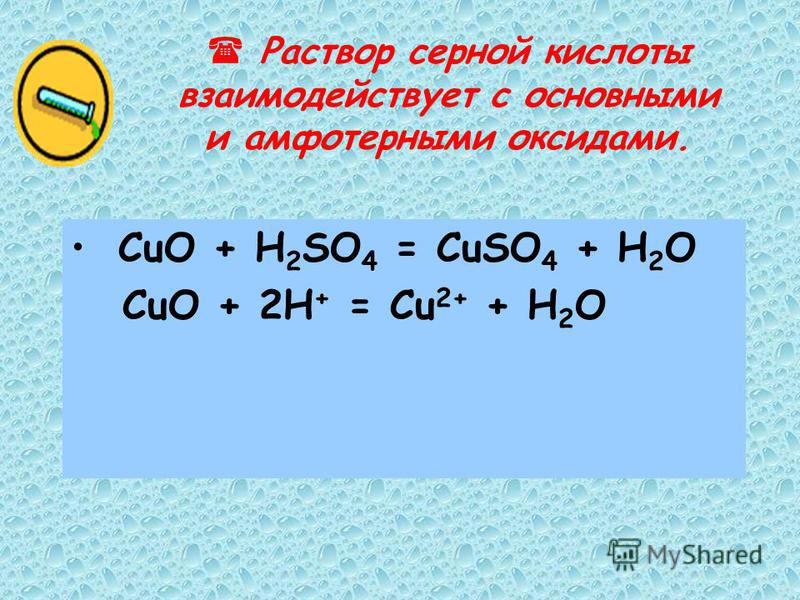 Энергетические барьеры для трех реакций гидролиза расположены в порядке SO2 + (h3SO4)-h3O > SO2 + (h3SO4)2-h3O > SO2 + h3SO4-h3O. Более того, сернистая кислота более прочно связана с кластерами гидратированной серной кислоты (или димера), чем соответствующий реагент (моногидратированный SO2). Следовательно, серная кислота способствует гидролизу SO2 как кинетически, так и термодинамически. Было выполнено кинетическое моделирование для изучения важности этих реакций при восстановлении атмосферного SO2. Результаты дадут новое представление о том, как ранее существовавшие аэрозоли катализируют гидролиз SO2, что приводит к образованию и росту новых частиц.
Энергетические барьеры для трех реакций гидролиза расположены в порядке SO2 + (h3SO4)-h3O > SO2 + (h3SO4)2-h3O > SO2 + h3SO4-h3O. Более того, сернистая кислота более прочно связана с кластерами гидратированной серной кислоты (или димера), чем соответствующий реагент (моногидратированный SO2). Следовательно, серная кислота способствует гидролизу SO2 как кинетически, так и термодинамически. Было выполнено кинетическое моделирование для изучения важности этих реакций при восстановлении атмосферного SO2. Результаты дадут новое представление о том, как ранее существовавшие аэрозоли катализируют гидролиз SO2, что приводит к образованию и росту новых частиц.
Похожие статьи
Механистические и кинетические исследования каталитического гидролиза COS в малых кластерах серной кислоты.
Ли К., Сонг С., Чжу Т., Ван С., Сун С., Нин П., Тан Л. Ли К. и др.
 Загрязнение окружающей среды. 2018 Январь; 232: 615-623. doi: 10.1016/j.envpol.2017.10.004. Epub 2017 9 октября.
Загрязнение окружающей среды. 2018.
PMID: 208
Загрязнение окружающей среды. 2018 Январь; 232: 615-623. doi: 10.1016/j.envpol.2017.10.004. Epub 2017 9 октября.
Загрязнение окружающей среды. 2018.
PMID: 208Синергетическая реакция SO 2 с NO 2 в присутствии H 2 O и NH 3 : потенциальный источник сульфатного аэрозоля.
Ван З., Чжан С., Lv G, Сунь Х., Ван Н., Ли З. Ван Цзи и др. Int J Mol Sci. 2019 31 июля; 20 (15): 3746. дои: 10.3390/ijms20153746. Int J Mol Sci. 2019. PMID: 31370230 Бесплатная статья ЧВК.
Химия атмосферы CH 2 OO: Гидролиз CH 2 OO в малых кластерах серной кислоты.
Ван Р., Вэнь М., Чен Х, Му Р., Цзэн З., Чай Г., Лили М., Ван З., Чжан Т. Ван Р и др.
 J Phys Chem A. 1 апреля 2021 г .; 125 (12): 2642-2652. doi: 10.1021/acs.jpca.1c02006. Epub 2021 23 марта.
J Phys Chem A. 2021.
PMID: 33755485
J Phys Chem A. 1 апреля 2021 г .; 125 (12): 2642-2652. doi: 10.1021/acs.jpca.1c02006. Epub 2021 23 марта.
J Phys Chem A. 2021.
PMID: 33755485Недавний прогресс в создании низкомолекулярных флуоресцентных зондов для обнаружения производных диоксида серы (HSO 3 — /SO 3 2- ).
Ян Б., Сюй Дж., Чжу Х.Л. Ян Б. и др. Свободный Радик Биол Мед. 2019 Декабрь; 145:42-60. doi: 10.1016/j.freeradbiomed.2019.09.007. Epub 2019 13 сентября. Свободный Радик Биол Мед. 2019. PMID: 31525454 Обзор.
Обзор технологий каталитического восстановления диоксида серы (SO 2 ) на сухой и влажной основе.
Нг К.Х., Лай С.И., Джамалудин Н.Ф.М., Мохамед А.Р.
 Нг К.Х. и др.
Джей Хазард Матер. 2022, 5 февраля; 423 (часть A): 127061. doi: 10.1016/j.jhazmat.2021.127061. Epub 2021 30 августа.
Джей Хазард Матер. 2022.
PMID: 34788939
Обзор.
Нг К.Х. и др.
Джей Хазард Матер. 2022, 5 февраля; 423 (часть A): 127061. doi: 10.1016/j.jhazmat.2021.127061. Epub 2021 30 августа.
Джей Хазард Матер. 2022.
PMID: 34788939
Обзор.
Посмотреть все похожие статьи
Цитируется
Теоретическое исследование реакций окисления сернистой кислоты/сульфита озоном с образованием серной кислоты/сульфата с атмосферными последствиями.
Шэн Ф., Цзинцзин Л., Ю С., Фу-Мин Т., Сюэмэй Д., Цзин-Яо Л. Шэн Ф. и др. RSC Adv. 20 февраля 2018 г.; 8(15):7988-7996. дои: 10.1039/c8ra00411k. eCollection 2018 19 февраля. RSC Adv. 2018. PMID: 35542014 Бесплатная статья ЧВК.
Каталитическое действие (H 2 O) n ( n = 1-3) кластеров на HO 2 + SO 2 → HOSO + 3 O 2 реакция в тропосферных условиях.

Ван Р., Яо К., Вэнь М., Тянь С., Ван Ю., Ван З., Ю. С., Шао С., Чен Л. Ван Р и др. RSC Adv. 2019 23 мая; 9(28):16195-16207. дои: 10.1039/c9ra00169g. Электронная коллекция 2019 20 мая. RSC Adv. 2019. PMID: 35521394 Бесплатная статья ЧВК.
Газофазная деградация 2-бутантиола, инициируемая радикалами ОН и атомами Cl: кинетика, выходы продуктов и механизм при 298 К и атмосферное давление.
Кардона А.Л., Гибилиско Р.Г., Бланко М.Б., Визен П., Теруэль М. Кардона А.Л. и др. RSC Adv. 22 июля 2019 г .; 9 (39): 22618-22626. doi: 10.1039/c9ra04051j. Электронная коллекция 2019 17 июля. RSC Adv. 2019. PMID: 35519461 Бесплатная статья ЧВК.
Повышенная гетерогенная гидратация SO 2 за счет иммобилизации пиридинового N на углеродных материалах.

Цзоу Л., Ян П., Лу П., Чен Д., Чу В., Сен В. Цзоу Л. и соавт. R Soc Open Sci. 2020 19 августа; 7(8):192248. doi: 10.1098/rsos.192248. Электронная коллекция 2020 авг. R Soc Open Sci. 2020. PMID: 32968503 Бесплатная статья ЧВК.
Гидролиз формилфторида, катализируемый серной и муравьиной кислотами в атмосфере.
Чжан Л., Лонг Б. Чжан Л. и др. АСУ Омега. 2019 ноябрь 7;4(21):18996-19004. doi: 10.1021/acsomega.9b01864. Электронная коллекция 2019 19 ноября. АСУ Омега. 2019. PMID: 31763521 Бесплатная статья ЧВК.
Типы публикаций
термины MeSH
вещества
Контактный процесс — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 3838
- Джим Кларк
- Школа Труро в Корнуолле
Контактный процесс используется при производстве серной кислоты. Эти модули объясняют причины условий, используемых в процессе, рассматривая влияние пропорций, температуры, давления и катализатора на состав равновесной смеси, скорость реакции и экономику процесса. Контактный процесс:
Эти модули объясняют причины условий, используемых в процессе, рассматривая влияние пропорций, температуры, давления и катализатора на состав равновесной смеси, скорость реакции и экономику процесса. Контактный процесс:
- Этап 1: Получение диоксида серы
- Этап 2: Преобразование диоксида серы в триоксид серы (обратимая реакция в основе процесса)
- Этап 3: Преобразование триоксида серы в концентрированную серную кислоту
Этап 1: Получение диоксида серы
Это можно сделать путем сжигания серы в избытке воздуха:
\[ S_{(s)} + O_2 (g) \rightarrow SO_{2\; (g)} \label{1}\]
или путем нагревания сульфидных руд, таких как пирит, в избытке воздуха:
\[4FeS_2 (т) + 11O_2 (г) \rightarrow 2Fe_2O_3 (т) + 8SO_2 (г) \label{2}\]
В любом случае используется избыток воздуха, чтобы образовавшийся диоксид серы уже смешанный с кислородом для следующего этапа.
Стадия 2: Преобразование диоксида серы в триоксид серы
Это обратимая и экзотермическая реакция.
\[2SO_2(g) + O_2(g) \rightleftharpoons 2SO_3(g) \;\;\; \Дельта{Н}=-196\; кДж/моль \label{3}\]
Схема технологического процесса для этой части процесса выглядит следующим образом:
Причины всех этих состояний будут подробно рассмотрены далее на странице.
Стадия 3: Преобразование триоксида серы в серную кислоту
Этого нельзя добиться простым добавлением воды к триоксиду серы; реакция настолько неконтролируема, что создает туман из серной кислоты. Вместо этого триоксид серы сначала растворяют в концентрированной серной кислоте:
\[ H_2SO_{4 (л)} + SO_{3(г)} \rightarrow H_2S_2O_{7 (л)} \label{4}\]
Продукт известен как дымящая серная кислота или олеум , который затем можно безопасно реагировать с водой с получением концентрированной серной кислоты – в два раза больше, чем первоначально использовалось для производства дымящей серной кислоты.
\[ H_2S_2O_{7 (ж)} + H_2O_{(ж)} \rightarrow 2H_2SO_{4 (ж)} \label{5}\]
Объяснение условий
Смесь диоксида серы и кислорода, поступающая в реактор находится в равных пропорциях по объему. Закон Авогадро гласит, что равные объемы газов при одинаковых температуре и давлении содержат одинаковое количество молекул. Это означает, что газы поступают в реактор в соотношении 1 молекула диоксида серы на 1 молекулу кислорода.
Закон Авогадро гласит, что равные объемы газов при одинаковых температуре и давлении содержат одинаковое количество молекул. Это означает, что газы поступают в реактор в соотношении 1 молекула диоксида серы на 1 молекулу кислорода.
Это избыток кислорода по сравнению с пропорциями, требуемыми уравнением.
\[2SO_{2(g)} + O_{2(g)} \rightleftharpoons 2SO_{3(g)} \;\;\; \Delta{H}=-196\;кДж/моль\]
Согласно принципу Ле Шателье увеличение концентрации кислорода в смеси приводит к смещению положения равновесия вправо. Поскольку кислород поступает из воздуха, это очень дешевый способ увеличить конверсию диоксида серы в триоксид серы.
Почему бы не использовать еще более высокую долю кислорода? В этом легко убедиться, если взять крайний случай. Предположим, у вас есть миллион молекул кислорода на каждую молекулу диоксида серы. Равновесие будет очень сильно смещено в сторону триоксида серы — практически каждая молекула диоксида серы будет преобразована в триоксид серы. Однако вы не будете производить много триоксида серы каждый день. Подавляющее большинство того, что вы пропускаете через катализатор, — это кислород, которому не с чем реагировать.
Однако вы не будете производить много триоксида серы каждый день. Подавляющее большинство того, что вы пропускаете через катализатор, — это кислород, которому не с чем реагировать.
Увеличивая долю кислорода, вы можете увеличить процент превращения диоксида серы, но в то же время уменьшить общее количество триоксида серы, производимого каждый день. Смесь 1:1 дает наилучший общий выход триоксида серы.
Температура
Соображения равновесия: Вам необходимо сместить положение равновесия как можно дальше вправо, чтобы получить максимально возможное количество триоксида серы в равновесной смеси. Прямая реакция (производство триоксида серы) является экзотермической.
\[2SO_{3(g)} + O_{2(g)} \rightleftharpoons 2SO_{3(g)} \;\;\; \Delta{H} = -196\, кДж/моль\]
Согласно принципу Ле Шателье этому будет способствовать понижение температуры. Система отреагирует изменением положения равновесия, чтобы противодействовать этому, другими словами, производством большего количества тепла. Чтобы получить как можно больше триоксида серы в равновесной смеси, нужна как можно более низкая температура. Однако 400 — 450°С — это не низкая температура!
Чтобы получить как можно больше триоксида серы в равновесной смеси, нужна как можно более низкая температура. Однако 400 — 450°С — это не низкая температура!
Соображения по скорости: Чем ниже температура, которую вы используете, тем медленнее становится реакция. Производитель пытается производить как можно больше триоксида серы в день. Нет смысла пытаться получить равновесную смесь, содержащую очень высокую долю триоксида серы, если для достижения равновесия реакции требуется несколько лет. Вам нужно, чтобы газы достигли равновесия за очень короткое время, пока они будут в контакте с катализатором в реакторе.
Компромисс: 400 — 450°C является компромиссной температурой, дающей довольно высокую долю триоксида серы в равновесной смеси, но за очень короткое время.
Давление
Соображения равновесия:
\[ 2SO_{2(g)} + O_{2(g)} \rightleftharpoons 2SO_{3(g)} \;\;\; \Delta H = -196\;кДж/моль\]
Обратите внимание, что в левой части уравнения три молекулы, а в правой только две. Согласно принципу Ле Шателье, если вы увеличите давление, система отреагирует на реакцию, которая будет производить меньше молекул. Это приведет к тому, что давление снова упадет. Чтобы получить как можно больше триоксида серы в равновесной смеси, нужно максимально высокое давление. Высокое давление также увеличивает скорость реакции. Однако реакция происходит при давлениях, близких к атмосферному давлению!
Согласно принципу Ле Шателье, если вы увеличите давление, система отреагирует на реакцию, которая будет производить меньше молекул. Это приведет к тому, что давление снова упадет. Чтобы получить как можно больше триоксида серы в равновесной смеси, нужно максимально высокое давление. Высокое давление также увеличивает скорость реакции. Однако реакция происходит при давлениях, близких к атмосферному давлению!
Экономические соображения: Даже при этих относительно низких давлениях конверсия диоксида серы в триоксид серы составляет 99,5%. Очень небольшое улучшение, которого вы могли бы достичь, увеличив давление, не стоит затрат на создание таких высоких давлений.
Катализатор
Соображения равновесия: Катализатор не оказывает никакого влияния на положение равновесия. Добавление катализатора не приводит к увеличению процентного содержания триоксида серы в равновесной смеси. Его единственная функция — ускорить реакцию.
Соображения по скорости: В отсутствие катализатора реакция настолько медленная, что практически никакая реакция не происходит в любое разумное время. Катализатор обеспечивает достаточно быстрое протекание реакции для установления динамического равновесия за очень короткое время, в течение которого газы фактически находятся в реакторе.
Катализатор обеспечивает достаточно быстрое протекание реакции для установления динамического равновесия за очень короткое время, в течение которого газы фактически находятся в реакторе.
Авторы и авторство
Эта страница под названием «Контактный процесс» распространяется по незаявленной лицензии и была создана, изменена и/или курирована Джимом Кларком.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Автор
- Джим Кларк
- Показать страницу Содержание
- нет на странице
- Теги
- Контактный процесс
= | Сбалансированное уравнение химической реакции
| Поиск |
Результаты поиска по химическому уравнению
Новости Только 5% НАСЕЛЕНИЯ знают
Рекламное объявление
1 результатов найдено
Отображение уравнения от 1 до 1 Страница 1 — Пожалуйста, прокрутите до конца, чтобы увидеть больше результатов
Уравнение Результат #1
Нажмите, чтобы увидеть более подробную информацию и рассчитать вес/моль >>
Oxidation-reduction reaction
| jpg» substance-weight=»18.01528 ± 0.00044″> H 2 O | + | Рекламное объявлениеДополнительная информация об уравнении H2 O + NO 2 + SO 2 → H 2 SO 4 + NOУсловия реакции h3O (вода) реагирует с NO2 (диоксидом азота) реагирует с SO2 (диоксидом серы) ?Температура: температура Объяснение: идеальные условия окружающей среды для реакции, такие как температура, давление, катализаторы и растворитель. Как могут происходить реакции с образованием h3SO4 (серная кислота) и NO (окись азота)?Явление после реакции h3O (вода) с NO2 (двуокись азота) после реакции с SO2 (двуокись серы)Нажмите, чтобы увидеть явление уравнения Какую другую важную информацию вы должны знать о реакцииУ нас нет дополнительной информации об этой химической реакции. Категории уравненияНажмите, чтобы увидеть более подробную информацию и рассчитать вес/моль >> Другие вопросы, связанные с химическими реакциями H2 O + NO 2 + SO 2 → H 2 SO 4 + NOВопросы, связанные с реагентом h3O (вода)и физические характеристики h3O (воды)? В каких химических реакциях используется h3O (вода) в качестве реагента? Вопросы, связанные с реагентом NO2 (двуокись азота)Каковы химические и физические характеристики NO2 (двуокиси азота)? В каких химических реакциях используется NO2 (двуокись азота) в качестве реагента? Вопросы, связанные с реагентом SO2 (диоксид серы)Каковы химические и физические характеристики SO2 (диоксида серы)? В каких химических реакциях используется SO2 (диоксид серы) в качестве реагента? Вопросы, связанные с продуктом h3SO4 (серная кислота)Каковы химические и физические характеристики h3SO4 (двуокиси серы)? Какие химические реакции сопровождаются образованием h3SO4 (серной кислоты)? Вопросы, связанные с продуктом NO (моноксид азота)Каковы химические и физические характеристики NO (двуокиси серы)? Каковы химические реакции, в результате которых NO (моноксид азота) является продуктом? Рекламное объявление 1 результатов найдено Дополнительная информация о веществах, которые используют уравнение Реакция h3O (nước) реакция с NO2 (nitơ диоксит) и SO2 (lưu hùynh диоксит) производят h3SO4 (аксит серный) , температурный режим Nhiệt độ. Реакция, в результате которой образуется вещество H3O (NướC) (вода)24HNO 3 + FECUS 2 → CU (№ 3 ) 2 + 10H 2 O + 2H 2 SO 4 + 18NO 2 SO 4 + 18NO. Fe (№ 3 ) 3 10FEO + 18H 2 SO 4 + 2KMNO 4 → 5FE 2 (SO 4 ) 3 + 18H 9H 01 2 O + 2MNSO 4 + K 2 SO 4 NAOH + C 6 H 5 BR → C 6 H 5 ONA + H 2 O + O + O + nabr 5 ONA + H 2 O + nabr 5 ONA + H 2 O + Nabr 5 ONA + H 2 o + nabr 5 Ona + H 2 7 который производит вещество NO2 (nitơ диоксит) (диоксид азота) 2Cu(NO 3 ) 2 → 2CuO + 4NO 2 + O 2 (6x-2y)HNO 3 x-y) (3xOy) H 2 O + 3x-2yNO 2 + xFe(NO 3 ) 3 24HNO 3 + FeCuS 2 → Cu(NO 3 ) 2 + 10H 2 O + 2H 2 SO 4 + 18NO 2 + Fe(NO 3 ) 3 Реакция, в результате которой образуется вещество SO2 (LưU Hùynh Dioxit) (диоксид серы)H 2 SO 4 + NA 2 SO 3 → H 2 O + NA 2 SO 4 2 2 1101101101101101011011010110101101011011011010110101101101110111010 2 11011011010110110110110110110110110110110110110110110110101101011010110101101 2 S + 3O 2 → 2H 2 O + 2SO 2 2SO 3 → O 2 + 2SO 2 Реакция с образованием вещества h3SO4 (axit sulfuric) (sulfuric acid) 24HNO 3 + FeCuS 2 → Cu(NO 3 ) 2 + 10H 2 O + 2H 2 SO 4 + 18NO 2 + Fe (№ 3 ) 3 2H 2 O + 2KMNO 4 + 5SO 2 → 2H 2 SO 4 + 2MNS 4 + K 4 + 2MNSO 4 + K 4 + 2MNSO 4 . |

 04.16
04.16

 Загрязнение окружающей среды. 2018 Январь; 232: 615-623. doi: 10.1016/j.envpol.2017.10.004. Epub 2017 9 октября.
Загрязнение окружающей среды. 2018.
PMID: 208
Загрязнение окружающей среды. 2018 Январь; 232: 615-623. doi: 10.1016/j.envpol.2017.10.004. Epub 2017 9 октября.
Загрязнение окружающей среды. 2018.
PMID: 208 J Phys Chem A. 1 апреля 2021 г .; 125 (12): 2642-2652. doi: 10.1021/acs.jpca.1c02006. Epub 2021 23 марта.
J Phys Chem A. 2021.
PMID: 33755485
J Phys Chem A. 1 апреля 2021 г .; 125 (12): 2642-2652. doi: 10.1021/acs.jpca.1c02006. Epub 2021 23 марта.
J Phys Chem A. 2021.
PMID: 33755485 Нг К.Х. и др.
Джей Хазард Матер. 2022, 5 февраля; 423 (часть A): 127061. doi: 10.1016/j.jhazmat.2021.127061. Epub 2021 30 августа.
Джей Хазард Матер. 2022.
PMID: 34788939
Обзор.
Нг К.Х. и др.
Джей Хазард Матер. 2022, 5 февраля; 423 (часть A): 127061. doi: 10.1016/j.jhazmat.2021.127061. Epub 2021 30 августа.
Джей Хазард Матер. 2022.
PMID: 34788939
Обзор.

 Катализаторы — это вещества, которые ускоряют темп (скорость) химической реакции, не потребляясь и не становясь частью конечного продукта.
Катализаторы не влияют на равновесные ситуации.
Катализаторы — это вещества, которые ускоряют темп (скорость) химической реакции, не потребляясь и не становясь частью конечного продукта.
Катализаторы не влияют на равновесные ситуации.
