что, как сбалансировать и часто задаваемые вопросы —
By Дипали Арора
H2SO4 + Ca (OH)2 это реакция между сильной кислотой и сильным основанием. Давайте обсудим некоторые важные факты об этой реакции в этой статье.
H2SO4 является королем кислот и также широко известен как масло купороса. Он используется по-разному, например, для очистки других металлов и производства различных химикатов, красителей и т. Д. Ca (OH)2 образуется при смешивании CaO (негашеной извести) с водой. Он белый и в кристаллической форме.
Котлеты из фарша с …
Please enable JavaScript
Котлеты из фарша с грибами, удивительные вкусные котлеты!😋
С помощью полностью сбалансированного химического уравнения мы узнаем различные аспекты этой реакции, такие как энтальпия реакции, тип реакции и т. д.
Что является произведением H
2SO4 и Са (ОН)2Случай4 (сульфат кальция) и H2O (вода) — это два продукта, которые образуются, когда H2SO4 и Са (ОН)2 реагируют друг на друга.
Са (ОН)2 + H2SO4 → CaSO4 + 2ч2O
Какой тип реакции Н
2SO4 + Ca (OH)2H2SO4 + Ca (OH)2 — это реакция нейтрализации в котором сильная кислота реагирует с сильным основанием с образованием соответствующей труднорастворимой соли.
Как сбалансировать H
2SO4 +Са(ОН)2- Напишите полное химическое уравнение скелета.
- Напишите названия всех элементов, входящих в химическое уравнение.
| Elements | Количество атомов на стороне реагента | Количество атомов на стороне продукта |
|---|---|---|
| Ca | 1 | 1 |
| O | 6 | 5 |
| H | 4 | 2 |
| S | 1 | 1 |
- Уравняйте количество атомов как на стороне реагента, так и на стороне продукта.
 .
.
H
2SO4 + Ca (OH)2 титрованиеТитрование H2SO4 с Са (ОН)2 в присутствии фенолфталеина является примером кислотно-щелочного титрования.
Используемый аппарат- Градуированный цилиндр
- бюретка
- фенолфталеин
- Мерная колба (помогает хранить раствор)
- Подставка для колец
- Маленькая воронка
- Колба Эрленмейера (поле титрования)
Индикаторные
Индикатор, используемый в H2SO4 + CaSO4 Реакцией является фенолфталеин, потому что он легко меняет цвет при определенном рН.
| Индикаторные | Цвет в нормальном состоянии | Цвет в базе | Цвет в кислотах |
|---|---|---|---|
| фенолфталеин | Pink | розовый | прозрачный |
Процедура
- Са (ОН)2 неизвестной молярности добавляют в колбу Эрленмейера.

- Следующим шагом будет добавление 2 капель фенолфталеина.
- Изменение цвета должно быть записано одновременно.
- 3-молярная серная кислота разбавляется до низкой концентрации.
- Бюретка используется для добавления нескольких капель к анализируемому веществу.
- Раствор постоянно перемешивают.
- Когда цвет начнет появляться, замедлите скорость капель, чтобы получить точный результат.
- Когда цвет станет светло-розовым, запишите количество титрованный раствор используется для расчета концентрации вашего аналита
- Для каждой другой концентрации серной кислоты повторите те же шаги.
Результаты титрования H2SO4 и Са (ОН)2 ненадежны, так как концентрации не остаются стабильными, поскольку внешние факторы вызывают нестабильность в испытаниях. Образующийся цвет не зависит от принятого раствора; скорее, это зависит от взятого индикатора, следовательно, образующийся цвет розовый.
Образующийся цвет не зависит от принятого раствора; скорее, это зависит от взятого индикатора, следовательно, образующийся цвет розовый.
H
2SO4 + Ca (OH)2 чистое ионное уравнениеИонное уравнение реакции имеет вид,
Ca2+ + 2ОН– + 2H+ SO42- →Случай4(с) +2H2O(L)
Чистое ионное уравнение выводится с использованием следующих шагов:
- Напишите полное сбалансированное уравнение.
- Са (ОН)2 + H2SO4 → CaSO4 + 2ч2O
- Добавьте вместе с ними физические состояния соединения.
- Са (ОН)2(вод) + H2SO4(водн.) → CaSO4(водн.) + 2H2О (водн.)
- Разбейте все соединения, растворимые в воде, на соответствующие ионы.

- Ca2+ + 2ОН– + 2H+ SO42- →Случай4(с) +2H2O(L)
- Вычеркните ионы, сходные как со стороны реагента, так и со стороны продукта.
- Са (ОН)2(вод) + H2SO4(водн.) → CaSO4(водн.) + 2H2О (водн.)
- Уравнение слева представляет собой результирующее ионное уравнение.
- Ca2+ + 2ОН– + 2H+ SO42- →CaSO4(с) +2H2O(L)
H
2SO4 + Ca (OH)2 сопряженные пары- H2SO4 является сильной кислотой и ее сопряженным основанием является HSO4–
- Пара сопряженных кислот Ca (OH)2 это Са (ОН)+.

H
2SO4 и Са (ОН)2 межмолекулярные силы- Существует три типа межмолекулярных сил между молекулами H2SO4: дисперсионные силы Ван-дер-Ваальса, диполь-дипольные взаимодействия и водородная связь .
- Са (ОН)2 представляет собой ионное соединение с сильными силами притяжения между его ионами.
H
2SO4 + Ca (OH)2 энтальпия реакцииРеакция энтальпия из H2SO4 + Ca (OH)2 составляет -23.61 кДж.
Н
2SO4 + Ca (OH)2 буферный растворРеакция между H2SO4 и Са (ОН)2 не могу сделать буферный раствор потому что это реакция нейтрализации и полностью ионизируется.
Н
2SO4 + Ca (OH)2 полная реакцияH2SO4 и Са (ОН)2 являются полными реакциями, потому что реагенты взаимно обмениваются своими ионами с образованием двух продуктов.
Н
2SO4 + Ca (OH)2 экзотермическая или эндотермическая реакцияРеакция между H2SO4 и Са (ОН)2 очень экзотермический потому что энтальпия реакции очень высока; следовательно, выделяется много тепла.
Н
2SO4 + Ca (OH)2 окислительно-восстановительная реакцияРеакция между H2SO4 и Са (ОН)2 не является окислительно-восстановительной реакцией, поскольку степени окисления элементов не изменяются, что объясняется ниже..Степени окисления элементов
Н
2SO4 + Ca (OH)2 реакция осажденияЭто не реакция осадка, потому что осадок не образуется, когда H2SO4 соединяется с Ca (OH)2. Вместо этого он образует растворимую соль.
Н
2SO4 + Ca (OH)2 обратимая или необратимая реакцияРеакция между H2SO4 и Са (ОН)2 является обратимым, поскольку эта реакция имеет тенденцию двигаться как в прямом, так и в обратном направлении.
Н
2SO4 + Ca (OH)2 реакция смещенияКогда Н2SO4 соединяется с Ca (OH)2, двойное смещение происходит потому, что происходит взаимный обмен ионами. Ca соединяется с SO42- ионы и H+ сочетается с ОН– ионы с образованием воды.
Заключение
Са (ОН)2 и Н2SO4 является кислотно-щелочной реакцией; следовательно, образующиеся продукты представляют собой соль и воду. Соль, CaSO4, вызывает постоянную жесткость воды и используется в качестве иссушать. Н2O имеет pH 7 и водородные связи между его молекулами.
Ответов пока нет | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
Посмотреть всех экспертов из раздела Учеба и наука | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
What, How to Balance & FAQs —
By Deepali Arora
H 2 SO 4 + Ca(OH) 2 представляет собой реакцию между сильной кислотой и сильным основанием. Давайте обсудим некоторые важные факты об этой реакции в этой статье.
H 2 SO 4 является королем кислот и также широко известен как купоросное масло. Он используется по-разному, например, для очистки других металлов и производства различных химикатов, красителей и т. д. Ca(OH) 2 получается при смешивании CaO (негашеной извести) с водой. Он белый и в кристаллической форме.
д. Ca(OH) 2 получается при смешивании CaO (негашеной извести) с водой. Он белый и в кристаллической форме.
Конденсатор и емкость | Лучшие 2…
Пожалуйста, включите JavaScript
Конденсатор и емкость | Best 2022
С помощью полностью сбалансированного химического уравнения мы узнаем различные аспекты этой реакции, такие как энтальпия реакции, тип реакции и т. д. ) 2
CaSO 4 (сульфат кальция) и H 2 O (вода) — два продукта, которые образуются при взаимодействии H 2 SO 4 и Ca(OH) 2 .
CA (OH) 2 + H 2 SO 4 → CASO 4 + 2H 2 O
Какой тип реакции H
2 SO 4 + CA (CA (CA ( OH) 2 H 2 SO 4 + Ca(OH) 2 представляет собой реакцию нейтрализации, при которой сильная кислота реагирует с сильным основанием с образованием соответствующей труднорастворимой соли.
Как сбалансировать H
2 SO 4 +Ca(OH) 2- Напишите полное химическое уравнение скелета.
- Напишите названия всех элементов, входящих в химическое уравнение.
| Элементы | Number of atoms on reactant side | Number of atoms on product side |
|---|---|---|
| Ca | 1 | 1 |
| O | 6 | 5 |
| H | 4 | 2 |
| S | 1 | 1 |
- число атомов на стороне реакции
H
2 SO 4 + CA (OH) 2 Титрование Титрование H 2 SO 4 с CA (OH) 2 В присутствии фенолфталеина является примером кислоты. -основное титрование.
-основное титрование.
- градуированный цилиндр
- Burette
- Phenolphthalein
- .0020
- Volumetric Flask (helps in storing the solution)
- Ring stand
- Small funnel
- Erlenmeyer Flask (Titration field)
Indicator
Индикатором, используемым в реакции H 2 SO 4 + CaSO 4 , является фенолфталеин, поскольку он легко меняет цвет при определенном значении pH.
| Indicator | Colour in normal condition | Colour in bases | Colour in acids |
|---|---|---|---|
| Phenolphthalein | Pink | pink | transparent |
Процедура
- Ca(OH) 2 неизвестной молярности добавляют в колбу Эрленмейера.

- Следующим шагом будет добавление 2 капель фенолфталеина.
- Изменение цвета должно быть записано одновременно.
- 3 Молярная серная кислота разбавлена до низкой концентрации.
- Бюретка используется для добавления нескольких капель к анализируемому веществу.
- Раствор постоянно перемешивается.
- Когда цвет начнет проявляться, уменьшите скорость капель, чтобы получить точный результат.
- Когда цвет станет светло-розовым, запишите количество титранта, используемого для расчета концентрации анализируемого вещества.
- Для каждой другой концентрации серной кислоты повторите те же шаги.
Результаты титрования H 2 SO 4 и Ca(OH) 4 и Ca(OH) 2 являются причиной нестабильности внешних факторов, так как концентрации не остаются нестабильными. Образующийся цвет не зависит от принятого раствора; скорее, это зависит от взятого индикатора, следовательно, образующийся цвет розовый.
Образующийся цвет не зависит от принятого раствора; скорее, это зависит от взятого индикатора, следовательно, образующийся цвет розовый.
H
2 SO 4 + CA (OH) 2 Чистое ионное уравнениеИонное уравнение для реакции составляет ,
CA 2+ + 2OH — + 2H + 2H + 2H + 2H . + SO 4 2- → CASO 4 (S) +2 H 2 O (L)
Уравнение чистого ионического
2020202020202020202020202. 20202020202020202020202. 2020202. (S) H 2 4 (S). все соединения, растворимые в воде, на соответствующие ионы.
все соединения, растворимые в воде, на соответствующие ионы.
- Вычеркните ионы, сходные как по реагенту, так и по продукту.
- Ca(OH) 2 (aq) + H 2 SO 4 (aq) → CaSO 4 (aq) + 2H 2 O(aq)
- The уравнение слева представляет собой результирующее ионное уравнение.
- CA 2+ + 2OH — + 2H + SO 4 2- → CASO 4 (S) +2 H → CASO 4 (S) +2 H .

H
2 SO 4 + Ca(OH) 2 conjugate pairs- H 2 SO 4 is a strong acid and its conjugate base is HSO 4 –
- Пара сопряженных кислот Ca(OH) 2 представляет собой Ca(OH) + .
H
2 SO 4 и CA (OH) 2 Межмолекулярные силы- Существуют три типа межмолекулярных сил между молекулами H 2 SO 4 : Van Der Disersion Dispersionion itsionion itsionion itsionion haalsion haalsion desersion it waals it waals it waals desersion wals desersion waals waals waals waals waals waals waals waals waals waals waals waals силы, диполь-дипольные взаимодействия и водородные связи.
- Ca(OH) 2 представляет собой ионное соединение с сильными силами притяжения между его ионами.

H
2 SO 4 + CA (OH) 2 Энтальпия реакцииРеакционная энтальпия H 2 SO 4 + CA (OH) 2 —23,61 KJ.
Is H
2 SO 4 + Ca(OH) 2 буферный растворраствор, потому что это реакция нейтрализации и полностью ионизируется.
Is H
2 SO 4 + Ca(OH) 2 полная реакцияH 2 SO 4 2900 взаимно с образованием двух продуктов.
IS H
2 SO 4 + CA (OH) 2 Экзотермическая или эндотермическая реакцияРеакция между H 2 SO 4 и CA (OH) 2 — очень экзотермическая потому что энтальпия реакции очень высока; следовательно, выделяется много тепла.
Is H
2 SO 4 + Ca(OH) 2 а окислительно-восстановительная реакция реакция, потому что нет изменения степени окисления элементов, что объясняется ниже . Степени окисления элементов
Степени окисления элементов Is H
2 SO 4 + Ca(OH) 2 реакция осажденияЭто не реакция осаждения, поскольку осадок не образуется, когда H 2 SO 4 соединяется с Ca(OH) 2 . Вместо этого он образует растворимую соль.
IS H
2 SO 4 + CA (OH) 2 Обратимая или необратимая реакцияРеакция между H 2 SO 4 и CA (OH) 2 Обратима, потому что это 4 и CA (OH) 2 , потому что это реакция имеет тенденцию двигаться как в прямом, так и в обратном направлении.
Is H
2 SO 4 + Ca(OH) 2 реакция замещения Когда H 2 SO 4 соединяется с Ca(OH) 2 , происходит двойное смещение, поскольку происходит взаимный обмен ионами. Ca соединяется с ионами SO 4 2-, а H + соединяется с ионами OH – с образованием воды.
Заключение
Ca(OH) 2 и H 2 SO 4 является кислотно-щелочной реакцией; следовательно, образующиеся продукты представляют собой соль и воду. Соль CaSO 4 вызывает постоянную жесткость воды и используется в качестве осушителя. Н 2 O имеет pH 7 и водородные связи между его молекулами.
6.4: Классификация химических реакций (кислоты и основания) (задачи)
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 106786
ЗАДАЧА \(\PageIndex{1}\)
Заполните и сбалансируйте следующие кислотно-основные уравнения:
- Газ HCl реагирует с твердым Ca(OH) 2 ( s ).

- Раствор Sr(OH) 2 добавляют к раствору HNO 3 .
- Ответить на
\(\ce{2HCl}(g)+\ce{Ca(OH)2}(s)\rightarrow \ce{CaCl2}(s)+\ce{2h3O}(l)\)
- Ответ б
\(\ce{Sr(OH)2}(водн.)+\ce{2HNO3}(водн.)\rightarrow \ce{Sr(NO3)2}(водн.)+\ce{2h3O}(l)\)
ЗАДАЧА \(\PageIndex{2}\)
Дополните и сбалансируйте следующие кислотно-основные уравнения:
- Раствор HClO 4 добавляют к раствору LiOH.
- Водный H 2 SO 4 реагирует с NaOH.
- Ba(OH) 2 реагирует с газообразным HF.
- Ответ
\(\ce{HClO4}(водн.)+\ce{LiOH}(водн.)\rightarrow \ce{LiClO4}(водн.)+\ce{h3O}(л)\)
- Ответ б
\(\ce{h3SO4}(водн.
 )+\ce{2NaOH}(водн.)\rightarrow \ce{Na2SO4}(водн.)+\ce{2h3O}(л)\)
)+\ce{2NaOH}(водн.)\rightarrow \ce{Na2SO4}(водн.)+\ce{2h3O}(л)\)
- Ответ c
\(\ce{2HF}(водн.)+\ce{Ba(OH)2}(водн.)\rightarrow \ce{BaF2}(водн.)+\ce{2h3O}(l)\)
- Нажмите здесь, чтобы посмотреть видео о решении
-
(Это видео имеет неправильное название, но является правильным решением проблемы )
ЗАДАЧА \(\PageIndex{3}\)
Дополните и сбалансируйте уравнения для следующих реакций кислотно-щелочной нейтрализации. Если в качестве растворителя используется вода, запишите реагенты и продукты как водные ионы. В некоторых случаях может быть более одного правильного ответа, в зависимости от количества используемых реагентов. 92+}(водн.)+\ce{2ClO4-}(водн. )+\ce{2h3O}(л)\)
)+\ce{2h3O}(л)\)
- Ответ б
\(\ce{SO3}(g)+\ce{2h3O}(l)\rightarrow \ce{h4O+}(водн.)+\ce{HSO4-}(водн.)\), (раствор H 2 СО 4 )
- Ответ c
\(\ce{SrO}(s)+\ce{h3SO4}(l)\rightarrow \ce{SrSO4}(s)+\ce{h3O}\)
ЗАДАЧА \(\PageIndex{4}\)
Дополните и сбалансируйте уравнения следующих реакций, каждая из которых может быть использована для удаления сероводорода из природного газа:
- \(\ce{Ca(OH)2}(s)+\ce{h3S}(g) \rightarrow\)
- \(\ce{Na2CO3}(водн.)+\ce{h3S}(г)\стрелка вправо \)
- Ответить
\(\ce{Ca(OH)2}(s)+\ce{h3S}(g)\rightarrow \ce{CaS}(s)+\ce{2h3O}(l)\)
- Ответить
\(\ce{Na2CO3}(водн.)+\ce{h3S}(г)\rightarrow \ce{Na2S}(водн.
 )+\ce{CO2}(г)+\ce{h3O}(л)\)
)+\ce{CO2}(г)+\ce{h3O}(л)\)
ПРОБЛЕМА \(\PageIndex{5}\)
Цикламат кальция Ca(C 6 H 11 NHSO 3 ) 2 — искусственный подсластитель, используемый во многих странах мира, но запрещенный в США. Его можно очистить в промышленных масштабах путем превращения в соль бария путем реакции кислоты C 6 H 11 NHSO 3 H с карбонатом бария, обработкой серной кислотой (сульфат бария очень нерастворим) и последующей нейтрализацией с помощью гидроксид кальция. Напишите уравнения этих реакций.
- Ответить
\(\ce{2C6h21NHSO3H}+\ce{BaCO3}\rightarrow \ce{Ba(C6h21NHSO3)2}+\ce{h3CO3}\)
\(\ce{Ba(C6h21NHSO3)2}+\ce{h3SO4}\rightarrow \ce{BaSO4}+\ce{2C6h21NHSO3H}\)
\(\ce{2C6h21NHSO3H}+\ce{Ca(OH)2}\rightarrow \ce{Ca(C6h21NHSO3)2}+\ce{2h3O}\)
Авторы
Пол Флауэрс (Университет Северной Каролины, Пембрук), Клаус Теопольд (Университет Делавэра) и Ричард Лэнгли (Государственный университет Стивена Ф.


 .
.



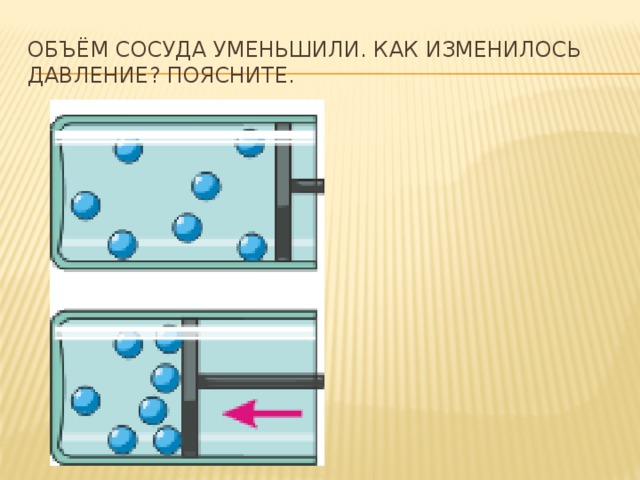
 При охлаждении его давление снизилось на 3*10(в 3ст)Па. На сколько уменьшилась внутренняя энергия газа? Ответ
При охлаждении его давление снизилось на 3*10(в 3ст)Па. На сколько уменьшилась внутренняя энергия газа? Ответ



 )+\ce{2NaOH}(водн.)\rightarrow \ce{Na2SO4}(водн.)+\ce{2h3O}(л)\)
)+\ce{2NaOH}(водн.)\rightarrow \ce{Na2SO4}(водн.)+\ce{2h3O}(л)\) )+\ce{CO2}(г)+\ce{h3O}(л)\)
)+\ce{CO2}(г)+\ce{h3O}(л)\)
 В итоге, занятие мне очень понравилось! Спокойное объяснение материала, дружелюбный настрой, подбадривание дистанционного ученика даже в самых непростых ситуациях — вот далеко не полный перечень качеств Владимира Александровича как дистанционного педагога. Мне следует учиться у такого замечательного репетитора!
В итоге, занятие мне очень понравилось! Спокойное объяснение материала, дружелюбный настрой, подбадривание дистанционного ученика даже в самых непростых ситуациях — вот далеко не полный перечень качеств Владимира Александровича как дистанционного педагога. Мне следует учиться у такого замечательного репетитора! Моя дочь существенно подняла свой уровень знаний по математике и начала демонстрировать хорошие оценки. Мы очень благодарны Надежде Васильевне за помощь в этом учебном году, надеемся на продолжение отношений осенью.
Моя дочь существенно подняла свой уровень знаний по математике и начала демонстрировать хорошие оценки. Мы очень благодарны Надежде Васильевне за помощь в этом учебном году, надеемся на продолжение отношений осенью.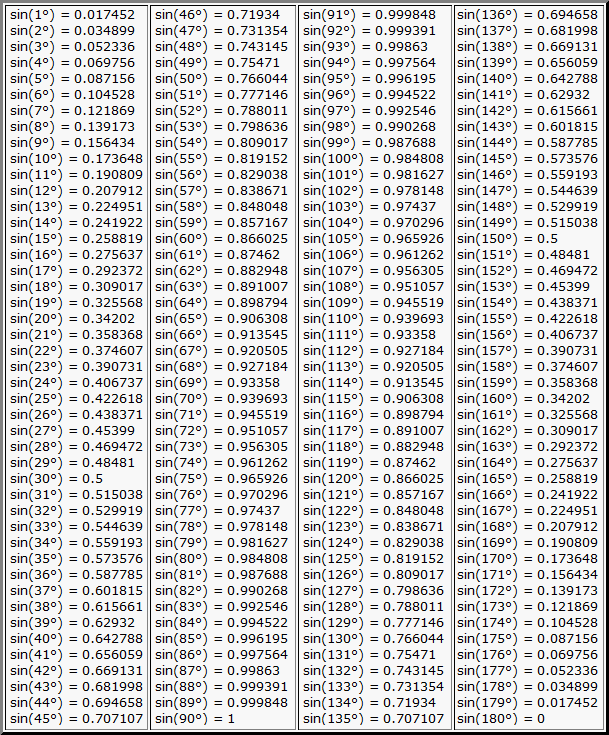 RU
RU
 Детально исследуются возможности и условия возникновения нелинейных резонансных колебаний. Анализируются периодические и почти-периодические режимы резонансных колебаний и их устойчивость.
Детально исследуются возможности и условия возникновения нелинейных резонансных колебаний. Анализируются периодические и почти-периодические режимы резонансных колебаний и их устойчивость.
 Собственные колебания твердого тела
Собственные колебания твердого тела Пространственная устойчивость колебаний твердого тела при почти периодических внешних силах
Пространственная устойчивость колебаний твердого тела при почти периодических внешних силах Интегральные кривые и формы пространственных движений тела
Интегральные кривые и формы пространственных движений тела ЭКСПЕРИМЕНТАЛЬНОЕ ИССЛЕДОВАНИЕ НЕЛИНЕЙНЫХ ПРОСТРАНСТВЕННЫХ КОЛЕБАНИЙ ТВЕРДЫХ ТЕЛ
ЭКСПЕРИМЕНТАЛЬНОЕ ИССЛЕДОВАНИЕ НЕЛИНЕЙНЫХ ПРОСТРАНСТВЕННЫХ КОЛЕБАНИЙ ТВЕРДЫХ ТЕЛ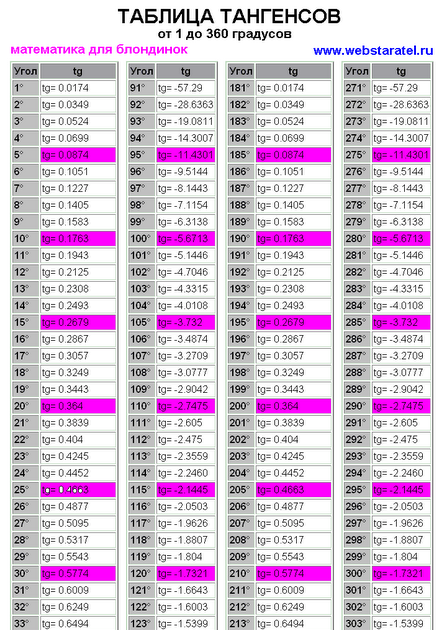 УСТОЙЧИВОСТЬ ДВИЖЕНИЯ ГИРОСКОПИЧЕСКИХ СИСТЕМ В УСЛОВИЯХ РЕЗОНАНСОВ
УСТОЙЧИВОСТЬ ДВИЖЕНИЯ ГИРОСКОПИЧЕСКИХ СИСТЕМ В УСЛОВИЯХ РЕЗОНАНСОВ
 )
) )
) )
) )
) )
) )
)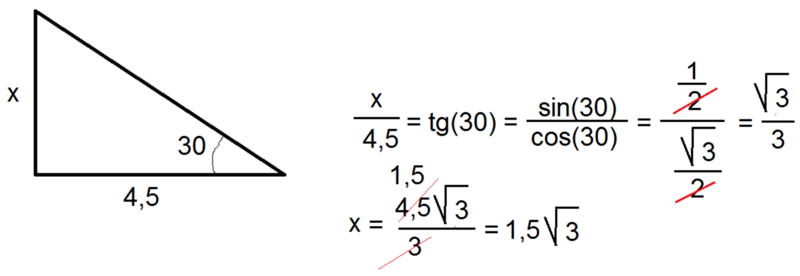 )
) )
) Рассказываем, как получилось создать такое оружие и чего от него можно ждать. Если кратко, дальнобойность украинского оружия еще больше вырастет — фактически в два раза.
Рассказываем, как получилось создать такое оружие и чего от него можно ждать. Если кратко, дальнобойность украинского оружия еще больше вырастет — фактически в два раза.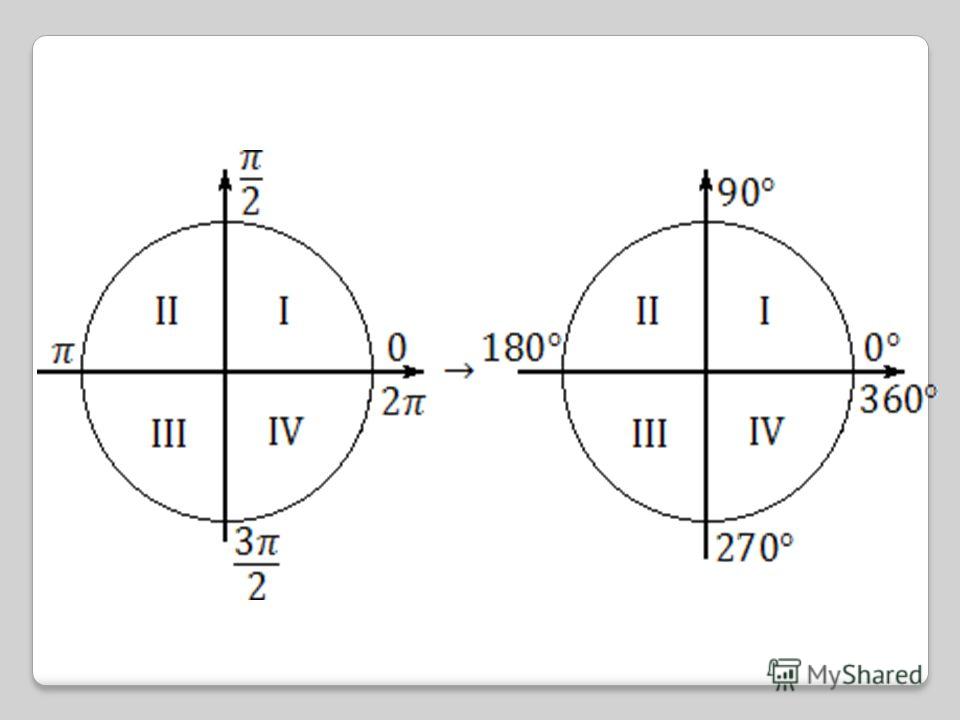
 Даже самые первые бомбы имели круговое вероятное отклонение или КВО около пяти метров (то есть половина сброшенных GBU-39 укладывается в круг пятиметрового радиуса), более совершенные версии имели КВО в один метр.
Даже самые первые бомбы имели круговое вероятное отклонение или КВО около пяти метров (то есть половина сброшенных GBU-39 укладывается в круг пятиметрового радиуса), более совершенные версии имели КВО в один метр.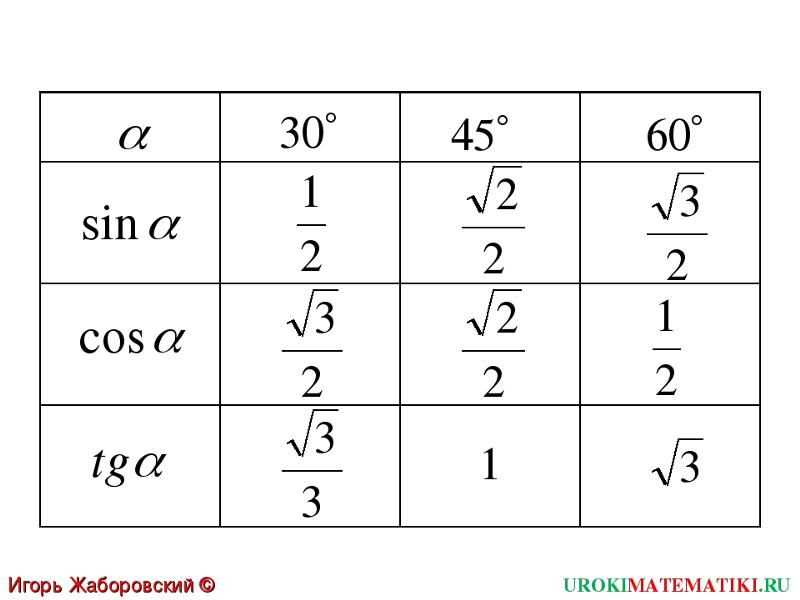
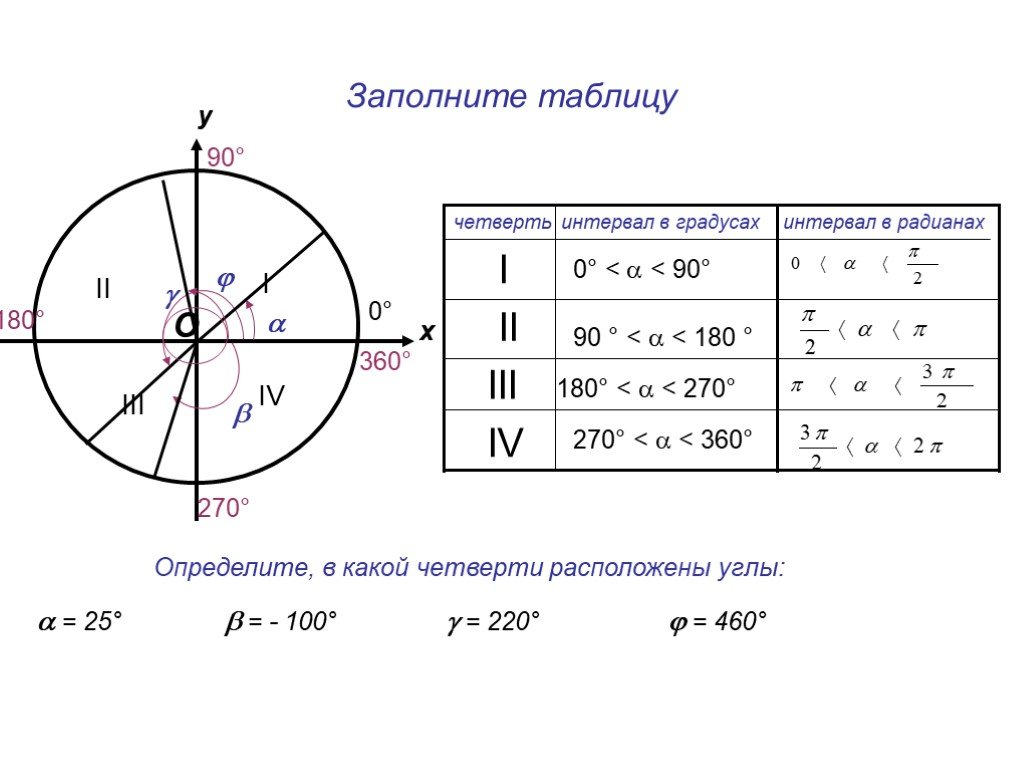 Дальность полета боеприпаса оказалась огромной: сначала 100 километров, потом 130 и наконец 150. При этом он может в случае перелета вернуться назад на огромное расстояние в 70 километров благодаря исключительной способности разворачиваться и планировать.
Дальность полета боеприпаса оказалась огромной: сначала 100 километров, потом 130 и наконец 150. При этом он может в случае перелета вернуться назад на огромное расстояние в 70 километров благодаря исключительной способности разворачиваться и планировать.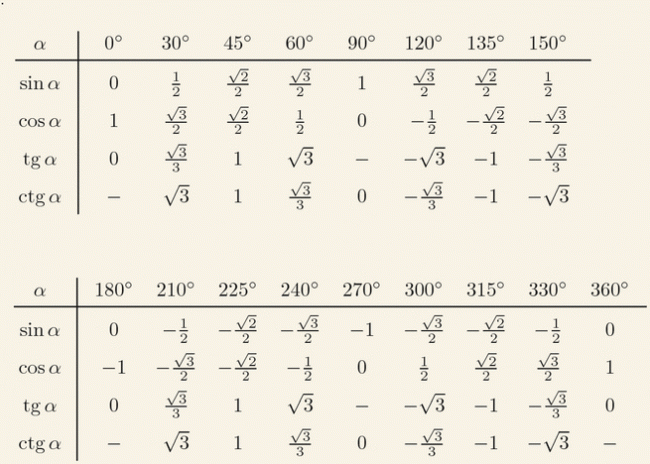
 А предполагаемая дешевизна бомб, вероятно, позволит поставлять их более-менее массово (что, впрочем, необязательно, так как производство таких боеприпасов, как бы просто оно ни было, только разворачивается).
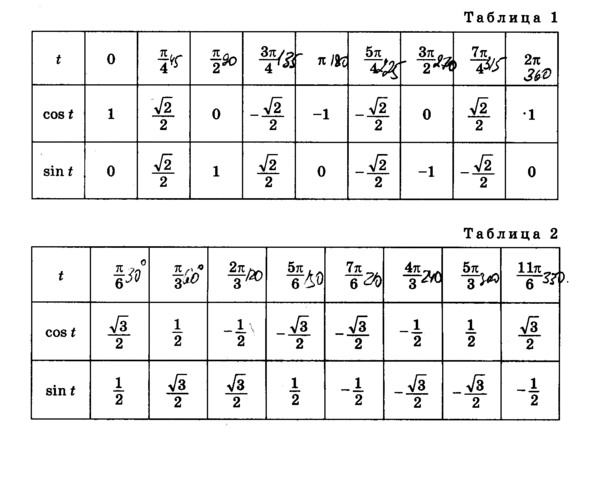
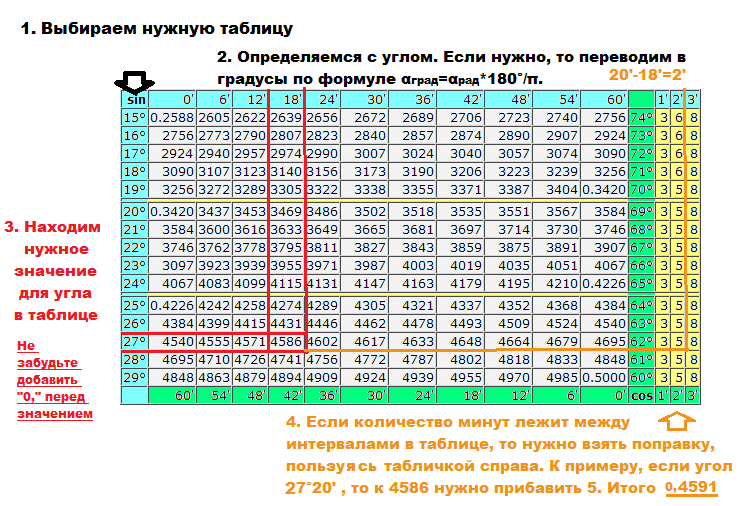
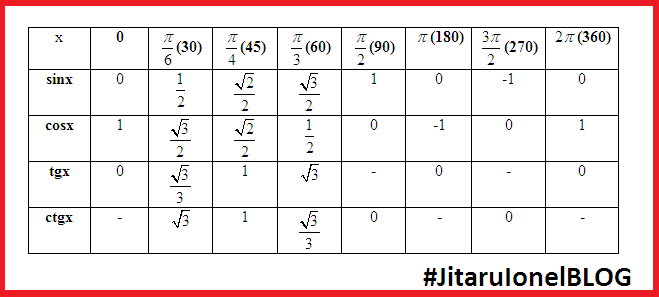
А предполагаемая дешевизна бомб, вероятно, позволит поставлять их более-менее массово (что, впрочем, необязательно, так как производство таких боеприпасов, как бы просто оно ни было, только разворачивается).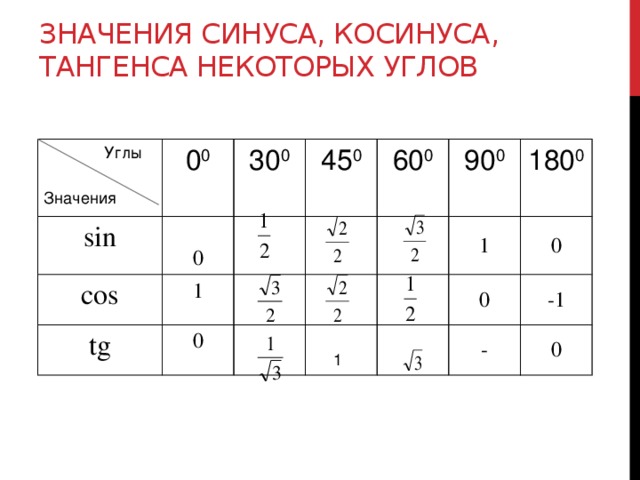 Тангенс 360 градусов также может быть выражен с помощью эквивалента данного угла (360 градусов) в радианах (6,28318 . . .)
Тангенс 360 градусов также может быть выражен с помощью эквивалента данного угла (360 градусов) в радианах (6,28318 . . .)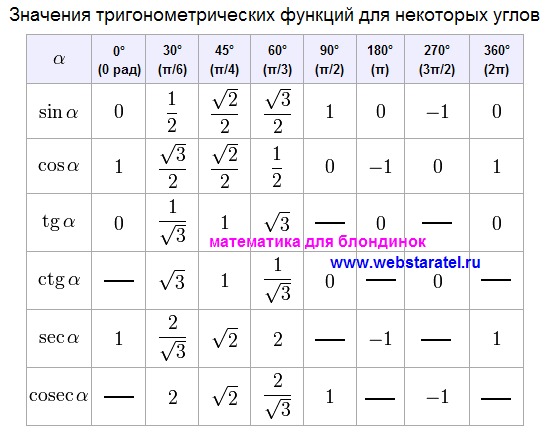
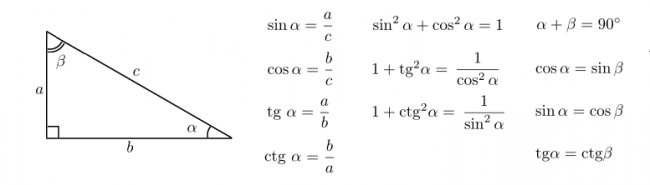 Найдите значение 4 тангенса (360°)/6 тангенса (45°).
Найдите значение 4 тангенса (360°)/6 тангенса (45°).  Наслаждайтесь решением реальных математических задач на живых уроках и станьте экспертом во всем.
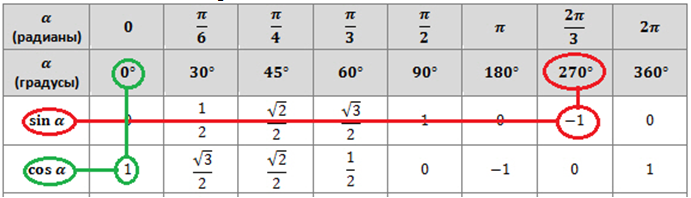
Наслаждайтесь решением реальных математических задач на живых уроках и станьте экспертом во всем. Значение tan 360° равно координате y (0), деленной на координату x (1). ∴ tan 360° = 0
Значение tan 360° равно координате y (0), деленной на координату x (1). ∴ tan 360° = 0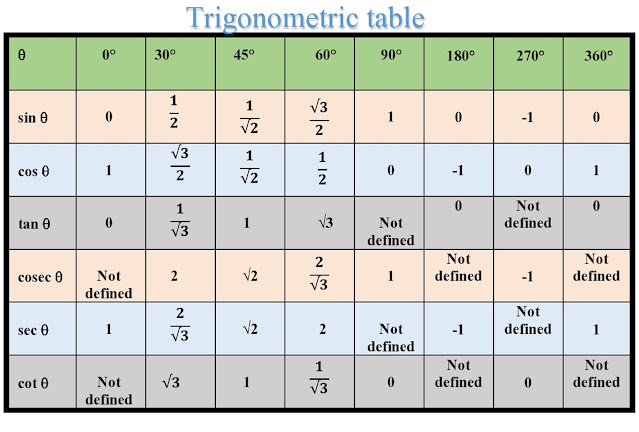
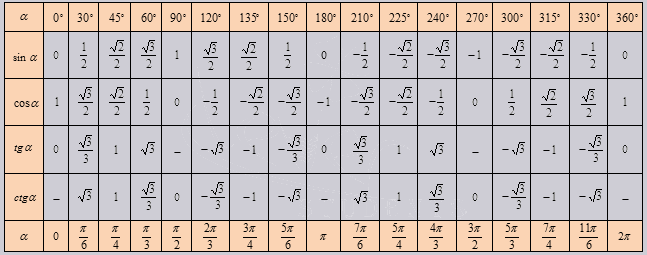 Это может быть много, чтобы взять все сразу, но на самом деле это очень просто. У вас есть свой набор правил, SOHCAHTOA, поэтому, если вы хотите найти синус, косинус или тангенс угла, вы можете это сделать!
Это может быть много, чтобы взять все сразу, но на самом деле это очень просто. У вас есть свой набор правил, SOHCAHTOA, поэтому, если вы хотите найти синус, косинус или тангенс угла, вы можете это сделать!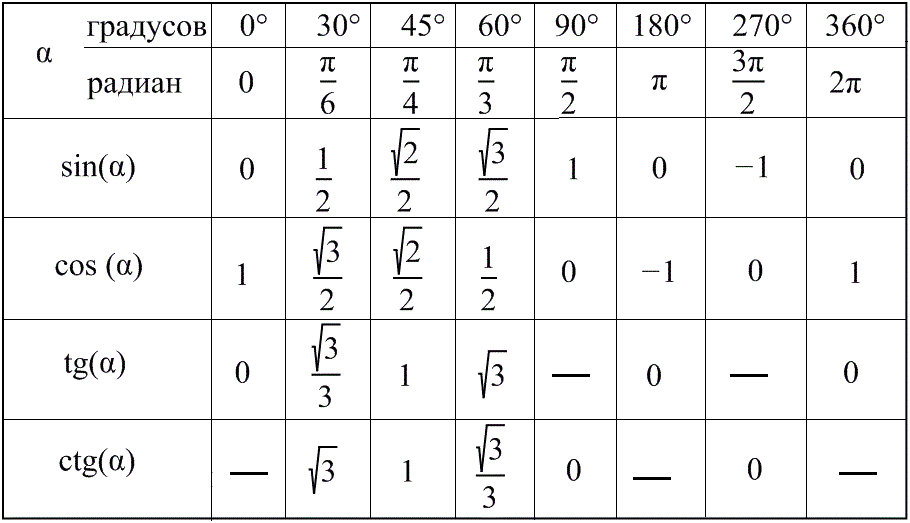 Для игр нам нужно беспокоиться только об ATan прямо сейчас, но мы доберемся до этого. Чтобы держать это в уме, помните следующее, относящееся к треугольнику выше:
Для игр нам нужно беспокоиться только об ATan прямо сейчас, но мы доберемся до этого. Чтобы держать это в уме, помните следующее, относящееся к треугольнику выше: Но как? Все, что у нас есть, это x и y, которые являются различиями в позициях x и y нашей мыши по сравнению с объектом. НО мы можем использовать ATan для получения угла A.
Но как? Все, что у нас есть, это x и y, которые являются различиями в позициях x и y нашей мыши по сравнению с объектом. НО мы можем использовать ATan для получения угла A.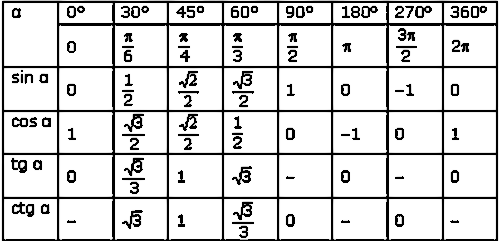 Проблема в том, что MMF2 принимает параметр как параметр y и параметр x. Это означает, что вам нужно ввести 2 отдельных значения: числитель дроби и знаменатель. Это делается для того, чтобы он мог определить угол, поскольку тангенс не может указывать 360 градусов, поэтому MMF2 использует логику положительных и отрицательных значений в направлении, чтобы определить, какой угол будет. Если вы изучите единичный круг, вы поймете, но на данный момент вам это не нужно, и он не включен в этот урок. Подводя итог, угол A = ATan2(YMouse-Y(«Объект»), XMouse-X(«Объект»)) Обычно он равен y/x, но, как мы сказали, нам нужны числитель и знаменатель как 2 отдельных параметра.
Проблема в том, что MMF2 принимает параметр как параметр y и параметр x. Это означает, что вам нужно ввести 2 отдельных значения: числитель дроби и знаменатель. Это делается для того, чтобы он мог определить угол, поскольку тангенс не может указывать 360 градусов, поэтому MMF2 использует логику положительных и отрицательных значений в направлении, чтобы определить, какой угол будет. Если вы изучите единичный круг, вы поймете, но на данный момент вам это не нужно, и он не включен в этот урок. Подводя итог, угол A = ATan2(YMouse-Y(«Объект»), XMouse-X(«Объект»)) Обычно он равен y/x, но, как мы сказали, нам нужны числитель и знаменатель как 2 отдельных параметра.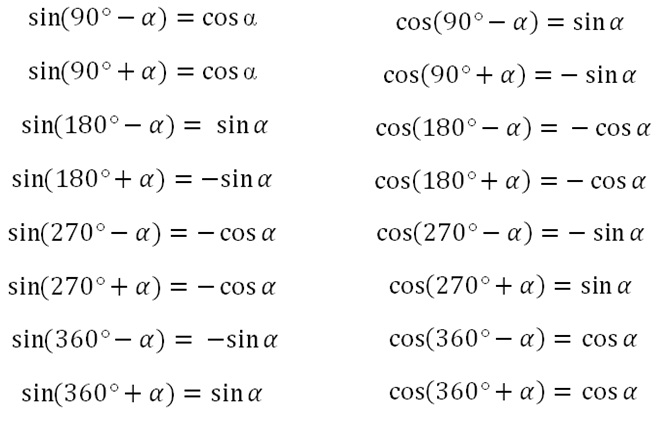 Если мы забудем указать это в нашем выражении, предполагается, что оно равно 1, и тогда x и y будут меньше или равны 1, и наш объект никуда не денется.
Если мы забудем указать это в нашем выражении, предполагается, что оно равно 1, и тогда x и y будут меньше или равны 1, и наш объект никуда не денется.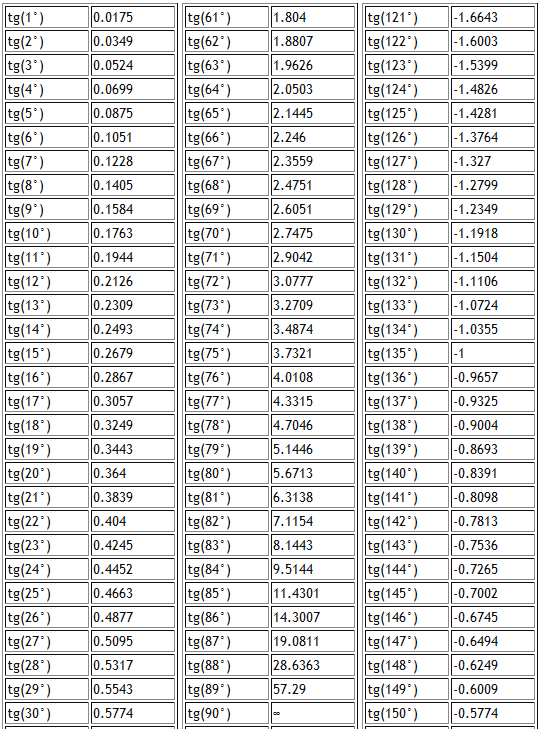


 {3}}{3}.\)
{3}}{3}.\)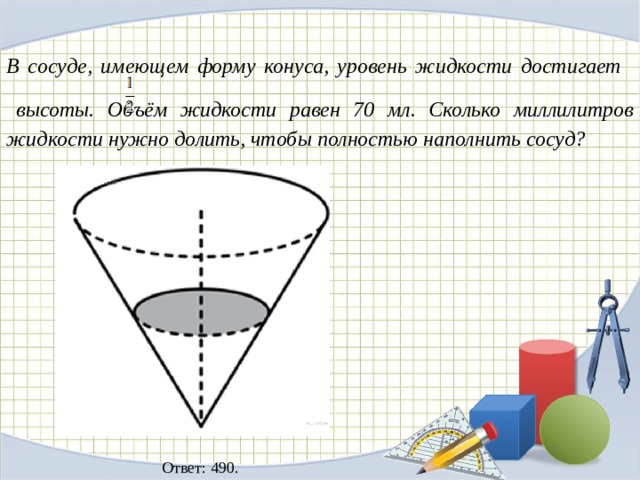
 Если вы уже загрузили файл, имя может быть написано с ошибкой или файл находится в другой папке.
Если вы уже загрузили файл, имя может быть написано с ошибкой или файл находится в другой папке. Это сообщает серверу, какой ресурс он должен использовать попытка запроса.
Это сообщает серверу, какой ресурс он должен использовать попытка запроса.
 )
)
 htaccess для большинства людей — через диспетчер файлов в cPanel.
htaccess для большинства людей — через диспетчер файлов в cPanel. htaccess и выберите Редактировать код в меню. Кроме того, вы можете щелкнуть значок файла .htaccess, а затем Редактор кода Значок вверху страницы.
htaccess и выберите Редактировать код в меню. Кроме того, вы можете щелкнуть значок файла .htaccess, а затем Редактор кода Значок вверху страницы. ) жидкость) (qt)столовая ложка (Can) (столовая ложка)столовая ложка (Imp) (столовая ложка)столовая ложка (США) (столовая ложка)чайная ложка (Can) (tsp)чайная ложка (Imp) (tsp)чайная ложка (U.S.) (tsp)
) жидкость) (qt)столовая ложка (Can) (столовая ложка)столовая ложка (Imp) (столовая ложка)столовая ложка (США) (столовая ложка)чайная ложка (Can) (tsp)чайная ложка (Imp) (tsp)чайная ложка (U.S.) (tsp) S.) (tbsp)чайная ложка (Can) (tsp)чайная ложка (Imp) (tsp)чайная ложка (U.S.) (tsp)
S.) (tbsp)чайная ложка (Can) (tsp)чайная ложка (Imp) (tsp)чайная ложка (U.S.) (tsp)
 119240471
119240471 000236588
000236588 00909218
00909218

 com › калькулятор производных
com › калькулятор производных
 date | дата:’ д МММ, гггг’}}
date | дата:’ д МММ, гггг’}}

 05.13
05.13  by 2013-2016
by 2013-2016


 е. -1
е. -1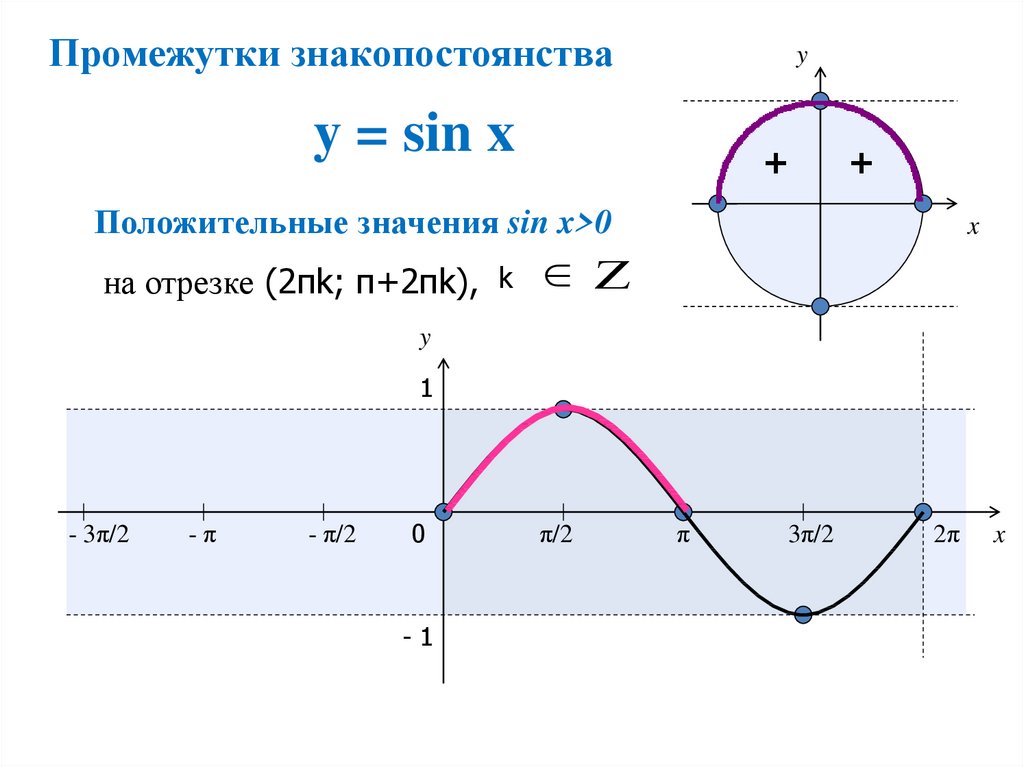
 (1)
(1)



 2.2)
2.2) Пусть
где F‘(x)
= f(x).
Пусть
где F‘(x)
= f(x).
 Интегрирование
требует индивидуального подхода к
каждой функции.
Интегрирование
требует индивидуального подхода к
каждой функции. е. интегрирование — это процесс, обратный дифференцированию. Но нельзя (не легко) каждый раз применять обратный процесс дифференцирования для вычисления интегралов. Правила интеграции очень помогли бы в этом отношении.
е. интегрирование — это процесс, обратный дифференцированию. Но нельзя (не легко) каждый раз применять обратный процесс дифференцирования для вычисления интегралов. Правила интеграции очень помогли бы в этом отношении.
 Если вы хотите увидеть, как выводится каждое из этих правил, нажмите на соответствующие ссылки.
Если вы хотите увидеть, как выводится каждое из этих правил, нажмите на соответствующие ссылки.
 Вот правила интегрирования этих обратных тригонометрических функций.
Вот правила интегрирования этих обратных тригонометрических функций. dx = sin -1 x + C
dx = sin -1 x + C
 В этом случае мы используем правило ILATE, где:
В этом случае мы используем правило ILATE, где: т. е.
т. е.


 Наиболее важные правила интегрирования следующие:
Наиболее важные правила интегрирования следующие: Однако все правила интегрирования не могут быть получены так просто. Для сложных функций вы можете обратиться ко всей этой странице.
Однако все правила интегрирования не могут быть получены так просто. Для сложных функций вы можете обратиться ко всей этой странице. .. + f(x n )), где h = (b — a)/n.
.. + f(x n )), где h = (b — a)/n.
 Правила применяются только тогда, когда интегралы существуют.
Правила применяются только тогда, когда интегралы существуют.
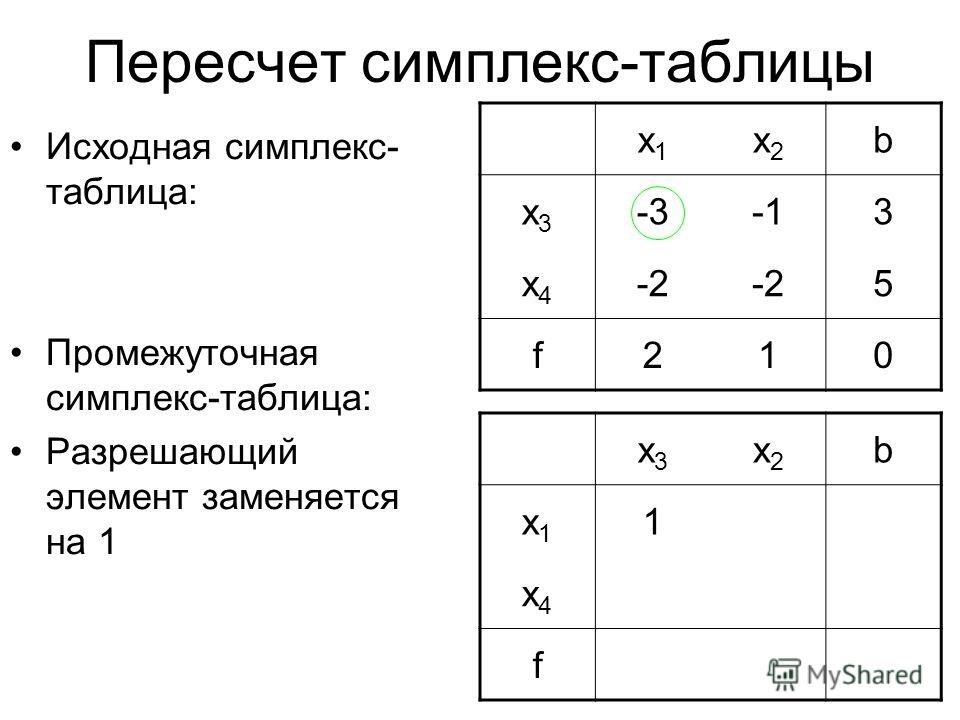
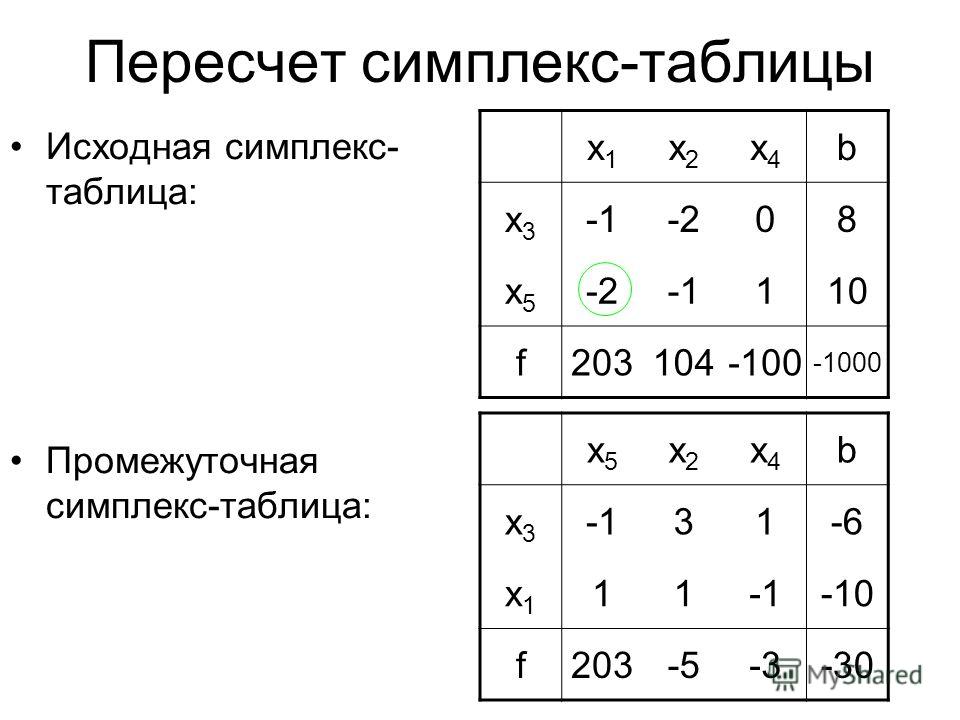
 Строка, соответствующая переменной x2 , получена в результате деления всех элементов строки x на разрешающий элемент РЭ=2 (см. табл.2) . На месте разрешающего элемента получаем 1. В остальных клетках столбца x2 записываем нули. Все остальные элементы, включая элементы индексной строки, определяются по правилу прямоугольника. Для этого выбираем из старого плана четыре числа, которые расположены в вершинах прямоугольника и всегда включают разрешающий элемент РЭ.
Строка, соответствующая переменной x2 , получена в результате деления всех элементов строки x на разрешающий элемент РЭ=2 (см. табл.2) . На месте разрешающего элемента получаем 1. В остальных клетках столбца x2 записываем нули. Все остальные элементы, включая элементы индексной строки, определяются по правилу прямоугольника. Для этого выбираем из старого плана четыре числа, которые расположены в вершинах прямоугольника и всегда включают разрешающий элемент РЭ.

 Разрешающий элемент РЭ=-1.
Разрешающий элемент РЭ=-1.
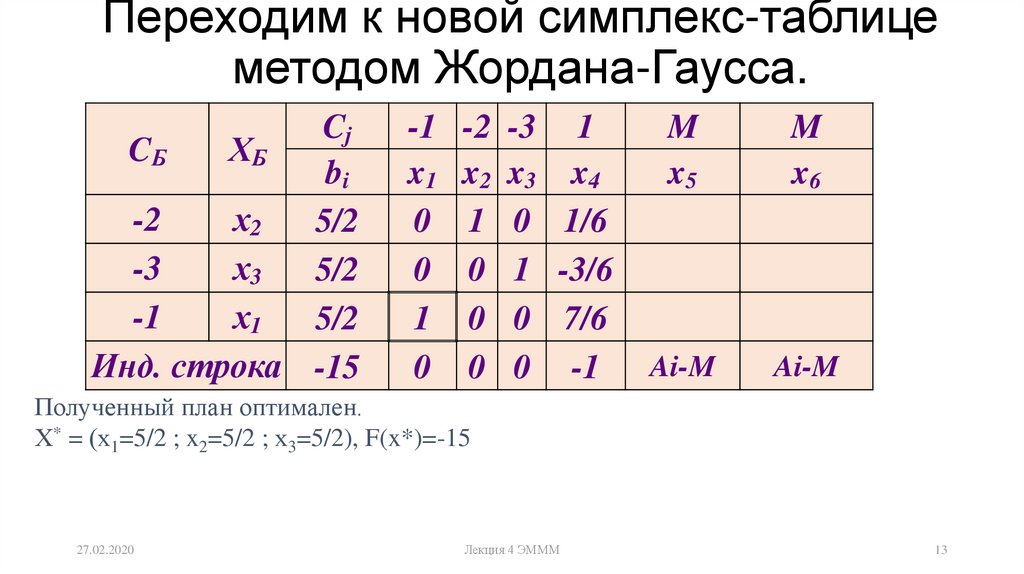
 На месте разрешающего элемента получаем 1. В остальных клетках столбца x3 записываем нули. Все остальные элементы, включая элементы индексной строки, определяются по правилу прямоугольника.
На месте разрешающего элемента получаем 1. В остальных клетках столбца x3 записываем нули. Все остальные элементы, включая элементы индексной строки, определяются по правилу прямоугольника.
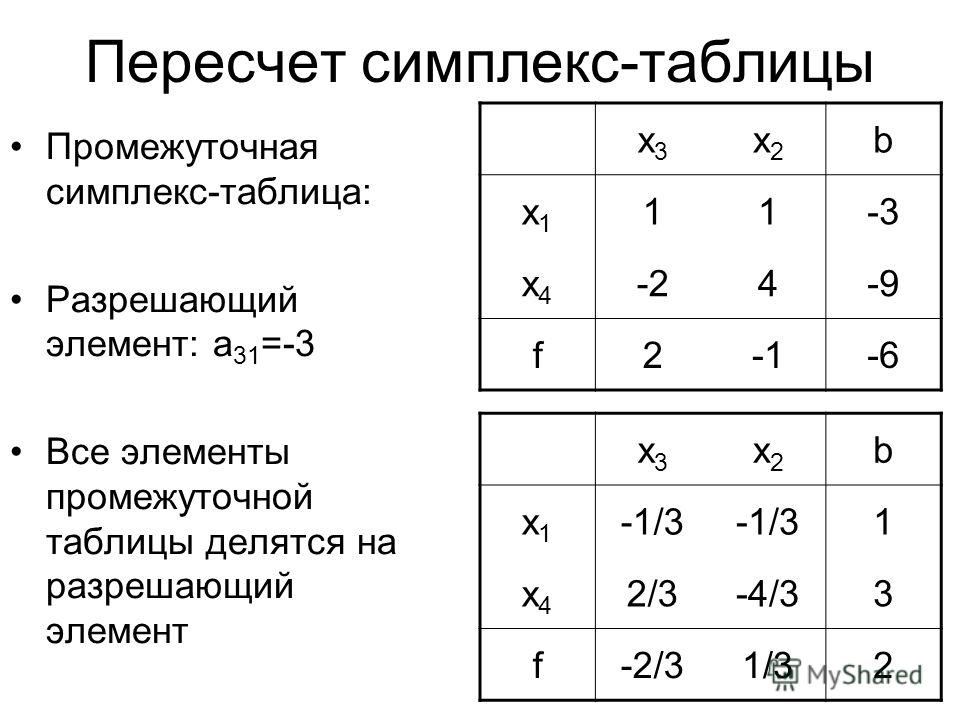 Поэтому одна из модификаций симплекс метода получила название табличный симплекс метод. Задача линейного программирования в каноническом виде:
Поэтому одна из модификаций симплекс метода получила название табличный симплекс метод. Задача линейного программирования в каноническом виде: Все дополнительные переменные мы приняли как базисные, а исходные переменные как небазисные (дополнительные записаны в первый столбец симплекс-таблицы а исходные в первую строку). При каждой итерации элементы симплекс-таблицы пересчитывают по определенным правилам.
Все дополнительные переменные мы приняли как базисные, а исходные переменные как небазисные (дополнительные записаны в первый столбец симплекс-таблицы а исходные в первую строку). При каждой итерации элементы симплекс-таблицы пересчитывают по определенным правилам. Знаки коэффициентов ограничивающих условий со знаком “≥” так же меняются на противоположные. В случае если условие содержит знак “≤” – коэффициенты запишутся без изменений.
Знаки коэффициентов ограничивающих условий со знаком “≥” так же меняются на противоположные. В случае если условие содержит знак “≤” – коэффициенты запишутся без изменений. Проверка на допустимость.
Проверка на допустимость.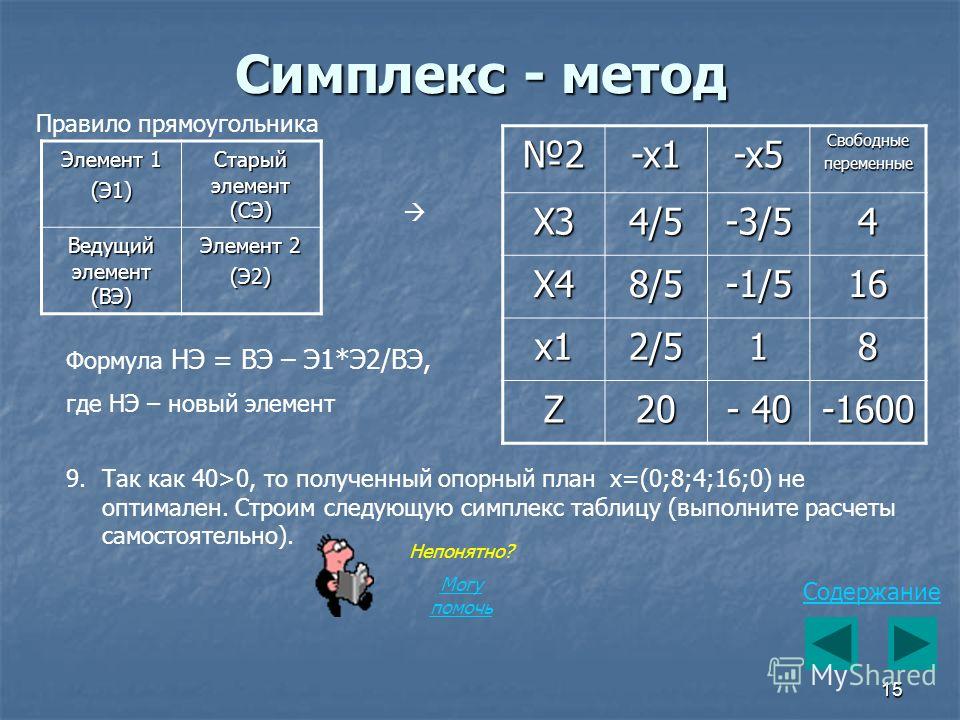
 Элемент ak,l – ведущий (разрешающий). Переменная, соответствующая ведущей строке (xk) исключается из базиса, переменная соответствующая ведущему столбцу (xl) включается в базис.
Элемент ak,l – ведущий (разрешающий). Переменная, соответствующая ведущей строке (xk) исключается из базиса, переменная соответствующая ведущему столбцу (xl) включается в базис.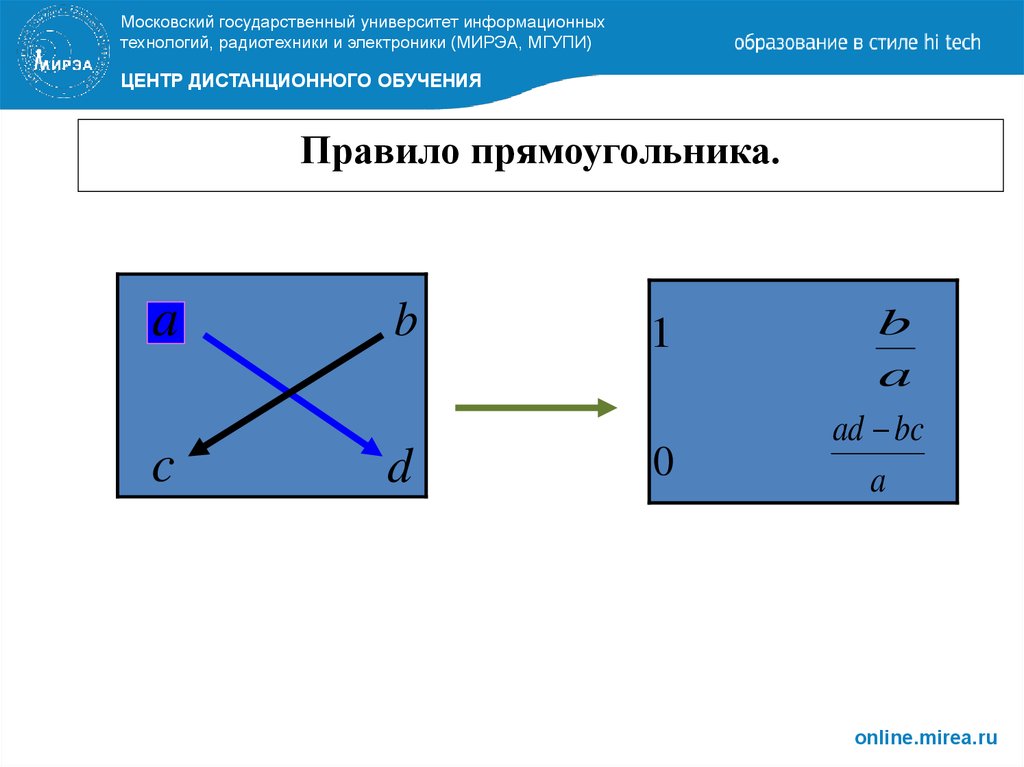
 Для удобства покупки
работы размещены на независимой бирже. Подробнее об условиях покупки тут.
Для удобства покупки
работы размещены на независимой бирже. Подробнее об условиях покупки тут.


 Все остальные элементы нового плана 2, включая элементы индексной строки, определяются по правилу прямоугольника.
Все остальные элементы нового плана 2, включая элементы индексной строки, определяются по правилу прямоугольника.
 Проверка критерия оптимальности.
Проверка критерия оптимальности.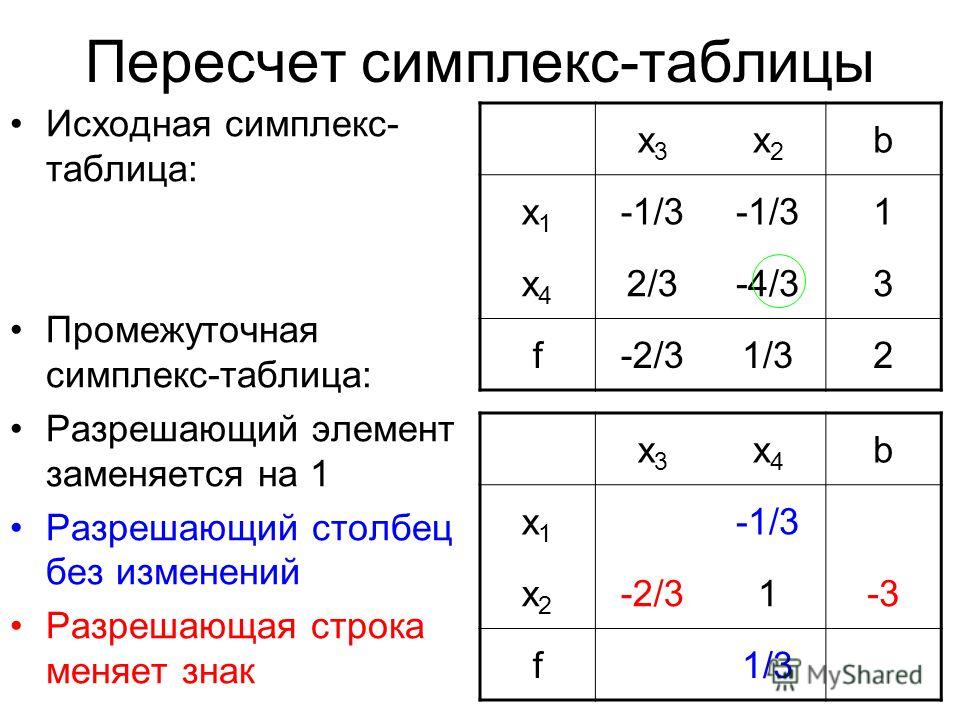 График x/y пространства решений показывает треугольник с вершиной в точке $x = \frac{1}{2}, y = \frac{1}{2}$. Чтобы максимизировать $y$, мы должны оказаться в этой точке.
График x/y пространства решений показывает треугольник с вершиной в точке $x = \frac{1}{2}, y = \frac{1}{2}$. Чтобы максимизировать $y$, мы должны оказаться в этой точке.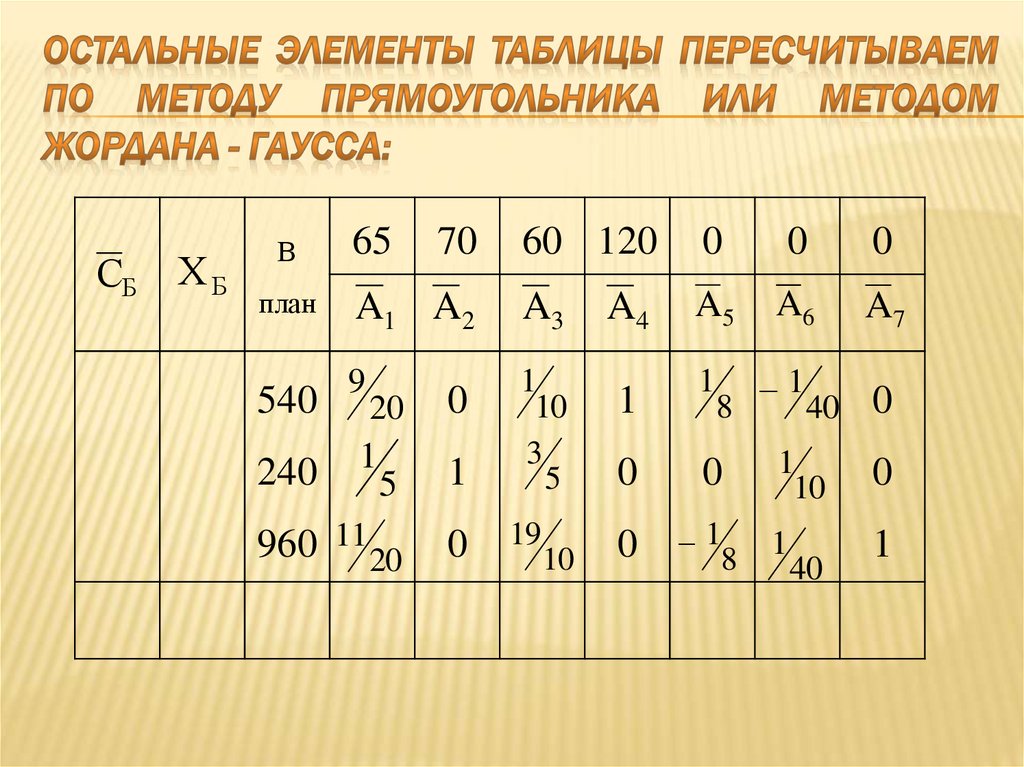 Но мы находимся в $x = 0, y = 1$, что даже не является решением, потому что $s_2$ является недопустимым значением. Давайте попробуем вместо этого выбрать строку 2, ту, у которой тестовый коэффициент равен 0:
$$1′:
\begin{bматрица}
& х & у & s_1 & s_2 & = \\
s_1 & 2 & 0 & 1 & -1 & 1 \\
у и -1 и 1 и 0 и 1 и 0 \\
&-1 & 0 & 0 & 1 & 0
\end{bmatrix}
$$
Но мы находимся в $x = 0, y = 1$, что даже не является решением, потому что $s_2$ является недопустимым значением. Давайте попробуем вместо этого выбрать строку 2, ту, у которой тестовый коэффициент равен 0:
$$1′:
\begin{bматрица}
& х & у & s_1 & s_2 & = \\
s_1 & 2 & 0 & 1 & -1 & 1 \\
у и -1 и 1 и 0 и 1 и 0 \\
&-1 & 0 & 0 & 1 & 0
\end{bmatrix}
$$
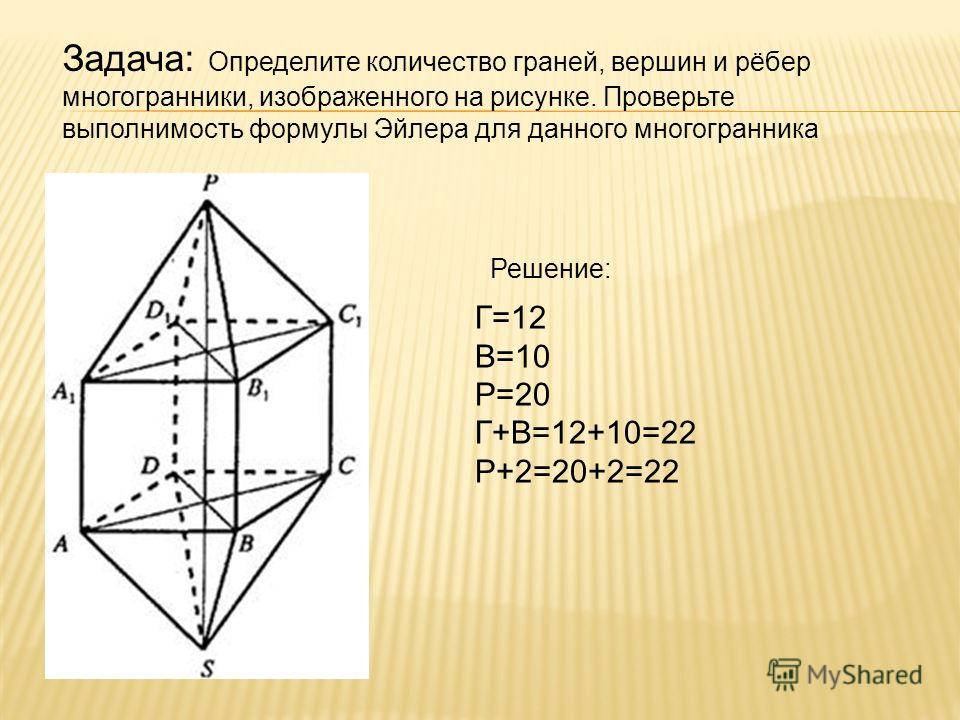 В течение нескольких тысяч лет это было самое большое рукотворное сооружение в мире, и это единственное из оригинальных чудес древнего мира, все еще существующих. Большая Пирамида, как и многие другие египетские пирамиды, имеет квадратное основание и по форме похожа на иллюстрацию выше.
В течение нескольких тысяч лет это было самое большое рукотворное сооружение в мире, и это единственное из оригинальных чудес древнего мира, все еще существующих. Большая Пирамида, как и многие другие египетские пирамиды, имеет квадратное основание и по форме похожа на иллюстрацию выше. Задачи на совместную работу (вариант 3)
Задачи на совместную работу (вариант 3)
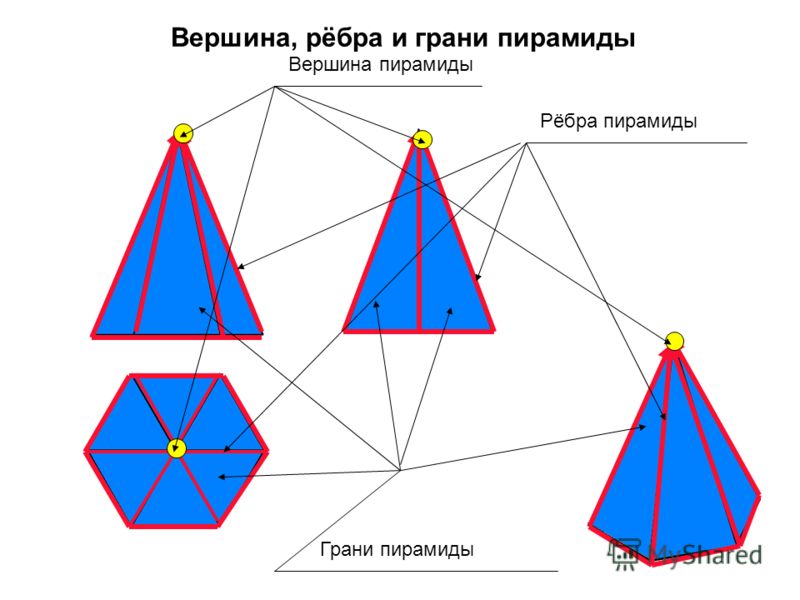
 — высота боковой грани
— высота боковой грани
 + просмотров
+ просмотров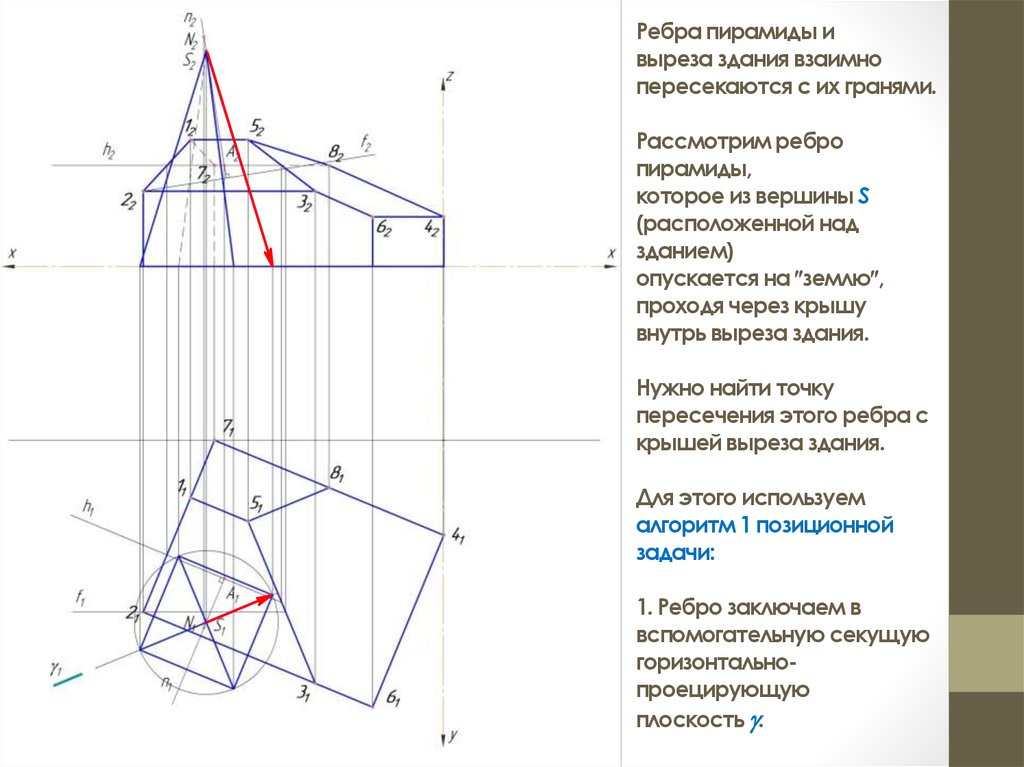 Используя их, выведем обобщенную формулу.
Используя их, выведем обобщенную формулу.